 届苏教版物质的制备及性质探究类实验单元测试Word格式文档下载.docx
届苏教版物质的制备及性质探究类实验单元测试Word格式文档下载.docx
- 文档编号:21067907
- 上传时间:2023-01-27
- 格式:DOCX
- 页数:10
- 大小:307.12KB
届苏教版物质的制备及性质探究类实验单元测试Word格式文档下载.docx
《届苏教版物质的制备及性质探究类实验单元测试Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《届苏教版物质的制备及性质探究类实验单元测试Word格式文档下载.docx(10页珍藏版)》请在冰豆网上搜索。
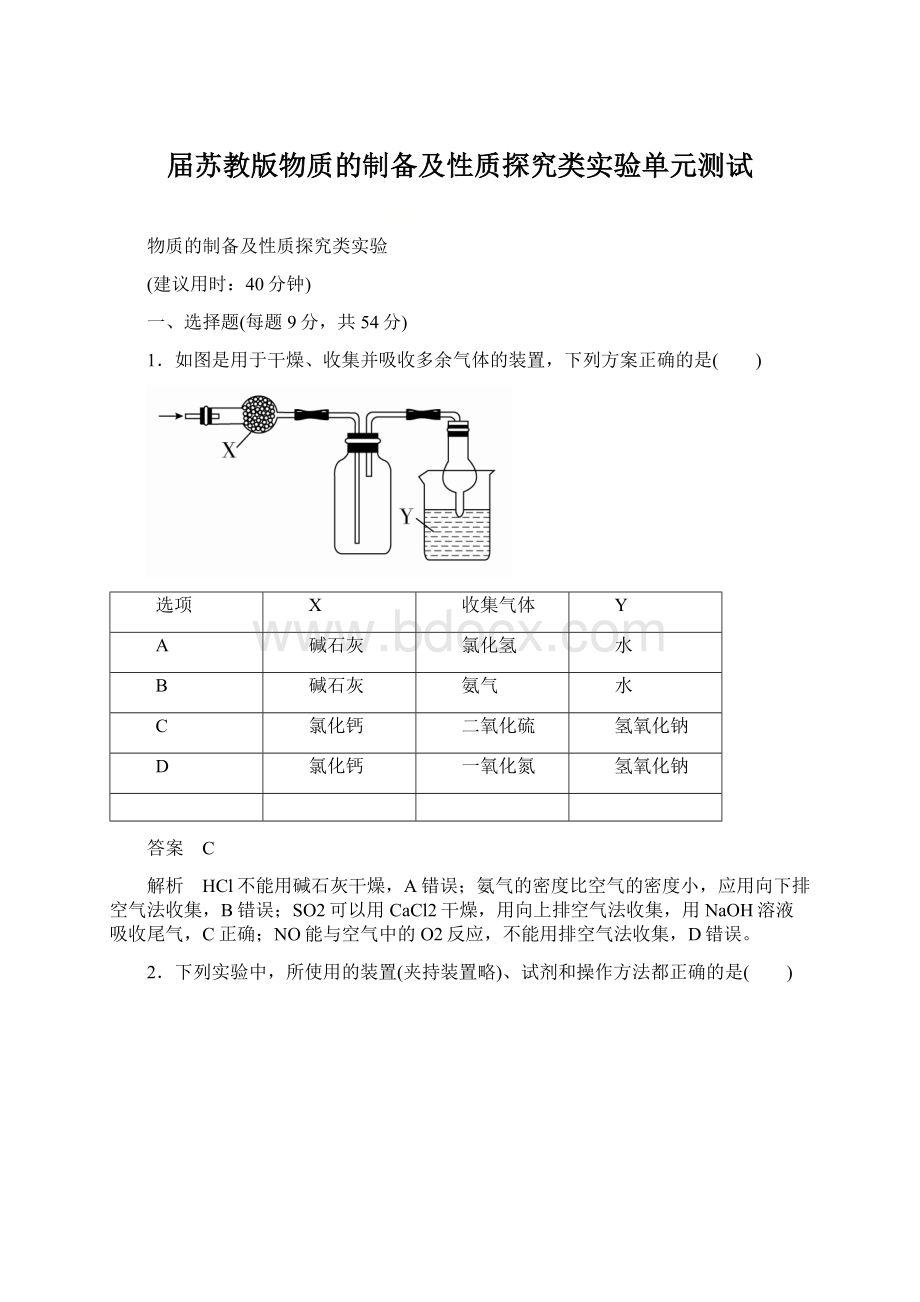
二氧化硫
氢氧化钠
D
一氧化氮
答案 C
解析 HCl不能用碱石灰干燥,A错误;
氨气的密度比空气的密度小,应用向下排空气法收集,B错误;
SO2可以用CaCl2干燥,用向上排空气法收集,用NaOH溶液吸收尾气,C正确;
NO能与空气中的O2反应,不能用排空气法收集,D错误。
2.下列实验中,所使用的装置(夹持装置略)、试剂和操作方法都正确的是( )
答案 A
解析 装置中的植物油能防止空气进入,生成的Fe(OH)2不被氧化,能观察到有白色Fe(OH)2沉淀生成,A正确;
配制一定物质的量浓度的溶液时,固体应先在烧杯中溶解,然后转入到容量瓶中定容,B错误;
实验室是用NH4Cl与Ca(OH)2固体反应制备NH3,而题目给出的一种药品为CaO,NH3极易溶于水,不能用排水法收集NH3,C错误;
该实验设计中,应将温度计水银球插入到液面以下,并且挥发出的乙醇也会使KMnO4酸性溶液褪色,无法判断是否生成了乙烯,D错误。
3.根据侯氏制碱原理制备少量NaHCO3的实验,经过制取氨气、制取NaHCO3、分离NaHCO3、干燥NaHCO3四个步骤。
下列图示装置和原理能达到实验目的的是( )
解析 A项,制NH3需要用NH4Cl固体和Ca(OH)2固体加热进行反应,错误;
B项,CO2应从长导管进短导管出,错误;
C项,制得的NaHCO3为固体,用过滤法分离,正确;
D项,加热时NaHCO3会分解,错误。
4.下列实验方案能达到实验目的的是( )
实验方案
实验目的或结论
将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色
可证明氧化性:
H2O2比Fe3+强
向1mL1%的NaOH溶液中加入2mL2%的CuSO4溶液,振荡,再加入0.5mL有机物Y,加热,未出现砖红色沉淀
说明Y中不含醛基
取ag铝箔与足量氢氧化钠溶液充分反应,逸出的气体通过浓硫酸后,测其体积为VL(已转化为标准状况下)
测定铝箔中氧化铝的含量
比较不同反应的反应热数据的大小
从而判断反应速率的大小
解析 A项将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中发生的反应可能有2Fe2++H2O2+2H+===2Fe3++2H2O,3Fe2++NO
+4H+===3Fe3++NO↑+2H2O,溶液变黄色,无法确定哪一个反应发生,无法比较H2O2和Fe3+的氧化性强弱,错误;
B项用新制Cu(OH)2悬浊液检验有机物中的醛基,必须保证碱性环境,题给NaOH溶液的量不足,无法检验有机物中是否含有醛基,错误;
C项取ag铝箔与足量NaOH溶液发生反应:
Al2O3+2OH-===2AlO
+H2O、2Al+2OH-+2H2O===2AlO
+3H2↑,通过测定生成H2的体积确定铝箔中铝的质量,进一步计算Al2O3的质量从而计算Al2O3的含量,正确;
D项化学反应速率与反应热的大小无关,错误。
5.下列有关实验操作和结论均正确的是( )
实验操作
结论
配制Fe(NO3)2溶液时加入适量的硝酸
抑制Fe2+水解
浓硫酸和蔗糖反应产生的气体通过足量的KMnO4溶液,气体全部被吸收且溶液紫红色褪去
“黑面包实验”产生
的气体具有还原性
往溶液中滴加NaOH溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝
原溶液中无NH
幼儿使用含NaF的牙膏可以使牙齿上的Ca5(PO4)3OH转化为Ca5(PO4)3F,防止蛀牙
Ksp[Ca5(PO4)3F]<
Ksp[Ca5(PO4)3OH]
答案 D
解析 亚铁离子发生水解生成氢氧化亚铁和氢离子,滴加HNO3时可以抑制Fe2+水解,但HNO3具有强氧化性,同时能氧化Fe2+,故A错误;
“黑面包实验”产生了CO2和SO2,SO2可以被KMnO4溶液吸收,CO2不可被KMnO4溶液吸收,故B错误;
检验NH
时,需往溶液中滴加浓NaOH溶液并加热,将湿润的红色石蕊试纸置于试管口,观察试纸是否变蓝,故C错误;
幼儿使用含NaF的牙膏可以使牙齿上的Ca5(PO4)3OH转化为Ca5(PO4)3F,防止蛀牙,难溶沉淀向更难溶沉淀转化,由于溶解度越小则Ksp越小,则溶度积:
Ksp[Ca5(PO4)3F]<Ksp[Ca5(PO4)3OH],故D正确。
6.下列关于实验的说法正确的是( )
实验目的
分离Fe(OH)3胶体和FeCl3溶液
将混合液倒入过滤器中过滤
证明Ksp(CuS)<Ksp(ZnS)
向10mL0.1mol/LNa2S溶液中滴入几滴0.1mol/LZnCl2溶液,产生白色沉淀,再加入CuSO4溶液,产生黑色沉淀
证明酸性:
H2CO3>H3BO3
向Na2CO3溶液中滴入过量H3BO3溶液,无气泡冒出
验证铁的吸氧腐蚀
将铁钉放入试管中,用盐酸浸没,产生气泡
解析 分离胶体与溶液应该用半透膜渗析,A错误;
ZnCl2与Na2S反应后Na2S有剩余,加入CuSO4溶液,剩余的Na2S和CuSO4反应产生黑色沉淀,不能比较两者溶度积的大小,B错误;
根据强酸制弱酸原理,向Na2CO3溶液中滴入H3BO3溶液,无气泡冒出,说明H3BO3不能与Na2CO3溶液反应生成H2CO3,因而不能产生二氧化碳气体,所以能够证明酸性:
H2CO3>H3BO3,C正确;
吸氧腐蚀发生在弱酸性或中性条件下,在酸性条件下发生的是析氢腐蚀,D错误。
二、非选择题(共46分)
7.(20分)硫代硫酸钠是一种重要的化工产品。
工业上常利用含硫废水生产Na2S2O3·
5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生成过程。
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)===Na2SO3(aq)+H2S(aq)(Ⅰ)
2H2S(aq)+SO2(g)===3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq)
Na2S2O3(aq) (Ⅲ)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若________________,则整个装置气密性良好。
装置D的作用是________________。
装置E中盛装的为________溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为________。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择________。
a.蒸馏水B.饱和Na2SO3溶液
c.饱和NaHSO3溶液D.饱和NaHCO3溶液
(4)实验中,为使SO2缓慢进入烧瓶C,采用的操作是______________________________。
(5)已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是______________________。
答案
(1)液柱高度保持不变'
防止倒吸'
NaOH(合理即可)
(2)2∶1 (3)c
(4)控制滴加硫酸的速度(合理即可)
(5)溶液变澄清(或浑浊消失)
解析
(1)两端活塞关闭,如果装置气密性良好,液柱高度应保持不变,如果装置气密性不好,液柱高度会下降。
分析装置图可知装置D是安全瓶,起防止倒吸的作用。
E为SO2气体的吸收装置,吸收二氧化硫用碱液,如氢氧化钠溶液等。
(2)C中Na2S和Na2SO3恰好完全反应,由反应(Ⅰ)、(Ⅱ)、(Ⅲ)可知,(Ⅰ)×
2+(Ⅱ)+(Ⅲ)×
3得到总反应:
2Na2S(aq)+Na2SO3(aq)+3SO2(g)
3Na2S2O3(aq),则C中Na2S和Na2SO3物质的量之比应为2∶1。
(3)二氧化硫溶于水,Na2SO3、NaHCO3均与SO2反应,故只有c项中饱和亚硫酸氢钠溶液适合。
(4)为使SO2缓慢进入烧瓶C,应控制滴加硫酸的速度。
(5)反应(Ⅲ)为S(s)+Na2SO3(aq)
Na2S2O3(aq),反应达到终点时,S完全溶解,可观察到浑浊消失。
8.(26分)以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
(1)经检验,现象Ⅰ中的白色沉淀是Ag2SO3。
用离子方程式解释现象Ⅰ:
______________________________________________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO
,含有Cu+、Cu2+和SO
。
已知:
Cu+
Cu+Cu2+,
Cu2+
CuI↓(白色)+I2。
①用稀H2SO4证实沉淀中含有Cu+的实验现象是______________________________________________。
②通过下列实验证实,沉淀中含有Cu2+和SO
a.白色沉淀A是BaSO4,试剂1是________________。
b.证实沉淀中含有Cu2+和SO
的理由是___________________
__________________________________________________________。
(3)已知:
Al2(SO3)3在水溶液中不存在。
经检验,现象Ⅲ的白色沉淀中无SO
,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和________。
②对于沉淀中亚硫酸根的存在形式提出两种假设:
ⅰ.被Al(OH)3所吸附;
ⅱ.存在于铝的碱式盐中。
对假设ⅱ设计了对比试验,证实了假设ⅱ成立。
a.将对比实验方案补充完整。
步骤一:
步骤二:
________________________________________________
(按如图形式呈现)。
b.假设ⅱ成立的实验证据是______________________________。
(4)根据实验,亚硫酸盐的性质有___________________________
__________________。
盐溶液间反应的多样性与____________有关。
答案
(1)2Ag++SO
===Ag2SO3↓
(2)①析出红色固体 ②a.HCl和BaCl2溶液 b.在I-的作用下,Cu2+转化为白色沉淀CuI,SO
转化为SO
(3)①Al3+、OH-
②a.
b.V1明显大于V2
(4)亚硫酸盐的溶解性、还原性、在水溶液中的酸碱性 两种盐溶液中阴、阳离子的性质和反应条件
解析
(1)饱和溶液中的Ag+与Na2SO3反应会生成更难溶的Ag2SO3。
(2)①根据现象Ⅱ和已知信息知,取少量洗涤干净的棕黄色沉淀,滴加稀硫酸,若有红色固体析出,则证明有Cu+。
②a.根据沉淀A是BaSO4,知加入的试剂1含Ba2+,可以选用盐酸酸化的BaCl2溶液。
b.由白色沉淀A为BaSO4可知原沉淀中的SO
被氧化为SO
,则加入KI时反应生成了I2,说明原沉淀中有Cu2+,即加入KI时Cu2+与I-反应生成白色沉淀CuI和I2,I2又与SO
反应生成SO
与I-,所以加入淀粉无明显现象。
(3)①根据题意知,现象Ⅲ的白色沉淀中无SO
,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色,推测沉淀中含有SO
和Al3+。
②与Al(OH)3相比,铝的碱式盐中每个铝离子所对应的氢氧根离子不足3个,因此可设计定量实验,记录数据V1,设计对比实验,记录数据V2,对比V1与V2即可得出结论。
(4)I2被还原,酸性KMnO4溶液褪色,均显示了亚硫酸盐的还原性,亚硫酸盐与Al3+发生双水解反应生成碱式盐,证明了亚硫酸盐在水溶液中水解而体现了酸碱性,根据实验流程及现象可知,盐溶液间反应的多样性和盐的性质及反应条件有关。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 届苏教版 物质 制备 性质 探究 实验 单元测试
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
