 版高中化学 第1章 第2节 元素周期律和元素周期表 第1课时 元素周期律学案 鲁科版必修2Word文件下载.docx
版高中化学 第1章 第2节 元素周期律和元素周期表 第1课时 元素周期律学案 鲁科版必修2Word文件下载.docx
- 文档编号:21015018
- 上传时间:2023-01-26
- 格式:DOCX
- 页数:15
- 大小:121.46KB
版高中化学 第1章 第2节 元素周期律和元素周期表 第1课时 元素周期律学案 鲁科版必修2Word文件下载.docx
《版高中化学 第1章 第2节 元素周期律和元素周期表 第1课时 元素周期律学案 鲁科版必修2Word文件下载.docx》由会员分享,可在线阅读,更多相关《版高中化学 第1章 第2节 元素周期律和元素周期表 第1课时 元素周期律学案 鲁科版必修2Word文件下载.docx(15页珍藏版)》请在冰豆网上搜索。
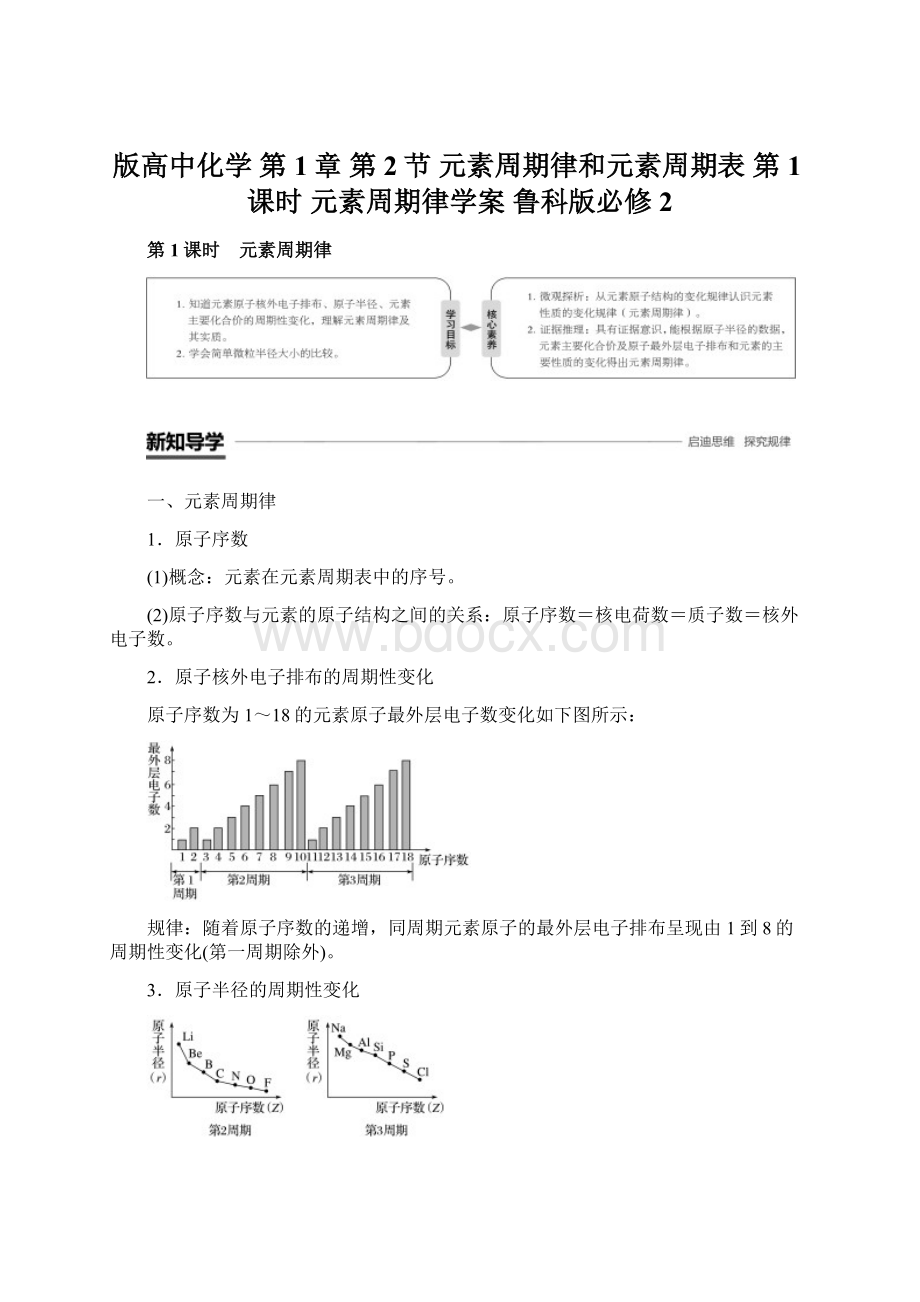
(3)H:
+1、-1、0价,如H2O、NaH、H2。
(4)金属元素只有正价无负价,非金属元素既有正价又有负价(F除外),多数非金属元素的正化合价出现变价。
例2
某元素X的最高价氧化物对应水化物的化学式是H2XO3,则X的简单气态氢化物的分子式为( )
A.HXB.H2X
C.XH3D.XH4
答案 D
解析 X元素的最高价氧化物对应的水化物的化学式为H2XO3,则X的最高正化合价为+4,说明X原子最外层有4个电子,最低负化合价为-4,形成的简单气态氢化物的分子式为XH4。
思维启迪——元素最高价与最低价的关系
(1)元素最高正化合价=最外层电子数(O、F除外)
(2)最低负化合价=最外层电子数-8(H除外)
(3)|最高正化合价|+|最低负化合价|=8(O、F、H除外)
二、微粒半径大小比较
1.同层——“序大径小”
电子层数相同,原子序数越大,原子半径越小。
实例:
r(Na)>r(Mg)>r(Al)>r(Si)>r(P)>r(S)>r(Cl)。
2.同最外层电子数——“序大径大”
最外层电子数相同,原子序数越大,原子(或离子)半径越大。
r(Li)<r(Na)<r(K),r(Li+)<r(Na+)<r(K+);
r(F)<r(Cl)<r(Br),r(F-)<r(Cl-)<r(Br-)。
3.同元素——“电多径大”
同种元素的不同微粒,其原子序数越多,半径就越大。
r(Na+)<r(Na),r(Cl-)>r(Cl);
r(Fe2+)>r(Fe3+)。
4.同结构——“序大径小”
电子层结构相同的离子,原子序数越大,离子半径越小。
r(O2-)>r(F-)>r(Na+)>r(Mg2+)>r(Al3+)。
(1)稀有气体元素原子半径的测量依据与其他原子半径的测量依据不同,不能进行比较。
(2)微粒电子层数和核电荷数、电子数都不相同时,可以借助“桥元素”比较。
如比较O和P原子半径时,P>
N>
O,或P>
S>
O。
例3
(2018·
雅安中学3月月考)下列各组元素中按微粒半径递增顺序排列的是( )
A.K Na LiB.N O F
C.Ca2+ K+ Cl-D.Ba2+ Ca2+ Mg2+
考点 元素周期律
题点 粒子半径的大小比较
解析 原子最外层电子数相同时,电子层数越多原子半径越大,则原子半径大小为Li<Na<K,A错误;
原子电子层数相同时,原子序数越大,则原子半径大小顺序为N>O>F,B错误;
离子电子层结构相同,核电荷数越大离子半径越小,则离子半径大小为Ca2+<K+<Cl-,C正确;
离子的最外层电子数相同,离子电子层越多,离子半径越大,则离子半径大小为Ba2+>Ca2+>Mg2+,D错误。
例4
已知原子序数小于18的元素的离子aA2+、bB+、cC2-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
A.原子半径:
A>
B>
D>
C
B.离子半径:
C2->
D->
B+>
A2+
C.原子序数:
d>
c>
b>
a
D.原子的最外层电子数目:
答案 B
解析 由4种离子具有相同的电子层结构可得a-2=b-1=c+2=d+1,a>
c,C项错误;
原子的最外层电子数目D>
C>
B,D项错误;
原子半径B>
D,A项错误。
思维启迪
电子层结构相同的离子,
离子半径:
序大径小;
原子最外层电子数:
阴多阳少;
原子序数:
阳大阴小。
1.元素的以下结构与性质,随着原子序数的递增不呈周期性变化的是( )
A.化合价
B.原子半径
C.元素原子的最外层电子排布
D.相对原子质量
解析 元素的化合价、原子半径、最外层电子排布等性质都随元素原子序数的递增而呈周期性变化,但相对原子质量的决定因素是原子中的质子数、中子数及同一元素的同位素原子在自然界中的百分数,故相对原子质量不呈周期性变化。
2.元素X、Y、Z的电子层数相同,原子序数依次增大,下列叙述一定正确的是( )
A.X、Y、Z原子的核内质子数依次增大
B.X、Y、Z的最高正化合价依次升高
C.X、Y、Z原子的原子半径依次增大
D.X、Y、Z单质的金属活动性依次增大
答案 A
解析 元素的原子序数等于原子核内的质子数,A项正确;
氟没有正价,氧没有最高正化合价,B项错误;
电子层数相同的原子,原子序数越大,原子半径越小,C项错误;
X、Y、Z中可能含有非金属,D项错误。
3.某主族元素的最高正价与最低负价的代数和为4,则该元素原子的最外层电子数为( )
A.4B.5
C.6D.7
解析 设该元素的最高正价为x,最低负价为y,则
解得x=+6,y=-2,因此该原子的最外层电子数为6。
4.(2017·
衡水高一检测)下列粒子半径之比大于1的是( )
A.
B.
C.
D.
解析 A项,r(K+)<r(K),
<1;
B项,r(Ca)>r(Mg),
>1;
C项,r(S)<r(P),
D项,r(Cl)<r(Cl-),
<1。
5.X和Y两元素的阳离子具有相同的电子层结构,X元素的阳离子半径大于Y元素的阳离子半径;
Z和Y两元素的原子核外电子层数相同,Z元素的原子半径小于Y元素的原子半径。
X、Y、Z三种元素原子序数的关系是( )
A.X>
Y>
ZB.Y>
X>
Z
C.Z>
YD.Z>
X
解析 已知电子层结构相同的阳离子,核电荷数大的则半径小;
具有相同电子层数的原子,随着原子序数增大,原子半径减小。
根据题意,X和Y两元素的阳离子具有相同的电子层结构,X元素的阳离子半径大于Y元素的阳离子半径,则X的原子序数小于Y的原子序数;
Z和Y元素的原子核外电子层数相同,且Z元素的原子半径小于Y元素的原子半径,则Y和Z两元素同周期,Z的原子序数大于Y的原子序数。
由此得出三种元素原子序数的关系为Z>
X。
6.已知Y为1~18号元素。
在水溶液中,YO
和S2-发生反应的离子方程式为YO
+3S2-+6H+===Y-+3S↓+3H2O,YO
中Y的化合价是________,Y元素原子的最外层电子数是__________,S2-的半径__________(填“大于”或“小于”)Y-的半径。
答案 +5 7 大于
解析 在氧化还原反应中得电子总数与失电子总数是相等的,即化合价升高总数等于降低总数。
硫元素化合价升高总数为2×
3=6,则Y元素化合价降低总数也是6,由此可知YO
中Y的化合价是+5价;
由Y-可知,Y原子得到1个电子变为稳定结构,故Y元素原子的最外层电子数是7;
因为Y是1~18号元素,又属于卤族元素,则Y是Cl,而Cl-与S2-具有相同的电子层结构但原子序数大于S2-,故其半径小于S2-的半径。
7.
(1)有下列四种微粒:
①
O ②
Na ③
Mg ④
N(用序号填空)。
Ⅰ.按原子半径由大到小顺序排列是_______________________________________________。
Ⅱ.微粒中质子数小于中子数的是_________________________________________________。
Ⅲ.在化合物中呈现的化合价的数值最多的是_______________________________________。
Ⅳ.能形成X2Y2型化合物的是________,能形成X3Y2型的化合物的是________。
(2)已知An+、B(n+1)+、Cn-、D(n+1)-都具有相同的电子层结构,则A、B、C、D的离子半径由大到小的顺序是________________________________,原子序数由大到小的顺序是__________________。
(3)X元素最高价氧化物对应的水化物为H3XO4,则它对应的气态氢化物的化学式为________,R元素的气态氢化物化学式为H2R,此元素最高价氧化物对应水化物的化学式________。
答案
(1)Ⅰ.②>
③>
④>
① Ⅱ.①② Ⅲ.④Ⅳ.①② ③④
(2)D(n+1)->
Cn->
An+>
B(n+1)+ B>
D
(3)XH3 H2RO4
解析
(1)Ⅰ.由
O、
N具有2个电子层,而
Na、
Mg具有3个电子层,因此Na、Mg的原子半径大于O、N的原子半径,而对于11Na、12Mg来说,由于Mg的核电荷数大,因此r(Na)>
r(Mg),同样r(N)>
r(O),故原子半径由大到小排列为r(Na)>
r(Mg)>
r(N)>
r(O)。
Ⅱ.由N=A-Z得中子数分别为N(O)=10、N(Na)=12、N(Mg)=12、N(N)=7。
Ⅳ.能形成X2Y2型化合物,则X可呈+1价而Y呈-1价,故为Na2O2;
能形成X3Y2型化合物,则X呈+2价,Y呈-3价,故为Mg3N2。
(2)当微粒具有相同电子层数时,核电荷数越大,核对最外层电子的吸引力就越大,其微粒半径就越小。
设An+、B(n+1)+、Cn-、D(n+1)-具有电子数为x,则质子数分别为x+n、x+(n+1)、x-n、x-(n+1),故离子半径由大到小的顺序为D(n+1)->
B(n+1)+。
(3)X元素的最高正价是+5价,则其最低化合价为-3价,故X元素氢化物的化学式为XH3;
R的最低化合价为-2价,其最高化合价为+6价,此元素最高价氧化物对应水化物的化学式为H2RO4。
[对点训练]
题组一 元素性质变化规律及应用
1.(2017·
济南高一检测)结合元素周期律的知识分析下列说法,其中正确的是( )
A.原子序数为15的元素的最高化合价为+5
B.随着元素原子序数的递增,原子最外层电子数总是从1到8重复出现
C.随着元素原子序数的递增,元素的最高化合价从+1到+7,最低化合价从-7到-1重复出现
D.B、C、N、O、F最高正价依次增加
解析 A项,P原子最外层为5个电子,最高化合价为+5,正确;
B项,H、He电子由1个到2个,错误;
C项,F无正价,负价从-4到-1,错误;
D项,O无最高正价,F无正价,错误。
2.(2017·
潍坊高一检测)下列关于各组元素性质的递变情况描述错误的是( )
A.Li、Be、B原子最外层电子数依次增大
B.P、S、Cl元素最高正价依次升高
C.N、O、F原子半径依次增大
D.Na、K、Rb的电子层数逐渐增多
3.如图中横坐标均表示11~17号元素按由小到大顺序排列的原子序数。
根据图像变化趋势判断,纵坐标表示其最高化合价的是( )
解析 11~17号元素,随原子序数的递增,最高化合价从+1→+7。
4.元素X、Y可组成化学式为XY3的化合物,则X、Y的原子序数不可能是( )
A.3和9B.7和1
C.13和17D.15和17
解析 A项,两元素分别为Li、F,只能形成化合物LiF;
B项,两元素分别为N、H,可形成NH3分子;
C项,两元素分别为Al、Cl,能形成化合物AlCl3;
D项,两元素分别为P、Cl,可形成PCl3和PCl5两种化合物。
5.(2017·
淮北高一检测)某元素原子L层电子数比K层的多5个,该元素的最高正化合价为( )
A.+5B.+6
C.+7D.无最高正化合价
解析 据题意可知该元素原子的核外电子排布为
,为氟元素,无最高正化合价。
6.如图是部分1~18号元素化合价与原子序数的关系图,下列说法正确的是( )
Z>Y>X
C.元素W的最高价和最低价代数和为4
D.Y和Z两者最高价氧化物对应的水化物不能相互反应
解析 根据随原子序数递增化合价变化特点分析知,X为O,Y为Na,Z为Al。
电子层数相同时,原子序数越大,半径越小;
同族自上而下原子半径逐渐增大,则半径:
Na>Al,Al>B,B>O,则Na>Al>O,A项错误;
Na、O、Al形成的离子核外电子排布相同,核电荷数越大,半径越小,故离子半径:
O2->Na+>Al3+,B项错误;
Na与Al的最高价氧化物对应的水化物分别为NaOH、Al(OH)3,两者能够反应,D项错误;
根据化合价知W为S,其最高价和最低价代数和为4,C项正确。
题组二 微粒半径大小比较
7.下列各元素原子半径依次增大的是( )
A.Na、Mg、AlB.Na、O、F
C.P、Si、AlD.C、Si、P
解析 比较元素原子半径的大小有两条规律:
①具有相同电子层数的元素,随着原子序数的递增,原子半径递减;
②具有相同最外层电子数的元素,随着电子层数的增加,原子半径增大。
A项,r(Na)>
r(Al);
B项,r(Na)>
r(O)>
r(F);
D项,r(Si)>
r(P)>
r(C)。
8.(2017·
淄博高一检测)下列微粒半径大小比较正确的是( )
A.Na+<Mg2+<Al3+<O2-
B.Na+>Al3+>S2->Cl-
C.Na<Mg<Al<S
D.Na<K<Rb<Cs
题点 微粒半径的大小比较
解析 A项,4种离子核外电子数相同,随着核电荷数增多,离子半径依次减小,即Al3+<Mg2+<Na+<O2-,A项错误;
因S2-、Cl-比Na+、Al3+多一个电子层,则S2-、Cl-半径比Na+、Al3+大,而S2-、Cl-和Na+、Al3+也分别适用“序小径大”的原则,则S2->Cl->Na+>Al3+,B项错误;
Na、Mg、Al、S的原子半径依次减小,C项错误;
Na、K、Rb、Cs最外层电子数相同,电子层数依次增多,半径依次增大,D项正确。
9.构成下列化合物的阴离子和阳离子的半径比值最大的是( )
A.LiIB.KCl
C.NaBrD.NaI
解析 离子半径:
r(Li+)<r(Na+)<
r(K+),r(Cl-)<
r(Br-)<
r(I-),故所给化合物中
比值最大。
题组三 元素周期律的综合应用
10.(2018·
清华大学附中月考)A、B、C三种元素的原子序数依次为a、b、c,它们的离子An+、Bn-、Cm-具有相同的电子层结构,且n>m,则下列关系正确的是( )
A.a>b>cB.a>c>b
C.a=b+m+nD.a=c-n-m
解析 离子An+、Bn-、Cm-具有相同的电子层结构,则有a-n=b+n=c+m,n>m,可知a>c>b,故A错误、B正确;
由关系式可知a=c+m+n,故C、D错误。
11.已知原子序数小于18的元素的离子aAm+、bBn+、cCm-、dDn-(m>
n)都具有相同的电子层结构,则下列叙述中正确的是( )
B.原子序数:
C.离子半径:
Cm->
Dn->
Bn+>
Am+
解析 四种离子具有相同的电子层结构,则阳离子对应的原子A、B比阴离子对应的原子C、D多1个电子层,且阳离子所带电荷数越多,其核电荷数越大,原子序数越大,原子半径越小;
阴离子所带电荷数越多,其核电荷数越小,原子序数越小,原子半径越大。
故有原子半径B>
D,原子序数a>
c,故A项和B项错误;
四种离子电子层结构相同,依据核电荷数越大,离子半径越小可知,离子半径Cm->
Dn->
Am+,故C项正确;
B,故D项错误。
12.已知X元素的阳离子和Y元素的阴离子具有与氩原子相同的电子层结构,则下列叙述正确的是( )
A.X的原子序数比Y的小
B.X原子的最外层电子数比Y的大
C.X的原子半径比Y的大
D.X元素的最高正价比Y的大
解析 利用举例法解答。
假设X为K元素,Y为Cl元素,则原子序数:
K>
Cl,最外层电子数:
Cl>
K,最高正化合价:
K。
[综合强化]
13.在原子序数11~18的元素中:
(1)原子半径最小的是________(填元素符号,下同);
只有正化合价的是________;
最高正化合价与最低负化合价绝对值之差为4的元素是________。
(2)与冷水剧烈反应生成H2的物质是________(填名称)。
与水反应能生成具有漂白性物质是________(填名称),反应的离子方程式是___________________________________________。
(3)化学性质最稳定的物质是_____________________________(填化学式)。
答案
(1)Cl Na、Mg、Al S
(2)钠 氯气 Cl2+H2O===H++Cl-+HClO (3)Ar
解析
(1)在11~18号原子中,半径最小的是Cl;
金属元素Na、Mg、Al只有正化合价;
S元素最高正化合价是+6,最低负化合价是-2,绝对值之差是4。
(2)金属钠与冷水剧烈反应生成H2和NaOH;
Cl2和水反应生成HCl和HClO,其中HClO有漂白性。
(3)稀有气体元素Ar原子最外层有8个电子,是稳定结构,通常不与其他物质发生反应,化学性质稳定。
14.原子序数是指元素在元素周期表中的序号,数值上等于原子核的核电荷数(即质子数)或原子的核外电子数。
今有A、B两种元素,其原子序数分别为9和15。
(1)写出元素符号:
A________,B________。
(2)A元素原子核外有______个电子层,最外层有______个电子。
(3)B元素最高正价为________,最低负价为________。
(4)A、B元素原子半径大小关系为r(A)________r(B)。
答案
(1)F P
(2)2 7 (3)+5 -3 (4)<
15.有A、B、C、D四种元素,A的最高正价与其最低负价的绝对值之差为6;
A、D次外层都是8个电子,A与D的化合物DA在水溶液中能电离出具有相同电子层结构的阴、阳离子;
B有两个电子层,其最高正价与最低负价的代数和为0;
C2-与氩原子具有相同的电子层结构。
(1)试写出上述各元素的符号:
A________,B________,C________,D________。
(2)画出下列粒子的结构示意图:
A__________________,C2-_________________________。
(3)写出A、D的最高价氧化物对应水化物反应的化学方程式:
_______________________。
答案
(1)Cl C S K
(2)
(3)HClO4+KOH===KClO4+H2O
解析 因为“A的最高正价与其最低负价的绝对值之差为6”,确定A为氯(Cl);
“B有两个电子层,最高正价与最低负价的代数和为0”,确定B为碳(C);
C2-的结构示意图为
,确定C为硫(S);
再由A推出D为钾(K)。
16.有A、B、C、D、E五种元素,它们的原子序数按E、C、D、A、B依次增大,E原子最外层有4个电子;
A-与B+的核外电子排布相同;
D的气态氢化物的化学式为H2D,最高价氧化物中D的质量分数为40%,且D原子核内质子数和中子数相等;
C的原子序数比D少9,比B少12。
(1)写出五种元素的符号:
A________,B________,
C________,D________,E________。
(2)画出A-、B+的结构示意图:
________、________。
(3)A、D最高价氧化物对应的水化物化学式分别为________、________。
(4)写出E的最高价氧化物与过量B的最高价氧化物对应的水化物反应的离子方程式:
________________________________________________________________________
________________________________________________________________________。
(5)写出B、C最高价氧化物对应的水化物之间相互反应的化学方程式:
答案
(1)Cl K N S C
(2)
(3)HClO4 H2SO4 (4)CO2+2OH-===CO
+H2O
(5)KOH+HNO3===KNO3+H2O
解析 D的氧化物分子式为DO3,D的质量分数为40%,可推出D的相对原子质量为32,从而推出D为S元素;
C原子序数比D少9,比B少12,则C为N元素,B为K元素;
A-与B+核外电子排布相同,则A为Cl元素;
E原子最外层有4个电子,且原子序数按E、C、D、A、B依次增大,则E为C元素。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 版高中化学 第1章 第2节 元素周期律和元素周期表 第1课时 元素周期律学案 鲁科版必修2 高中化学 元素周期律 元素 周期表 课时 鲁科版 必修
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
链接地址:https://www.bdocx.com/doc/21015018.html


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
