 高考化学工艺流程试题解题思路模型.docx
高考化学工艺流程试题解题思路模型.docx
- 文档编号:20980819
- 上传时间:2023-04-25
- 格式:DOCX
- 页数:43
- 大小:458.73KB
高考化学工艺流程试题解题思路模型.docx
《高考化学工艺流程试题解题思路模型.docx》由会员分享,可在线阅读,更多相关《高考化学工艺流程试题解题思路模型.docx(43页珍藏版)》请在冰豆网上搜索。
高考化学工艺流程试题解题思路模型
2020-2021高考化学工业流程图解题模型
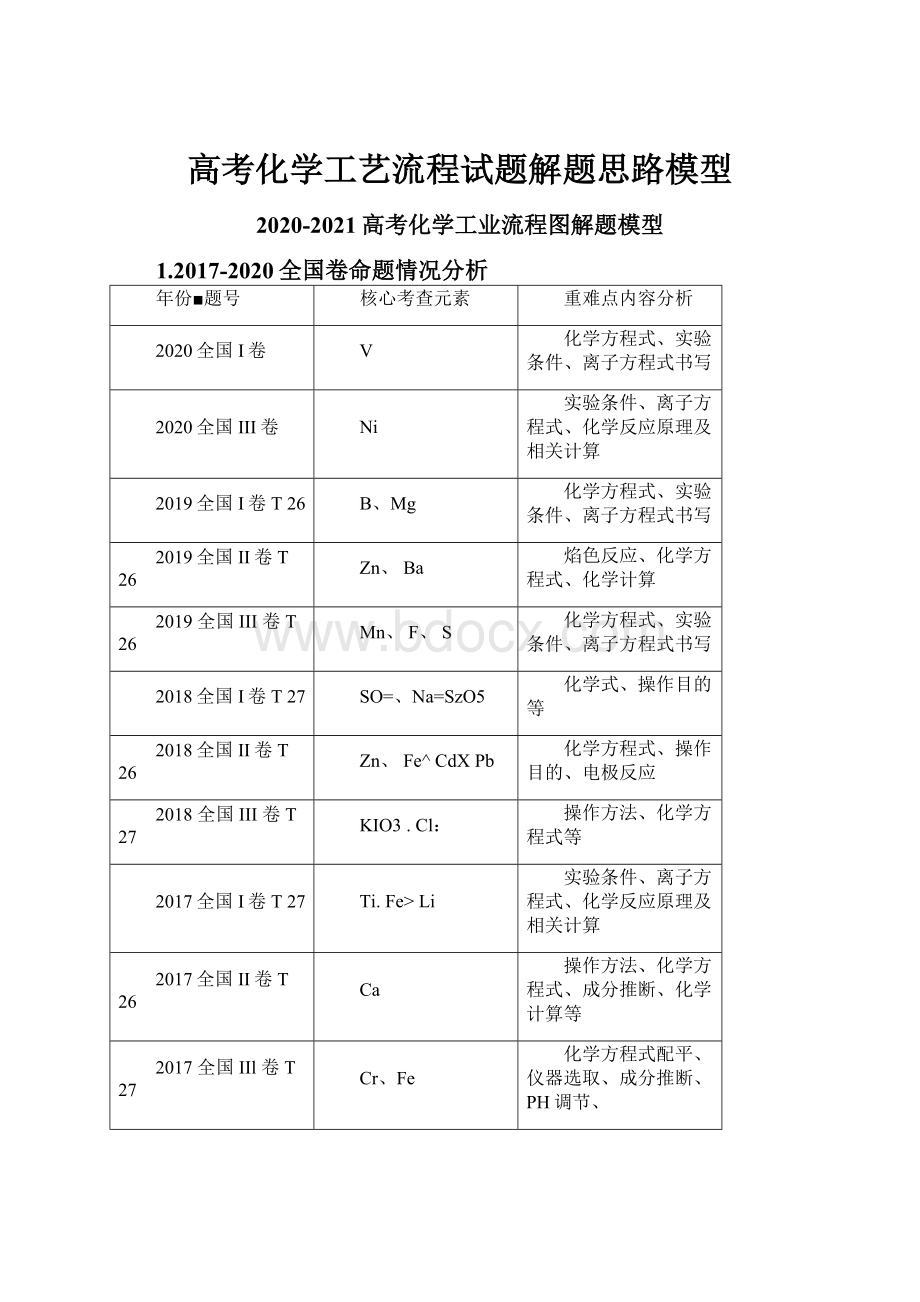
1.2017-2020全国卷命题情况分析
年份■题号
核心考查元素
重难点内容分析
2020全国I卷
V
化学方程式、实验条件、离子方程式书写
2020全国III卷
Ni
实验条件、离子方程式、化学反应原理及相关计算
2019全国I卷T26
B、Mg
化学方程式、实验条件、离子方程式书写
2019全国II卷T26
Zn、Ba
焰色反应、化学方程式、化学计算
2019全国III卷T26
Mn、F、S
化学方程式、实验条件、离子方程式书写
2018全国I卷T27
SO=、Na=SzO5
化学式、操作目的等
2018全国II卷T26
Zn、Fe^CdXPb
化学方程式、操作目的、电极反应
2018全国III卷T27
KIO3.Cl:
操作方法、化学方程式等
2017全国I卷T27
Ti.Fe>Li
实验条件、离子方程式、化学反应原理及相关计算
2017全国II卷T26
Ca
操作方法、化学方程式、成分推断、化学计算等
2017全国IIl卷T27
Cr、Fe
化学方程式配平、仪器选取、成分推断、PH调节、
离子方程式书写、产率计算
二、工业流程思路分析
1、常见解题思路图:
m原料预处理e⅛t杂、净化②
图4工业个产流程主线与核心
(1)流程图一般三大部分(见上图):
原料预处理、核心化学反应、分离提纯。
(2)流程中要分析“进”、“出”物质和仍然留在溶液中的离子等
2.识别流程图
1.呈现模式
(3)一般默认进的物质过量,确保每一步目标元素利用率或转化率最高,产品产率最髙,减少损失。
詈理处翌蔭社塑乞目标产物精处黑目标产品
料AI
循环利用
「排放物的
无害化处理
2.识图方法
图1图2图3
图1箭头表示反应物加入同时生成物出来:
图2箭头表示反应物分步加入和生成物出来:
图3箭头表示循环反应。
3.细分析,看措施,推用意,理关系
1原料和产品:
从某种原料出发,要得到最终产品,必须除去什么元素、引进什么元素?
关注杂质离子的去向及产品的生成,有时需要逆向推倒。
2步骤与目的:
加入某种试剂(什么反应),进行相应操作,其目的是什么?
结合后而步骤进行思考。
特别关注化合价变化和溶液酸碱性(两大主旋律)。
3信息和迁移:
新信息一般是重要的暗示和突破口,所给的信息一左有用,但需要提炼、重组、分解和迁移,结合设问分析、判断,正确作答
4感觉和结果:
对于比较陌生的流程,不必纠结于某步骤不能看懂,要从宏观上把握整个流程,抓大放小,关注步骤的结果,跟着感觉走。
三、教材课本经典流程模型建立:
1、高中化学三大流程模型分析
核心反应
碳酸化
过濾
(碎液2';
循环利用
图1侯氏联合制碱汰流程图
9
NH4Cl
2.教材精彩流程分析:
海带中碘的提取
2Γ+C12=h+2CΓ
工业上制纯碱
NH4Cl
纯碱
φNH3+H2O+CO2+NaCl^=NaHCO31+NH4C1
22NaHCO^J=Na2CO3+H2O+CO2T
工业上利用黄铁矿(Fe2S)制取硫酸
14FcS2+lICh2Fe2O3+8SO2
22SO2+O2r催化利2SO3
3SO3+H2O^=H2SO4
氯碱工业
φ2NaCl+2H2O=≤^=2NaOH+H2T+Cl2↑
2Ch+2NaOH^=NaCl+NaC10+H20
32C12+2Ca(OH)2=CaC12+Ca(ClO)2+2H2O
占燃
ΦC12+H2≤≡2HC1
从铝土矿中提炼铝
流程[
1Abθ3+6HC1^=2AlCh+3H2O
Fe2O3+6HCl^=2FeCh+3H2O
2Hel+NaOH^=NaCl+H2O
FCCI3+3NaOH^=FC(OH)3J+3NaCl
AICh+4NaoH^=NaAlO2+3NaCI+2HιO
3NaAlO2+Cθ2+2H2O^=AI(OH)3∣+NaHCO3
NaOH+CO2^=NaHCO3
42A1(OH)5=^=A12O3+3H2O
52AbCh(熔融)••逑电4A1+3O2T
冰晶石
四、工业流程中实验操作和精选例题
(一)工业流程第一步:
原料的预处理
1、原料预处理方法及操作目的:
1酸浸:
溶解、去氧化膜等,使得可溶性的离子进入溶液中,不溶物过滤去除。
2碱浸:
去油污(酯)、溶解铝、二氧化硅、氧化铝等,使得可溶性的离子进入溶液中,不溶物过滤去除。
3水浸:
与水反应或溶解,使原料变成离子进入溶液中。
4研磨(雾化、粉碎):
增大反应接触面积,以加快化学反应速率或使反应更充分
5灼烧(焙烧、锻烧):
使物质高温分解或者氧化去除杂质改变物质结构,使物质能溶解。
如从海带中提取碘时的灼烧就是为了除去可燃性杂质。
6加入苴他物质:
如有机物醇、四氯化破、无机盐等,其作用是反应、溶解。
关键词浸取液(浸岀液)固体加水、酸、碱等溶解得到的离子的溶液。
浸取率(浸出率)一固体溶解后,离子在溶液中的含量的多少。
注意与浸取速率(浸出速率)的差别。
2、高考真题及模考练习:
1.(2015-全国卷【节选)硼及其化合物在工业上有许多用途。
以铁硼矿(主要成分为Mg2B2O5∙H2O和FcQb还有少⅛Fe2O3.FeO.CaO.AI2O3和SiO?
等)为原料制备硼酸(H3BO3)W工艺流程如下所示:
铁硼亠
硫酸
矿粉
浸出
过滤If
浸进
—粗硼酸
滤渣含镁盐母液
为提高浸出速率,除适当增加硫酸浓度外,还可采取的措施有__
2.某工厂生产硼砂过程中产生的固体废料,主要含有MgeO3、MgSiO3.CaMg(CO3)2.AlO和Fe2O3^,回收英中镁的工艺流程如下:
固体废料
硫酸NaoII溶液
NaO严液爾过滤H调PH却12.5P-滤液」
MgCl2-
滤液U—
-Mg(OH)2—
试回答在"浸出"步骤中,为提髙镁的浸出率,可采取的措施有(两条即可)。
3・稀土是一种不可再生的战略性资源,被广泛应用于电子信息、国防军工等多个领域。
一种从废弃阴极射
线管(CRT)荧光粉中提取稀土元素轮(Y)的工艺流程如下:
0.8molβL**
废弃CRT
荧光粉预处理
I
盐酸广濾渣
5m,,pL二不参与反应的杂质
滤液-
盐酸
滤液(含Mg2+)丫2。
3・鬲竽烧滤渣
Vl
L-滤液
滤渣
DDTC
已知:
废弃CRT荧光粉的化学组成(某些不参与反应的杂质未列出)
成分含量/%
YU):
ZnO
Al2O3
PbO2
MgO
预处理前
24.28
41.82
7.81
1.67
0.19
预处理后
68.51
5.42
4.33
5.43
0.50
试回答步骤I中进行原料预处理的目的为O
4.确(Te)位于元素周期表第VlA族,由该元素组成的物质可用作石油裂化的催化剂,电镀液的光亮剂,玻璃的着色材料,合金材料的添加剂等。
晞化铜渣是电解精炼铜时产生的一种矿渣,其主要含Cu2Te.Au、
Ag等,利用下列工艺流程可回收晞:
Nar)Il双魚水
浓浴液
滤液IF酸浸2H■滤渣2
确粉
晞化铜渣
H2SO4.
Na2SO3
适量H2SO4^空气软化水
II2SO4
已知:
TCo2的熔点为733°C,微溶于水,可溶于强酸和强碱。
“酸浸1"需加热,加热的目的是
参考答案;
1.适当加热,搅拌
2.适当提高硫酸浓度,适当升温
3.加速溶解、加快反应速率,提高浸出率
4.加快反应速率,提高原料转化率
(二)、工业流程必考条件控制:
温度的控制
1、加热:
加快反应速率或溶解速率;促进平衡向吸热方向移动;
除杂,除去热不稳泄的杂质,如NaHCO3、Ca(HCo3)2、KMno,R、NH4Cl等物质:
使沸
点相对较低的原料气化
2、降温:
防止某物质在髙温时会溶解(或分解):
使化学平衡向着题目要求的方向移动(放热方向);
使某个沸点较高的产物液化,使其与苴他物质分离:
降低晶体的溶解度,减少损失
3、控温:
(用水浴或汕浴控温)
防止某种物质温度过髙时会分解或挥发:
为了使某物质达到沸点挥发岀来;
使催化剂的活性达到最好:
防I上副反应的发生:
降温或减压可以减少能源成本,降低对设备的要求,达到绿色化学的要求。
4
4、控制温度的方法及答题模板:
升温方法:
洒精灯加热,洒精喷灯加热,水浴、汕浴、沙浴加热,水蒸气加热,加热水,吹热风加热
降温方法:
冷冻法,冰水浴,减压蒸餾,减压烘干,减压蒸发等。
条件变化
思维方向
解析
正面结果
是否提高生产效率
平衡是否可以正向移动,提髙产率
看是否为可逆反应,且是否为吸热反应
负面结果
是否发生副反应
1注意题目给出的副反应发生的条件;
2注意温度升高易被氧化的物质:
醛类、酚类、XSOF等;
3有机实验中使用浓硫酸时注意是否发生炭化、氧化等副反应
是否有物质挥发
1注意题给低沸点物质,如液漠等;
2注意是否有气体参与反应过程,气体在溶液中的溶解度一般
随温度的升高而降低
是否有物质分解
注意反应中是否有镀盐、硝酸盐、结晶水合物、碳酸酸式盐、双氧水、氨水等热稳定性较差的物质参与
平衡是否向逆向移动
注意温度变化造成的平衡移动是否使反应向有利的方向移动
5、高考模考精选习题及答案:
例1:
实验室用硫酸厂烧渣(主要成分为Fe2O3及少量FeS.SiO?
等)制备聚铁(碱式硫酸铁的聚合物和
绿矶(FeSO4∙7H2O),过程如下:
烧渣足量0?
、稀硫酸
固体W(S、SiO2等)晋*溶液X警5溶液Z∙70f-r>聚铁胶体才聚饮
③I
溶液Y-^一绿矶
(5)在⑥中.将溶液Z控制到70〜80°C的目的是
例2(2017全国I)Li√ΠQi2和LiFCPCh都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FCTiO3,
还含有少⅛MgO.SiCh等杂质)来制备,工艺流程如下:
钛铁矿竺
酸浸
Tiθ2∙汎O兰竺忌甘空ULi瓚S巴竺—LijisO12
水解沉淀氨水旦幻过滤汎淀高温锻烧①
滤液①一—一"
过滤L滤液②磐竺F鹽J⅛H3,IW
磷酸讥旋离温锻烧②
Tio2・xH?
O沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
温度/°C
30
35
40
45
50
TiO2-XH2O转化率%
92
95
97
93
88
分析40C时TiO2XH2O转化率最髙的原因
总结:
在设问中如果出现回答选择某温度或某一温区的原因时,应从低于该温度或温区下限和髙于该温度或温区上限两个方而回答。
例3实验室以工业废渣(主要含CaSO4-2H2O,还含少⅛SiO2.Al2O3.Fe2O3)为原料制取轻质CaCO3和(NH4)
(NH4)2CO3溶液
滤液
濾渣
废渣粉末
2SO4晶体,其实验流程如下:
*(NH4)2SO4晶体
废渣浸取在如图所示的装置中进行。
控制反应温度在60~70搅拌,反应3小时。
温度过髙将会导致
CaSO4的转化率下降,其原因是
例4精炼铜工业中阳极泥的综合利用具有重要意义。
一种从铜阳极泥(主要含有铜、银、金、少量的線)中
铜阳极泥一I分铜}
i.H2SO4.M2O2
ii.NaCl
分铜渣
MCkNaClOi
Na2SO.,
HiSO4
分金液
分银潢
沉银液
AgCl
分离提取多种金属元素的工艺流程如下:
分铜液
"分铜''时,如果反应温度过髙,会有明显的放岀气体现象,原因是.
例5(2016全国【II)过氧化钙微溶于水,溶于酸,可用作分析试剂、医用防腐剂、消毒剂。
以下是一种
制备过氧化钙的实验方法。
CaCo≡-≡>滤液響;辭》-‰白色晶体
(1)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液呈—性(填“酸二
“碱”或“中”。
将溶液煮沸,趁热过滤。
将溶液煮沸的作用是O
(2)步骤③中反应需要在冰浴下进行,原因是o
例6碳酸锂广泛应用于化工、冶金、陶瓷、医药、制冷、焊接、锂合金等行业。
制备流程如下:
已知:
碳酸锂的溶解度(g・L1)见下表。
温度/°C
0
10
20
30
40
50
60
80
100
Li2CO3
1.54
1.43
1.33
1.25
1.17
1.08
1.01
0.85
0.72
(1)硫酸化焙烧工业反应温度控制在250〜300°C,主要原因是
(2)“沉锂“需要在95°C以上进行,主要原因是参考答案:
1、升高温度促进Fey的水解,过高温度不利于聚铁的形成(或者完全水解
2、低于40°.TiO2XH2O转化反应速率随温度升髙而增加:
超过40°C,双氧水分解与氨气逸出导致TiO2XH2O
转化反应速率下降
3、温度过高,(NH4)2CO3分解
4、"分铜时,如果反应温度过高,双氧水发生分解,会有明显的气体放出现象
5、酸性,除去水中溶解的二氧化碳。
防止氨水及过氧化氢的分解和挥发
6、防止浓硫酸蒸发。
Li2CO3的溶解度小,得到的Li2CO3多
(三)工业流程基本操作:
分离与提纯
(1)过滤
1基本要领:
一贴二低三靠四洗。
2洗涤的流程:
为什么要洗?
用什么洗?
怎么洗涤?
是否洗干浄?
a:
为什么洗:
去除晶体表而的杂质;把目标产物尽可能洗出来,提升产率。
b:
用什么洗:
蒸懈水、冷水、有机溶剂(醇酮陋)等:
如用酒精洗硫酸亚铁披晶体可降低晶体因溶解造成损失,可以除去表而的水酒精易挥发,易干燥。
c:
怎么洗涤:
沿着玻璃棒向过滤器中加入蒸憾水(英他溶剂)至浸没沉淀,待英自然流下后,重复2~3次。
d:
是否洗干净(离子检验):
取最后一次洗涤液少许于试管中,滴加某试剂(其他操作),产生什么现象?
则证明是否洗干净
3特殊的过滤方法:
减压过滤(吸滤、抽滤):
减压过滤装置由真空泵、布氏漏斗、吸滤瓶组成。
(2)结晶(重结晶)
1产物类型:
溶液中含单一溶质时,所得晶体不带结晶水,如氯化钠溶液结晶过程为蒸发结晶:
所得晶体带有结晶水,如硫酸铜溶液得到CuSO4∙5H2O的晶体过程为蒸发浓缩、冷却结晶、过滤。
2:
分离
溶液中含两种以上溶质时,要得到溶解度受温度影响小的溶质采用蒸发结晶、趁热过滤,
如除去NaCl中少疑的KCI;要得到溶解度受温度影响大的溶质采用蒸发浓缩、冷却结晶、过滤,如除去
KCl中少量的NaCl晶体
3晶体F燥的方法:
自然晾干、滤纸吸干、在干燥器中干燥、烘干(热稳泄性较好),低温减压干燥(热稳立性差)
(3)萃取(分液)
1方法介绍:
当向混合物中加入有机试剂(苯、四氯化碳等)后分离的,且题目信息有涉及溶解度不同时考虑萃取。
2常见的萃取:
常见液-液萃取(如用苯或CCI4萃取水中的渙),固-液萃取(如用洒精浸取黄豆中的豆油以提髙汕产量)。
3产物的分离:
一般萃取分液后的混合溶液采取蒸餾的方式分离。
4实际应用:
海带中提取碘(灼烧、溶解、过滤、氧化、萃取、蒸饴)。
(4)反萃取
像这种将富集在四氯化碳中的碘单质利用化学转化法重新富集在水中的方法即为反萃取法。
(4)蒸慵(分懈):
题目信息有涉及沸点不同的物质时,考虑蒸馅,常见混合液体或液-l⅛l体系。
2、高考模考例题及答案:
1.(2017-全国卷III节选)重洛酸钾是一种重要的化工原料,一般由珞铁矿制备,賂铁矿的主要成分为FeOCr2O3,还含有硅、铝等杂质。
制备流程如图所示:
有关物质的溶解度如图所示。
向“滤液3"中加入适⅛KC1,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体。
冷却到(填标号)得到的K2Cr2O7固体产品最多。
a.80oCb.60oCc.40°Cd.IOoC
OOOOOOO
0^4684鞘畫Ag、一OOgH20)
步骤⑤的反应类型是__」
2.磷酸铁锂电池被广泛应用于各种电动汽车,其正极是通过将磷
酸铁锂(LiFePO4).导电剂、黏结剂和乙块黑等按比例混合.再涂于铝箔上制成。
一种从废旧磷酸铁锂电池
正极材料中回收某些金属资源的工艺流程如下:
NaOIl溶液出So4JI2O2NH3-H2O.NaOHNa2CO3
废旧磷酸
铁锂电池T碱浸正极材料
滤液1
已知:
①LbC03的溶解度:
0°C为1.54g:
IOOOC为0.72g°
“沉锂“时,所得Li2CO3应选择(填“冷水”或“热水J进行洗涤,判断SCCh已洗涤干净的操作
和现象为O
3・(201&太原模拟)髙氮酸NH4ClO4是复合火箭推进剂的重要成分,实验室可通过下列反应制取。
80cC水175*NH4Cl溶液
氯酸钠
426g
反应得到的混合溶液中NHQO4和NaCl的质量分数分别为0.30和0.15,从混合溶
NH4ClO4
液中获得较多NH4C1O4晶体的实验操作依次为(填操作名称)
.冰水洗涤.干燥。
用冰水洗涤的目的是
4・硫酸锌被广泛应用于医药领域和工农业生产。
工业上由氧化锌矿(主要成分为
4
/
T
Jai
CK
√1
\]
b
Cl
/
/
/
/
/
-J
F
Ja
N
U
Cl
2040608
80
250
60
40
20
100
温度/r
N8ΩO4S挟箕滦
ZnO.另含ZnSio3、FCCo3.CUO等)生产ZnSO4∙7H2O的一种流程如图:
稀硫酸高谥酸押锌粉
滤潼X遞潼Y谑渣Z
已知硫酸锌的溶解度与温度之间的关系如下表:
温度/°C
0
20
40
60
80
100
溶解度/g
41.8
54.1
70.4
74.8
67.2
60.5
从硫酸锌溶液中获得硫酸锌晶体的实验操作为、冷却结晶、过滤•烘干操作需在减压低温条件下进行,原因是
5.CoC12∙6H2O是一种饲料营养强化剂。
可由水钻矿[主要成分为Co2O3>CO(OH)3,还含有少⅛Fe2O3.
AI2O3.MnO等]制取,其工艺流程如下:
CoCl√6H.0
操作1(相产品i
沉淀萃取液
已知:
①流程中部分阳离子以氢氧化物形式沉淀时溶液的PH见下表・
、过滤和减压烘干:
制得的
40
20
CoC12∙6H2O在烘干时需减压烘干的原因是
以硼镁泥为原料制取MgSO4-7H2O的工艺流程如下:
MgSO4-7H:
0
沉淀物
Fe(OH)3
Fe(OH)2
CO(OH)2
AI(OH)3
Mn(OH)2
开始沉淀
2.7
7.6
7.6
4.0
7.7
完全沉淀
3.7
9.6
9.2
5.2
9.8
②CoC12∙6H2O熔点为860加热至IlO-120*C时,失去结晶水生成CoCl2.
实验操作“操作1"为
6.硼镁泥主要成分是MgO(占40%),还含有Na2B4θ7^CaO>Al2O3>Fe2O3.FC0、MnO.SKh等杂质。
本实验中多次用到抽滤操作,英装置如图,相比普通过滤,抽滤的优点是
7.某混合物A含有KAI(SO4)2.AKh和Fe2O3,在一左条件下可实现下图所示的物质之间的变化:
-IWC-OH
一!
溶液
IV
彳沉淀Dl
In
x 一瘠液一 过址U範J溶液E LIhIV四步中对于溶液和沉淀的分离釆取的方法是: 获得沉淀后,要对沉淀进行洗涤,请 简述洗涤沉淀的操作是C 8.某工厂的电镀污泥中含有铜、铁等金属化合物。 为实现资源的回收利用并有效防止环境污染,设汁如下 工艺流程: 过滤后的沉淀表而通常附着有一些杂质离子,为得到纯净产物,需要进行洗涤,确左沉淀洗涤干净的操 作及现象是O参考答案: Ld复分解反应 2•热水取最后一次洗涤液少许,向其中滴加盐酸酸化的氯化领溶液,无沉淀生成,则证明已洗净 3•蒸发浓缩冷却结晶过滤减少洗涤过程中NH4ClO4晶体的损失氨气与浓盐酸反应放出热量 4.蒸发浓缩,防止温度过高结晶水合物分解 5•蒸发浓缩: 冷却结晶: 降低烘干温度,防止产品分解: 6.加快过滤速度、得到较干燥的沉淀 7•过滤(沿玻璃棒)向漏斗中注入蒸懈水,至浸没沉淀后,待水自然流下,重复操作2-3次。 &取最后一次洗涤液,加入BaCl2溶液,如出现白色沉淀,未洗涤干净,反之洗涤干净 (四)工业流程评价问题: 1.减损增产: (1)减损: 某操作使流程中损失(浪费)减少。 如用冰水或乙醇洗涤产物,减少产物的损失。 (2)增产: 或者某操作使产品总量增加。 如提纯粗盐后,NaCl质量反而高于本来的质量。 2.髙能污染: (1)髙能: 反应中能耗过高,常见有电解,加热等操作会使得能耗变高。 ⑵污染: 流程中有污染物生成。 如NOx、Cb等。 3.原子经济: 仕)原子: 指提高原子利用率,反应物是否尽可能多的转化为生成物。 (2)经济: 指工业生产中要符合经济效益,原材料成本尽可能降低。 4.试剂循环: 反应中的副产物能够再次投入使用,达到试剂的循环。 二: 髙考模考精选例题及答案 1.(2018新课标3卷】KIOM是一种重要的无机化合物,可作为食盐中的补碘剂。 回答下列问题: 利用"KCIO=氧化法〃制备KIO3工艺流程如下图所示: MOX KCIOX H2O 滤液 KIOs也可采用“电解法〃制备,装置如图所示。 ③与”电解法嘟比,"KCIOm氧化法〃的主要不足之处有(写出_点)。 已知: (I)N2H4-H2O沸点约118°C,具有强还原性,能与NaCIO剧烈反应 生成N2o (2)步骤II合成N2H4-H2O的装置如题19图T所示。 NaClO碱性溶液与 尿素水溶液在40°C以下反应一段时间后,再迅速升温至110°C继续 反应。 「使用冷凝管的目的是 3.[2017江苏卷】(15分)某科研小组采用如下方案回收一种光盘金属层中的少量Ag(金属层中其他金属含 量过低,对实验的影响可忽略)。 15%NaCIO溶液(过童)10%氮水 预处理E的光盘碎片 NaoH滚液调PH淤液 (I)HNOs也能氧化Ag,从反应产物的角度分析,以HNO昇弋替NaeIo的缺点是4、氯化亚铜是一种重要的化工原料,广泛应用于有机合成、石油、汕脂、染料等工业。 一种利用低品位铜 矿(CU2S、CUS及FeO和Fe2O3等)为原
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 化学 工艺流程 试题 解题 思路 模型
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #全自动电容电感测试仪.docx
#全自动电容电感测试仪.docx
