 肠外营养注射液Word文件下载.docx
肠外营养注射液Word文件下载.docx
- 文档编号:20786031
- 上传时间:2023-01-25
- 格式:DOCX
- 页数:8
- 大小:19.57KB
肠外营养注射液Word文件下载.docx
《肠外营养注射液Word文件下载.docx》由会员分享,可在线阅读,更多相关《肠外营养注射液Word文件下载.docx(8页珍藏版)》请在冰豆网上搜索。
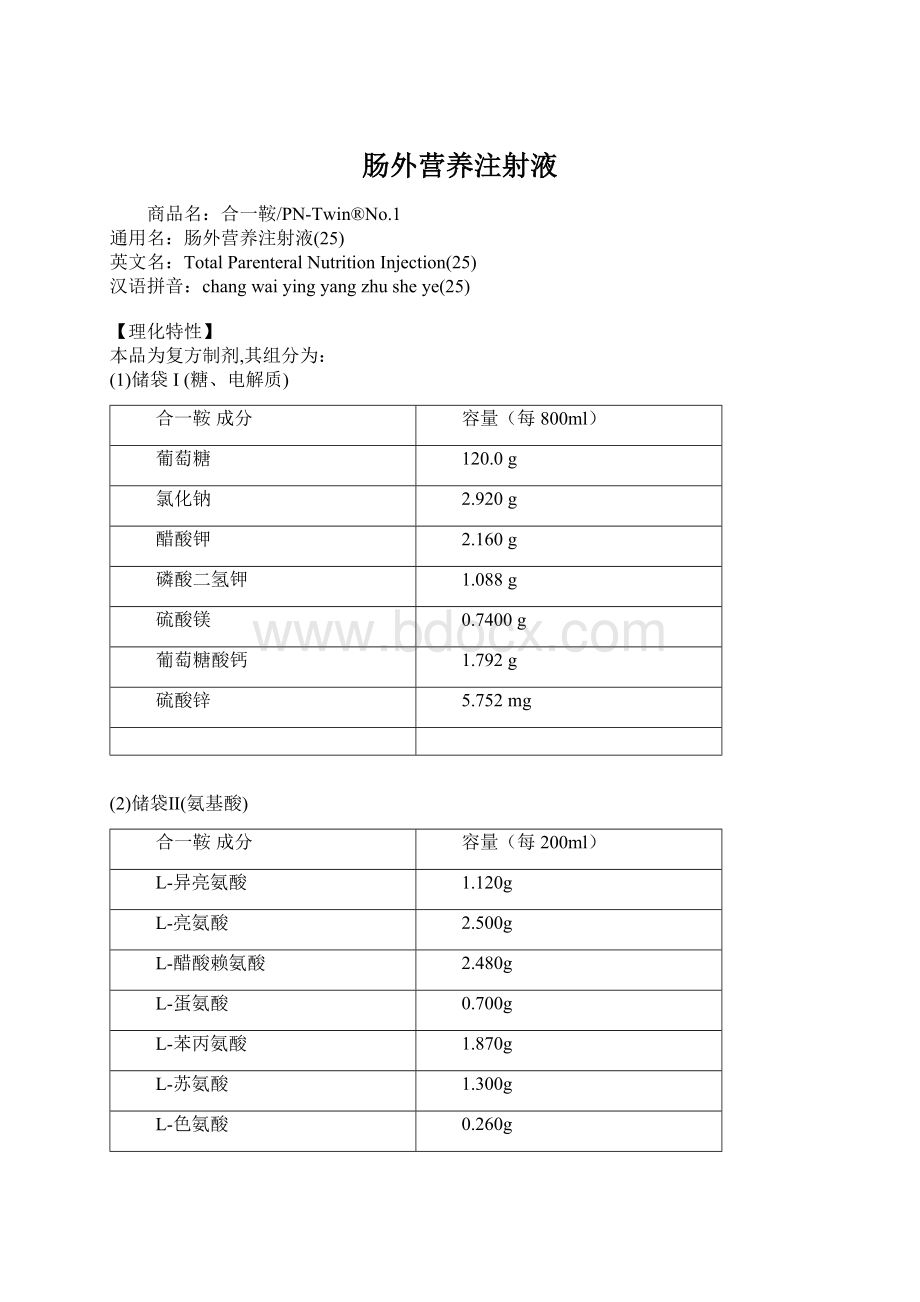
硫酸锌
5.752mg
(2)储袋Ⅱ(氨基酸)
容量(每200ml)
L-异亮氨酸
1.120g
L-亮氨酸
2.500g
L-醋酸赖氨酸
2.480g
L-蛋氨酸
0.700g
L-苯丙氨酸
1.870g
L-苏氨酸
1.300g
L-色氨酸
0.260g
L-缬氨酸
0.900g
L-丙氨酸
1.240g
L-精氨酸
1.580g
L-天冬氨酸
0.760g
L-半胱氨酸
0.200g
L-谷氨酸
L-组氨酸
1.200g
L-脯氨酸
0.660g
L-丝氨酸
0.440g
L-酪氨酸
0.070g
甘氨酸
2.140g
氨基酸浓度
10.360%
添加剂
每200mL
亚硫酸氢钠
0.030g
(3)混合后
本品
合一鞍
容积
每1000ml
糖
120.0g
葡萄糖浓度
12.00%
电
解
质
Na+★
50mEq
K+
30mEq
Mg++
6mEq
Ca+
8mEq
Cl-
SO4-
醋酸盐★★
34mEq
磷酸盐
8mmol
葡萄糖酸盐
Zn++
20μmol
总氨基酸含量
20.720g
2.072%
自由氨基酸含量
20.0g
自由氨基酸浓度
2.00%
EAA/NEAA
1.09
非蛋白热量
480kcal
总热量
560kcal
非蛋白热量/N
158
总氮
3,040mg
★含Na+稳定剂
★★含来自氨基酸的醋酸盐
性状:
(1)混合前
I
II
颜色
无色、澄明
pH
4.0~5.0
5.5~6.5
渗透压比
约4
约3
(2)混合后
约5
容器标准:
所用储袋的标准如下:
塑料容器的总体积
约1,900ml(产品体积1,000ml)
【药理作用】
合一鞍联用维生素通过中央静脉给大鼠使用后的营养效果几乎和那些口服同样剂量的卡路里制剂或服用对照营养溶液的大鼠相同。
此外,实验已证明葡萄糖、电解质和氨基酸的比率在大鼠试验中是适宜的。
【适应症】
对不能或者不能充分经口和/或经胃肠摄取营养的和那些需要静脉营养的患者,本品可作为患者补充水、电解质、氨基酸和热量的营养制剂。
【用法用量】
治疗开始时且糖耐量未知或已降低时作为初始液,或者当患者由于发病引起糖耐量下降且需要限制葡萄糖摄入时作为维持液。
使用时打开隔离层,使I和II混合制成初始液或维持液。
一般来说,成年患者通过中央静脉连续滴注24小时给予2000ml的初始液或维持液。
根据患者的年龄、症状和体重,剂量可适当增减。
肠外营养(TPN)治疗时因缺乏维生素B1可能引起严重的酸中毒,故应同时给予必需量的维生素B1(每天3mg以上)。
混合方法:
合一鞍是两储袋式产品,在塑料储袋I和II之间有隔断。
储袋I含有葡萄糖和电解质,储袋II含有氨基酸。
【药物相互作用】
药物
临床症状
机理·
风险因素
强心苷
洋地黄中毒(全身倦怠、食欲不振、恶心、头痛、呕吐、腹泻、黄视症、心率不齐),如出现上述症状,停止给药。
钙是本品的成分、可诱发强心苷类中毒,通过加强心肌作用而导致心律失常。
【不良反应】
在总的研究病例380例患者中只有1例(0.3%)出现不良反应,该不良反应可能是由葡萄糖超负荷引起的超负荷综合症。
另外,报告了17例(4.5%)并发症主要是肝功异常或由于肠外营养(TPN)治疗导致的高血糖症(在许可时)。
1.重大副作用
(1)酸中毒:
可能发生严重的酸中毒(参见[警告])
(2)高血糖症:
由于合一鞍是高浓度葡萄糖制剂,输注时有时可能出现高血糖症,高渗尿糖症和口渴。
一旦出现这种情况,需采取相应举措如使用胰岛素。
2.其他不良反应
发生率不明
0.1—小于5%
肝脏
GOT、GPT增高
血液
高钙血症
大量快速给药
脑水肿、肺水肿、外周水肿或水中毒
【禁忌】
1.高钠血症的患者(合一鞍的电解质组分可能加重高钠血症患者的症状)。
2.高氯血症的患者(合一鞍的电解质组分可能加重高氯血症患者的症状)。
3.高钾血症的患者、少尿症患者、阿迪森病患者和高氮血症的患者(症状可能由于难以从肾脏中排出钾而加重)。
4.高磷酸血症的患者或者甲状旁腺机能衰退的患者(合一鞍中的电解质成分可能加重高磷酸血症患者的症状)。
5.高镁血症患者或甲状腺机能减退的患者(合一鞍中的电解质组分可能加重高镁血症患者的症状)。
6.高钙血症的患者(合一鞍中的电解质组分可能加重高钙血症患者的症状)。
7.肝昏迷患者或者有肝昏迷可能性的患者(本品可能促使氨基酸不平衡并且可能恶化或诱发肝昏迷)。
8.严重肾功能障碍的患者(由于体内氮含量和水负荷增加,该制剂可能使肾功能进一步恶化)。
9.氨基酸代谢异常的患者(本品可能促使氨基酸不平衡)。
【药物过量】
尚不明确
【注意事项】
1.慎重给药(下列患者应慎用)
(1)菌血症患者(可能由于循环障碍导致败血症休克)。
(2)高渗性脱水患者(本品中的电解质组分可能加重脱水症状)。
(3)由肾脏疾病导致肾衰的患者(由于水和电解质调节障碍可能导致循环衰竭)。
(4)严重烧伤的患者(由于循环血量的增加可能增加心脏负荷)。
(5)肾衰不伴有高钾血症的患者(由于钠负荷引起排钾困难或由于氮负荷引起血尿素氮增高可能引起肾衰程度的进一步恶化)。
(6)心衰的患者(由于循环血量的增加可能增加心脏负荷)。
(7)由于梗阻性泌尿系疾病造成的尿量减少的患者(由于水排出障碍而加重症状)。
(8)糖尿病患者(可能诱发高血糖症)。
(9)尿崩症患者(由于过量水和电解质的输注,可能诱发水、电解质代谢紊乱)。
(10)严重酸中毒的患者(电解质组分可以加重酸中毒症状)。
(11)有胰腺功能障碍的患者如胰腺炎,胰腺硬化症和胰腺脓肿等的患者(可能导致糖耐受障碍如高血糖症等)。
2.重要的基本注意事项
(1)本品作为提供中央静脉营养,通过多种成分组合发挥有效作用的营养输注液,不能作为患者需要某种特定输注组分治疗来使用。
例如:
严重的肝功能障碍的患者。
(2)逐渐增加葡萄糖浓度,例如以较低葡萄糖浓度溶液开始,以避免引起高血糖症和尿糖的发生。
(3)停止给药的时候,要逐步降低葡萄糖浓度,例如使用低浓度葡萄糖溶液以避免出现因突然停药可能引起的低血糖症。
(4)合一鞍用作中央静脉营养开始时且糖耐量未知或已降低时的初始液,或者当糖耐量由于发病而降低和需要限制热量输入时作为中央静脉营养法的维持液。
3.使用时的注意事项:
(1)给药前
1)溶液混浊时请勿使用。
2)打开包装后立即使用,完毕后丢弃所有剩余物。
(2)给药期间
最好要求患者给药期间的排尿量达到每天不少于500m1,或每小时不少于20ml。
(3)制备方法
给药前打开隔离部分,混合溶液I和溶液II,并且立即使用。
(4)制备过程
1)不要和其他含有碳酸根离子、磷酸根离子的药品混合使用,因为这些离子可以引起沉淀。
2)建议避免直接在本品容器内混入脂肪乳。
(5)给药途径
建议避免直接滴注末梢静脉。
4.应用时的注意事项:
(1)不需要空气针。
(2)即用即开(包装),以避免溶液变色(包装内附有一氧气吸收剂以维持制剂的稳定性)。
(3)不要毁坏外包装,否则溶液会变色。
(4)如制剂变色、泄漏或在外包装上发现水滴,请不要使用。
(5)在橡胶塞上的密封膜被撕掉的情形下,制剂不能使用。
(6)仔细阅读塑胶袋上印的度量并作为标准。
(7)在橡胶塞子上"
O"
标记点上垂直插入注射针头。
如果针刺入时成角度,可能刺穿容器并引起漏液。
(8)如果两储袋之间的隔断部分已经被打开,制剂不能使用。
[警告]
肠外营养(TPN)治疗时,务必同时应用维生素B1,因为肠外营养治疗时未同时应用维生素B1可能导致严重的酸中毒(参考"
用法用量"
项)。
如果怀疑严重酸中毒是由于缺乏维生素B1而引起的,立即经静脉快速输注维生素B1制剂100~400mg。
患者在肠外营养治疗过程中,可能因为原发病和并发症引发酸中毒。
当酸中毒症状出现时应终止肠外营养治疗并给予相应治疗,如使用碱制剂。
【孕妇及哺乳期妇女用药】
1.对孕妇仅在判断治疗益处大于危险性时才能给药。
[本品对孕妇怀孕期安全性的评估尚未确立]
2.对哺乳期的妇女不要使用本制剂,如果给药不可避免,则避免哺乳。
[哺乳期妇女患者用药的安全性尚未确立]
【儿童用药】
对儿童安全性评价尚未确立(没有儿科使用经验)
【老年患者用药】
由于高龄患者的生理功能通常减退,有必要对这些患者予以特殊关照,如减小剂量或减慢给药速度。
【储藏】
室温保存
【有效期】三年
【剂型规格】
20.72g(总氨基酸)/1000ml/袋,7袋/箱
进口药品注册证号:
X20010172
【生产企业】
国内联络处:
广州市医药进出口公司
广州市沙面北街59号邮编:
510130
电话:
(020)81910162
广州绿十字药业有限公司
地址:
广州经济技术开发区蕉园路2号
(020)834862098348621182221197
传真:
(020)8348620582221868
邮编:
510730
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 营养 注射液
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
