 细胞周期的关键分子调节机制论文 1Word下载.docx
细胞周期的关键分子调节机制论文 1Word下载.docx
- 文档编号:20755541
- 上传时间:2023-01-25
- 格式:DOCX
- 页数:10
- 大小:367.63KB
细胞周期的关键分子调节机制论文 1Word下载.docx
《细胞周期的关键分子调节机制论文 1Word下载.docx》由会员分享,可在线阅读,更多相关《细胞周期的关键分子调节机制论文 1Word下载.docx(10页珍藏版)》请在冰豆网上搜索。
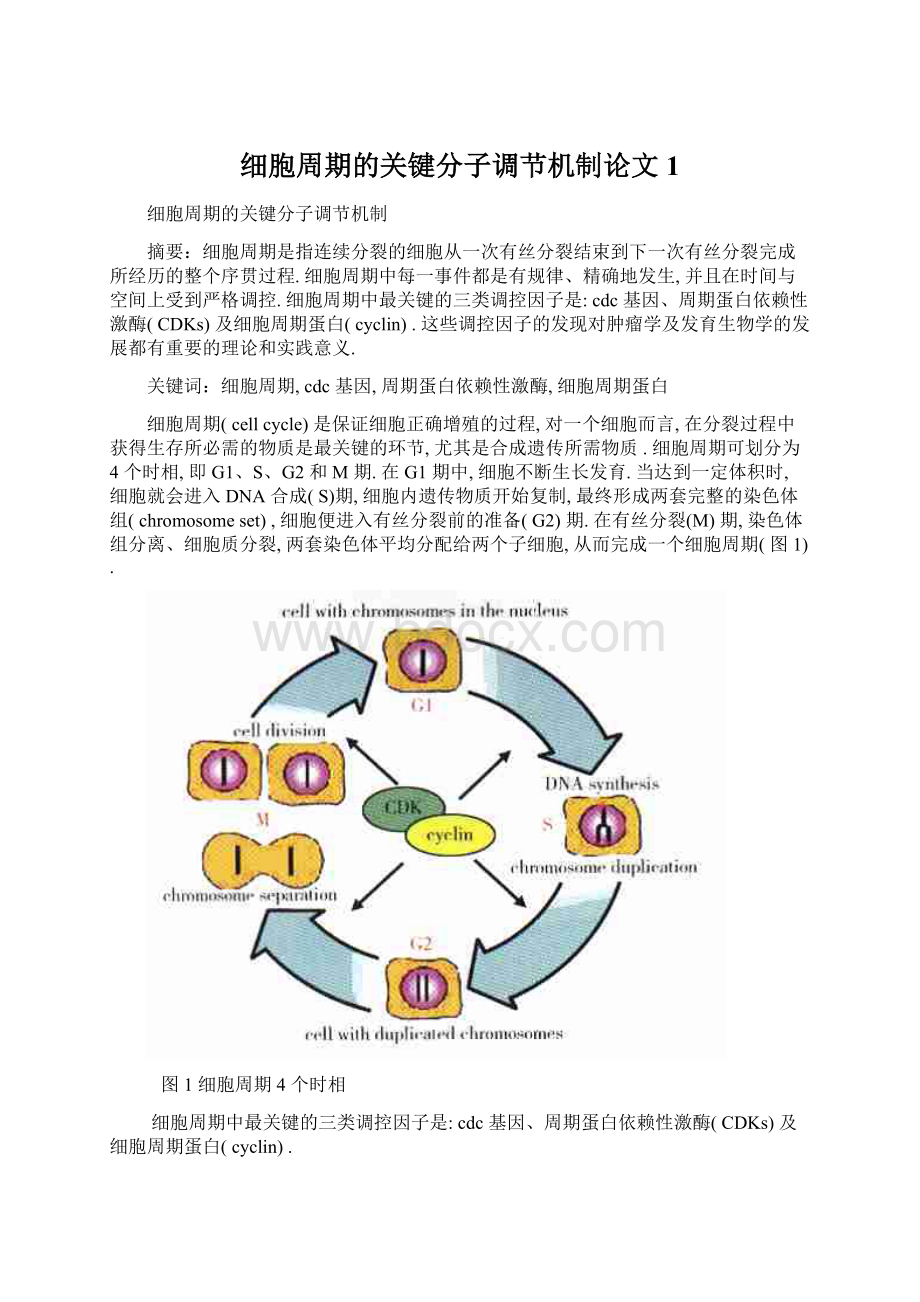
cdc3、10、11、13等调控细胞质的分裂,名为cdc28的基因,启动细胞从G1期进入S期.该基因编码的蛋白质是其他cdc基因产物执行功能的前提,所以又被称为start基因。
2.周期蛋白依赖性激酶(CDK)
2.1CDK的发现
20世纪70年代中期,纳斯采用遗传学方法和分子生物学方法,在对裂殖酵母的细胞周期进行研究时,从中发现了cdc2基因,该基因在细胞分裂调控中起着关键作用,它控制细胞从G2期进入M期.罗纳斯又发现cdc2基因还有着与start基因相同的作用,即在细胞从G1期向S期的转换进程中起调控作用。
1987年,保罗纳斯从人体中发现了细胞周期的一个关键调节物质CDK(周期蛋白依赖性激酶cyclindependentkinase),并发现CDK在控制细胞分裂(从G2期到有丝分裂期)中有关键作用,它可使其他蛋白质磷酸化,从而使细胞沿着细胞周期各时相发育,不断地分裂增殖。
CDK在进化中高度保守.
2.2CDK的功能
CDK的主要生物学作用是启动DNA的复制和诱发细胞的有丝分裂,从而驭动细胞周期,在细胞发育过程中起着非常重要的作用。
研究表明:
这种激酶的周期性激活与失活是推动细胞周期进行的主要因素。
2.3CDK激酶的激活
CDK激酶的激活作用依赖于可逆的蛋白质磷酸化作用,即通过磷酸基与靶蛋白结合来构筑这种生命体代谢过程中最基本的公共通路。
靶蛋白的磷酸化改变了靶蛋白的功能,使它处于高度活跃或完全静止的状态。
由于激酶把碑酸醋涂抹在许多不同的靶蛋白上,从而可同时改变细胞中的不同进程,将高强度的细胞分裂信号传遍细胞内部。
3.周期蛋白(cyclin)
3.1周期蛋白(cyclin)的发现
20世纪80年代早期,蒂莫西亨特采用国王海胆(Arbacia)作为实验模型,第一个发现了周期蛋白(cyclin)分子。
由于其表达水平随细胞周期而剧烈起伏,而被命名为周期蛋白.该蛋白在细胞周期中周期性地生成,然后降解。
3.2周期蛋白(cyclin)的功能
周期蛋白(cyclin)与CDK分子结合,从而对CDK的活性进行调控,选择性地将磷酸基团连接在某些蛋白质分子上。
周期蛋白的周期性降解,是细胞周期调控的一个重要机制。
不同的cyclin分别在某一个细胞周期时相表达,又在另一个时相降解,这种性质是细胞周期调控的一种独特现象.cyclin这种独特的性质被亨特察觉,通过进一步研究,他发现细胞周期的运转必需有cyclin的参与,cyclin缺陷型细胞停滞在G1或G2期,无法进行有丝分裂.
4.细胞周期调控的分子机制
在多细胞真核生物中,参与细胞周期调控的核心蛋白分子主要分为3大类,分别是:
周期蛋白依赖性激酶(CDK)、周期蛋白(Cyclin)及“细胞周期蛋白依赖性激酶抑制因子”(Cdkinhibitor,CKI)。
其中,Cdk是细胞周期调节的中心环节,Cyclin是Cdk的正调节因子,CKI是Cdk的抑制因子。
4.1细胞周期的驱动和调控机制
作为“细胞周期发动机”,Cdk在细胞周期的调节中起关键作用。
各种Cdk在细胞周期的各个特定时问被激活,通过磷酸化底物,驱使细胞完成细胞周期。
这就是细胞周期的驱动机制。
(图3)
图3S期起始调控的分子机制示意图
4.2在整个细胞周期过程中,细胞内各种Cdk的含,即活化的Cdk与非活化的Cdk的总量不变,改变的只是它们之间的比例。
这个比例的改变主要受三方面的调节:
(1)Cdk只有通过与特定的Cyclin形成二聚复合物才能发挥作用
(2)Cdk的激活还需要在其保守的苏氨酸和酪氨酸残基上发生磷酸化
(3)Cdk的活性可被Cdk抑制蛋白(CKI)抑制
4.2.1Cdk只有通过与特定的Cyclin形成二聚复合物才能发挥作用
目前,在高等真核细胞中Cyclin主要包括8个成员(A~H),它们在细胞周期的不同时相,结合不同的Cdk发挥不同的作用。
根据Cyclin发挥作用时相的不同,通常将其分为四类:
G一Cyclin、G/S—Cyclin、S-Cyclin和M—Cyclin.
图4各种cyclin-cdk复合物作用的细胞周期时相
在结构上,所有的Cyclin分子均有一个相对保守区域,称为细胞周期蛋白盒(Cyclinbox),其主要功能是与Cdk结合而改变Cdk的蛋白质构象,激活Cdk的蛋白激酶活性,具有激酶活性的Cdk使周期蛋白特定的氨基酸残基磷酸化,使后者的三维构象发生变化,从而引起一系列的链式反应,调控细胞周期进程.
4.2.2Cdk的激活还需要在其保守的苏氨酸和酪氨酸残基上发生磷酸化
这个磷酸化是由Cdk激活激酶(Cdk—activa—tingkinase,CAK,即Cdk7/CyclinH)完成的。
CAK可以磷酸化Cdkl的Thr一161位点,使其活化,改变Cdk的分子构象,促进Cdk与Cyclin结合,所以促进了细胞周期的进程.
4.2.3Cdk的活性可被Cdk抑制蛋白(CKI)抑制
CKI通过直接结合Cdk,或与Cdk—Cyclin复合体作用,抑制Cdk的作用,调节细胞周期。
目前,将CK1分为两大家族
⒈具有广泛抑制Cdk作用的“Cdk抑制蛋白/激酶抑制蛋白”家族
⒉具有特异性抑制作用的“Cdk4抑制因子”
因此,正常的细胞周期需要Cdk的正调节因子Cyclin与负调节因子CKI的精确协同与平衡,一旦这种平衡失稳就会造成细胞的失控性增殖,发生癌变。
4.3细胞周期的监控机制——“检验点”机制
细胞周期是高度有组织和精确的时序调控过程,它严格地沿着G一S—G一M的顺序循环运转,为保证这一过程的正常进行,细胞形成一套检验细胞周期中DNA合成和染色体分配的机制,即“细胞周期检测点”。
这些监测机制可以检测到DNA结构的受损或复制不全,还能检测到细胞分裂过程中所需的蛋白复合物的缺失。
在酵母细胞中,当发生影响细胞周期正常运行的事件时,检测点相关的信号转导通路将被激活,它们可以使Cdc2p酪氨酸残基持续的磷酸化而抑制Cdk的活化,从而阻止有丝分裂期的发生;
或通过其它机制在有丝分裂期的较晚时期阻断细胞周期的继续进行。
在哺乳动物细胞中,当DNA损伤时,还可通过p53基因的作用将细胞周期阻断于s期。
阻断细胞周期的进行后,“检测点”机制采取诱导基因转录、促进DNA的修复等有效的补救措施以排除故障。
当故障排除后,细胞周期才能恢复运转。
当损伤过大,细胞无法修复时,检测点将启动细胞凋亡程序以清除那些带有病变倾向的细胞,减少对机体的危害。
目前为止可以将所发现的细胞周期检测点分为三种:
⒈DNA损伤检测点,它包括两个关键性检测点:
G/S转换点和G/M转换点
⒉DNA复制检测点,其在s期中负责DNA复制的进度
⒊纺锤体组装检测点,其在分裂期起作用,检测纺锤体有无组装、染色体是否正确排列并与纺锤体连接,以及染色体是否正确分配等
这些检测机制保证了DNA在分子水平上的精确复制及在细胞水平上的精确分离
检测点对细胞周期进程进行严格的监督,使DNA复制和有丝分裂准确无误地进行,保证遗传的稳定性。
它们的缺失将导致细胞在没有正确完成前一时相就进入下一时相,细胞将出现严重的遗传性损伤甚至癌变,最终导致机体死亡。
5.现状前景及仍存在的问题
5.1现状前景
细胞周期调控的分子机制的揭示,将有助于人们理解肿瘤细胞中染色体是如何进行重排、丢失或不均等地分配到子代细胞中,从而使人们有可能更好地对肿瘤进行预防、诊断及治疗。
5.2仍存在的问题
细胞增殖,尤其是它的调控机制仍远未彻底阐明,譬如:
参与周期调控的基因绝非仅此几个,它们在促进或是阻止周期进行中究竟起何作用,它们与START、CDK有何关系,高等动物细胞与酵母的周期调控有何差别等问题,都值得人们进一步思索与探讨。
参考文献
1NurseP.Regulationoftheeukaryoticcellcycle.EuropeanJCancer,1997,33(7):
1002~1004
2BartlettR,NurseP.YeastasamodelsystemforunderstandingthecontrolofDNAreplicationineukaryotes.Bioessays,1990,12(10):
457~463
3HartwellLH.Macromoleculesynthesisintemperature2sensitivemutantsofyeast.JBacteriology,1967,93(5):
1662~1670
4HartwellLH.Celldivisionfromageneticperspective.JCellBiol,1978,77:
627~637
5HartwellLH.GeneticcontrolofthecelldivisioncycleinyeastÒ
:
genescontrollingDNAreplicationanditsinitiation.JMolBiol,1971,59:
183~194
6ReidBJ,HartwellLH.RegulationofmatinginthecellcycleofSaccharymycescerevisiae.JCellBiol,1977,75:
355~365
7EvansT,RosenthalET,HuntT,etal.Cyclin:
aproteinspecifiedbymaternalmRNAinseaurchineggsthatisdestroyedateachcleavagedivision.Cell,1983,33:
389~396
8HuntT,LucaFC,RudermanJV.Therequirementsforproteinsynthesisanddegradation,andthecontiolofdestructionofcyclinsAandBinthemeioticandmitoticcellcyclesoftheclamembryo.JCellBiol,1992,116(3):
707~724
9HartwellLH,CulottiJ,PringleJR,etal.Geneticcontrolofthecelldivisioncycleinyeast.Science,1974,183:
46~51
10HuntT.Cyclinsandtheirpartners:
fromasimpleideatocomplicatedreality.SeminCellBiol,1991,2(4):
213~222
11BandaraLR,AdamczewskiJP,HuntT,etal.CyclinAandtheretinoblastomageneproductcomplexwithacommontransctiptionfactor.Nature,1991,352(6332):
249~251
12NurseP,ThuriauxP.RegulatorygenescontrollingmitosisinthefissionyeastSchizosacchharomycespombe.Genetics,1980,96(3):
13SimanisV,HaylesJ,NurseP.ControlovertheonsetofDNAsynthesisinfissionyeast.PhilosTransRSocLondBBiolSci,1987,317(1187):
507~516
14NurseP.UniversalcontrolmechanismregulatingonsetofM2phase.Nature,1990,344(6266):
503~508
15SimanisV,NurseP.Thecellcyclecontrolgenecdc2+offissionyeastencodesaproteinkinasepotentiallyregulatedbyphosphorylation.Cell,1986,45
(2):
261~268
16LiA,BlowJJ.TheoriginofCDKregulation.NatureCellBiology,2001,3:
182~184
17GouldKL,NurseP.Tyrosinephosphorylationofthefissionyeastcdc2+proteinkinaseregulatesentryintomitosis.Nature,1989,342(6245):
14~15
18FelixMA,LabbeJC,DorseM,etal.Triggeringofcyclindegradationininterphaseextractsofamphibianeggsbycdc2kinase.Nature,1990,346(6282):
379~382
19HartwellLH,TedA.WeinertChekpoints:
Controlsthatensuretheorderofcellcycleevents.Science,1989,246:
629~633
20PaulovichAG,HartwellLH.AcheckpointregulatestherateofprogressionthroughSphasetoDNAdamage.Cell,1995,82:
841~847
21PaulovichAG,ArmourCD,HartwellLH.ThesaccharomycescerevisiaeRAD9,RAD17,RAD24andMEC3genesarerequired
fortoleratingirreparable,ultraviolet2inducedDNAdamage.Genetics,1998,150
(1):
75~93
22DpUrsoG,GrallertB,NurseP.DNApolymerasealpha,acomponentofthereplicationinitiationcomplex,isessentialforthecheckpointcouplingStomitosisinfissionyeast.JCellSci,1995,108:
3109~3118
23HartwellLH,SzankasiP,RobertCJ,etal.Integratinggeneticapproachesintothediscoveryofanticancerdrugs.Science,1997,278(5340):
1064~1068
24ZhangP.Thecellcycleanddevelopment:
redundantrolesofcycleregulators.CurrentOpioninCellBiology,1999,11:
655~662
25 齐云.发现调控细胞循环周期的神秘物质.世界科学,2001,11:
7—8.
26颜亮,陈勇.生理学或医学奖:
加深对生命基本过程的理解.大众科技报,2001—10—14(5).
27 刘元亮,姚慧华,冠世琪等.科学认识论和方法论.北京:
清华大学出版社,1987.
28 陈衡.科学研究的方法论.北京:
科学出版社,1982.
29 郝水.细胞如何调控基因组的有序活动.李喜先.21世纪100个科学难题.长春:
吉林人民出版社,1999,607—614.
30 蔡如鹏.细胞“引擎”驱动癌症研究.科学时报,2001,(6):
10—16.
31 申景平,卢圣栋.癌症的靶向性基因治疗.世界科学,2000,1:
31.
32 DanFerber,李伟.与癌症治疗副作用抗衡的新疗法.世界科学,2000,1:
33刘擎,余龙.酵母:
一种模式生物.生命的化学,2000;
20
(2):
61
34赵炬才,张广泉.细胞周期调控与骨肉瘤.中华骨科杂志,2000;
20:
44246
35吴家睿.检查点:
细胞周期的质量监督.生命的化学,1999;
5:
1992202
36SerranoM.,HannonG.J.,BeachD.,etal.AnewregulatorymotifincellcyclecontrolcausingspecificinhibitionofcyclinDPCDK4.Nature,1993;
366(16):
704
37KondoT.,etal.Mol.Cell.Biol.,1999;
19:
1136
38ShimomuraT.,etal.Mol.Cell.Biol.,1998;
18:
5485
39NavasT.A.,etal.GenesDev.,1996;
10:
2632
40SugimotoK.,etal.Mol.Cell.Biol.,1997;
17:
5905
41HartwellL.H.,KastanM.B.Cellcyclecontrolandcancer.Science,1994;
266:
182121828
42NoboriT.,MiuraK.,WuD.J.,etal.Deletionsofthecyclindependentkinase4inhibitorgeneinmultiplehumancancers.Nature,1993;
368:
753
43HunterT.,PinesJ.CyclinsandcancerÒ
cyclinDandCDKinhibitorscomeofage.Cell,1994;
79:
5732582
44赵晓荣,顾焕华,翁新宪等.细胞周期蛋白(cyclin)D在鼻咽癌中的表达及功能初步分析.生物化学与生物物理学报,2000;
32
(2):
1922196
45OhtsuboM.,ThoedorasA.M.,SchumacherJ.,etal.HumancyclinE.,anuclearproteinessentialfortheG12to2Sphasetransition.Mol.Cell.Biol.,1995;
15:
261222624
46GirardF.,StrausfeldU.,FernandezA.,etal.CyclinAisrequiredfortheonsetofDNAreplicationinmammalianfibroblasts.Cell,1991;
67:
116921179
47HarrisH.TheBirthoftheCel1.NewHaven:
YaleUniversi—tyPress,1999.
48NurseP.Alongtwentiethcenturyofthecellcycleandbe—yo
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 细胞周期的关键分子调节机制论文 细胞周期 关键 分子 调节 机制 论文
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
![ISO-8501[1].1-2007-涂装表面清洁度的目视评定-(中文译本).doc](/Images/s.gif)