 最新初三化学化学科普阅读题题20套带答案Word格式.docx
最新初三化学化学科普阅读题题20套带答案Word格式.docx
- 文档编号:20488010
- 上传时间:2023-01-23
- 格式:DOCX
- 页数:17
- 大小:255.39KB
最新初三化学化学科普阅读题题20套带答案Word格式.docx
《最新初三化学化学科普阅读题题20套带答案Word格式.docx》由会员分享,可在线阅读,更多相关《最新初三化学化学科普阅读题题20套带答案Word格式.docx(17页珍藏版)》请在冰豆网上搜索。
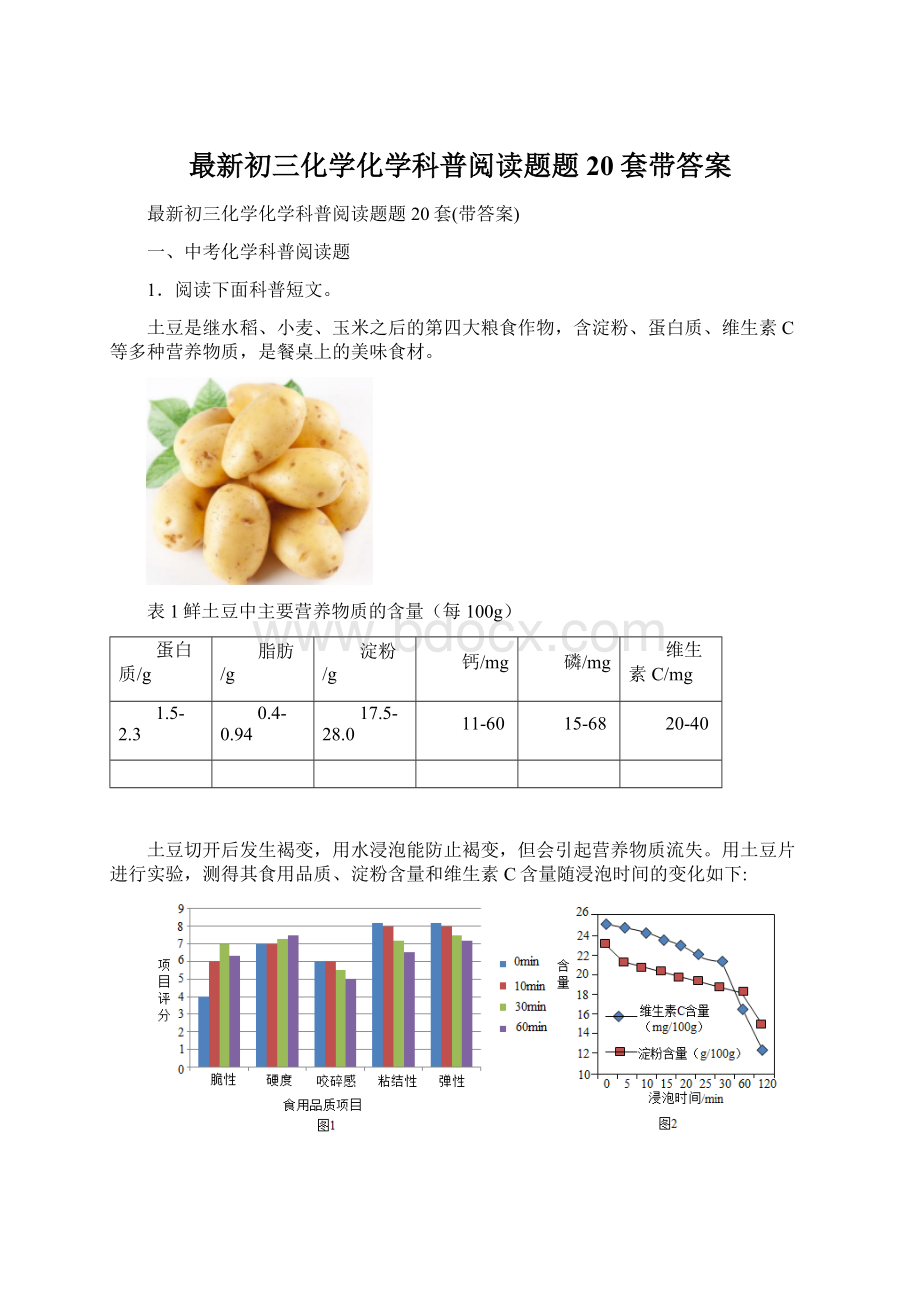
土豆片的淀粉含量与浸泡时间的关系是_______________________。
(4)変绿、发芽的土豆不宜食用,其原因是___________________________________。
(5)下列说法正确的是_____________。
A土豆是四大粮食作物之一B土豆中维生素C含量最高
C用水泡可防止土豆片褐変D土豆开发应用的前景广阔
【答案】元素ABC在其他条件相同时,在研究范围内,土豆片的淀粉含量随浸泡时间的延长而降低土豆变绿、发芽时,龙葵素含量显著增高,而龙葵素多食可导致中毒ACD
【解析】
【分析】
【详解】
(1)一般情况下,没有特别说明,表1中“钙”、“磷”是指元素,故此空填写:
元素;
(2)A、由图1可知:
60min内,浸泡30min比10min脆性分值高,故符合题意;
B、浸泡10min,硬度、咬碎感跟0min比,均无明显变化,故符合题意;
C、由图1可知:
60min内,随着浸泡时间的增加,粘结性、弹性分值均降低,故符合题意。
(3)由图2可知,随横坐标数值的增加,曲线的纵坐标在逐渐减少,故填写:
在其他条件相同时,在研究范围内,土豆片的淀粉含量随浸泡时间的延长而降低;
(4)由题干文字可知,変绿、发芽的土豆不宜食用,其原因是土豆变绿、发芽时,龙葵素含量显著增高,而龙葵素多食可导致中毒;
(5)A、由题干文字可知,土豆是四大粮食作物之一,故符合题意;
B、由表1可知,土豆中维生素C含量不是最高,“磷”和“钙”的含量有可能比它高,故不符合题意;
C、由题干文字可知,用水泡可防止土豆片褐変,故符合题意;
D、由题干文字可知,土豆开发应用的前景广阔,故符合题意。
2.阅读下面材料,回答问题:
炼草成油不是梦
化石能源的大量使用会产生大量CO2,同时产生一些有污染的烟气,威胁全球生态。
为了有效改善生态,有的国家利用富含纤维素的草本植物、可食用作物(包括玉米、大豆、甘蔗)为原料,制造草油。
用可食用作物制造生物燃料是最简单可行的,但是并非长久之计,因为没有足够的耕地来满足发达国家对液态燃油的需求。
其实,可转化为草油的原料有很多,从木材废料到农业废弃物,再到“能源生物”,这些原料耕作成本低、产量大。
这些植物都能够在农田的边际土地上快速生长,它们的种植不会干扰和危及粮食作物的生长。
放眼全球,每年可利用上述物质能转化的生物燃料相当于340亿~1600亿桶原油,已超过全球每年30亿桶原油的消耗量。
纤维素类草本植物能转化成任何类型的燃料,如乙醇、普通汽油、柴油甚至航空燃油。
在2011年,第一个商业化生物燃料炼制厂已建成。
人类历史上的能源新纪元﹣﹣﹣﹣﹣草油时代就要到来。
(1)开发清洁可再生的能源是当今能源发展方向,其原因是_____(写一条)。
(2)生物燃料的能量来源于自然界中的_____能。
(3)纤维素类草本植物能转化为乙醇,乙醇属于_____(填“可再生”或“不可再生”)能源,其燃烧的化学方程式为_____。
(4)“草油的大量使用可缓解温室效应”的说法是错误的,原因是_____(写一条)。
(5)推动草油业的发展,可提高周边农户的收入,给出你的建议_____(写一条)。
【答案】化石能源不可再生且燃烧时会产生大量的二氧化碳等温室气体太阳可再生C2H5OH+3O2
2CO2+3H2O草油燃烧也会产生二氧化碳在农田的边际土地上多种植能制作草油的作物
(1)化石能源不可再生且燃烧时会产生大量的二氧化碳等温室气体,所以开发清洁可再生的能源是当今能源发展方向。
(2)生物燃料的能量来源于自然界中的太阳能。
(3)纤维素类草本植物能转化为乙醇,乙醇属于可再生能源,其燃烧生成二氧化碳和水,化学方程式为:
C2H5OH+3O2
2CO2+3H2O。
(4)草油中含有碳元素,草油燃烧也会产生二氧化碳,所以“草油的大量使用可缓解温室效应”的说法是错误的。
(5)在农田的边际土地上多种植能制作草油的作物,推动草油业的发展,可提高周边农户的收入。
3.2016年1月29日《科技日报》报道:
科学家首次将从空气捕获的二氧化碳用氢气将其转化为甲醇,同时有水生成。
该研究即可除去大气中的温室气体二氧化碳,生成的甲醇还能作为汽油的替代燃料。
二氧化碳转化成甲醇的过程中,一个关键的因素是找到合适的均相催化剂。
此次研究人员开发出在高温下不会分解的金属钌催化剂,稳定性好,可重复使用。
(1)图1是科学家正在研究的二氧化碳循环利用技术:
①二氧化碳与氢气在催化剂、高温条件下,除生成甲醇(CH4O)外,还生成一种常温下为液态的化合物,写出反应的化学方程式_____,甲醇中碳元素的化合价为_____。
②从图中分析得出的下列结论中,正确的是_____。
(填序号)
A该技术符合低碳经济的理念
B水生成氢气的过程中所用的催化剂一定是二氧化碳
C该技术有助于缓解全球面临的能源危机
D液化石油气、汽油、甲醇均由碳、氢、氧三种元素组成
(2)在加油站贴有“严禁烟火”的标志的原因是_____,试从微观角度解释:
_____。
(3)二氧化碳转化成甲醇的微观示意图,如图2所示。
①该反应生成物中的化合物有_____种,其中属于氧化物的是_____(写出化学式)。
②请写出甲醇完全燃烧的化学方程式_____。
③下列关于催化剂的说法正确的是_____。
(用序号作答)
a.能改变化学反应的速率,自身的质量不变;
b.反应过程中,自身的性质不变;
c.反应过程中,自身的化学性质不变;
d.能加快化学反应的速率,自身的质量不变。
【答案】3H2+CO2
CH3OH+H2O﹣2AC可燃性的气体与空气的混合物在点燃时易发生爆炸分子在不断运动2H2O2CH3OH+3O2
2CO2+4H2Oac
二氧化碳和氢气在复合催化剂催化作用下生成甲醇和水,组成化合物中元素正负化合价的代数和为零,甲醇和氧气在点燃生成水和二氧化碳。
(1)①二氧化碳和氢气在复合催化剂催化作用下生成甲醇(CH3OH)和水,化学方程式为
,设甲醇中碳元素的化合价为x,则
。
②A、二氧化碳循环利用,符合低碳经济的理念,故A正确;
B、水生成氢气的过程中所用的催化剂不一定是二氧化碳,故B不正确;
C、二氧化碳循环利用,该技术有助于缓解全球面临的能源危机,故C正确;
D、液化石油气和汽油主要是碳氢类化合物、甲醇中共有碳、氢、氧三种元素,故D不正确。
故选AC。
(2)可燃性的气体与空气的混合物在点燃时易发生爆炸,所以在加油站贴有“严禁烟火”的标志,从微观角度解释是分子在不断运动。
(3)①化合物是由多种元素组成的纯净物,氧化物是由两种元素组成的纯净物,其中一种是氧元素的化合物,所以该反应生成物中的化合物有2种,其中属于氧化物的是H2O。
②甲醇和氧气在点燃的条件下生成水和二氧化碳,化学方程式为
③a、催化剂能改变化学反应的速率,自身的质量不变,故a正确;
b、反应过程中,催化剂自身的化学性质不变,故b不正确;
c、反应过程中,催化剂自身的化学性质不变,故c正确;
d、催化剂能改变化学反应的速率,自身的质量不变,故d不正确。
故选ac。
【点睛】
催化剂在化学反应中,只能改变化学反应速率,自身的化学性质反应前后不变。
4.阅读下面科普短文然后回答问题。
氢能源汽车
氢能汽车是以氢气为主要能量的汽车。
一般的内燃机,通常注入柴油或汽油。
氢能汽年有许多优点,首先是干净卫生,氮气燃烧府的产物是水,不会污染环境;
其次是氮气在燃烧时比汽油的发热量高。
近年来,国际上以氨为燃料的“燃科电池受动机”技术取得重大突破,而“燃料电池汽车”已成为推动“氮经济”的发动机,
氢气可以通过电解水、水煤气转化等方法大量制取,而且不需要对汽车发动机进行大的改装,因此氢能汽车具有广阔的应用前示,推广氢能汽车需要解决三个技术问题:
大量制取廉价氯气的方法;
解决氢气的安全储运问题:
解决汽车所常的高性能、廉价的氧供给系统。
随着储氢材料的研究进展,科学家们研制的高效率氮燃料电池,减小了氢气损失和热量散失。
我国在氢能汽车研发领域取得重大突破。
据国内媒体报道,现代FE氢燃料电池车亮相2017广州车展,该车采用了第四代氢燃料电池技术,内部有三个同尺寸的储氢罐组成,实现了世界最高的氢气存储密度,最大续航能力可达800公里。
(1)汽油、柴油是_________炼制的产品。
(填一种化石燃料)
(2)氢气燃烧的化学方程式是________。
(3)氢燃料电池车的优点是_______________。
(答出一点即可)
(4)2017年广州车展的现代FE氢燃料电池车还具有以下特殊的性能____________。
(5)你认为氢能汽车具有广阔的应用前景的依据是____________。
(6)下列说法正确的是_______。
A.目前,通过电解水获取的氢气价格昂贵
B.氢能汽车行驶时可将机械能转变为化学能
C.我国在氢能源汽车的研究领域已取得重大突破
D.以汽油为燃料的汽车行驶时可向空气中排放有毒气体和烟尘
【答案】石油
干净卫生,氢气燃烧后的产物是水,不会污染环境;
氢气在燃烧时比汽油的发热量高;
(答出一点即可)世界最高的氢气存储密度,最大续航能力可达800公里氢气可以通过电解水、水煤气转化等方法大量制取,而且不需要对汽车发动机进行大的改装ACD
(1)汽油、柴油是石油炼制的产品;
(2)氢气与氧气在点燃的条件下反应生成水;
(3)氢燃料电池车的优点是:
干净卫生,氢气燃烧产物是水,不污染环境,氢气在燃烧时比汽油的发热量高;
(4)2007年广州车展的现代FE氢燃料电池车还具有以下特殊的性能:
最高的氢气储存密度,最大续航能力可达800公里;
(5)氢气可以通过电解水、水煤气转化等方面大量制取,而且不需要对汽车发动机进行大的改装,所以氢能汽车具有广阔的应用前景;
(6)A、目前通过电解水获得氢能,成本高、效率低,应寻找合适的催化剂,故正确。
B、氢能汽车行驶时可将化学能转化为机械能,故错误;
C、我国在氢能源汽车的研究领域已取得重大突破,故正确;
D、汽油燃烧能产生有毒气体和烟尘,所以以汽油为燃料的汽车行驶时可向空气中排放有毒气体和烟尘,故正确。
故填:
ACD。
5.“嫦娥一号”的成功发射,使全国人民欢欣鼓舞.请同学们阅读下列航天技术中的化学短文并回答有关问题.
材料一:
2007年10月24日19时10分,“嫦娥一号”卫星发射成功.下图是中国月球探测工程标志图案.它以中国书法,抽象地勾勒出一轮圆月,一双脚印踏在其上,象征着月球探测的终极梦想.整体图形由一弧两点巧妙形成古文“月”字,同时代表“绕”、“落”、“回”三步走战略,此作品中国的意味十足,简洁而明朗,体现了传统和现代的完美结合.
材料二:
人类要在月球活居住,首先离不开淡水和氧气,而月球上既没有水又没有空气.科学家发现月球的沙土中含有丰富的含氧钛铁矿,成分为TiO2、Fe2O3的混合物,将这些矿石利用CO来还原提炼单质钛和铁,若用氢气还原,可以得到淡水.将这些矿石通电,还可以从中分离出氧气.
请你从化学视角来见证这一伟大时刻:
(1)据了解,发射前8h开始加注火箭第三级使用的燃料液氢和液氧.其中液氧的主要作用是________,液氢的主要作用是________,液氢的使用大大减轻了发射的质量,其原因主要是________.写出液氢燃烧方程式________.
(2)从铁生锈条件来分析,月球上铁制品________(填“易”或“不易”)生锈,原因是:
________.
(3)现利用CO来还原TiO2、Fe2O3的混合物提炼单质钛和铁,装置如图所示,试回答:
①写出A中CO还原TiO2的化学方程式________.
②就实验操作顺序的问题两位同学出现了分歧.小月认为先通一段时间CO排空,然后再点燃C和A中的酒精灯.小亮认为这样做不好,他的理由是________.小亮认为先点燃C和A中的酒精灯,然后再通CO,小月又提出反对,她的理由是________.老师认为他们的反对意见都有一定道理.请你帮助这两位同学解决他们的困难,你的办法是________________.
(4)小勇同学进一步探究钛铁矿中Fe2O3的质量分数,取10g钛铁矿样品进行实验,待完全反应后,用磁铁吸引铁粉,并称得铁粉的质量为5.6g,试求算钛铁矿中Fe2O3的质量分数为多少________?
【答案】助燃作燃料密度小2H2+O2
2H2O不易月球上既没有水又没有空气2CO+TiO2
Ti+2CO2CO有毒,对空气有污染CO与容器内空气混合,点燃后可能会发生爆炸先通一段时间CO,同时点燃C处的酒精灯,排尽玻璃管内空气,然后再点燃A处的酒精灯(或先用气球收集尾气,然后再点燃酒精灯)80%
(1)氧气具有助燃性,火箭中的液氧起助燃作用,液氢是燃料;
氢气的密度小,质量轻,氢的使用大大减轻了发射的质量;
液氢与氧气在点燃的条件下反应生成水,反应方程式为2H2+O2
2H2O。
(2)月球上没有氧气和水,故不易生锈。
(3)①CO与TiO2在高温的条件下反应生成钛和二氧化碳,反应方程式为2CO+TiO2
Ti+2CO2;
②一氧化碳是有毒的气体,直接排放在空气中会造成空气污染;
A装置中应该先通入一段时间的一氧化碳在点燃酒精灯,防止一氧化碳的燃烧而引起爆炸;
为了防止一氧化碳污染空气和A装置中爆炸,应该先通一段时间CO,同时点燃C处的酒精灯,排尽玻璃管内空气,然后再点燃A处的酒精灯(或先用气球收集尾气,然后再点燃酒精灯)。
(4)设样品中氧化铁的质量为x
x=8g
钛铁矿中Fe2O3的质量分数为
×
100%=80%
答:
钛铁矿中Fe2O3的质量分数为80%。
6.阅读下面科普短文。
钠是一种活泼金属,其原子的结构示意图为
钠在空气中极易被氧化,用小刀一切,就能观察到它的本来面目:
银白色有金属光泽。
钠还能与水反应,生成氢氧化钠和氢气。
目前,世界上多数采用电解熔融氯化钠的方法来制得金属钠。
氯化钠的熔点为801℃,将氯化钠和氯化钙按质量比2:
3混合共熔,可得到熔融温度约为580℃的共熔物,降低了电解所需的温度。
电解时,正极放出氯气,负极产生的金属钠和金属钙同时浮在共熔物,从管道溢出。
把熔融的金属混合物冷却到105~110℃,金属钙结晶析出,通过过滤可以分离出金属钠。
金属钠的应用非常广泛,可以用于制造过氧化钠(Na2O2)等化合物。
还能用于生产更加昂贵的金属钾,以钠和氯化钾为原料,在高温条件下,生成钾和氯化钠,生成的钾能以蒸汽的形式分离出来。
依据文章内容,回答下列问题:
(1)在钠的原子结构中,与钠元素化学性质密切相关的是__________。
(2)钠具有的物理性质有__________。
(3)金属钠通常保存在石蜡油中,目的是隔绝__________。
(4)钠能与水反应,化学方程式为__________。
(5)写出用钠制取钾的化学方程式__________。
【答案】
(1)最外层电子
(2)银白色固体(有金属光泽、质地软)
(3)隔绝水和氧气
(4)2Na+2H2O2NaOH+H2↑
(5)Na+KCl
NaCl+K↑
试题分析:
(1)最外层电子数决定元素化学性质;
(2)钠的物理性质有:
有金属光泽,银白色;
(3)金属钠通常保存在石蜡油中,目的是隔绝水和氧气;
(4)根据题目信息可知,钠与水反应,生成氢氧化钠和氢气;
(5)钠与氯化钾在高温条件下生成氯化钠和钾。
考点:
元素化学性质,物质性质,灭火原理。
7.阅读下面科普短文。
巧克力是极具营养价值的食品,某巧克力部分营养成分见下表。
可可豆是制作巧克力的主原料,含水、单宁、可可脂等物质。
制作巧克力时,可可豆发酵过程中减少了单宁的含量,从而降低了可可的苦味,同时生成二氧化碳、醋酸等物质。
再通过精炼,让巧克力拥有滑顺的口感,通过去酸使巧克力透出清香,回火铸型后得到成型的巧克力。
可可脂是一种主要由三种脂肪酸构成的脂肪,熔点在34~36℃,恰好低于口腔温度,但高于体表(手掌)温度。
几种固体脂的融化曲线如图所示。
某巧克力的营养成分
项目每100g
热量520kJ
糖类59.5g脂肪31.93g蛋白质5.78g
钠48mg
钾331mg
巧克力含有丰富的多源苯酚复合物,是防止心脏病的天然卫士。
巧克力中的糖分还能起到缓解压力,消除抑郁情绪的作用。
巧克力由于可可脂的特性,在夏天,表面会形成白色晶状物,类似白霜,影响观感,并不影响巧克力的质量,可放心食用。
(1)由表可知该巧克力中含量最高的营养素是_______________。
(2)可可豆发酵的过程属于_________(填“物理”或“化学”)变化。
(3)根据图可知,10℃时固体脂指数最小的是__________。
(4)解释巧克力“只融在口,不融在手”这句广告词中蕴含的科学原理________。
(5)下列说法正确的是_________。
A心脏病患者可适当食用巧克力
B巧克力中因含有单宁等物质使其略带苦味
C巧克力在口中能瞬间融化是因为其固体脂指数随温度变化大
【答案】糖类化学奶油可可脂是一种主要由三种脂肪酸构成的脂肪,熔点在34~36℃,低于口腔温度,但高于手掌温度,在口腔中变成液体,在手掌中是固体ABC
(1)由表可知,该巧克力中含量最高的营养素是糖类,100g中含有59.5g。
(2)可可豆发酵的过程中生成二氧化碳、醋酸等物质,属于化学变化。
(3)根据图可知,10℃时固体脂指数最小的是奶油约为20,其他固体脂指数均大于20。
(4)巧克力“只融在口,不融在手”这句广告词中蕴含的科学原理是;
可可脂是一种主要由三种脂肪酸构成的脂肪,熔点在34~36℃,低于口腔温度,但高于手掌温度,在口腔中变成液体,在手掌中是固体。
(5)
A、巧克力含有丰富的多源苯酚复合物,是防止心脏病的天然卫士,心脏病患者可适当食用巧克力,说法正确;
B、可可豆发酵过程中减少了单宁的含量,从而降低了可可的苦味,说明巧克力中因含有单宁等物质使其略带苦味,说法正确;
C、根据几种固体脂的融化曲线可知,巧克力在口中能瞬间融化是因为其固体脂指数随温度变化大,说法正确。
故选ABC。
8.我国著名化学家徐光宪院士说:
“化学是不断发明和制造对人类更有用的新物质的科学”。
在分子一原子层面上改变原子的排列方式就可以创造新物质。
石墨在超高压和高温的条件下某些碳原子(方框中的碳原子a)受到挤压,凸出到层间的空间中,与上一层正六边形的碳原子形成正四面体的排列形式,就得到金刚石(方框中的碳原子a对应的石墨中的碳原子a)。
1985年,英国化学家克罗托发现C60,提出C60是由12个正五边形和20个正六边形构成封闭的完美对称的笼状分子,由于C60分子的形状和结构酷似英国式足球,所以又被形象地称为“足球烯”。
C60在常温下是紫红色晶体,具有金属光泽。
1991年,日本科学家发现了碳纳米管,它是碳原子以正六边形排列而成的管状结构,直径一般为几纳米到几十纳米。
碳纳米管的管状结构决定了它的弹性和弯曲性都比较优异,可制作金属催化剂载体,作为贮氢。
材料制作燃料电池等,碳纳米管还可用于纳米机器人、计算机芯片等前沿领域。
2004年,英国科学家成功制得石墨烯,这种碳单质的碳原子是以正六边形紧密排列的单层结构。
石墨烯具有很多优异性能:
表面积大、透光率高、导电性强、机械性能优异等,使石墨烯在透明电极、太阳能电池、传感器、手机屏幕、电脑触摸屏等方面有着良好的应用前景。
科学家在一定条件下可以选取石墨烯片段包裹成足球烯,也可以将片段卷起来得到碳纳米管。
依据文章内容,回答下列问题。
(1)短文中涉及到的碳单质共有_____种。
(2)文中提到“在超高温和高压的条件下,石墨可以转变为金刚石”,这一变化是_____变化。
(3)C60在常温下是_____色晶体,猜想C60的一种化学性质可能是_____(用化学方程式表示),它与金刚石性质上存在明显差异,可能的原因是_____。
(4)碳纳米管机械加工:
性能优异,弹性较好,易于弯曲,这些性质都源于它是_____结构。
(5)石墨烯具有较高的导电性和透光性,可以用来制作_____。
(6)结合本文,你认为从微观角度创造新物质的可能途径有_____。
【答案】5化学变化紫红色C60+60O2
60CO2或C60+120CuO
120Cu+60CO2↑碳原子的排列方式不同管状透明电极、手机屏幕、电脑触摸屏(任答其一)在分子、原子层面上改变原子的排列方式
(1)短文中涉及到的碳单质有石墨、金刚石、C60、碳纳米管、石墨烯。
共5种。
(2)“在超高温和高压的条件下,石墨可以转变为金刚石”,有新物质生成,属于化学变化;
(3)C60在常温下是紫红色晶体,具有金属光泽;
C60是碳的一种单质,可能具有可燃性,燃烧的产物是二氧化碳,可能具有还原性,与氧化铜在高温下反应生成铜和二氧化碳,反应方程式为:
C60+60O2
60CO2;
C60+120CuO
120Cu+60CO2↑;
C60与金刚石性质上存在明显差异,可能的原因是:
碳原子的排列方式不同;
(4)碳纳米管是碳原子以正六边形排列而成的管状结构,直径一般为几纳米到几十纳米。
碳纳米管的管状结构决定了它的弹性和弯曲性都比较优异;
(5)石墨烯具有很多优异性能:
(6)结合本文,碳的五种单质本质区别是碳原子排列方式不同,从微观角度创造新物质的可能途径是:
在分子、原子层面上改变原子的排列方式。
9.阅读下面的科普短文
在离地面约25km高空处有一层厚度极薄的气体层,主要成分是臭氧(O3),它是地球上一切生命的保护层。
与O2不同,通常状况下O3是淡蓝色气体,有难闻的
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 最新 初三化学 化学 科普 阅读 20 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
