 版高考化学大二轮增分攻略专题强化训练17 化学工艺流程文档格式.docx
版高考化学大二轮增分攻略专题强化训练17 化学工艺流程文档格式.docx
- 文档编号:20477746
- 上传时间:2023-01-23
- 格式:DOCX
- 页数:15
- 大小:299.18KB
版高考化学大二轮增分攻略专题强化训练17 化学工艺流程文档格式.docx
《版高考化学大二轮增分攻略专题强化训练17 化学工艺流程文档格式.docx》由会员分享,可在线阅读,更多相关《版高考化学大二轮增分攻略专题强化训练17 化学工艺流程文档格式.docx(15页珍藏版)》请在冰豆网上搜索。
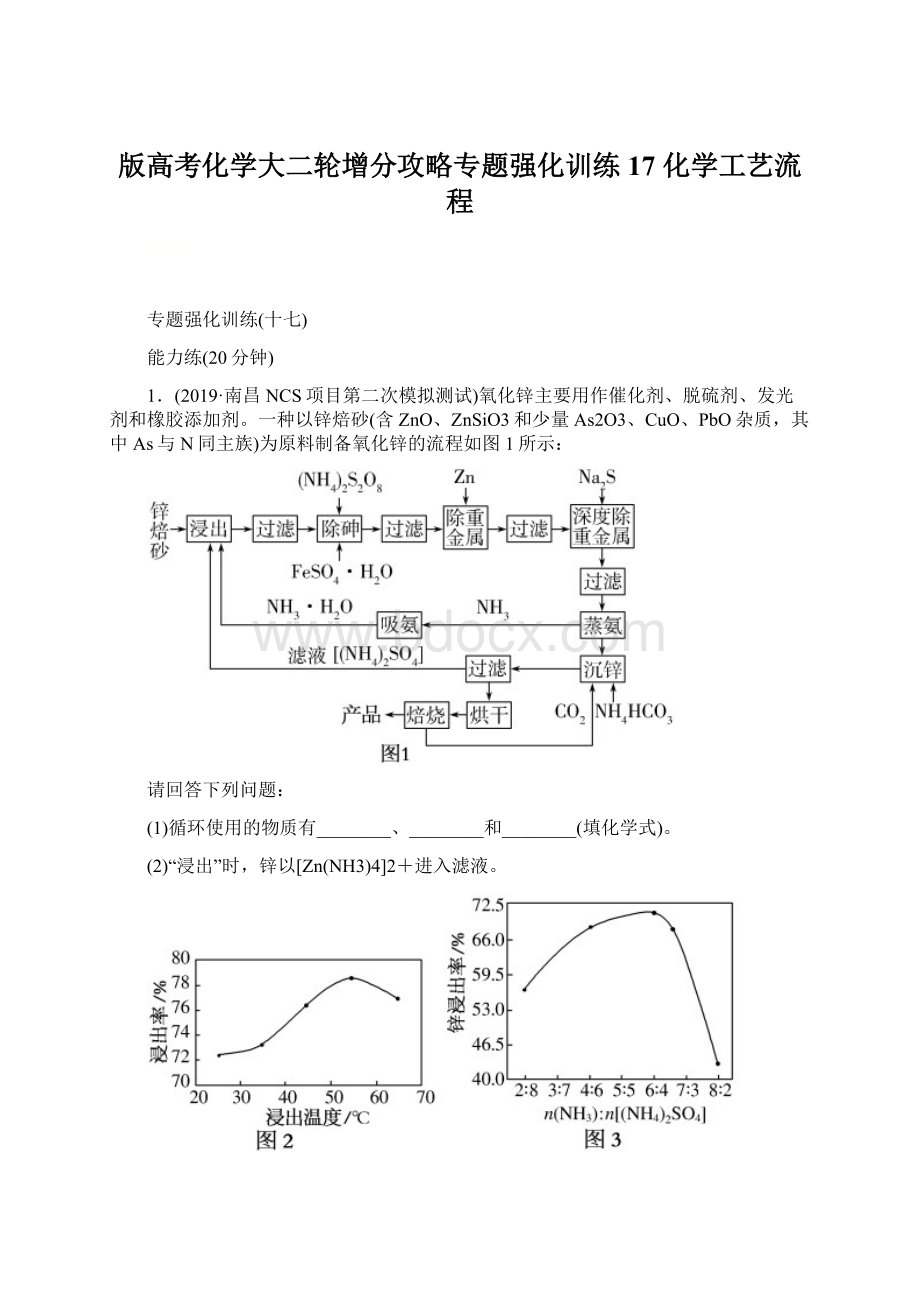
以便除去砷元素。
(4)根据锌焙砂所含杂质,“除重金属”和“深度除重金属”除去的重金属是铜和铅。
(5)“蒸氨”时Zn(NH3)4SO4发生分解反应:
Zn(NH3)4SO4
ZnSO4+4NH3↑。
[答案]
(1)NH3·
H2O或NH3 (NH4)2SO4 CO2
(2)①温度升高,氨气挥发,溶液浓度下降,浸出率下降 ②C
(3)+2 把+3价砷氧化成AsO
以便除去砷元素
(4)铜和铅 (5)Zn(NH3)4SO4
ZnSO4+4NH3↑
2.(2019·
长沙四校二模)一种从冶铅废渣中提取铅的工艺流程如图所示:
已知:
醋酸铅易溶于水,难电离。
火法炼铅是将方铅矿(主要成分为PbS)在空气中焙烧,生成PbO和SO2。
回答下列问题:
(1)用方铅矿火法炼铅的反应的化学方程式为_______________
________________________________________________________。
(2)火法炼铅的废气中含SO2,可将废气通入过量氨水中进行处理,反应的离子方程式为____________________________________
(3)冶铅废渣用硫酸洗涤后,生成的PbSO4表面常含有铜单质,为了溶解铜单质,常需要同时加入一定量的H2O2溶液,写出溶解铜单质发生反应的离子方程式____________________________;
为加快此反应的速率,下列方法合理的是________(填标号)。
A.搅拌 B.适当加热 C.减压
(4)将饱和Na2CO3溶液加入滤渣1中发生的反应为CO
(aq)+PbSO4(s)PbCO3(s)+SO
(aq),以PbCO3和焦炭为原料在高温条件下可制备金属铅,用化学方程式表示制备过程____________。
(5)工业上常用等体积的饱和NaHCO3溶液代替饱和Na2CO3溶液,将一定量的PbSO4转化为PbCO3。
PbSO4与NaHCO3或Na2CO3的物质的量之比不同时,PbSO4的转化率如表所示。
Ⅰ
n(PbSO4)∶n(NaHCO3)
1∶1.5
1∶2
1∶3
PbSO4的转化率%
95.5
96.9
97.8
Ⅱ
n(PbSO4)∶n(Na2CO3)
98
依据表中数据,物质的量之比相同时,Ⅱ中PbSO4的转化率比Ⅰ中的略大,原因是__________________________________________
__________________________________________________________。
[解析]
(1)由火法炼铅是将方铅矿在空气中焙烧,生成PbO和SO2,可知发生反应的化学方程式为2PbS+3O2
2PbO+2SO2。
(2)SO2与过量的氨水反应生成亚硫酸铵,反应的离子方程式为2NH3·
H2O+SO2===2NH
+SO
+H2O。
(3)酸性条件下铜被H2O2氧化为Cu2+,反应的离子方程式是Cu+H2O2+2H+===Cu2++2H2O;
搅拌能加快反应速率,适当升高温度可使反应速率加快,该反应没有气体参与,减压对反应速率无影响,故选AB。
(4)以PbCO3和焦炭为原料制备Pb的反应的化学方程式为PbCO3
PbO+CO2↑、2PbO+C
2Pb+CO2↑(或PbO+C
Pb+CO↑)。
(5)物质的量之比相同时,Na2CO3溶液中c(CO
)比NaHCO3溶液中的大,故Ⅱ中PbSO4的转化率比Ⅰ中的略大。
[答案]
(1)2PbS+3O2
2PbO+2SO2
(2)2NH3·
+H2O
(3)Cu+H2O2+2H+===Cu2++2H2O AB
(4)PbCO3
Pb+CO↑)
)比NaHCO3溶液中的大
3.(2019·
济南模拟)工业上,从精制黑钨矿(FeWO4、MnWO4)中提取金属钨的一种流程如图所示,该流程同时获取副产物Fe2O3和MnCl2。
Ⅰ.过程①~④中,钨的化合价均不变;
Ⅱ.常温下钨酸难溶于水;
Ⅲ.25℃时,Ksp[Fe(OH)3]=1.0×
10-38、
Ksp[Mn(OH)2]=4.0×
10-14。
(1)上述流程中的“滤渣1”除MnO2外还有________,“气体”除水蒸气、HCl外还有________(均填化学式)。
(2)过程①中MnWO4参与反应的化学方程式为____________________________________;
FeWO4参与的反应中氧化剂与还原剂的物质的量之比为________。
(3)已知:
WO3(s)+3H2(g)===W(s)+3H2O(g) ΔH=akJ·
mol-1
WO3(s)===WO3(g) ΔH=bkJ·
写出WO3(g)与H2(g)反应生成W(s)的热化学方程式:
(4)过程⑦在25℃时调pH,至少应调至________(当离子浓度等于1.0×
10-5mol·
L-1时,可认为其已沉淀完全)。
(5)过程⑧要获得MnCl2固体,在加热时必须同时采取的一项措施是_____________________________________________________。
(6)钠钨青铜是一类特殊的非化学计量比化合物,其通式为NaxWO3,其中0<
x<
1,这类化合物具有特殊的物理化学性质,是一种低温超导体。
应用惰性电极电解熔融的Na2WO4和WO3混合物可以制备钠钨青铜,写出WO
在阴极上放电的电极反应式:
_______________________________________________________。
[解析]
(1)分析整个流程图可知,精制黑钨矿经过程①、②处理后,其中的Fe、Mn转入滤渣,而W转入滤液。
碱性条件下,Fe2O3稳定,故滤渣1中还应有Fe2O3。
滤渣1中的MnO2与浓盐酸在加热条件下生成Cl2,故气体中还含一定量的Cl2。
(2)由“过程①~④中,钨的化合价均不变”及滤渣1中含MnO2可知,过程①中O2为氧化剂,同时生成了Na2WO4和CO2,故过程①中MnWO4参与反应的化学方程式为:
2MnWO4+O2+2Na2CO3
2Na2WO4+2CO2+2MnO2。
过程①中,FeWO4中的+2价Fe被氧化为+3价Fe,1molFeWO4反应失去1mol电子,氧化剂为O2,1molO2反应得到4mol电子,根据得失电子守恒可知,FeWO4参与的反应中氧化剂与还原剂的物质的量之比为1∶4。
(3)根据盖斯定律,由第一个热化学方程式减去第二个热化学方程式可得:
WO3(g)+3H2(g)===W(s)+3H2O(g) ΔH=(a-b)kJ·
mol-1。
(4)过程⑦的目的是使Fe3+完全转化为Fe(OH)3沉淀而不使Mn2+沉淀,当Fe3+沉淀完全时c(OH-)=
=1.0×
10-11mol·
L-1,此时若使Mn2+沉淀,则所需c(Mn2+)=
=4×
108mol·
L-1,不存在此浓度的含Mn2+溶液,即此时Mn2+不会生成沉淀,故至少应调至pH=3。
(5)MnCl2在水溶液中水解生成Mn(OH)2和HCl,加热会促进MnCl2水解,故要获得MnCl2固体,需在HCl氛围中加热,以抑制其水解。
(6)由题意可知WO
在阴极上放电的产物为WO
,对比WO
、WO
的元素组成,结合物质为熔融状态,可知另外一种生成物为O2-,故电极反应式为WO
+xe-===WO
+O2-。
[答案]
(1)Fe2O3 Cl2
(2)2MnWO4+O2+2Na2CO3
2Na2WO4+2MnO2+2CO2 1∶4
(3)WO3(g)+3H2(g)===W(s)+3H2O(g) ΔH=(a-b)kJ·
(4)3.0 (5)通入HCl气体,在HCl气氛中加热
(6)WO
+O2-
拔高练(25分钟)
武汉调研)亚铁氰化钾{K4[Fe(CN)6]·
3H2O}俗称黄血盐,常用于检验Fe3+,也是食盐防结剂。
以生产电石的副产物氰熔体[Ca(CN)2和NaCN的混合物]为原料,制备亚铁氰化钾的流程如下:
(1)“浸取”需控制在80℃以下进行,原因是
_____________________________________________________。
(2)用硫酸亚铁晶体配制FeSO4溶液时还需加入____________________。
(3)对“滤液”处理可获得一种实验室常用干燥剂,它的化学式是________________________。
(4)“加热”使HCN气体逸出发生“反应Ⅲ”,生成K4[Fe(CN)6]、二氧化碳和氢气,该反应的化学方程式为
____________________________________________________。
(5)“反应Ⅲ”后的溶液经蒸发浓缩、冷却结晶、________、________、干燥即得产品。
(6)工业上,以石墨为电极,电解亚铁氰化钾溶液可以制备铁氰化钾{K3[Fe(CN)6],可用于检验Fe2+},阳极的电极反应式为______________________________________________________。
(7)设计如图实验探究牺牲阳极的阴极保护法原理。
得出结论:
①锌能保护铁;
②__________________________。
[解析]
(1)温度过高,会促进CN-水解,生成有毒的HCN,污染环境,故需控制温度低于80℃。
(2)为防止硫酸亚铁氧化变质,应加入铁粉,为防止其水解,应加入稀硫酸。
(3)分析流程图可知,获得的常用干燥剂是CaCl2。
(4)根据题给条件知“反应Ⅲ”的反应物为HCN、K2CO3、Fe,生成物为K4[Fe(CN)6]、CO2、H2,结合原子守恒和得失电子守恒可得反应的化学方程式为:
6HCN+2K2CO3+Fe===K4[Fe(CN)6]+2CO2↑+H2↑+2H2O。
(5)从溶液中得到溶质一般需经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥操作。
(6)阳极发生氧化反应,Fe元素由+2价变为+3价,电极反应式为:
[Fe(CN)6]4--e-===[Fe(CN)6]3-。
(7)由操作(ⅰ)及实验现象可知,在该原电池中Zn被腐蚀,铁被保护,电解液中无Fe2+,在U形管铁极附近滴加铁氰化钾溶液后产生了蓝色沉淀,则说明有二价铁生成,即铁被铁氰化钾氧化生成了Fe2+。
[答案]
(1)温度过高,促进CN-水解,生成有毒的HCN,污染环境
(2)稀硫酸和铁屑 (3)CaCl2
(4)2K2CO3+6HCN+Fe===K4[Fe(CN)6]+2CO2↑+H2↑+2H2O (5)过滤 洗涤
(6)[Fe(CN)6]4--e-===[Fe(CN)6]3-
(7)铁被铁氰化钾氧化生成了Fe2+
合肥第二次质量检测)铍铜是广泛应用于制造高级弹性元件的良好合金。
某科研小组从某废旧铍铜元件(主要含BeO、CuS,还含少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如图:
ⅰ.铍、铝元素化学性质相似;
BeCl2熔融时能微弱电离。
ⅱ.常温下Ksp[Cu(OH)2]=2.2×
10-20,Ksp[Fe(OH)3]=4.0×
10-38,Ksp[Mn(OH)2]=2.1×
10-13。
(1)滤液A的主要成分除NaOH外,还有__________________(填化学式);
写出反应Ⅰ中含铍化合物与过量盐酸反应的离子方程式________________________________________________________。
(2)滤液C中含NaCl、BeCl2和少量HCl,为得到较纯净的BeCl2溶液,下列实验操作步骤最合理的顺序是________;
电解熔融BeCl2制备金属铍时,需要加入NaCl,其作用是____________。
①加入过量的NaOH;
②加入过量的氨水;
③加入适量的HCl溶液;
④过滤;
⑤洗涤。
(3)反应Ⅱ中CuS的氧化产物为S单质,该反应的化学方程式为________________________________________________________。
(4)常温下,若滤液D中,c(Cu2+)=2.2mol·
L-1、c(Fe3+)=0.008mol·
L-1,c(Mn2+)=0.21mol·
L-1,向其中逐滴加入稀氨水,生成的沉淀F是________(填化学式);
为了尽可能多地回收铜,所得滤液G的pH最大为________。
[解析]
(1)废旧铍铜原件中含有BeO、CuS、FeS、SiO2,根据已知信息ⅰ,可知BeO属于两性氧化物,能与NaOH发生反应,CuS、FeS不与氢氧化钠反应,SiO2属于酸性氧化物,能与氢氧化钠反应,因此滤液A的主要成分是NaOH、Na2SiO3、Na2BeO2;
BeO
与过量盐酸反应生成氯化铍和水,其离子方程式为BeO
+4H+===Be2++2H2O。
(2)由于Be元素、铝元素化学性质相似,可向滤液C中先加入过量的氨水,生成Be(OH)2沉淀,过滤、洗涤后再向沉淀中加入适量的HCl溶液,即得到较纯净的BeCl2溶液,故最合理的步骤顺序是②④⑤③;
熔融BeCl2微弱电离,则加入NaCl可增强熔融盐的导电性。
(3)根据题意可知,CuS中S转化为S单质,则MnO2中Mn被还原为Mn2+,根据得失电子守恒、原子守恒可知,其化学方程式为MnO2+CuS+2H2SO4===S+MnSO4+CuSO4+2H2O。
(4)根据已知信息ⅱ可知,Cu2+开始沉淀时,c(OH-)=
=
mol·
L-1=1×
10-10mol·
L-1,Fe3+开始沉淀时,c(OH-)=
=
L-1=
×
10-12mol·
L-1,Mn2+开始沉淀时,c(OH-)=
10-6mol·
L-1,则向滤液D中逐滴加入稀氨水,首先沉淀的是Fe3+,所以产生的沉淀F为Fe(OH)3;
滤液E中含有Cu2+和Mn2+,Cu2+开始沉淀时c(OH-)=1×
L-1,c(H+)=
L-1=10-4mol·
L-1,pH=4,为使Cu2+尽可能多地沉淀,同时不能使Mn2+沉淀,由前面分析可知,Mn2+开始沉淀时c(OH-)=1×
L-1,即pH=8,故滤液G的pH最大为8。
[答案]
(1)Na2SiO3、Na2BeO2 BeO
+4H+===Be2++2H2O
(2)②④⑤③ 增强熔融盐的导电性
(3)MnO2+CuS+2H2SO4===S+MnSO4+CuSO4+2H2O
(4)Fe(OH)3 8.0
江西八所重点中学联考)锶(Sr)为第五周期第ⅡA族元素,其化合物六水氯化锶(SrCl2·
6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
①经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+杂质;
②SrSO4、BaSO4的溶度积常数分别为3.3×
10-7、1.1×
10-10;
③SrCl2·
6H2O的摩尔质量为267g·
(1)工业上天青石焙烧前先研磨粉碎,其目的是________________________________。
(2)工业上天青石隔绝空气高温焙烧,若0.5molSrSO4中只有硫元素被还原,转移了3mol电子。
写出该反应的化学方程式_______________________________________________________。
(3)加入硫酸的目的是________________________。
为了提高原料的利用率,滤液1中Sr2+的浓度应不高于________mol·
L-1(注:
此时滤液1中Ba2+浓度为1×
L-1)。
(4)滤渣1的主要成分是________,滤液1经蒸发浓缩、冷却结晶、过滤后,需对所得的六水氯化锶晶体进行洗涤、干燥。
证明六水氯化锶晶体已洗涤干净的实验操作及现象为____________。
(5)工业上常通过电解熔融SrCl2制锶单质。
由SrCl2·
6H2O制取无水氯化锶的方法是____________。
[解析]
(1)粉碎天青石的目的是增大反应物的接触面积,加快反应速率。
(2)依题意,SrSO4中只有S元素被还原,因为0.5molSrSO4完全反应转移3mol电子,所以,+6价硫元素的还原产物为S,氧化产物为CO,根据原子守恒,可知另一种产物为SrO,据此写出反应的化学方程式。
(3)结合信息①和硫酸锶、硫酸钡的溶度积数据知,加入硫酸的目的是除去钡离子,提高产品纯度。
c(Ba2+)=1×
L-1时,c(SO
)=
L-1=1.1×
L-1,为提高原料利用率,Sr2+不能生成沉淀,故c(Sr2+)<
L-1=0.03mol·
L-1。
(4)结合信息①可知,溶液中含有Sr2+、Cl-和Ba2+,加入硫酸后生成了硫酸钡,故滤渣1的主要成分为硫酸钡。
六水氯化锶晶体上附着有SO
,可通过检验洗涤液中是否含有SO
来确认是否洗净。
(5)锶位于第五周期第ⅡA族,与钙同主族,根据元素周期律知,氢氧化锶的碱性比氢氧化钙强,说明氯化锶在水中不水解,故可直接灼烧SrCl2·
6H2O制得SrCl2。
[答案]
(1)增加反应物的接触面积,提高化学反应速率
(2)SrSO4+3C
SrO+3CO↑+S
(3)除去溶液中的Ba2+杂质 0.03
(4)BaSO4 取少量最后一次洗涤液于试管中,滴加少量BaCl2溶液,无白色沉淀生成,说明沉淀洗涤干净
(5)直接加热SrCl2·
6H2O(或灼烧等)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 版高考化学大二轮增分攻略专题强化训练17 化学工艺流程 高考 化学 二轮 攻略 专题 强化 训练 17 工艺流程
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
