 95学年度高雄市高级中学数学及自然科能力竞赛复赛化学科实验试题Word文档格式.docx
95学年度高雄市高级中学数学及自然科能力竞赛复赛化学科实验试题Word文档格式.docx
- 文档编号:20442372
- 上传时间:2023-01-23
- 格式:DOCX
- 页数:41
- 大小:124.03KB
95学年度高雄市高级中学数学及自然科能力竞赛复赛化学科实验试题Word文档格式.docx
《95学年度高雄市高级中学数学及自然科能力竞赛复赛化学科实验试题Word文档格式.docx》由会员分享,可在线阅读,更多相关《95学年度高雄市高级中学数学及自然科能力竞赛复赛化学科实验试题Word文档格式.docx(41页珍藏版)》请在冰豆网上搜索。
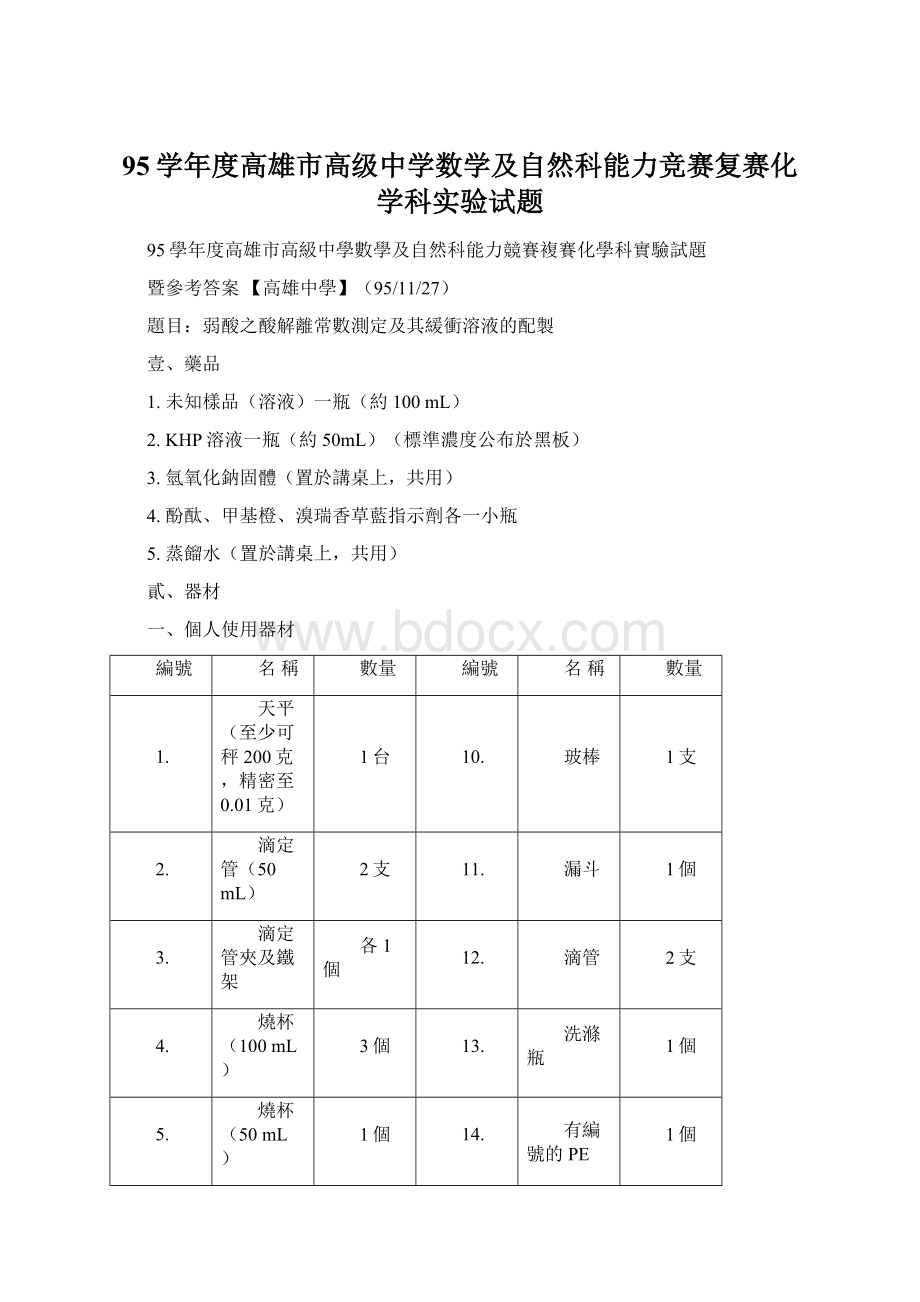
量瓶(50mL、100mL、250mL)
16.
秤量紙
5張
8.
刻度吸量管(10mL)
17.
刷子(清洗玻璃器材用)
9.
安全吸球
18.
工程用計算機
二、共用器材(置於講桌上)
酸鹼度計、紙巾
參、說明
未知樣品為一單質子酸(HA)之水溶液,濃度介於0.1~0.5M之間。
請利用所提供之藥品、器材,設計實驗(寫出實驗步驟及數據處理過程):
一、測定此未知樣品溶液中,單質酸(HA)的濃度與其pKa值。
二、取此未知樣品10.0mL,配製pH值為5.0之緩衝溶液50mL(請將所配緩衝溶液置於有編號PE瓶中繳回評分)。
肆、實驗步驟:
一、配製NaOH溶液250ml。
答:
配製0.1MNaOH溶液250ml:
秤取1.0克(0.025莫耳)NaOH(不可以秤量紙裝NaOH)置於100ml燒杯中,加入些許蒸餾水使其溶解,再置入250ml量瓶中,加入蒸餾水至刻度,充分混合後,備用。
二、以KHP溶液標定NaOH溶液。
1.以吸量管吸取10mlKHP溶液置於三角錐瓶中並加入1、2滴酚酞指示劑,以NaOH溶液滴定之。
2.取同量於KHP溶液之蒸餾水,加入1、2滴酚酞指示劑,以NaOH溶液滴定,作為空白滴定。
3.計算NaOH溶液之濃度(利用N1V1=N2V2)。
4.重複以上步驟數遍,並取平均值。
三、未知酸溶液之濃度測定。
1.以吸量管量取10ml未知酸溶液置於三角錐瓶中並,加入1、2滴酚酞指示劑,以0.10MNaOH溶液滴定。
2.取10ml蒸餾水,加入1、2滴酚酞指示劑,以NaOH溶液滴定,作為空白滴定。
3.計算未知酸溶液之濃度(利用N1V1=N2V2)。
4.重複以上步驟數遍,並取平均值(未知酸濃度為0.25M)。
四、以酸鹼度計測定未知酸之酸解離常數。
1.以吸量管量取10ml未知酸溶液並加入步驟三標定時所使用NaOH溶液體積之一半量(12.5mL)。
2.以酸鹼度計測定以上溶液之pH值,此pH值即為未知酸之pKa值(未知酸pKa參考值為4.77)。
五、pH=5之緩衝溶液配製。
以吸量管分別量取10ml未知酸溶液(0.25M)和15.73ml之NaOH溶液(0.10M),置入50ml量瓶中,並加蒸餾水稀釋至刻度,充分混合後即得pH為5之緩衝溶液。
伍、問題
一、所測得之未知弱酸濃度為:
0.25
M。
二、所測得之未知弱酸pKa值為:
4.77
。
※評分標準:
1.實驗步驟、數據處理等。
(20%)
2.所測未知弱酸之濃度是否準確?
(10%)
3.所測未知弱酸之pKa是否準確?
4.所配製之緩衝溶液pH值是否接近5.0?
5.實驗基本操作及技巧。
6.實驗室安全、環保及其他事項。
95學年度台灣省高級中學數學、資訊及自然學科能力競賽化學科實驗試題
暨參考答案【台南女中】
(第9區)(95/11/17)
分析碳酸氫鈉固體試樣中Na2CO3與NaHCO3的含量
壹、說明
利用双重指示劑滴定法定量工業級碳酸氫鈉固體試樣中Na2CO3與NaHCO3的重量百分率濃度。
貳、實驗器材
(一)個人使用器材
天平(可精秤至小數點第二位)
水流過濾裝置(過濾瓶、瓷漏斗、鐵製水流過濾器、橡皮軟管、濾紙)
1組
滴定管、滴定管夾與鐵架
100mL、250mL容量瓶(附塞子)
各1支
100mL燒杯
秤量瓶(附蓋子)
玻璃漏斗
25mL、50mL量筒
試藥匙
20mL球形吸量管
洗滌用毛刷
(二)共用材料
1.蒸餾水2.衛生紙
參、實驗藥品
1.未知濃度的鹽酸溶液(試液A)50mL一瓶
2.待測試樣D(或E)一包
3.酸鹼指示劑(酚酞、甲基橙、甲基紅)各一瓶
4.純的Na2CO3固體約1克
肆、實驗步驟
(一)配製標準鹽酸水溶液
1.精取40.0mL未知濃度的鹽酸溶液(試液A),置入250mL容量瓶內,加入蒸餾水配製得250mL標準鹽酸水溶液(試樣B),將部份試液B填裝入滴定管內備用。
2.精秤0.3~0.4克純的Na2CO3(S)置於100mL燒杯內,加約20.0mL蒸餾水溶解之,滴入2~3滴酸鹼指示劑,並以試液B標定之,紀錄試液B滴定體積,並計算試液B之體積莫耳濃度。
(二)固體試樣中Na2CO3與NaHCO3的濃度定量
1.精秤所有待測固體試樣重量,並置入100mL燒杯內,加入20.0mL蒸餾水攪拌溶解之。
2.以水流過濾器進行過濾操作,以約10.0~20.0mL蒸餾水洗滌未溶解固體,收集所有濾液,置入100mL容量瓶內,以蒸餾水稀釋成100mL溶液(試液C)。
3.精取20.0mL試液C,置入100mL燒杯內,滴加2~3滴適當酸鹼指示劑,以試液B滴定至終點,紀錄其滴定體積,隨後再滴入2~3滴另一種酸鹼指示劑,繼續滴定至溶液顏色變化為止,紀錄第二階段試液B之滴定體積。
五、實驗結果待測試樣編號:
D(E)
(一)配製標準鹽酸水溶液部分
1.純的Na2CO3重量為0.38克,試液B滴定體積22.8(11.4)mL,使用酸鹼指示劑為甲基橙(酚酞),滴定終點溶液顏色變化為橙→紅(紅→無),試液B之濃度為0.314M,試液A的濃度為1.96M。
2.寫出相關的計算式
MB=0.314M
(二)Na2CO3與NaHCO3濃度之定量
1.固體試樣重3.98克。
酸鹼指示劑名稱
滴定終點溶液顏色變化
試液B之滴定體積(mL)
Na2CO3重量百分濃度(%)
NaHCO3重量百分濃度(%)
第一階段滴定
酚酞
紅→無
6.1ml
25.64%
44.07%
第二階段滴定
甲基橙
橙黃→紅
19.4ml
2.寫出相關計算式
Na2CO3含量:
NaHCO3含量:
3.您精取20.0mL溶液是使用何種容器量取?
安全吸球、吸量管(20ml)
4.將0.80克NaOH(S)與2.52克NaHCO3(S)混合再經加水溶解後,會發生何種化學反應變化?
其是否為緩衝溶液?
(A)NaOH+NaHCO3→Na2CO3+H2O
(B)是緩衝溶液
暨參考答案【屏東中學】
(第10區)(95/11/10)
化學反應實驗
壹、實驗器材
滴定管(50mL)
溫度計(100℃)
鐵架及滴定管夾
錐形瓶刷
錐形瓶(250mL)
2個
抹布
1塊
6個
刮勺
吸量管(10mL)
3支
秤量紙
3張
鑷子
量筒(50mL)
細砂紙(10cm*10cm)
1張
滴管
19.
洗滌瓶
20.
安全眼鏡
1付
天平(精密到0.01g)
21.
實驗衣
1件
方格紙
22.
標籤紙
(二)共用器材
1.蒸餾水2.廚房紙巾3.廢液瓶(桶)
貳、實驗藥品
1.未知濃度硫酸銅溶液(每人50mL)
2.1M硫酸溶液(每人60mL)
3.鋅片(寬1cm、長5cm)
4.鋅片(寬1cm、長2cm)
5.銅線(長30cm)
1瓶
3片
2片
2條
參、實驗步驟
(一)測量硫酸銅溶液的濃度
1.分別量取10,15,20mL的硫酸銅溶液倒入三個50ml燒杯中。
2.取1×
5cm2鋅片三片,用細砂纸磨光後秤重,同時紀錄其重量,之後將其分別放入步驟1之燒杯內,待反應完後,用鑷子取出鋅片,以蒸餾水洗淨,再以紙巾擦乾後再秤重。
3.紀錄上述實驗中鋅片反應前、反應後所減少的重量,並回答問題1~3。
(二)影響鋅與稀硫酸反應的因素
1.於三個50ml燒杯內分別加入20mL1.0M稀硫酸。
2.分別加入已磨光的(a)1×
2cm2鋅片、(b)30cm銅線、(c)1×
2cm2鋅片加30cm銅線(兩者需接觸)於此三個燒杯內。
3.觀察並回答問題4,5。
圖一纏繞銅線圖二鋅片加銅線的成品
肆、問題
1.寫出實驗
(一)的反應方程式。
2.求出實驗
(一)中硫酸銅溶液的濃度。
(Zn:
65.39;
Cu:
63.55;
S:
32.07;
O:
16.00)
平均濃度:
0.95M
3.利用方格紙將實驗
(一)中三次所用的硫酸銅溶液的體積(mL)為y座標,以鋅片減少的重量(g)為x座標作圖。
請問這個圖形之斜率所代表的意義為何?
設硫酸銅溶液的體積為V1與V2,濃度為m
鋅片相對應減少的重量為W1與W2
鋅的原子量為M,斜率為S
4.寫出實驗
(二)裡步驟2.(a)的反應方程式。
5.簡要說明在實驗
(二)中你所觀察到的現象及這些現象所可能反應的化學原理。
(a)氣泡產生(有反應)
(b)無氣泡產生(無反應)
(c)鋅片及銅線上皆有氣泡產生氧化還原
94學年度高雄市高級中學數學及自然學科競賽複賽化學科實驗試題
(94/11/23)
雙質子酸鉀鹽分子量的測定
一、說明:
一個含C、H、O的雙質子酸,如果以NaOH滴定,兩個當量點可以分別用甲基橙(pH變色範圍:
3.1-4.4)和酚酞(pH變色範圍:
8.0-9.6)兩個指示劑來決定。
現有此雙質子酸之單鉀鹽,請以酸鹼滴定的方法求得此鹽類的分子量。
(滴定次數依所提供)
二、器材:
(個人器材)
50mL(或100mL)量筒
漏斗(填充滴定液用)
錐形瓶(125mL)
滴定管夾與鐵架
藥勺
滴管(含橡皮套)
天平(最小刻度0.01克)
三、藥品:
1.未知雙質子酸之單鉀鹽(約5克)
2.約0.2MNaOH標準溶液100mL(正確的濃度當場宣佈)
3.甲基橙指示劑
4.酚酞指示劑
5.蒸餾水(共用)
四、實驗步驟:
稱取約1克的雙質子酸鉀鹽,並溶於蒸餾水中,加入數滴的適當之指示劑,以NaOH標準溶液滴定至指示劑變色(滴定次數依所提供〝未知雙質子酸之單鉀鹽〞之限量自行安排)。
五、結果記錄:
雙質子酸鉀鹽稱取重量(g)
滴定使用NaOH水溶液體積(mL)
第一次滴定
1.00g
23.6
第二次滴定
23.5
第三次滴定
23.7
……
六、問題:
(所有計算必須寫出算式)
(A)滴定時你所用的指示劑為酚酞。
(B)計算出每一次滴定測得之此雙質子酸鉀鹽的分子量。
設雙質子酸鉀鹽的分子量為M1
H+的mole數=OH-的mole數
則
M1=204.70
分子量為204.70
設雙質子酸鉀鹽的分子量為M2
M2=205.57
分子量為205.57
設雙質子酸鉀鹽的分子量為M3
M3=203.84
分子量為203.84
(C)由實驗得到此雙質子酸鉀鹽的平均分子量為204.70g/mol。
平均分子
=
=204.70
(D)你實驗所得到平均分子量的平均誤差由計算誤差的公式
,計算得到為0.58。
平均A誤差公式:
=
=0.58
94學年度台灣省高級中學數學、資訊及自然學科能力競賽化學科實驗試題
(第十區,94/11/11)
未知過錳酸鉀溶液濃度之測定
壹、藥品:
一、未知濃度之過錳酸鉀溶液(每人約100mL)
二、草酸固體(每人約2g)
三、3M硫酸溶液(每人約100mL)
四、蒸餾水(置於講桌上,共用)
《注意》︰草酸溶液是有毒的,勿將含有草酸的溶液倒入水槽,而須將其倒入標有「Permanganate/Oxalateresidues」的廢液瓶中。
貳、個人器材:
滴定管(50.00mL)
2支
陶瓷纖維網
1片
滴定管架及滴定管夾
各1套
溫度計
錐形瓶(250mL)
滴定管刷
量瓶(100.0mL)
錐形瓶刷
燒杯(500mL)
燒杯(250mL)
計算機(無程式)
量筒(50.0mL)
三腳架
滴管(PE,3mL)
刮勺
玻棒(15cm)
表玻璃
天平(精密到0.01g)
酒精燈
1座
參、說明:
利用氧化還原滴定求未知濃度之過錳酸鉀溶液。
本實驗配製標準的草酸溶液,在酸性條件下,以所配製的草酸溶液標定過錳酸鉀溶液。
請依據所提供的器材和藥品為條件,設計最佳的實驗過程。
肆、實驗過程:
請將實驗原理、實驗流程、實驗步驟記錄於下。
反應式如下:
離子式:
2MnO4-+5C2O42-+16H+――→2Mn2++10CO2+8H2O
分子式:
2KMnO4+5Na2C2O4+8H2SO4――→2MnSO4+10CO2+8H2O+5Na2SO4+K2SO4
實驗步驟如下:
1.秤取2.25克的草酸以量瓶配置成0.25M的草酸溶液
2.在錐形瓶中加入10mL0.25M草酸溶液與10mL3M硫酸溶液後,以酒精燈加熱錐形瓶直到瓶內溶液溫度約60˚C後,移去火源。
3.以過錳酸鉀溶液滴定錐形瓶內溶液,直至溶液維持紫色為止,記錄過錳酸鉀溶液使用體積。
4.重複步驟2,3二次。
伍、實驗結果:
請將實驗數據與相關計算記錄於下。
計算方程式:
過錳酸鉀溶液溶液濃度(M)=
數據如下:
過錳酸鉀溶液使用體積(mL)
過錳酸鉀溶液溶液濃度(M)
第一次
7.0
0.14
第二次
7.1
第三次
過錳酸鉀溶液濃度為0.14M。
(第九區,94/11/1)
◆藥品:
數量
1.鄰苯二甲酸氫鉀
約3g
2.溶液B
約50ml
3.NaOH
約10g(置於共用桌上,使用前領取)
(置於共用桌上,使用前領取)
5.蒸餾水
◆個人使用器材:
1.天平(約200±
0.01g)
9.錐形瓶(250ml)
2.滴定管(50ml×
2)含架
10.錐形瓶(125ml)
3.吸量管(10.0ml)
11.漏斗
4.量瓶(250ml)
12.刷子
5.秤量瓶(約15ml)
13.玻棒
6.量筒(10ml)
14.洗滌瓶
7.燒杯(250ml)
15.秤量紙
約5張
8.燒杯(100ml)
16.標籤
約10片
溶液的配製與濃度的測定
鄰苯二甲酸氫鉀為一弱酸,pKa為2.95,分子量為204.23g/mol。
因其具高純度、安定性及不含水合物等特性,故可當作標準物質來標定NaOH溶液的濃度。
溶液濃度的定義有好幾種,例如容積莫耳濃度(M)的定義為每公升溶液中所含某溶質的莫耳數;
重量莫耳濃度(m)的定義為每公斤溶劑所溶解某溶質的莫耳數;
莫耳分率(x)的定義為某溶質的莫耳數除以溶液中溶劑和溶質的總莫耳數。
現在請利用現有的藥品、器材,自行設計最佳的實驗步驟,完成下列的實驗要求並回答下列所附的問題:
一、實驗要求:
(一)配製約0.1M之NaOH溶液(溶液A)250ml,並以鄰苯二甲酸氫鉀標定其濃度。
(二)測定未知濃度之鄰苯二甲酸氫鉀溶液(溶液B,其濃度介於0.3~0.9M之間)之濃
度(包括容積莫耳濃度、重量莫耳濃度及莫耳分率)和密度。
(三)取10.0ml之溶液B配製成0.100m之鄰苯二甲酸氫鉀溶液(溶液C)並測定其容積莫耳濃度和密度。
二、問題:
(一)標定後之NaOH溶液(溶液A)之濃度為0.100M(請計算至小數點第三位)(5%)
(二)溶液B之濃度為0.482M(容積莫耳濃度)(請計算至小數點第三位)(10%)
0.511m(重量莫耳濃度)(請計算至小數點第三位)(10%)
0.912%(莫耳分率)(請計算至小數點第三位)(5%)
(三)溶液B之密度為1.041g/ml(請計算至小數點第三位)(5%)
(四)溶液C之容積莫耳濃度為0.094M(請計算至小數點第三位)(10%)
(五)溶液C之密度為1.004g/ml(請計算至小數點第三位)(5%)
(六)請寫出配製溶液A之詳細步驟。
(5%)
秤取約1g之NaOH,溶解後置入250ml之量瓶中,稀釋至刻度線。
(七)請寫出標定溶液A之詳細步驟和結果。
精秤0.612gKHp(鄰苯二甲酸氫鉀),溶於約10ml蒸餾水中,加入1、2滴酚酞,以溶液A滴定,至終點記錄所耗溶液A之體積為30.0ml,得溶液A之濃度為
(八)請寫出測定溶液B之濃度(包括容積莫耳濃度、重量莫耳濃度及莫耳分率)之詳細步驟和結果。
(15%)
精取溶液B5.0ml,加入1、2滴酚酞,以溶液A滴定,至終點記錄所耗溶液A之體積為24.1ml,得溶液B之容積莫耳濃度為
測定溶液B之密度為1.041(見問題九)。
故重量莫耳濃度為
x100﹪=0.912﹪
莫耳分率為為
0.482
(九)請寫出測定溶液B之密度的詳細步驟和結果。
精取10.0ml溶液,精秤其重為10.41g,故密度為
(十)請寫出配製溶液C之詳細步驟。
精取10.0l溶液B和38.20g蒸餾水混合。
(十一)請寫出測定溶液C之容積莫耳濃度的詳細步驟和結果。
精取20.0ml溶液C,加1、2滴酚酞,以溶液A滴定,至終點耗溶液A18.8ml,故溶液C之容積莫耳濃度為
(十二)請寫出作完本實驗心得或感想。
略
93學年度高雄市高級中學數學、資訊及自然科能力競賽化學科實驗試題
【高雄中學】
(93/11/19)
利用酸鹼滴定法定量水中鈣離子含量
酸鹼容積標定定量分析法操作簡便明確,有關水中金屬離子的定量檢定,可以過量鹼液與金屬離子形成難溶性沉澱物,經過濾分離沉澱物再定量濾液中存在的氫氧根離子含量,以計算出原試液中金屬離子的濃度。
◆個人使用器材:
1.天平(最小刻度至少0.01克)
10.玻棒
2.容量瓶250mL
11.試藥匙
3.燒杯100mL
4個
12.水流抽濾裝置{含抽濾器、橡皮管、抽濾瓶(附橡皮塞、瓷漏斗與適用濾紙4張)}
4.量筒50mL、25mL
13.玻璃漏斗
5.球形移液管10mL
14.滴定管50mL
6.刻度吸量管10mL
15.滴定管架(含鐵架與鐵夾)
7.安全吸球
16.滴管
8.稱量瓶
17.洗滌瓶
9.稱量紙
18.錐形瓶250mL
◆共用器材:
蒸餾水、紙巾
三、實驗操作:
(一)配製約0.40M標準NaOH水溶液250ml
稱取適當重量的NaOH(S)置於100ml燒杯內,加入50ml蒸餾水攪拌溶解後,倒入250ml容量瓶加水稀釋至刻度,再將此溶液裝入滴定管內備用。
精取10ml標準單質子酸的鄰苯二甲酸氫鉀(KHP,分子量為204)溶液,置於100ml燒杯內,並滴加2滴酸鹼指示劑,再以上述配製的NaOH溶液滴定並計算出鹼液的濃度。
(二)配製約0.20M標準HCl水溶液250ml
精取適當體積濃度為4.0~5.0M濃的鹽酸溶液置入250ml容量瓶內,加入蒸餾水至刻度,取此酸液裝入另一支滴定管內備用,取10ml此酸液,再以上
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 95 学年度 高雄市 高级 中学数学 自然 能力 竞赛 复赛 化学 实验 试题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
