 临床试验启动会议纪要Word下载.docx
临床试验启动会议纪要Word下载.docx
- 文档编号:20319526
- 上传时间:2023-01-21
- 格式:DOCX
- 页数:10
- 大小:18.76KB
临床试验启动会议纪要Word下载.docx
《临床试验启动会议纪要Word下载.docx》由会员分享,可在线阅读,更多相关《临床试验启动会议纪要Word下载.docx(10页珍藏版)》请在冰豆网上搜索。
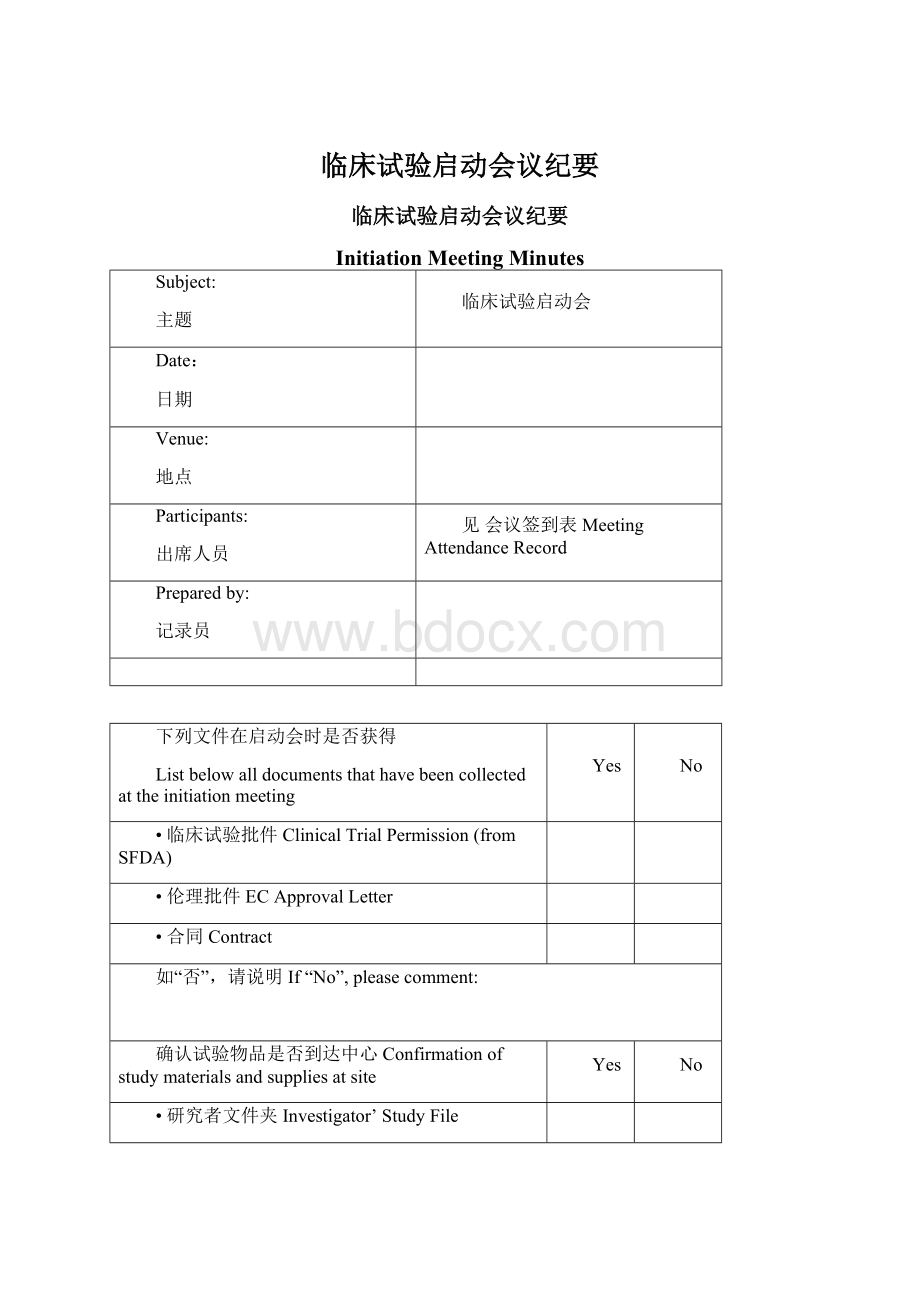
No
•临床试验批件ClinicalTrialPermission(fromSFDA)
•伦理批件ECApprovalLetter
•合同Contract
如“否”,请说明If“No”,pleasecomment:
确认试验物品是否到达中心Confirmationofstudymaterialsandsuppliesatsite
•研究者文件夹Investigator’StudyFile
•试验基本文件Protocol,CRF,ICF,Sourcedocument,Subjectdiary
•研究药物包括签收单Studydrug,includingreceipt
•试验所需设备或材料StudySupplies/materials
•应急信件或盲底EmergencyEnvelopand/orRandomizationList
会中讨论DiscussedintheMeeting
1.受试者入组SubjectsRecruitment
–本中心计划入组数SitePlannedSubjectRecruitmentNo.:
–预期入组期限ExpectedRecruitmentDuration:
2.研究程序StudyProcedure
–研究时间StudyTimeline
–研究方案SignedProtocol
Version/Date:
–伦理批准的知情同意书
–ICFApprovedbyEC
–病例报告表CRF
–原始病历Sourcedocument
–受试者日记SubjectDiary
–受试者评估程序SubjectAssessmentProcedure
–样本处理和保存BiologySampleHandlingandStorage
–中心实验室程序CentralLabProcedure(ifapplicable)
–受试者退出SubjectWithdrawal
–应急信封/随机程序EmergencyEnvelop/RandomizationProcedure
3.药物管理StudyDrugManagement
–药物储存DrugStorage
–药物接收、发放和计数DrugReceipt,DispensingandAccountability
–药物归还/销毁DrugReturn/Destruction
–紧急破盲程序EmergencyUnblindingProcedure
4.安全性问题SafetyIssues
–不良事件记录AdverseEventRecording
–严重不良事件的记录、报告和跟踪
–SAERecording,ReportingandFollow-up
–发生怀孕的报告程序ProceduresincaseofPregnancy
5.数据记录DataRecording
–CRF的填写和更改CRFCompletion&
Correction
–差异报告处理DiscrepancyReporthandling
6.试验文档StudyDocuments
–研究者文件夹以及存档Investigator’sStudyFile&
Archiving
7.任务分配及授权TaskAuthorization
–完成方案签字页SignatureSheetforProtocol
–完成任务授权表TaskAuthorizationFormTaskAuthorizationForm
启动会主要内容记录
(请根据试验项目要求进行记录,可附页)
附件:
1、会议签到表
2、方案签字页(研究者签名样张)
3、任务授权表
会议签到表
MeetingAttendanceRecord
方案号
ProtocolNo.:
方案名称
StudyTitle:
会议名称
MeetingName:
启动会
会议地点
MeetingVenue:
会议时间
MeetingTime:
申办者
Sponsor:
参加人员签名
NameofParticipants
工作单位
Company/Hospital
职称
Title
联系电话
Tel
传真
Fax
电子邮箱
方案签字页(签名样张)
Investigator’sSignatureSheetforProtocol
ProtocolNo:
方案版本/日期
ProtocolVersion&
date:
研究题目
中心编号
StudyCenterNo:
研究中心
StudyCenter:
主要研究者
PI:
监查员
Monitor:
Ihavethoroughlyreadandreviewedthestudyprotocol.Havingreadandunderstoodtherequirementsandconditionsofthestudyprotocol.Iagreetoconductorinstructthisprojectandfollowthetimescheduleindicatedinprotocol.IunderstandthatitisprotocolviolationifrevisetheprotocolwithoutapprovalfromEthiccommittee.
我已完全阅读了研究方案,并明白了方案的要求。
我同意遵循方案及时间规程来执导该项临床研究。
我亦知道没有伦理委员会的批准就修改方案是违反方案的。
IagreetoperformtheclinicalstudyaccordingtotheChineseGoodClinicalPracticeprinciplesandregulatoryauthorityrequirementsforsourcedocumentverificationandauditing/inspectionofthestudy.
我同意按中国GCP原则进行临床试验,并接受法规部门对原始资料的核查和对临床试验的稽查/视察。
Iagreetousethestudymaterial,includingmedication,onlyasspecifiedintheprotocol.
我同意只应用方案所规定的试验用品包括研究药物。
SignatureofInvestigatorandStudyGroup研究小组签字
姓名正楷
PrintedName
Date
签名
Signature
任务分配及授权表
StudyCenterTaskAuthorizationForm
ProtocolNo.
研究者
Investigator
Monitor
StudyTitle
StudyCenter
CenterNo.
职责Responsibility
1.主要研究者
2.PrincipalInvestigator
3.合作研究者
4.Co-investigator
5.知情同意书
6.InformedConsentForm
7.体检/病史
8.PhysicalExam/History
9.病人入选排除
10.PatientInc/ExclCriteria
11.CRF填写及更改
12.CRFEntryandCorrection
13.伦理联系
14.ECContacting
15.严重不良事件报告
16.SAEReporting
17.病人联系/随访
18.SubjectContact/FollowUp
19.药物管理
20.DrugManagement
21.样本管理
22.BiologySampleManagement
23.应急信封
24.EmergencyEnvelop
25.其它,请描述:
26.Others,pleasespecify:
姓名正楷PrintedName
科室
Dept.
任务分配
Task(listtheNo.intheaboveresponsibility)
签名及姓名缩写
Signature&
Initials
授权日期
Datewhenauthorized
主要研究者签名
Investigator’sSignature:
日期Date:
//
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 临床试验 启动 会议纪要
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
