 普陀补习班 新王牌第二学期经典问题解析.docx
普陀补习班 新王牌第二学期经典问题解析.docx
- 文档编号:20123601
- 上传时间:2023-04-25
- 格式:DOCX
- 页数:13
- 大小:205.41KB
普陀补习班 新王牌第二学期经典问题解析.docx
《普陀补习班 新王牌第二学期经典问题解析.docx》由会员分享,可在线阅读,更多相关《普陀补习班 新王牌第二学期经典问题解析.docx(13页珍藏版)》请在冰豆网上搜索。
普陀补习班新王牌第二学期经典问题解析
第二学期经典问题解析
问题1:
酸性、碱性、中性溶液的鉴别
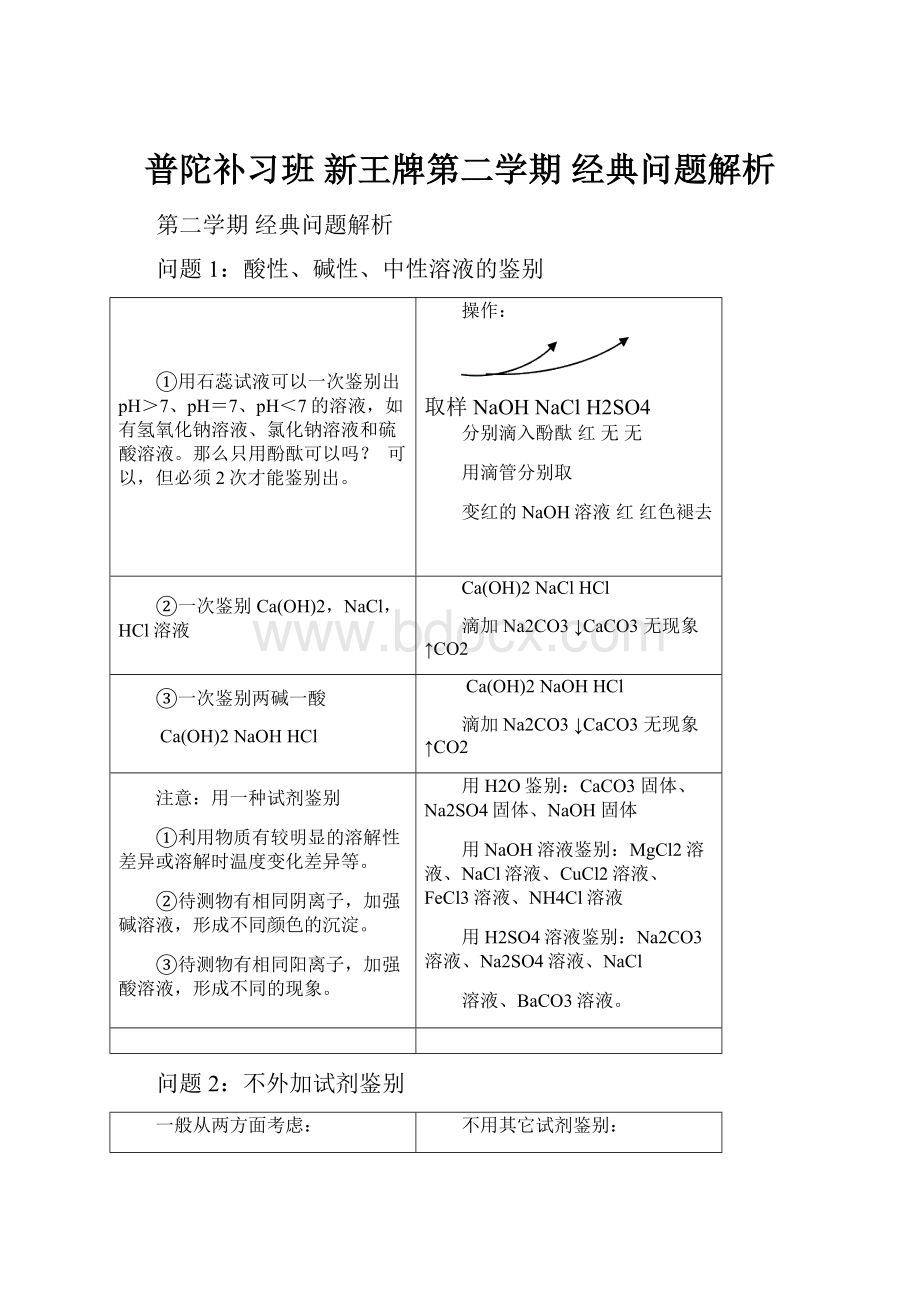
①用石蕊试液可以一次鉴别出pH>7、pH=7、pH<7的溶液,如有氢氧化钠溶液、氯化钠溶液和硫酸溶液。
那么只用酚酞可以吗?
可以,但必须2次才能鉴别出。
操作:
取样NaOHNaClH2SO4
分别滴入酚酞红无无
用滴管分别取
变红的NaOH溶液红红色褪去
②一次鉴别Ca(OH)2,NaCl,HCl溶液
Ca(OH)2NaClHCl
滴加Na2CO3↓CaCO3无现象↑CO2
③一次鉴别两碱一酸
Ca(OH)2NaOHHCl
Ca(OH)2NaOHHCl
滴加Na2CO3↓CaCO3无现象↑CO2
注意:
用一种试剂鉴别
①利用物质有较明显的溶解性差异或溶解时温度变化差异等。
②待测物有相同阴离子,加强碱溶液,形成不同颜色的沉淀。
③待测物有相同阳离子,加强酸溶液,形成不同的现象。
用H2O鉴别:
CaCO3固体、Na2SO4固体、NaOH固体
用NaOH溶液鉴别:
MgCl2溶液、NaCl溶液、CuCl2溶液、FeCl3溶液、NH4Cl溶液
用H2SO4溶液鉴别:
Na2CO3溶液、Na2SO4溶液、NaCl
溶液、BaCO3溶液。
问题2:
不外加试剂鉴别
一般从两方面考虑:
①利用某些物质的特殊性质(如颜色、气味、溶解性等)首先鉴别出来,然后再利用该试剂“顺藤摸瓜”去鉴别其它物质。
②采用一种试剂与其它物质相互反应时出现不同的现象进行综合分析。
不用其它试剂鉴别:
Na2SO4溶液、MgSO4溶液、CuSO4溶液、NaOH溶液。
④无现象③白色沉淀①蓝色溶液②蓝色沉淀
FeCl3溶液、H2SO4溶液、NaCl溶液、NaOH溶液。
不用其它试剂鉴别:
BaCl2溶液、Na2SO4溶液、HCl溶液、Na2CO3溶液。
↓—↓↓————↑↓—↑
下列是否能不用其它试剂鉴别:
A.NaOH、MgCl2、KCl、NaCl
B.K2CO3、BaCl2、HNO3、H2SO4
C.H2SO4、HCl、Na2CO3、NaNO3
D.AgNO3、HCl、HNO3、NaCl
现有甲、乙、丙、丁四种无色溶液,分别是碳酸钠、硫酸、氯化钡、盐酸中的一种。
将它们两两混合,部分现象记录于下表,试推断甲、乙、丙、丁分别是
甲
乙
丙
丁
乙
无明显现象
有气体产生
有沉淀生成
丙
有气体产生
有气体产生
有沉淀生成
A.Na2CO3H2SO4HClBaCl2B.H2SO4Na2CO3BaCl2HCl
C.HClH2SO4Na2CO3BaCl2D.HClBaCl2H2SO4Na2CO3
问题3:
鉴别NaCl、Na2SO4、Na2CO3溶液
方法一
NaCl
Na2SO4
Na2CO3
先Ba(NO3)2
—
BaSO4白↓(不溶于酸)
BaCO3白↓(溶于酸)
后HNO3
白↓不消失
产生↑(CO2),白↓消失
注:
后加HNO3是为了区别白↓BaSO4是还是BaCO3
方法二
NaCl
Na2SO4
Na2CO3
先HNO3
—
—
产生↑(CO2)
后Ba(NO3)2
(酸化的Ba(NO3)2)
—
白↓(BaSO4)
注:
先加HNO3是为了检验并除去CO3根,以便后续确定白↓为BaSO4
问题4:
三个酸根的检验顺序问题
证明混合溶液中存在NaCl、Na2SO4、Na2CO3
注意:
①加入的试剂不能包含需要检验的“部分”。
②检验的顺序一般为碳酸根、硫酸根、盐酸根(用硝酸银检验盐酸根时,溶液中只能有硝酸根存在,不能有碳酸根、硫酸根、氢氧根,因为会产生干扰)。
问题5:
酸碱混合后的pH问题
一元酸与一元碱NaOH+HCl
1mol1mol
①若两者等mol混合1mol1mol所得溶液pH=7
②若两溶液等质量m等浓度C%
<
所得溶液pH<7
(即所含溶质质量相等)(因为盐酸过量)
二元酸与一元碱2NaOH+H2SO4
2mol1mol
①若两者等mol混合2mol2mol所得溶液pH=7
(因为硫酸过量)
2NaOH+H2SO4
2mol1mol
换算成质量比为8098(此时两者恰好完全反应)
②若两溶液等质量m等浓度C%98<98(假设所给溶质都为98克)
(即所含溶质质量相等)所得溶液pH>7
(因为氢氧化钠过量)
酸碱恰好中和,所得溶液pH不一定等于7
如:
Cu(OH)2+H2SO4→CuSO4+2H2O(还包括)
强酸弱碱盐,所以所得溶液其pH<7
问题6:
物质是否共存问题
溶液中的溶质是否共存,取决于这些物质相互之间是否发生反应,只有相互之间不发生反应的才能共存。
相互之间要发生反应的部分:
H——OHH——CO3
Cu——OHCa——CO3
Mg——OHBa——CO3
Fe——OHBa——SO4
NH4——OHAg——Cl
下列溶液是否共存?
Na2SO4、Ba(OH)2、HCl
MgCl2、NaOH、Na2CO3
HCl、Na2CO3、CaCl2
FeSO4、Ba(OH)2、HNO3
KNO3、Na2SO4、CuCl2、Mg(NO3)2
问题7:
证明A、B、C三种金属“活泼性”的问题(中间原则)
①两端单质,中间盐溶液
AB盐C
②两端盐溶液,中间单质
A盐BC盐
③活泼单质,不活泼盐溶液
ABC盐
问题8:
金属与酸反应,产生氢气的“量”的问题
(1)等质量的不同金属与足量的同种浓度的同种酸反应,所产生H2质量的关系
例:
将等质量的Mg、Al、Zn、Fe分别与足量相同浓度的硫酸反应,所产生H2质量(物质的量越大,其质量或体积都越大)的关系.
解:
假设金属的质量均为m克,产生的氢气的物质的量分别是X、Y、Z、W。
根据化学方程式得:
Mg+H2SO4→MgSO4+H2↑
11
X=
mol
2Al+3H2SO4→2Al2(SO4)3+3H2↑
23
Y=
mol
Fe+H2SO4→FeSO4+H2↑
11
Z=
mol
Zn+H2SO4→ZnSO4+H2↑
11
W=
mol
由此可得:
Y>X>Z>W
即产生质量Al>Mg>Fe>Zn
(2)等molHCl(或等质量等浓度的盐酸)+过量Mg、Al、Zn、Fe
金属足量,酸完全参加反应。
等质量等浓度的盐酸中氢元素的质量是相等的,因而得到的氢气质量也相等(因为氢气的氢来源于酸中的氢)。
HCl——H2
1mol0.5mol
2mol1mol
…………
10mol5mol
(3)等molMg、Al、Zn、Fe+过量HCl
因为:
只有2Al—3H2是2:
3,
而Mg—H2Fe—H2Zn—H2均为1:
1
所以图形如下:
问题9:
用CuO、H2SO4、Fe冶炼Cu的问题
方法一:
CuO+H2SO4→CuSO4+H2O(烧杯、玻璃棒——溶解)
Fe+CuSO4→FeSO4+Cu(漏斗、铁架台——过滤)
方法二:
Fe+H2SO4——→FeSO4+H2↑(制H2装置)
CuO+H2
Cu+H2O(H2还原CuO装置)
评价:
方法一更好。
操作简单,安全,制取相同质量的Cu,所用原料(Fe和H2SO4)少。
因为方法二中,有部分H2用于“早出晚归”,用1molH2实际还原的CuO小于1mol。
问题10:
金属单质与混合盐溶液的置换问题
将一定量的Fe粉加入Cu(NO3)2和AgNO3的混合溶液中充分反应后过滤,滤渣和滤液中可能出现的情况如下:
说明:
①金属之间的置换顺序是两者距离越远越优先反应(“距离产生美”)
②相互能反应的成分一定不共存。
问题11:
金属的回收问题
1、某工厂排放的废液中含有Zn(NO3)2和AgNO3,为回收金属Ag,设计如下方案:
(1)先在废液中加过量的锌粉,过量的目的是。
(2)滤液B中含有;
2、某小组同学从实验室废液中提取到了银、铜和铁的混合物。
为了得到铜和银,他们继续对该混合物进行如下操作:
①滤液B中溶质成分有。
②写出CuO与H2SO4反应的化学方程式。
③滤液D中溶质的成分有(填化学式)。
④含有硫酸亚铁的滤液有(填框图中的字母)。
问题12:
混合物的提纯(除杂质)问题
除杂试剂要过量,过量试剂要除尽。
粗盐NaCl中常含有CaCl2,MgCl2,Na2SO4等杂质。
现要从粗盐提纯得到较纯的氯化钠晶体,其操作过程如下:
先将粗盐加水配成溶液。
说明;以上是每一步只除去一种杂质。
其中第①步与第②步的顺序可以颠倒。
(其中,也可以用Ba(OH)2代替NaOH和BaCl2。
)
问题13:
证明混合物中的成分问题
(1)NaOH固体敞口放置在空气中:
如何证明属于哪种情况?
只需证明NaOH是否存在。
注意;①不能用指示剂,因为Na2CO3、NaOH都是碱性的。
②不能用CuSO4溶液,因为
Cu(OH)2、CuCO3都是蓝色沉淀。
操作方法
(2)生石灰干燥剂放置在空气中:
固体成分:
①CaO或②CaO和Ca(OH)2或③Ca(OH)2和CaCO3或④CaCO3
操作
现象
结论
取样,加一定量水
若无放热现象
没有CaO存在
静止片刻,取上层清夜,滴加酚酞
若溶液变红
证明存在Ca(OH)2
取下层固体,滴加过量盐酸
若有气泡产生
证明还存在CaCO3
没有变质部分变质完全变质
(3)电解食盐水生产氢氧化钠固体时获得的产品:
操作
现象
结论
取样配成溶液,加过量HNO3
若有气泡产生
证明存在Na2CO3
继续滴加AgNO3溶液
若产生白色沉淀
证明还存在NaCl
产品中一定存在NaOH,可能存在NaCl、Na2CO3。
(因而NaOH不需证明)
问题:
如何证明混合溶液中NaOH、NaCl、Na2CO3都存在?
(4)一包白色固体的成分判断;
有一包白色固体,可能含有Na2CO3、Na2SO4、CaCO3、Cu(NO3)2、KCl、CaCl2。
进行如下操作;
第一步;
取样,加水,得无色溶液
获得结论:
①无Cu(NO3)2,因为其是蓝色
②无CaCO3,因为其是白色沉淀
③Na2CO3和CaCl2不能同时存在,因为两者不能共存(即需要考虑是否有不能共存的问题)
第二步;
继续在溶液中滴加Ba(NO3)2,有白色沉淀,再加稀硝酸,沉淀不消失。
想一想;这步为什么不用BaCl2?
获得结论:
①一定有Na2SO4
②一定没有CaCO3,Cu(NO3)2,Na2CO3,CaCl2。
③可能含有KCl。
问题;如何证明KCl是否存在?
方法一;用焰色反应。
取原溶液进行焰色反应,透过鈷玻璃看,焰色为紫色,证明存在KCl。
方法二;在原溶液中加过量Ba(NO3)2(目的:
证明并除尽Na2SO4,以免干扰后续的检验),过滤后,再加AgNO3,若还有白色沉淀,证明存在KCl。
注意;①在原溶液中不能直接加AgNO3(因为是在Na2SO4中鉴别KCl)。
②在整个过程的第二步中加的是Ba(NO3)2而非BaCl2,目的不引入“Cl”。
问题14:
试剂加入混合物溶液中的反应顺序问题
①将Ba(OH)2溶液加入HCl和Na2SO4混合溶液中
②将HCl溶液加入NaOH和Na2CO3混合溶液中
③将Ba(OH)2溶液加入CuCl2和Na2SO4混合溶液中
④将Na2CO3溶液加入HCl和CaCl2混合溶液中
⑤将Ba(OH)2溶液加入HCl和MgSO4混合溶液中
问题15:
用实验室制取的氢气还原铜的氧化物来确定该氧化物的组成比问题
用Zn和HCl制出的H2来还原铜的氧化物,确定该铜的氧化物的组成比。
实验步骤:
计算;若原铜的氧化物质量=7.2克,干燥剂在反应后增重=0.9克
则生成的H2O的质量=0.9克,即0.05molH2O其中含氧原子也是0.05mol,即0.8克。
而水中的氧元素就是铜的氧化物中的氧元素。
∴MCu=M铜的氧化物-MO=7.2-0.8=6.4克
∵MCu:
MO=6.4:
0.8=8:
1
根据化学式CuxOy得
∴铜的氧化物的化学式为Cu2O
注意;①若实验过程中去掉碱石灰,对实验结果会产生何影响?
空气中的水蒸气进入干燥剂中,使测出的“生成的H2O的质量”偏大。
②若AgNO3溶液和浓H2SO4互换位置,对实验结果会产生何影响?
从AgNO3溶液中带出的水蒸气进入干燥剂,使MH2O偏大,导致MO偏大,而
M铜的氧化物的质量不变,则MCu偏小,最终使MCu:
MO也偏小。
问题16:
天平的平衡问题
在托盘天平两端的烧杯中分别放等质量等浓度的盐酸,此时天平平衡。
若再在天平左右两边烧杯中分别加入等质量的Zn(相对原子质量65)和Fe(相对原子质量56),则天平的指针将如何偏转?
①若金属过量,则等mol的HCl中产生mol的H2因而天平的指针将依然平衡。
②若HCl过量,则等m的Fe和Zn,产生H2多的是Fe,跑掉的H2越多,留在烧杯中的就越少,因而天平的指针将偏向Zn一边。
③若不清楚量的相对大小则无法判断。
问题17:
合金的问题
有5克铁和另一种金属的合金与足量的稀硫酸反应,产生H20.2克,则另一种金属是?
R+H2SO4→RSO4+H2↑(考虑生成+2价的盐)
11
得0.1mol有0.1mol
所以;
Cu(不产生H2)Mg(24<50<56)Zn(56,65均>50)Al(等质量情况下产生H2最多)
×√×√
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 普陀补习班 新王牌第二学期 经典问题解析 普陀 补习班 王牌 第二 学期 经典 问题 解析
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #全自动电容电感测试仪.docx
#全自动电容电感测试仪.docx
