 中考化学每日一练中考化学最后冲刺Word文件下载.docx
中考化学每日一练中考化学最后冲刺Word文件下载.docx
- 文档编号:19890016
- 上传时间:2023-01-11
- 格式:DOCX
- 页数:24
- 大小:635.94KB
中考化学每日一练中考化学最后冲刺Word文件下载.docx
《中考化学每日一练中考化学最后冲刺Word文件下载.docx》由会员分享,可在线阅读,更多相关《中考化学每日一练中考化学最后冲刺Word文件下载.docx(24页珍藏版)》请在冰豆网上搜索。
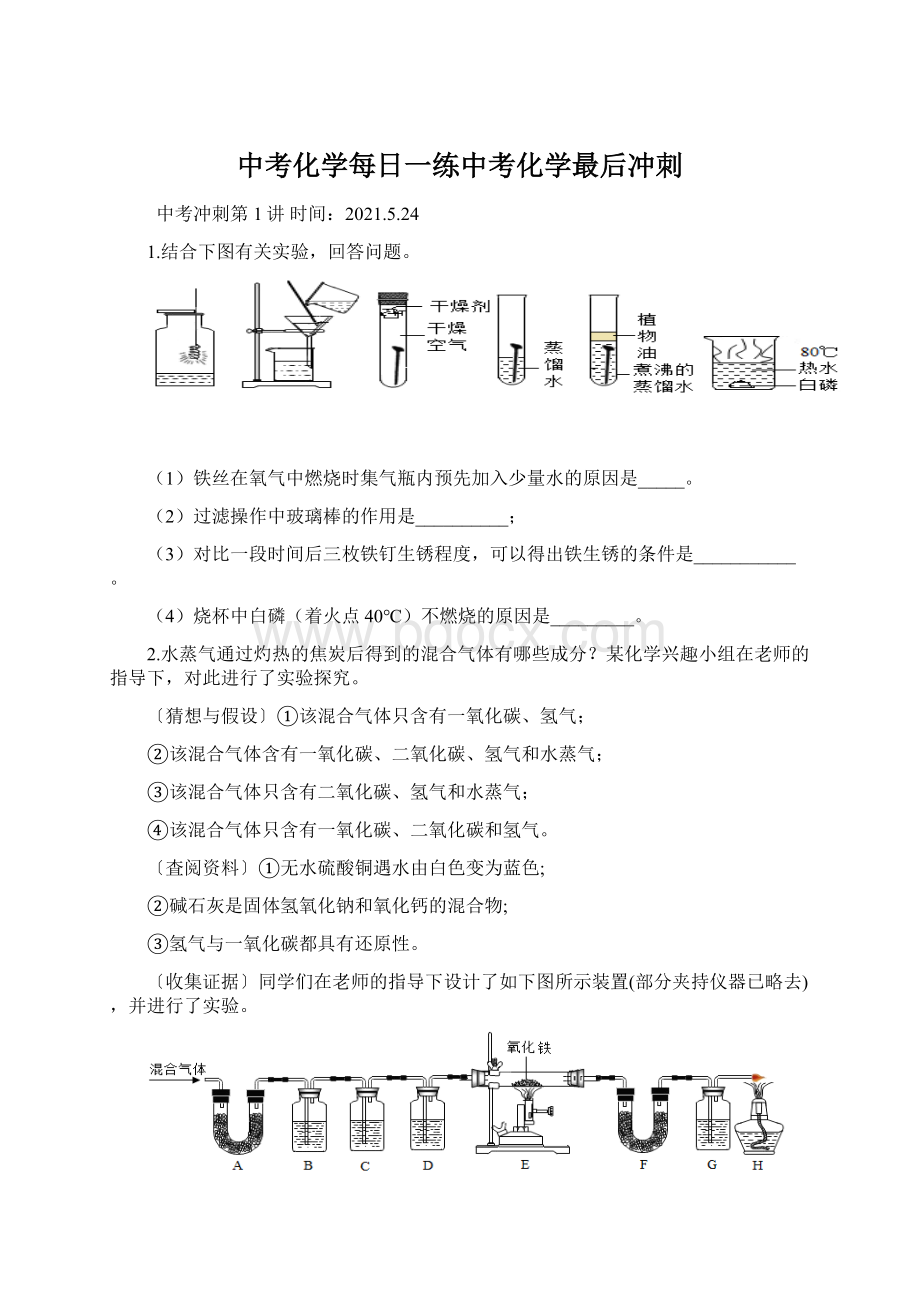
1.综合复习时,同学们又来到化学实验室进行实验,加强对酸的化学性质的整体认识。
他们将适量的稀盐酸分别滴加到六只试管中进行实验(如图所示),请回答下列问题:
(1)上述六只试管中有气泡产生的是_________________(填序号),相关反应的化学方程式为_______(只写出一个)。
(2)能证明“C试管中发生了化学反应”的现象是_________________________。
(3)有一只试管中的物质不与稀盐酸反应,原因是______________________。
2.硝酸钾和氯化铵的溶解度曲线如图1所示。
某化学兴趣小组的同学进行了如图2所示实验,R是硝酸钾、氯化铵中的一种物质。
(1)硝酸钾和氯化铵两种物质的溶解度均随温度的升高而___________。
(2)由图1可知:
t1℃时,氯化铵饱和溶液中溶质与溶液的质量比为_________。
(3)结合图1和图2判断:
烧杯内的物质R是________。
①、②、③三种情况下,一定是饱和溶液的有____(填序号)。
3.【查阅资料】③在化学反应中,金属钴Co和铁一样,也能与稀盐酸发生反应放出氢气,反应的化学方程式为_____
___________________;
钴在氧气中燃烧生成Co3O4,化学方程式为_________________________________。
钴元素有着广泛的用途:
钴及其化合物在材料生产、化工生产、医疗中都有着广泛的应用。
钴在电池制造中需求量增长很快,钴酸锂(已知:
化学式为LiCoO2,锂元素化合价为+1)常用作手机电池的正极材料,其中钻元素的化合价为____________。
【深入探讨】
【产生问题】既然钴与铁的单质具有相似的性质,那么两种元素的化合物是否也有相似的化学性质?
【设计并实验验】
(1)根据所学知识,同学们已知下列反应可以进行,并进行实验:
观察记录实验现象:
氧化亚铁为黑色固体;
实验a中,随着稀盐酸的加入,黑色固体逐渐溶解,溶液呈现浅绿色;
实验b中,加入氢氧化钠溶液后出现白色沉淀,静置在空气中,沉淀物颜色发生变化,最后变为红褐色。
【查阅资料得知:
原因是溶液中的Fe(OH)2遇空气中的氧气生成Fe(OH)3】
(2)同学们欲探究钴元素化合物的性质,设计并进行了如下实验:
请你依据实验现象,完成下列问题:
I.实验①中,取少量灰黑色的氧化钴放入试管中,加入稀盐酸,固体被溶解,溶液呈红色,写出反应的化学方程式________________。
另取一支试管加入少量氧化钴,滴入浓盐酸,固体被溶解溶液呈绿色。
说明反应后钴离子在溶液中呈现的颜色与加入酸的____________有关。
Ⅱ.实验②中,加入氢氧化钠溶液,出现青蓝色沉淀。
将试管静置在空气中,沉淀物颜色发生变化,最终变为棕色,试推测沉淀物颜色变化可能与空气中的____________有关。
通过实验探究,同学们得出结论:
铁和钴两种元素的化合物化学性质相似。
中考冲刺第3讲时间:
2021.5.26
1.某反应的微观示意图如下,该反应的化学方程式是__________,其中由原子直接构成的物质是___________。
请结合图示,从微观的角度谈一下对化学反应的认识__________。
2.下图为高炉冶铁、炼钢并用生产的钢来探究白铜成分的流程图。
(已知硫酸镍的化学式为NiSO4)
(1)用高炉冶铁的主要反应原理是____________(用化学方程式表示)。
(2)分析流程图,三脱装置中发生反应的基本反应类型______________。
(3)向精炼炉中吹入氩气使钢水循环流动,各成分均匀混合,相当于化学实验中_________(填一种仪器的名称)的作用。
(4)铁与镍相比,铁的金属活动性_________镍(选填“>
”、“=”或“<
”),判断依据是__________(用化学方程式表示)。
(5)通过以上信息,得出白铜的成分是__________,其硬度比纯铜____________(填“大”或“小”)。
3.化学是一门以实验为基础的自然科学。
根据所学知识回答以下问题:
(1)实验室制取二氧化碳,应选用以下药品①块状石灰石②碳酸钠粉末③稀盐酸④稀硫酸中
___________(填序号)。
现有大理石粉末和稀硫酸,你认为_____________(填“能”或“否”)用于实验室制取二氧化碳。
(2)实验室有以下装置,根据要求回答问题:
Ⅰ.写出标号仪器的名称①__________,②_____________。
Ⅱ.对比装置B、C,有错误的是____________(填序号,下同)。
Ⅲ.实验室要制取二氧化碳应选择的发生装置是______________,收集装置是______________;
利用制取二氧化碳的发生和收集装置还能制取另外一种常见气体,利用此装置制取该气体的化学方程式是______________。
Ⅳ.下图是同学们进行“铁丝在氧气中燃烧的性质实验”时的几种操作方式,更能提高实验成功率的方式是_________(填序号)。
(3)有的同学完成上述实验后,提出“铁丝能否在二氧化碳中燃烧呢?
”,他们设计了如下方案:
(已知在点燃的条件下,镁带能在二氧化碳中剧烈燃烧。
)
方案①:
将弯成螺旋状的细铁丝系上一根火柴,点燃火柴,待火柴快燃尽时,插入装有二氧化碳的集气瓶中,观察铁丝能否被引燃。
方案②:
将弯成螺旋状的细铁丝系上一段镁带,点燃镁带,待镁带快燃尽时,插入装有二氧化碳的集气瓶中,观察铁丝能否被引燃。
你认为方案___________(填①或②)更为科学,理由是______________。
中考冲刺第4讲时间:
2021.5.27
1.某兴趣小组在实验室发现盛有固体氢氧化钠的试剂瓶破裂瓶盖处有“白毛”状物质(如图),根据所学知识,他们推断“白毛”状固体物质中含有碳酸钠,依据是。
他们取5g白色固体,加水配成20g溶液倒入烧杯中,将40g氯化钡溶液分成四等份,分4次加入烧杯中,充分反应后测得数据如下表:
实验次数
1
2
3
4
加入氯化钡溶液的质量/g
10
烧杯中所得溶液的质量/g
28.03
36.06
44.09
54.09
(1)第次实验,加入
氯化钡与碳酸钠恰好完全反应。
(2)求5g白色固体中碳酸钠的质量。
(写出计算过程,结果保留两位小数)
2.在两只烧杯中分别放入相同质量的镁、锌两种金属,然后向两只烧杯中分别倒入相同质量、相同质量分数的稀硫酸,反应产生氢气的质量与消耗硫酸的质量关系如图。
综合以上信息得到以下结论,合理的是()
A.从图象可以看出,金属镁比金属锌的活动性强
B.若两种金属都有剩余,二者得到的氢气质量相同
C.若硫酸有剩余,二者得到氢气的质量相同
D.若两种金属完全溶解,二者消耗硫酸的质量相同
3.16.白铜(Cu-Ni)是工业上常用的一种合金,金属镍(Ni)的金属活泼性与铁相似,且化合价显+2价。
为测定20g某白铜样品中镍的质量,设计了如下实验:
试问:
(1)将白铜研碎的目的是。
(2)白铜样品中镍的质量g。
(3)所用稀硫酸中溶质的质量分数(写出计算过程)。
中考冲刺第5讲时间:
2021.5.28
1.某未知溶液,可能含有Na+、Cu2+、Ba2+、SO42-、Cl-中
几种,为确定溶液中含有的离子,实验如下:
①取未知溶液2~3mL于试管中,滴加足量BaCl2溶液,有白色沉淀生成,静置;
②取①中上层清液,滴加AgNO3溶液,有白色沉淀生成;
③另取未知溶液2~3mL于试管中,滴加NaOH溶液,有蓝色沉淀生成。
分析实验过程,回答:
(1)溶液中一定存在的离子是__________________。
(2)溶液中一定不存在的离子是__________________。
(3)溶液中可能存在的离子是__________________。
2.某实验探究小组为验证氢气的还原性,在教师指导下:
【查询资料】Ⅰ.反应原理:
Ⅱ.无水硫酸铜是白色粉末状固体,遇水变蓝色
【实验过程】
①仪器a的名称是____________,仪器b的名称是_______________。
②写出A装置中发生反应的化学方程式_______________。
③装置D处硬质玻璃管中观察到的实验现象是_______________。
④装置B的作用是_______________,装置E的作用是_______________。
⑤氢气是一种可燃性气体,为确保实验安全。
实验中,需要持续通入一段时间氢气,再点燃D处酒精灯,这样操作的目的是_______________。
3..小雨同学为验证镁、铁、锌三种金属的活动性,进行了下图所示实验:
①实验中,小雨观察到的现象是_____________,由此得出三种金属的活动性:
镁>
锌>
铁;
②小明还补充了铁片与硫酸铜溶液反应的实验,实验中观察到的现象是______________,有关反应的化学方程式为____________。
由此得出铁、铜两种金属的活动性:
铁_____________铜(填“>
”“=”“<
”)。
中考冲刺第6讲时间:
2021.5.31
1.化学课堂上学生探究了如图所示的几个实验:
(1)图1实验中,蜡烛熄灭的原因是__________。
(2)图2实验中,使紫色干花(用石蕊溶液浸泡过)变红的物质是____(填化学式)。
(3)图3实验中,滴入氢氧化钠浓溶液后,可观察到的实验现象是________,发生反应的化学方程式是_____。
2.生铁是由铁和碳组成的合金。
某化学兴趣小组的同学为了测定某稀盐酸中溶质的质量分数,取一定量的该生铁样品,分四次加入稀盐酸200g,充分反应后,实验数据如下:
次数
稀盐酸质量/g
50
氢气质量/g
0.2
m
0.1
请根据有关信息完成下列问题:
(1)m=_____。
(2)该稀盐酸中溶质的质量分数。
(请写出计算过程,计算结果精确到0.1%)
3.(双选题)有一包固体样品,可能由氢氧化钠、硫酸钠、硝酸镁、硝酸铜、碳酸钙中的一种或几种物质组成。
为确定该样品的组成,某兴趣小组同学取适量样品进行探究。
探究过程如下:
根据以上信息判断,下列说法正确的是
A.白色沉淀a的成分是碳酸钙
B.该样品中一定存在氢氧化钠、硝酸镁、硫酸钠、碳酸钙,一定不存在硝酸铜
C.该样品中一定存在硫酸钠、碳酸钙、硝酸镁,一定不存在硝酸铜和氢氧化钠
D.若步骤①②保持不变,用硝酸钡溶液代替步骤③中的氢氧化钡溶液,则不需要进行步骤④的探究,也能确定该样品的组成
4.生铁和钢都是铁和碳的合金,生铁含碳量为2%~4.3%,钢含碳量为0.03%~2%,化学兴趣小组的同学为确定该铁合金是生铁还是钢,他们取11.5g铁合金样品盛放到锥形瓶中,将100g稀盐酸分成5等份,分5次加入锥形瓶,每次待充分反应后记录实验数据。
实验数据整理如下表所示:
加盐酸前
第1次
第2次
第3次
第4次
第5次
加入稀盐酸的质量(g)
20
锥形瓶内物质的总质量(g)
11.5
31.4
71.2
91.1
111.1
【查阅资料】碳不与稀盐酸反应。
请回答下列问题:
(1)根据质量守恒定律,该反应中生成气体的总质量为。
(2)实验数据表中m的值为。
(3)请通过计算确定该铁合金是生铁还是钢(写出计算过程,计算结果保留到0.1%)。
中考冲刺第7讲时间2021.6.1
1.实验室制取气体时需要的部分装置如下图所示,请回答下列问题。
【信息】二氧化碳不易溶于饱和碳酸氢钠溶液。
(1)实验室中可用过氧化氢溶液与二氧化锰制取氧气,反应的化学方程式为_____,应选用的发生装置是_____(选填装置字母序号)。
(2)实验室中用石灰石和稀盐酸制取一瓶干燥、纯净的二氧化碳气体,所选装置的连接顺序为:
气体发生装置→____→_______→D(选填装置字母序号)。
(3)确定实验室制取气体的反应原理时,下列因素中不需要考虑的是___(选填字母序号)。
A药品容易获得,能生成所要制取的气体
B反应条件易于控制,反应速率适中
C操作简便易行,安全可靠,节能环保
D所要制取气体的颜色和气味
2.回收利用废旧金属具有重要意义。
某机械厂金属废料的成分是Zn、Cu、ZnO和CuO,某化学小组利用该金属废料回收铜并制取氧化锌和硫酸铜。
请回答下列问题。
【活动一】回收铜并制取氧化锌,实验方案如下:
(1)步骤I所得滤液a中溶质的成分是____(填写化学式)。
(2)步骤III加入试剂甲的名称是______。
(3)步骤IV加入适量NaOH溶液的目的是________。
【活动二】利用活动一回收的铜制取硫酸铜,设计方案如下:
方案A:
方案B:
【信息】
(4)方案A中氧化铜与稀硫酸反应的化学方程式为____。
(5)小组同学从绿色化学的视角分析方案B不合理,理由是____(写出一条即可)。
中考冲刺第8讲2021.6.2
1.新型冠状病毒肺炎疫情防控期间,要合理搭配饮食,以保证基本营养素的均衡摄取,增强身体免疫力;
要合理使用消毒剂进行杀菌消毒。
(1)下列物质富含蛋白质的是______(填写字母标号)。
A水果、蔬菜B花生油、奶油C纯牛奶、蛋清D米饭、馒头
(2)下列物质常用于制作消毒剂,其中属于氧化物的是________(填写字母标号)。
A过氧乙酸(CH3COOOH)B二氧化氯(ClO2)
C苯酚(C6H6O)D次氯酸钙[Ca(ClO)2]
(3)体积分数为75%的酒精常用于手和皮肤消毒。
因易燃,使用时要注意远离火源。
乙醇燃烧的化学方程式是____________。
(4)“84”消毒液的有效成分是次氯酸钠(NaClO),适用于物体表面以及室内环境等方面的消毒。
NaClO中氯元素的化合价是______。
2.现有含杂质氯化镁的氯化钾,欲除去杂质,配制氯化钾溶液,操作流程见下图。
(1)加入氢氧化钾溶液,反应的化学方程式是________。
(2)过滤。
有关过滤操作的叙述不正确的是_______(填写字母标号)。
A用少量水润湿滤纸,并使滤纸与漏斗壁之间留有气泡
B漏斗下端的管口要紧靠烧杯内壁
C玻璃棒要靠在三层滤纸的一边
D滤纸边缘要低于漏斗口,液面要低于滤纸边缘
(3)蒸发。
把液体倒入蒸发皿,进行加热,在加热过程中,用玻璃棒不断搅拌,目的是______。
(4)天平调零。
如图所示,先把游码移至零刻度线处,如果指针静止时偏向右侧,则应该把右端的平衡螺母往_____旋动(填写“左”或“右”)。
(5)配制溶液。
称量氯化钾固体的质量和量取水的体积时,天平示数(单位:
克)和量筒读数(单位:
毫升)分别如图所示,则所配氯化钾溶液中溶质的质量分数是_______。
(水的密度可近似看做1g/cm3)
中考冲刺第9讲2021.6.3
1.某化工产品的成分是碳酸钙、氢氧化钙和硫酸钡,现取该化工产品样品20g放入锥形瓶内,向其中加适量水,振荡,然后再向锥形瓶中滴加溶质质量分数为10%的稀盐酸,反应生成二氧化碳的质量与加入稀盐酸的质量关系如图所示。
(1)该样品中钙元素的质量分数是_____(只填空,不列式计算)。
(2)计算该样品中氢氧化钙的质量。
2.水是生命之源,也是实验室常用的溶剂。
(1)生活中既能降低水的硬度,又能杀菌消毒的方法是_______。
(2)含氮物质进入水中会使水质恶化,这里的“氮”是指_______(填序号)。
A.原子
B.分子
C.元素
(3)在某温度下,分别向盛有等质量蒸馏水的两烧杯中逐渐加入固体溶质甲和乙,图中x表示所加固体的质量,y表示溶液中溶质与水的质量比。
a点对应的乙物质的溶液为_______(选填“饱和”或“不饱和”)溶液;
该温度时甲物质的溶解度为____g。
3.无水氯化钙在工业上有广泛的用途。
以石灰石矿粉(含有SiO2、Fe2O3、MgSO4等杂质)为原料,生产无水氯化钙的流程如下图:
回答下列问题:
(1)从流程图中推知:
SiO2具有的化学性质是__________。
(2)氧化铁与盐酸反应的化学方程式为_________________。
(3)滤渣3中除有Ca(OH)2外,还有_________(填化学式,下同)。
(4)产品中的杂质除极少量H2O外,最有可能含的是__________。
4.请你仔细分析如图所示的实验过程和提供的数据,并进行计算。
(1)反应后烧杯中溶液质量为_____g。
(2)应后所得溶液中溶质的质量分数是多少_____?
(写出计算过程,精确到0.1%)
中考冲刺第10讲2021.6.3
1.认识消毒剂过氧乙酸,过氧乙酸(C2H4O3)是一种高效绿色的消毒剂。
(1)下列有关过氧乙酸的说法,正确的是___________(填选项序号)。
A是一种氧化物B由三种元素组成C分子中含有臭氧(O3)分子D氧元素的质量分数最大
(2)凡是含有“
”结构的物质都具有杀菌消毒作用。
研究发现,过氧乙酸分子结构中也含有“
”结构,所以过氧乙酸也具有杀菌消毒作用。
获得这一结论所运用的科学方法属于___________推理(填选项序号)。
A归纳B演绎C类比
(3)过氧乙酸具有如下性质:
A无色易挥发液体B有酸性C有很强的腐蚀性D易溶于水和乙醇E不稳定,易分解放出氧气
F有毒性其中属于化学性质的有__________________(填选项序号)。
(4)醋酸(C2H4O2)与过氧化氢在室温下混合均匀,即可反应生成过氧乙酸和水,写出该反应的化学方程式__________________________。
(5)配制1L溶质质量分数为0.5%的过氧乙酸溶液。
现有以下物品:
水、溶质质量分数20%的过氧乙酸溶液、量筒(规格分别为1000mL、50mL)、塑料桶、铁桶、木棍、口罩、护目镜、橡皮手套。
①需要20%的过氧乙酸溶液____________mL(计算时,将水、20%和0.5%过氧乙酸溶液的密度都近似为1g/cm3)。
②戴好防护用品,用_____________mL量筒量取所需20%的过氧乙酸溶液倒入塑料桶中,按比例兑水,用木棍搅拌后,盖好桶盖备用。
③请你根据(3)中过氧乙酸的性质分析,进行配制时,不用铁桶的理由是_______。
2.化学与航天
2019年12月27日长征五号系列运载火箭(以下简称“胖五”)发射成功。
(1)“胖五”两种发动机分别采用液氢、液氧做推进剂和煤油、液氧做推进剂,而旧的长征火箭采用的推进剂是有毒的偏二甲肼(N2H4)和液态四氧化二氮(N2O4),其燃烧时还会因泄露和不充分燃烧产生大量氮的氧化物。
①“胖五”的两种推进剂中属于可燃物的是_____________________。
②科学家发现,煤在一定条件下加氢制得煤油,称之为煤的液化,属于__________变化。
③写出煤油(以C12H16为例)完全燃烧的化学方程式_______________________。
④从环境保护的角度分析,“胖五”的两种发动机采用的推进剂优点是_________________。
(2)铝合金在火箭制造中被广泛应用。
①铝合金中的铝化学性质活泼,原因是_______________________________。
②铝在岩石圈中以化合物形式存在,工业采用电解氧化铝的方法冶炼铝,写出反应的化学方程式_______________________。
3..探究瓜子中二氧化硫的含量
有媒体报道:
某品牌瓜子被查出二氧化硫残留量超标。
为了测定购买的瓜子中二氧化硫的含量,小莉进行以下探究活动。
(1)查阅资料
①二氧化硫是无色气体,化学性质与二氧化碳相似,但能与氧气反应。
②二氧化硫可用作干果的防腐剂。
我国食品添加剂标准规定,二氧化硫在干果中残留量≤04g/kg。
③在沸水浴加热的条件下,瓜子中的二氧化硫可以全部释放出来。
④氮气化学性质不活泼,一般条件下不和其他物质发生反应。
(2)实验
小莉利用下图所示装置进行实验。
①实验原理:
乙装置用于吸收瓜子样品释放出的二氧化硫,碱溶液可选用______,发生反应的化学方程式为_________;
丙装置的作用是吸收氮气流带出的水蒸气,发生反应的化学方程式为_______。
②实验步骤:
第一步:
在U型管中放入瓜子样品500g,按图示连接好仪器,向其中通入氮气。
第二步:
通入氮气一段时间后,称得乙、丙装置总质量为458.5g。
第三步:
再次连接好仪器,持续通入氮气,同时向烧杯中加入沸水
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 中考 化学 每日 最后 冲刺
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
