 初三化学期中考试前必知必会的内容Word下载.docx
初三化学期中考试前必知必会的内容Word下载.docx
- 文档编号:19812564
- 上传时间:2023-01-10
- 格式:DOCX
- 页数:15
- 大小:83.14KB
初三化学期中考试前必知必会的内容Word下载.docx
《初三化学期中考试前必知必会的内容Word下载.docx》由会员分享,可在线阅读,更多相关《初三化学期中考试前必知必会的内容Word下载.docx(15页珍藏版)》请在冰豆网上搜索。
现象:
化学方程式:
2.将稀盐酸滴加到石灰石上,并将产生的气体通入澄清石灰水中
3.将稀盐酸滴加到碳酸钠粉末上,并将产生的气体通入澄清石灰水中
4.碳在氧气中燃烧:
在空气中:
。
在氧气中:
。
5.硫粉在空气中燃烧:
。
。
6.铁在氧气中燃烧:
。
7.汞与氧气受热反应:
8.氧化汞加强热分解:
9.红磷在空气中燃烧:
“测定空气里氧气含量”的实验:
(1)实验现象:
① 。
②待装置 后,打开止水夹,
。
产生此现象的原因是。
(注意烟、雾的区别:
是固体小颗粒,而 是小液滴)
(2)实验结论:
第二单元课题3氧气的制法
1.加热氯酸钾(有少量的二氧化锰):
氯酸钾:
色固体 二氧化锰:
色固体
2.加热高锰酸钾:
高锰酸钾:
色固体
3.实验室用双氧水制氧气:
4.化学方程式:
过氧化氢溶液:
色溶液(俗称:
)
1.催化剂定义:
能 化学反应的速率,但本身的 和 在反应前后没有发生改变的物质。
2.选择发生装置应该从哪些方面来考虑?
①
②
高锰酸钾制氧气发生装置要点:
1.加热固体试管口应略向下倾斜
—( )
2.导管伸入试管一端应刚刚露出橡胶塞
3.铁夹应夹在试管中上部
—( )
4.应用酒精灯外焰加热
5.加热KMnO4应在试管口放一团棉花
3.收集装置要点
①排水法:
氧气能用排水法收集的原因:
因为
②向上排空气法
氧气能用向上排空气法收集的原因:
4.验满方法
5.检查装置气密性的方法:
6.实验室用高锰酸钾制取氧气,用排水法收集的操作:
① ② ③ ④ ⑤ ⑥ ⑦
“收”:
排水法收集:
开始出来的为 ,等到气泡 放出时才开始收集。
“离、熄”颠倒会造成的后果:
。
“水倒吸”的原因:
。
7.黑色固体:
白色固体:
第三单元课题1
上述实验中的实验现象:
产生该现象的原因:
由分子构成的物质有(试举两例)、。
由原子直接构成的物质有(试举两例)、。
化学反应的微观实质是。
第四单元课题2
生物体中含量最多的物质是。
自来水厂净化水的主要流程(填操作名称)是→→→消毒。
净水程度最高的方法是。
过滤操作中玻璃棒所起的作用是。
过滤后,滤液仍浑浊的可能原因有、。
活性炭所起的作用是,该变化是(选填“物理”或“化学”)变化。
区分硬水与软水的常用试剂是。
在生活中常用于硬水软化的方法是。
第四单元课题3
1.电解水实验:
通电一段时间后,与负极相连的试管中所收集的气体为(填名称,下同),与正极相连的试管中所收集的气体为,正极与负极产生的气体的体积比为,该实验说明水是由组成的。
该反应的化学方程式是。
2.氢气
氢气溶于水;
同温同压(相同条件)下,氢气的密度于空气的密度。
氢气在空气中燃烧产生色火焰,在火焰上方罩一个干冷的小烧杯,观察到的现象是。
氢气燃烧的化学方程式是。
点燃或加热氢气前必须进行。
3.水蒸发与电解水对比
水蒸发过程中,从分子原子的角度上看,水分子_______(填“变”或“不变”),只是_______在改变,因而属于_______变化(填“物理”或“化学”),变化前后水的化学性质_______(填“变”或“不变”);
电解水的实验中,从分子原子的角度看,反应前后_______改变,_______
没有变。
期中总复习
一、物质的分类
1.概念框架
物质……
2.定义
(1)由 叫做单质。
(2)由 叫做化合物。
(3)由 叫做氧化物。
二、化学方程式总结
1.默写产生氧气的5个化学方程式;
氧气参加的7个化学方程式。
2.默写产生二氧化碳的3个化学方程式;
二氧化碳参加的2个化学方程式。
3.默写产生水的5个化学方程式;
水参加的1个化学方程式。
4.默写产生沉淀的两个化学方程式。
答案:
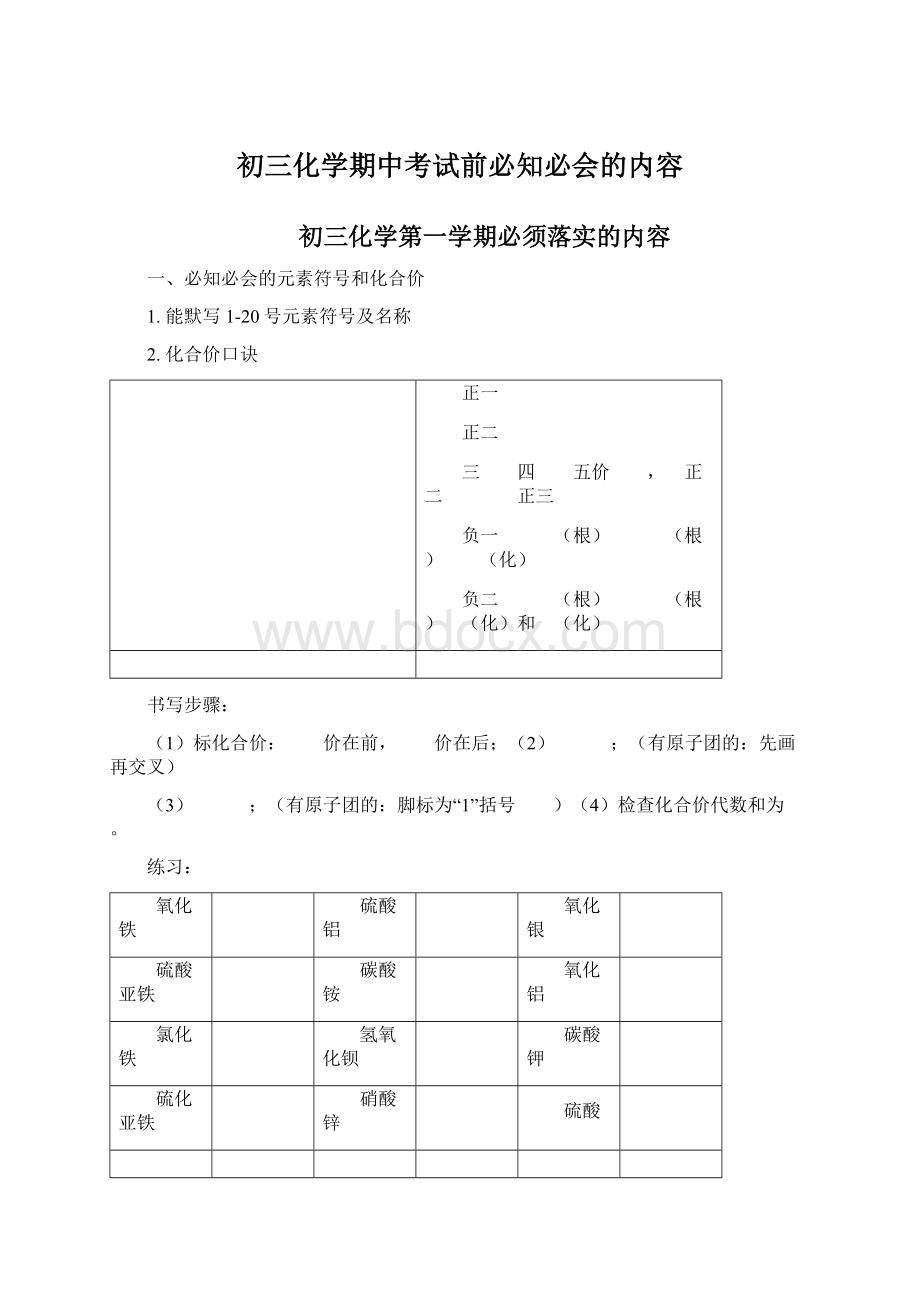
化合价口诀
4
(亚铁)
(铁)
3
3
正一钠钾银氢铵
正二镁钙铜钡锌
三铝四硅五价磷, 正二亚铁正三铁
负一硝酸(根)氢氧(根)氯(化)
负二碳酸(根)硫酸(根)氧(化)和硫(化)
正价在前,负价在后;
(2)交叉;
先画括号再交叉)
(3)约简;
脚标为“1”括号省)(4)检查化合价代数和为零。
Fe2O3
Al2(SO4)3
Ag2O
FeSO4
(NH4)2CO3
Al2O3
FeCl3
Ba(OH)2
K2CO3
FeS
Zn(NO3)2
H2SO4
产生蓝色絮状沉淀
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
固体逐渐减小,产生大量无色气泡,气体能使澄清石灰水变浑浊。
CaCO3+2HCl=CaCl2+H2O+CO2↑
Ca(OH)2+CO2=CaCO3↓+H2O
白色粉末逐渐减少,产生大量无色气泡,气体能使澄清石灰水变浑浊。
Na2CO3+2HCl=2NaCl+H2O+CO2↑
C+O2点燃CO2
黑色的木炭变红热,生成能使澄清石灰水变浑浊的无色气体。
黑色的木炭剧烈燃烧,发出白光,放出大量热,生成能使澄清石灰水变浑浊的无色气体。
S+O2点燃SO2
黄色固体燃烧,发出淡蓝色火焰,放热,生成一种有刺激性气味的无色气体。
黄色固体剧烈燃烧发出明亮的蓝紫火焰,放出大量热,生成一种有刺激性气味的无色气体。
3Fe+2O2点燃Fe3O4
银白色固体红热。
银白色固体剧烈燃烧,火星四射,放出大量热,生成一种黑色固体。
2Hg+O2△2HgO
2HgO△2Hg+O2↑
4P+5O2点燃2P2O5
暗红色固体燃烧,发出黄色火焰,放热,生成大量白烟。
1.“测定空气里氧气含量”的实验:
①暗红色固体在空气中燃烧,产生黄色火焰,放热,生成大量白烟。
②待装置冷却至室温后,打开止水夹,①烧杯中的水倒吸入集气瓶中,②且吸入水的体积约占瓶中原空气体积的1/5。
产生此现象的原因是①红磷燃烧只消耗氧气,且只生成固体,压强减少,小于外界大气压;
②氧气约占空气体积的1/5
烟是固体小颗粒,而雾是小液滴)
氧气约占空气总体积的1/5(或表述为:
空气中氧气的体积分数约为1/5)
加热氯酸钾(有少量的二氧化锰):
2KClO3MnO22KCl+3O2↑
白色固体 二氧化锰:
黑色固体
加热高锰酸钾:
2KMnO4△K2MnO4+MnO2+O2↑
暗紫色
实验室用双氧水制氧气:
2H2O2MnO22H2O+O2↑
无色溶液(俗称:
双氧水)混合物
过氧化氢是纯净物
3.催化剂定义:
能改变化学反应的速率,但本身的质量和化学性质在反应前后没有发生改变的物质。
4.选择发生装置应该从哪些方面来考虑?
①反应物的状态
②反应所需的条件
4.加热固体试管口应略向下倾斜
—(防止水蒸气在试管口冷凝,倒流回热的试管底部,使试管炸裂)
5.导管伸入试管一端应刚刚露出橡胶塞
—(保证试管内空气顺利排出,使收集的氧气纯净)
6.铁夹应夹在试管中上部
—(便于预热,防止炸裂)
---(防止加热时KMnO4粉末进入导管堵塞导管、发生爆炸、污染气体)
因为氧气不易溶于水,且不与水发生反应。
在相同条件下,氧气的密度比空气的密度略大,且不与空气中的物质发生反应
将一根带火星的木条放在集气瓶的瓶口,若带火星的木条复燃,则氧气已满;
反之,未满。
连接仪器,将导气管的一端放入水中,双手紧握试管,观察导气管口是否有气泡产生。
若有气泡产生,则装置气密性良好,反之,则不好。
查装定点收离熄
开始出来的为空气,等到气泡大量的、连续不断放出时才开始收集。
有水会倒吸回热的试管,使试管炸裂。
熄灭酒精灯后试管内的温度降低,压强减小,小于外界大气压,所以大气压将水压入试管。
木炭(C)、二氧化锰(MnO2)、四氧化三铁(Fe3O4)
五氧化二磷(P2O5)、碳酸钠(Na2CO3)、碳酸钙(CaCO3)、氯酸钾(KClO3)、氯化钾(KCl)
A烧杯中的无色液体变红,B烧杯中的液体无明显变化。
B烧杯中的浓氨水挥发出氨分子,氨分子运动到A烧杯中,溶于水形成氨水显碱性,使酚酞由无色变为红色。
由分子构成的物质有(试举两例)水、二氧化碳。
(答案合理即可)
由原子直接构成的物质有(试举两例)金属单质、稀有气体的单质。
(或金刚石、石墨、硅等)
化学反应的微观实质是分子破裂,原子重新组合。
生物体中含量最多的物质是水。
自来水厂净化水的主要流程(填操作名称)是沉淀→过滤→吸附→消毒。
净水程度最高的方法是蒸馏。
过滤操作中玻璃棒所起的作用是引流。
过滤后,滤液仍浑浊的可能原因有滤纸破损、漏斗内液面高于滤纸上边缘。
活性炭所起的作用是吸附,该变化是物理(选填“物理”或“化学”)变化。
区分硬水与软水的常用试剂是肥皂水。
在生活中常用于硬水软化的方法是煮沸。
电解水实验:
通电一段时间后,与负极相连的试管中所收集的气体为氢气(填名称,下同),与正极相连的试管中所收集的气体为氧气,正极与负极产生的气体的体积比为1:
2,该实验说明水是由氢元素和氧元素组成的。
该反应的化学方程式是2H2O
2H2↑+O2↑。
氢气难溶于水;
同温同压(相同条件)下,氢气的密度小于空气的密度。
氢气在空气中燃烧产生淡蓝色火焰,在火焰上方罩一个干冷的小烧杯,观察到的现象是烧杯内壁出现无色液滴(或白雾)。
氢气燃烧的化学方程式是2H2+O2
2H2O。
点燃或加热氢气前必须进行验纯。
期中总复习基础知识
单质
纯净物氧化物
化合物
混合物
(提示:
进行物质分类判断时,应先写化学式再进行判断。
)
1.定义
(1)由同种元素组成的纯净物叫做单质。
(2)由不同种元素组成的纯净物叫做化合物。
(3)由两种元素组成,其中一种元素是氧元素的化合物叫做氧化物。
产生氧气的5个化学方程式
氧气参加的7个化学方程式
2KMnO4
K2MnO4+MnO2+O2↑
2H2+O2
2H2O
2H2O2
2H2O+O2↑
C+O2
CO2
2H2↑+O2↑
4P+5O2
2P2O5
2HgO
2Hg+O2↑
白磷自燃:
4P+5O2==2P2O5
△
2KClO3
2KCl+3O2↑
S+O2
SO2
3Fe+2O2
Fe3O4
2Hg+O2
2HgO
产生二氧化碳的3个化学方程式
二氧化碳参加的2个化学方程式
CaCO3+2HCl=CaCl2+H2O+CO2↑
Na2CO3+2HCl=2NaCl+H2O+CO2↑
Ca(OH)2+CO2=CaCO3↓+H2O
2NaOH+CO2=Na2CO3+H2O
产生水的5个化学方程式
水参加的1个化学方程式
Ca(OH)2+CO2=CaCO3↓+H2O
产生沉淀的两个化学方程式
2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 初三化学 期中 考试 前必知必会 内容
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
