 第2章氧和二氧化碳的转运docWord文档格式.docx
第2章氧和二氧化碳的转运docWord文档格式.docx
- 文档编号:19695122
- 上传时间:2023-01-08
- 格式:DOCX
- 页数:11
- 大小:26.66KB
第2章氧和二氧化碳的转运docWord文档格式.docx
《第2章氧和二氧化碳的转运docWord文档格式.docx》由会员分享,可在线阅读,更多相关《第2章氧和二氧化碳的转运docWord文档格式.docx(11页珍藏版)》请在冰豆网上搜索。
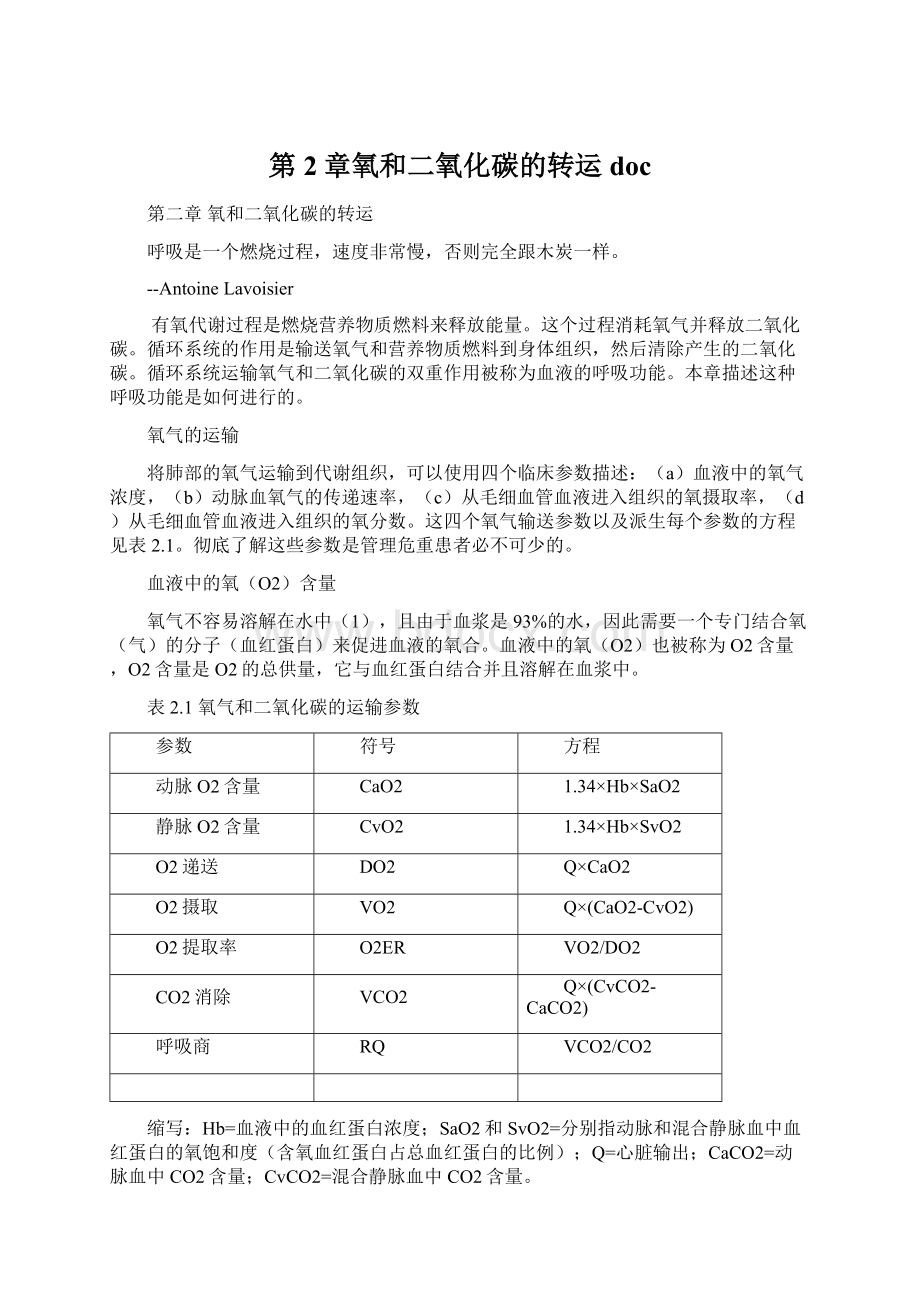
CO2消除
VCO2
(CvCO2-CaCO2)
呼吸商
RQ
VCO2/CO2
缩写:
Hb=血液中的血红蛋白浓度;
SaO2和SvO2=分别指动脉和混合静脉血中血红蛋白的氧饱和度(含氧血红蛋白占总血红蛋白的比例);
Q=心脏输出;
CaCO2=动脉血中CO2含量;
CvCO2=混合静脉血中CO2含量。
与O2结合的血红蛋白(氧合血红蛋白)
与O2结合的血红蛋白(HbO2)浓度由公式2.1
(2)中的变量决定。
HbO2=1.34×
SO2(2.1)
Hb是血液中的血红蛋白浓度(通常以g/dL表示,即g/100mL);
1.34是血红蛋白的氧结合能力(以每g血红蛋白多少mLO2表示);
SO2是血液中氧合血红蛋白占总血红蛋白的比例(SO2=HbO2/总Hb),也称作血红蛋白的氧饱和度。
HbO2与Hb浓度的单位(g/dL)相同。
公式2.1表示:
当血红蛋白与O2完全饱和时(即当SO2=1时),每g血红蛋白通常结合1.34mL的氧气。
通常1g血红蛋白能结合1.39mL的氧气,但一小部分循环血红蛋白(3%到5%)以高铁血红蛋白和碳氧血红蛋白的形式存在,因为这些形式的Hb结合O2的能力降低,因此1.34mL/g这一较低值被认为更能代表总血红蛋白池的O2结合能力(3)。
笔记:
O2=氧(气);
Hb=血红蛋白
溶解的O2
血浆中溶解的O2浓度取决于氧在水(血浆)中的溶解度和血液中的氧分压(PO2)。
O2在水中的溶解度是随温度变化的(溶解度随温度的降低略有增加)。
在正常体温(37℃)和PO2为1mmHg时,0.03mL的O2能溶解在1升的水中(4)。
表现为溶解系数为0.03mL/L/mmHg(或0.003mL/100mL/mmHg)。
溶解O2的浓度(单位mL/dL)(体温正常)可由公式2.2描述。
溶解的O2=0.003×
PO2(2.2)
这个公式显示血浆中氧的溶解度有限。
例如,如果PO2是100mmHg,1L的血液将只包含3mL溶解的O2。
表2.2动脉和静脉血中氧的正常水平※
动脉血
静脉血
PO2
90mmHg
40mmHg
Hb的O2饱和度
0.98
0.73
与O2结合的Hb
197mL/L
147mL/L
2.7mL/L
1.2mL/L
总O2含量
200mL/L
148mL/L
血容量†
1.25L
3.75L
O2的容积
250mL
555mL
带※值是在体温37℃和血红蛋白15g/dL(150g/L)时测得。
带†的值是在总血容量(=L)的基础上估计的,动脉血容量=0.25×
总血容量,静脉血容量=0.75×
总血容量。
Hb:
血红蛋白;
PO2:
O2分压。
动脉O2含量/动脉含O2量(CaO2)
动脉血的O2浓度(CaO2)可通过公式2.1和2.2的结合,使用动脉血的SO2和PO2来定义(SaO2和PaO2)。
CaO2=(1.34×
SaO2)+(0.003×
PaO2)(2.3)
结合的O2、溶解的O2和总O2在动脉血中的正常浓度见表2.2。
每L动脉血中大约有200mL的氧,只有1.5%(3mL)溶解在血浆中。
一个平均体型的成人在休息时的耗氧量为250mL/min,这意味着,如果我们被迫单靠血浆中溶解的O2,那必须要有89L/min的心脏输出来维持有氧代谢。
这强调了血红蛋白在运输氧气中的重要性。
静脉O2含量/静脉含O2量(CvO2)
静脉血中的O2浓度(CvO2)可以与CaO2一样以相同的方式计算,使用静脉血的血氧饱和度(O2饱和度)和氧分压计算(SvO2和PvO2)。
CvO2=(1.34×
SvO2)+(0.003×
PvO2)(2.4)
SvO2和PvO2的最佳测量方法是通过取自肺动脉的集合或“混合静脉”的血样本来测量(使用肺动脉导管,见第9章)。
如表2.2所示,SvO2的正常值是73%(0.73),PvO2的正常值是40mmHg,CvO2的正常值约为15mL/dL(150mL/L)
简化的O2含量公式
血浆中溶解的O2浓度是如此小,它通常会从O2含量公式中被消除。
因此可认为血液的O2含量与相当于与Hb结合的O2(见方程2.1)。
O2含量≈1.34×
SO2(2.5)
贫血与低氧血症
医生经常使用动脉氧分压(PaO2)作为血液中含有多少氧的指征。
然而,如公式2.5所示,血红蛋白浓度是血液中氧含量的主要决定因素。
图2.1显示了血红蛋白和PaO2对血液中氧水平影响的比较。
此图显示血红蛋白浓度和PaO2对动脉血氧含量比例变化的影响。
血红蛋白减少50%(从15到7.5g/dL)相当于CaO2减少50%(从200到101mL/L),而PaO2降低50%(从90到45mmHg)仅引起CaO2降低18%(从200到163mL/L)。
此图表明,贫血对血液氧合作用的影响比低氧血症要大的多。
它也应作为一个提醒,以避免使用PaO2来评估动脉的氧合作用。
PaO2应该被用来评估肺部的气体交换效率(见第19章)。
血液中O2的缺乏
循环血液中总的O2容量可通过血液中血容量的产物和O2的浓度来计算。
定卖血和静脉血中O2量的估计见表2.2。
动脉和静脉血中结合的O2容量为微薄的805mL。
这一容量是多么的有限,试想一个平均体型的成人在休息时全身的O2含量是250mL/min。
这意味着,血液中的O2容量只能维持机体3到4min的有氧代谢。
因此,如果一个患者停止呼吸,你只有宝贵的几分钟时间在其血液中氧储存完全耗尽前开始给他行辅助呼吸操作。
血液中数量有限的O2也可通过葡萄糖的氧化代谢来表示,葡萄糖的有氧代谢公式为:
C6H12O6+6O2=6CO2+6H2O。
这个公式表明,完整的1mol葡萄糖氧化利用6mol的氧气。
为了确定血液中的O2是否足够维持血液中葡萄糖的代谢,有必要将血液中的葡萄糖和氧气的量用mmol这一单位来表示。
(这里显示的值基于90mg/dL或90/180=0.5mmol/dL的血糖水平,5L的血容量,805mL或805/22.2=36.3mmol的总血液O2):
血液中总的葡萄糖…………………….25mmol
血液中总的O2…………………………36.3mmol
葡萄糖代谢需要的O2…………………150mmol
这表明血液中的O2只有总量的20%到25%为血液中葡萄糖的完全氧化代谢所需。
贫血
低氧血症
正常
图2.1图表显示血红蛋白浓度(Hb)和动脉氧分压(PaO2)的等量降低(50%)对动脉血中氧浓度的影响。
为什么O2这么少?
一个显而易见的问题是为什么一个需要氧气维持生存的机体被设计为在氧气有限的环境中进行新陈代谢?
答案可能与氧气的潜在毒性有关。
众所周知,氧气通过产生有毒的代谢产物能造成致命的细胞损伤(超氧化物自由基,过氧化氢和羟自由基),因此,在细胞附近限制氧气浓度,可能是保护细胞避免氧诱导细胞损伤的机制。
氧诱导的损伤(氧化性损伤)在临床疾病中的作用是非常激动人心和活跃的研究领域,本章结尾的参考书目包括一本教科书(生物学和医学领域中的自由基),这是关于这一学科的最好的单一信息资源。
丰富的血红蛋白
与血液中氧容量小相反,循环血红蛋白的总量似乎过多。
如果正常血清Hb是15g/dL(150g/L)且正常血容量是5L(70mL/kg),那么循环的血红蛋白的总量时750g(0.75kg)或1.65磅。
为了证明血液中血红蛋白池的规模庞大,图2.2中的插图比较了血红蛋白与正常体重的心脏的重量。
心脏的重量只有300g,因此,循环的血红蛋白池的重量是心脏的2.5倍!
这意味着,每60秒,心脏必须在循环系统中推动超过自身两倍以上重量的移动。
所有的血红蛋白都是必要的吗?
稍后所示,当从全身毛细血管的氧提取达到最大时,静脉血中40%到50%的血红蛋白仍与氧饱和。
这意味着,几乎有一半的循环血红蛋白不是用来支持有氧代谢。
那这多余的血红蛋白用来做什么呢?
运送二氧化碳,见本章节后面所述。
图2.2平衡标尺显示循环血红蛋白与正常体重的心脏相比时多余的重量。
氧输送/氧递送(DO2)
进入肺部血流的氧气通过心输出量进入重要的器官。
这种情况发生的速度被称为氧输送(DO2)。
DO2描述了每分钟到达全身毛细血管的氧气量(mL)。
它相当于动脉血氧含量(CaO2,单位mL/L)和心输出量(Q,单位L/min)的产物(2,5,6,7)。
DO2=Q×
CaO2×
10(2.6)
(乘以10是用来转换CaO2的单位,从mL/dL到mL/L,因此,DO2的单位为mL/min。
)如果将CaO2分解成其组成部分(1.34×
SaO2),公式2.6可以改写为:
SaO2×
10(2.7)
当用肺动脉导管来测量心输出量(见第9章),DO2可用公式2.7计算。
成人休息时的正常DO2为900-1100mL/min,或500-600mL/min/m2,校正身材时(见表2.3)。
表2.3氧气和二氧化碳运输参数的正常范围
绝对范围
调整身材的范围※
心输出量
5-6L/min
2.4-4.0L/min/m2
900-1100mL/min
520-600mL/min/m2
200-270mL/min
110-160mL/min/m2
0.20-0.30
160-220mL/min
90-130mL/min/m2
0.75-0.85
校正身材后的值※通过绝对值除以患者的体表面积(单位m2)计算。
氧摄取/摄氧量(VO2)
当血液达到全身毛细血管,氧从血红蛋白中分离出来,并进入组织。
这一现象发生的速度称为氧摄取(VO2)。
氧摄取描述没分钟离开毛细血管,进入组织的氧气的体积(单位mL)。
由于氧气不能在组织中储存,因此,VO2也是衡量组织耗氧量的一个指标。
VO2(mL/min)可通过心输出量(Q)和动静脉血氧含量差(CaO2-CvO2)来计算。
VO2=Q×
(CaO2-CvO2)×
10(2.8)
(乘以10与解释DO2时的原因一样。
)这种派生VO2的方法被称为烦Fick氏法,因为公式2.8是Fick方程的一个变化(心输出量是派生的变量:
Q=VO2/CaO2-CvO2)(8)。
因为CaO2和CvO2的公式相同(1.34×
10),公式2.8可重新描述为:
(SaO2-SvO2)(2.9)
这个公式表示VO2使用的是在临床实践中可以测量的变量。
在这个公式中决定VO2的因素见图2.3所示。
健康成人在休息时VO2的正常范围是200-300mL/min,或110-160mL/min/m2,当校正身材时(见表2.3)。
图2.3决定氧从微循环中摄取(VO2)的因素的示意图。
SaO2和SvO2=动脉血和静脉血中血红蛋白的氧饱和度;
PO2=氧分压;
Hb=一个血红蛋白分子。
Fick(菲克)和全身的VO2
改良的菲克公式中的VO2不等于全身的VO2,因为它不包括肺部的O2消耗量(8,9,10)。
通常情况下,肺部的VO2代表低于全身5%的VO2(9),但它在肺部炎症性疾病的患者中可占全身VO2的20%(这在ICU患者中很常见)(10)。
这种差异在VO2用作血流动力学管理终结点时可能是重要的(见第11章),因为全身VO2的低估可能导致VO2增加的过度的管理。
VO2的直接测量(在下面介绍)更能准确地表述全身的VO2。
VO2的直接测量
全身VO2可通过监测氧气从肺部消失的速率来直接测量。
这可以用一个专门配备氧气分析仪的仪器完成,氧气分析仪是连接到近端气道(通常是在气管插管患者)以测量吸入或呼出气体的O2浓度。
这个装置记录和显示的VO2是作为分钟通气量(VE)和吸入与呼出气体中氧气的分数浓度(FiO2和FeO2)的产物。
VO2=VE×
(FIO2-FEO2)(2.10)
VO2的直接测量比计算出的(菲克)VO2更准确,因为它更接近全身的VO2。
它与菲克VO2相比还有其它几个优势,这些都将在第11章描述。
直接测量VO2的主要缺点是许多ICU都缺乏这一监测设备,并且需要训练有素的人员来操作这些设备。
氧提取率(O2ER)
递送到毛细血管并进入组织的这部分氧是一个氧运输效率的指标。
这可通过氧提取率(O2ER)这一参数来监测,O2ER是指氧气摄取与氧气递送的比率。
O2ER=VO2/DO2(2.11)
这个比率可以乘以100,一百分数表示。
因为VO2和DO2的公式相同(Q×
10),因此,公式2.11可减少为只有两个测量变量的公式:
O2ER=(SaO2-SvO2)/SaO2(2.12)
当SaO2接近1.0(通常情况下),O2ER与(SaO2-SvO2)的差大致相当:
O2ER≈(SaO2-SvO2)。
O2ER通常约为0.25(范围=0.2-0.3),如表2.3所示。
这意味着,运送到全身毛细血管的氧只有25%进入组织。
虽然通常O2的提取低,但他是可调节的,并且当氧输送受损时O2的提取可增加。
O2提取的适应性是组织氧合控制的一个重要因素,见下所述。
氧摄取的控制
氧气运输系统的运作,以保持在氧供变化时(不同的DO2)有恒定流量的氧气进入组织(恒定的VO2)。
O2的提取来调整O2输送的变化的能力使这种行为能实现(11)。
VO2的控制系统可通过重新排列O2提取公式(公式2.11)使VO2成为因变量来描述:
VO2=DO2×
O2ER(2.13)
这个公式表明,如果O2输送的变化随O2提取呈等效和相互的变化,那么VO2会表示不变。
然而,如果O2的提取固定不变,那么DO2的变化将随VO2呈等量变化。
因此,O2提取来调整DO2的变化的能力决定保持恒定VO2的能力。
DO2和VO2的关系
O2输送和O2摄取之间的正常关系见图2.4所示(11)。
当O2输送(DO2)开始减少低于正常时(途中箭头表示),O2摄取(VO2)最初保持不变,表明O2提取(O2ER)在DO2降低时呈增加趋势。
DO2进一步减,最终导致VO2出现开始降低的拐点。
当O2提取提高到50%至60%的最高水平(O2ER=0.5-0.6),VO2开始从固定不变到不断变化转换。
一旦O2ER达到最大,DO2的进一步减少会导致VO2的等量减少,因为O2ER是固定的且不能进一步增加。
当这种情况发生时,VO2被称为处于供应-依赖,并且有氧代谢率受氧供限制。
这种情况称为氧化障碍(12)。
当有氧代谢(VO2)开始下降,高能磷酸(ATP)的氧化产物开始下降,导致细胞功能受损,病最终导致细胞死亡。
这个过程的临床表现是临床休克和渐进的多器官功能衰竭(13)。
临界DO2
在VO2成为供应-依赖时的DO2,被成为临界氧输送(临界DO2)。
这是全力支持有氧代谢的最低的DO2,可通过DO2-VO2曲线中的曲折处确定(见图2.4)。
尽管临界DO2能识别无氧阈值的能力,但临界DO2的临床价值有限。
首先,临界DO2在重症患者的研究中变化很大(11,13,14),且在任何ICU的任何患者中都无法预测临界DO2。
第二,DO2-VO2曲线可以是曲线的(即,VO2从固定不变到不断变化没有一个单一的过渡点)(15),在这种情况下,无法确定临界DO2。
DO2:
DO2的比率可能是比临界DO2更能确定(和避免)无氧阈值的一个有用的参数。
保持DO2:
4:
1或更高的VO2比率被推荐作为避免重症患者无氧阈值的一个管理策略。
图2.4该图显示当O2输送逐步下降时O2输送()和O2摄取()间的正常关系,由箭头表示。
二氧化碳的运输
二氧化碳(CO2)是氧化代谢的主要终产物,因为它很容易与水化合形成碳酸,如果能累积,它可以是严重酸中毒的一个来源。
从体内消除CO2的重要性在通气控制系统中的作用是显而易见的,该系统能保持动脉PO2(PaCO2)的稳定。
5mmHgPaCO2的增加可能会导致每分钟通气量增加两倍。
为了产生相等的通气量的增加,动脉氧分压必须下降至55mmHg(16)。
通气控制系统要注意高碳酸血症和忽略低氧血症的这一趋势是耐人寻味的,因为它表明,与促进有氧代谢相比(通过提供氧气),通气系统更关注代谢废物(CO2)的清除。
二氧化碳的水合
据报道,成人身体总的CO2量是130L(17),根据一个成人身体总水量平均只有40至45L,这似乎是可能的。
CO2与水发生化学反应产生碳酸的趋势可以解释这种困境。
CO2发生水合和转变为碳酸是一个连续的过程,这会创建一个永久的梯度驱动CO2进入溶液。
因为CO2不断消失,故溶液中的CO2总量可能会超过溶液的体积。
如果你曾经打开过一个热的香槟酒瓶,你就已经目睹了多少CO2可以溶解在溶液中。
二氧化碳运输方案
CO2运输是一个复杂的过程,见图2.5所示。
CO2运输的核心是它与水的反应。
该反应的第一阶段涉及碳酸的形成。
这通常是一个缓慢的反应,大约需要40秒来完成(18)。
碳酸酐酶的存在使反应速度大大增加,不到10毫秒(msec)即可完成(18)。
碳酸酐酶局限存在于红细胞,血浆中则不存在。
因此,CO2仅在红细胞快速与水结合,这会产生一个压力梯度,从而推动CO2进入细胞。
图2.5CO2运输中涉及的化学反应。
括号中的数值表示每个部分通常在1L静脉血中的量。
双箭头表示有利的途径。
碳酸能瞬间分解产生氢离子和碳酸氢盐离子。
在红细胞中生成的很大一部分碳酸氢盐通过与氯化物交换被泵回到血浆。
在红细胞中生成的氢离子通过血红蛋白缓冲。
通过这种方式,进入红细胞的CO2被分解和部分储存(血红蛋白)或排出(碳酸氢钠),以创造更多的CO2进入红细胞。
这些过程创建一个汇点,以容纳大量的CO2在红细胞中。
红细胞中的一小部分CO2在血红蛋白上与游离氨基反应产生氨基甲酸,氨基甲酸分解形成氨甲酰残基(HbNHCOO)和氢离子。
这个反应为血红蛋白提供另一个作为缓冲剂的机会。
血液中的CO2含量
血液中不同的CO2测量结果见表2.4。
如同氧气,CO2以溶解的形式存在,且溶解的CO2浓度由二氧化碳分压(PCO2)和CO2在水中的溶解系数确定(即0.69mL/L/mmHg,37℃)(19)。
动脉和静脉血中溶解的CO2含量见表2.4(20)。
与氧气一样,溶解的CO2只是血液中总CO2含量的一小部分。
血液中CO2的总含量是几个部分的总和作用的结果,包括在血浆和红细胞中溶解的CO2和碳酸氢盐的浓度,以及红细胞中氨甲酰CO2的含量。
这些部分在静脉血中的正常值见图2.5所示。
如果这些值相加,总的CO2含量是2.3mEq/L,17mEq/L在血浆中,6mEq/L在红细胞中。
血浆中CO2的(数量)优势是蒙蔽人的,因为大多数的血浆成分是以碳酸氢盐的形式存在,这部分碳酸氢盐已从红细胞中排除。
表2.4动脉和静脉血中CO2的正常水平※
PCO2
45mmHg
溶解的CO2
27mL/L
29mL/L
总CO2含量
490mL/L
530mL/L
CO2容积
613mL
1988mL
带※的值的体温是37℃。
带†量是根据总血容量(TBV)5L来估计的,动脉血容量为0.25×
TBV,静脉血容量为0.75×
TBV。
PCO2=CO2分压。
表2.5血液蛋白质的缓冲能力
血红蛋白
血浆蛋白质
固有缓冲能力
0.18mEqH+/g
0.11mEqH+/g
在血液中的浓度
150g/L
38.5g/L
总的缓冲能力
27.5mEqH+/g
4.2mEqH+/g
因为容易分解成离子(氢离子和碳酸氢根离子),CO2浓度往往用离子当量(mEq/L)来表示,如图2.5所示。
转换为体积单位(mL/L或mL/dL)是可能的,因为1mol的CO2将占据22.3L的体积。
因此:
CO2(mL/L)=CO2(mEq/L×
22.3)
表2.4包括血液中的CO2含量,以体积单位表示(20)。
需要注意的是血液中的CO2总量(约2.6L)是血液中O2的3倍以上(805mL)。
血红蛋白作为一个缓冲剂
图2.5显示了血红蛋白通过缓冲红细胞中水化的CO2所产生的氢离子,在CO2的运输中起着核心作用。
血红蛋白的缓冲能力见表2.5所示(21)。
请注意,血红蛋白总的缓冲能力是所以血浆蛋白的缓冲能力的6倍以上。
血红蛋白的缓冲作用是由于分子中的38组氨酸残基上的咪唑基团。
这些咪唑基团的解离系数pK为7.0,因此,它们在pH在6至8这一范围中起到有效地缓冲作用(缓冲剂在一个pH的两侧pK范围都是有效的)(20)。
相比之下,碳酸氢盐缓冲系统有一个6.1的pK,所以这个缓冲系统在pH从5.1到7.1这一范围是有效的。
比较血红蛋白和碳酸氢盐的缓冲范围显示,在临床上遇到的pH范围中(pH值7~8),与碳酸氢盐相比,血红蛋白是一种更有效的缓冲剂!
血红蛋白这方面的功能更值得关注。
为何血红蛋白会多余?
如前所述,血液中血红蛋白的含量远远超过需要输送氧气的量,考虑血红蛋白在CO2输送中所扮演的角色,很可能多余的血红蛋白是用来运输CO2。
考虑到血液中大量的CO2(见表2.4),很容易理解为什么血液中会有这么多的血红蛋白。
图2.6动脉血(O2饱和度=98%)和静脉血(O2饱和度=70%)的CO2解离曲线。
两点表示动脉和静脉血液中CO2的含量。
括号显示血红蛋白去饱和作用(霍尔丹效应)以及从动脉血到静脉血过程中增加CO2含量的代谢的CO2产物(PCO2效应)的相对贡献。
霍尔丹效应
血红蛋白在不饱和形式下有更大的缓冲能力,完全不饱和的血液可以结合额外的60mL/L的CO2。
因氧合血红蛋白去饱和作用引起CO2含量的增加被称为霍尔丹效应。
图2.6显示的CO2解离曲线显示,霍尔丹效应在静脉血吸收CO2过程中起了重要作用。
图上的两个点显示,静脉血CO2含量比动脉血高40mL/L。
括号表明静脉血增加的CO2含量中的60%是由于CO2分压(PCO2)的增加,而另外的40%是因为氧合血红蛋白的去饱和作用。
因此,霍尔
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 二氧化碳 转运 doc
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
