 急性髓系白血病的规范化诊断和预后分层全文Word文档格式.docx
急性髓系白血病的规范化诊断和预后分层全文Word文档格式.docx
- 文档编号:19676349
- 上传时间:2023-01-08
- 格式:DOCX
- 页数:7
- 大小:321.96KB
急性髓系白血病的规范化诊断和预后分层全文Word文档格式.docx
《急性髓系白血病的规范化诊断和预后分层全文Word文档格式.docx》由会员分享,可在线阅读,更多相关《急性髓系白血病的规范化诊断和预后分层全文Word文档格式.docx(7页珍藏版)》请在冰豆网上搜索。
CBFB-MYH11
急性巨核细胞白血病
急性早幼粒细胞白血病伴t(15;
17)(q22;
q21);
PML/RARAa
急性嗜碱细胞白血病
AML伴t(9;
11)(p21.3;
q23.3);
MLLT3-KMT2A
急性全髓增殖性疾病伴骨髓纤维化
AML伴t(6;
9)(p23;
q34.1);
DEK-NUP214
髓系肉瘤
AML伴inv(3)(q21.3q26.2)或t(3;
3)(q21.3;
q26.2);
GATA2、MECOM(EVI1)
唐氏综合征相关髓系增殖
AML伴t(1;
22)(p13.3;
q13.3);
RBM15-MKL1
短暂异常髓系增生
AML伴BCR/ABL1
唐氏综合征相关髓系白血病
AML伴NPM1突变
母细胞性浆细胞样树突状细胞瘤
AML伴CEBPA双等位基因突变
系列不明急性白血病
AML伴RUNX1突变
急性未分化型白血病
AML伴髓系发育不良相关改变
MPAL伴t(9;
22)(q34.1;
q11.2);
BCR-ABL1
治疗相关髓系肿瘤
MPAL伴t(v;
11q23.3);
KMT2A重排
AML,不另说明(NOS)
MPAL,B/髓系,NOS
AML伴微分化
MPAL,T/髓系,NOS
AML无成熟标记
AML伴成熟标记
注:
a表中的预后因素与治疗方法密切相关,随着治疗新方法的引入,预后因素也会随着变化
1.形态学诊断:
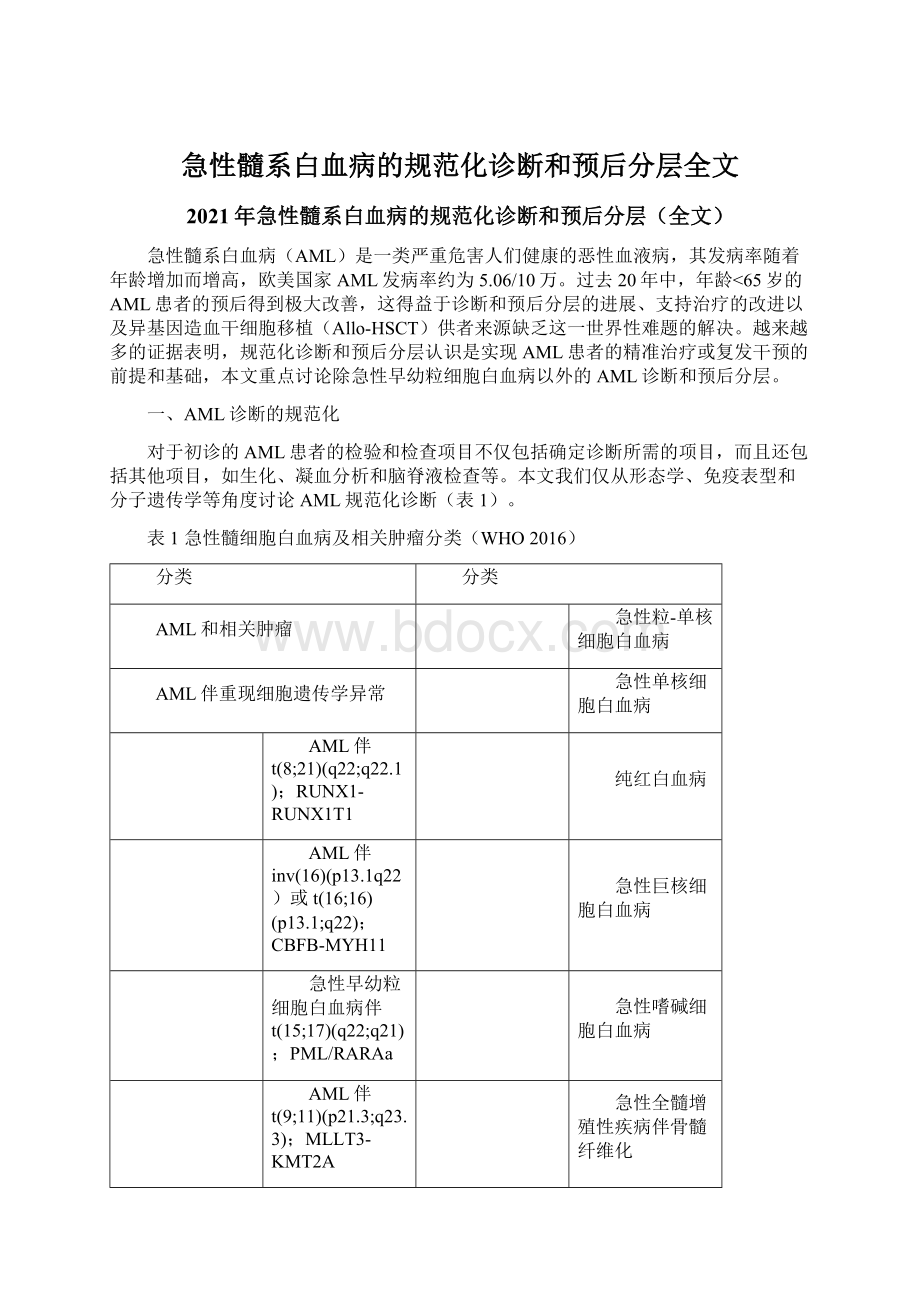
AML形态学诊断基于骨髓涂片计数500个有核细胞,其中髓系来源的原始细胞≥20%;
这些细胞应包括原始粒细胞、原始单核细胞和/或幼稚单核细胞及原始巨核细胞,但不包括形态异常的成熟单核细胞。
按照世界卫生组织(WHO)的最新分类标准,计算原始细胞占有核细胞的比例时应该以骨髓全部有核细胞作分母。
骨髓涂片的细胞组化染色应包括苏丹黑B、髓过氧化物酶和酯酶染色等。
AML初诊时还应人工分类计数外周血涂片200个有核细胞。
对于具有t(15;
17)、t(8;
21)、inv(16)或t(16;
16)细胞遗传学异常的初诊患者而言,即使原始细胞的比例不足20%,仍可确定AML的诊断。
此外,对于骨髓穿刺出现“干抽”的疑诊AML患者,骨髓活检是必需项目。
2.免疫表型分析:
用于诊断AML的抗原标记如下:
(1)髓系祖细胞表达CD34、CD117、CD33、CD13和HLA-DR;
近年的研究提示可用CD38和CD123、CD133等来确定白血病干细胞,但白血病干细胞确定并未常规用于表型分析。
(2)粒细胞表达CD65、胞内髓过氧化物酶(MPO)、CD13、CD33,CD11b和CD15,而CD16仅表达在成熟粒细胞。
此外,不表达MPO,但表达其他粒细胞标记可以诊断AML微分化型,有别于急性未分化型白血病。
(3)单核细胞表达CD14、CD36、CD64,还可表达CD13、CD33和CD11b。
(4)巨核细胞表达有CD41(糖蛋白Ⅱb/Ⅲa)、CD42(糖蛋白Ⅰb)和CD61(糖蛋白Ⅱb/Ⅲa)。
(5)红系标记有CD235a(血型糖蛋白A)、CD36。
用于诊断混合表型急性白血病(MPAL)的抗原标记包括:
(1)髓系标记:
MPO(流式细胞仪、免疫组织化学或细胞组化检测)或者单核分化标记(至少具备以下2种:
非特异酯酶染色、CD11c、CD14、CD64或溶菌酶)。
(2)T淋系标记:
胞内CD3强表达(用针对CD3ε链的抗体)。
(3)B淋系标记:
CD19强表达,并伴以下1种抗原强表达:
胞内CD79a、CD22或CD10或者是CD19弱表达,伴以下2种抗原强表达:
胞内CD79a、CD22或CD10。
T或B淋系抗原强表达是指相应抗原的表达水平与正常T或B细胞抗原表达的荧光强度相当或更强。
此外,对于怀疑母细胞性浆细胞样树突状细胞瘤的初诊白血病患者,还应该增加以下免疫表型检测标记:
CD4、CD56、CD123和TCL1等。
3.细胞遗传学/分子遗传学分析:
对于疑诊AML患者,常规细胞遗传学检查(G和/或R显带)是必检项目;
用于WHO关于“AML伴重现细胞遗传学异常”以及“AML伴骨髓发育不良相关改变”的疾病分类(表1)。
此外,部分涉及表观遗传学(如KMT2A[MLL]、CREBBP、NSD1)和核孔复合体的组份(如NUP98、NUP214)等的基因,虽然被认为是参与白血病发生的基因,但并未被正式用于AML的疾病分类。
细胞遗传学检测至少应分析20个具备中期分裂相的骨髓细胞以便确定正常或异常核型;
欧洲白血病网络(ELN)共识建议应该在5~7d出具细胞遗传学结果的报告以尽早确定AML的预后分层。
如果常规细胞遗传学检查未能检测到异常,就应借助免疫荧光原位杂交技术(FISH)去检测RUNX1-RUNX1T1、CBFB-MYH11、KMT2A(MLL)和MECOM(EVI1)等基因重排或5q、7q缺失等。
4.分子生物学分析:
AML分子生物学检测应包括:
(1)用于疾病分类的基因突变,如NPM1、CEBPA和RUNX1等。
(2)FLT3突变,既包括ITD(含突变和野生等位基因的比例),又包括TKD(D835和I836密码子的突变),这些突变不仅具有预后预测意义,而且是酪氨酸激酶抑制剂的靶点。
(3)TP53和ASXL1突变,提示预后不良。
如果AML患者被怀疑伴发胚系易感基因,应该采取患者口腔颊黏膜/毛发/皮肤成纤维细胞样本,在有经验的实验室对已知的白血病易感基因进行检测(如CEBPA、DDX41、RUNX1、ANKRD26、ETV6、GATA2、TP53等)。
二、AML预后分层的规范化
依据近年来国内外学者关于AML预后分层的研究,可以将其分为初诊时的预后分层以及根据微小残留病(MRD)检测的预后分层。
1.初诊AML患者的预后分层:
2017年ELN专家共识发布了依据初诊时细胞遗传学/分子遗传学指标确定的预后分层(表2),该分层体系将初诊AML划分为预后良好、预后中等和预后不良组,为患者诱导缓解后个体化治疗提供了重要依据。
除此之外,多种生物学参数与AML患者的不良预后密切相关,这些生物学参数包括年龄≥60岁(国外部分学者认为≥75岁)、骨髓增生异常综合征(MDS)或骨髓增殖性肿瘤(MPN)继发的AML、治疗相关AML、初诊时WBC增高(≥10万/μl)、诱导2个疗程未达到完全缓解以及合并中枢神经系统白血病。
此外,东部肿瘤合作组体能(ECOG)评分≥3及造血干细胞移植合并症指数≥3也与化疗和/或造血干细胞移植后非复发死亡增高密切相关。
表2
AML患者预后分层(2017ELN共识)a
危险分层
细胞遗传/分子生物学异常
预后良好
t(8;
q22.1)RUNX1-RUNX1T1
inv(16)(p13.1q22)或者t(16;
16)(p13.1;
q22)
CBFB-MYH11
NPM1突变不伴发FLT3突变或FLT3-ITDlowb
CEBPA双等位基因突变
预后中等
NPM1突变和FLT3-ITDhighb
野生型NPM1不伴FLT-ITD突变或伴有FLT3-ITDlowb(不伴不良细胞遗传学异常)
t(9;
MLLT3-KMT2A
c
未分到预后良好或预后不良组的细胞遗传学异常
预后不良
t(6;
t(v;
inv(3)(q21.3q26.2)
或者
t(3;
q26.2);
GATA2,MECOM(EVI1)
-5
del(5q);
-7;
-17/abn(17p)
复杂染色体异常d,染色单体
野生型NPM1以及FLT3-ITDhighb
RUNX1突变
e
ASXL1突变
TP53突变
f
a表中的预后因素与治疗方法密切相关,随着治疗新方法的引入,预后因素也会随着变化,AML为急性髓系白血病,ELN为欧洲白血病网络;
b
low代表低等位基因比例(<
0.5);
high代表高等位基因比例(≥0.5);
最近的研究提示具有NPM1突变的AML患者如果同时伴有FLT3-ITDlow,则提示预后良好,无需选择异基因造血干细胞移植治疗;
c预后优于少见的、重现的不良基因突变;
d3个以上的不相关的细胞遗传学异常,不伴WHO确定的易位或倒位其中之一,包括t(8;
21),inv(16)或t(16;
16)、t(9;
11)、t(v;
11)(v;
q23.3)、t(6;
9)、inv(3)或t(3;
3);
AML
伴BCR-ABL1;
e这些突变伴良好细胞遗传学异常时,不被认为是不良预后因素;
fTP53突变与复杂染色和染色单体密切相关
2.基于MRD的AML预后分层:
近年来,MRD在AML预后分层中的作用备受关注、并在疗效评估方面有逐步取代血液形态学(HCR)的趋势;
尤为重要的是AML患者接受治疗后的MRD定量检测不仅实现了ELN分层中预后良好组患者的再分层,而且实现了MRD指导的干预和/或治疗,降低了复发率、提高了生存率。
3.MRD的概念:
MRD是指白血病患者经化疗和/或造血干细胞移植(HSCT)等治疗获得HCR后(骨髓涂片经瑞吉染色后,光学显微镜检测原始细胞≤5%)患者体内残存的白血病细胞;
健康成人每公斤(kg)体重骨髓有核细胞数是(10~13)×
109/kg,一例体重70kg的患者骨髓有核细胞数量为(0.7~0.9)×
1012,如果以形态学缓解的5%为阈值,那么急性白血病患者获得HCR时,体内还剩余1010左右的白血病细胞。
与形态学上每20个骨髓有核细胞可发现1个白血病细胞相比,MRD检测的敏感度为10-2~10-6(图1)。
AML患者获得HCR后部分患者会发生早期复发,其他患者白血病负荷进一步降低进入MRD状态;
进入MRD状态的患者部分会发生晚期复发,另一部分患者白血病负荷进一步降低,进入用现有的FCM、RQ-PCR和二代测序技术(NGS)等实验室手段检测不到白血病细胞的状态,即多数文献报道的MRD阴性状态,该状态下患者体内仍存在白血病细胞。
遗憾的是国内外学者仍然不清楚AML患者经过诱导治疗、巩固治疗后体内的白血病负荷低于多少“阈值”就可停止治疗,并被治愈(图1)。
▲图1
微小残留病与急性白血病肿瘤复发和复发的关系及检测方法
4.用于AML患者MRD检测的分子和/或抗原标记:
AMLMRD检测标记有:
(1)白血病特异基因,如RUNX1-RUNX1T1、PML/RARA、CBFB-MYH11、TLS-ERG、NPM1突变以及KMT2A(也称为MLL)重排等。
(2)泛白血病基因,如WT1、PRAME等。
(3)利用白血病异常免疫表型(LAIPs)、与正常骨髓表型相鉴别(D-F-N)以及检测白血病干细胞(LSC)等方法借助FCM检测MRD。
5.MRD检测方法:
尽管FISH、FCM、RQ-PCR以及NGS等方法被用于AML的MRD检测,但FCM和RQ-PCR仍是最常用的方法。
RQ-PCR可以检测60%左右AML患者的白血病特异性和非特异性基因,敏感度为10-5~10-6;
MFC能够检测90%以上AML患者体内存在的异常白血病细胞,其检测敏感度为10-3~10-4;
NGS检测白血病特异性基因的敏感度可达10-5~10-6。
2018年ELN工作组关于AMLMRD检测共识推荐包括:
(1)FCM技术:
①应用LAIPs和D-F-N方法借助FCM检测AML患者MRD,不推荐用外周血标本,骨髓标本室温运输,可储存3d;
②推荐0.1%为FCM检测AML患者MRD预后分层的阈值。
(2)分子学技术:
①PCR借助白血病特异基因检测AMLMRD具有高度敏感度,被认为是伴特异性基因的AML患者MRD检测的金标准,遗憾的是不足40%的AML患者存在适合MRD检测的分子标记;
②数字PCR和NGS仅用临床研究,不推荐常规用于AML患者MRD检测。
6.AML患者MRD检测的时间点和阈值:
根据文献报道和北京大学血液病研究所的临床实践及研究成果,AML患者MRD检测的时间点如下:
(1)诱导治疗的第8天;
(2)诱导治疗后;
(3)巩固治疗后;
(4)造血干细胞移植前;
(5)造血干细胞移植后6个月内每个月1次,2年内每3~6个月1次;
(6)临床医师怀疑疾病有进展的任何时间点都可行MRD检测。
AML患者预后分层的MRD阈值因检测方法不同而各异。
尽管ELN推荐FCM检测的AML患者MRD阈值为0.1%,但部分研究显示MRD水平<
0.1%可以区分出预后良好的人群。
北京大学团队发现,与初诊时的RUNX1-RUNX1T1转录本水平相比,巩固治疗后下降3log10可以将预后良好的t(8;
21)AML患者划分为高危和标危人群,因为该团队将3log10定义为区分MRD阴性和阳性的阈值。
此外,黄晓军教授团队还将CBFB-MYH11转录子下降3log10定义为区分AML伴inv(16)(p13.1;
q22)或t(16;
16)(p13.1;
q22)患者巩固治疗后MRD阴性和阳性的阈值。
遗憾的是,关于泛白血病基因WT1的阈值目前尚存争议。
根据最新文献报道和我们所在团队的研究结果,将基于MRD的AML患者预后分层归纳如下:
(1)按照巩固治疗后RUNX1-RUNX1T1或NPM1转录本下降水平可将ELN共识中预后良好组的AML伴t(8;
21)以及AML伴NPM1突变患者再分层为高危组和低危组,对于两类转录本降低<
3log10或<
4log10的高危患者应该选择Allo-HSCT来改善其不良预后。
(2)对于移植前MRD阳性的AML患者而言,单倍型相合移植(Haplo-SCT)的复发率显著低于HLA同胞相合移植,生存率显著提高,提示Haplo-SCT可克服移植前MRD对预后的不良影响。
(3)移植后MRD阳性患者的复发率显著高于MRD阴性患者,供者淋巴细胞回输或干扰素或靶向药物抢先干预可以克服移植后MRD对预后的不良影响。
三、小结
过去十余年间,尽管AML的规范化诊断和预后分层与Allo-HSCT及CAR-T细胞治疗等手段的结合使患者的预后得到改善,但是关于诊断和分层的规范化仍有许多问题需要解决。
首先,能否借助单细胞测序、转录组、3D基因组等新技术完善现有的AML诊断和分层,亦或建立新的预后分层体系;
其次,基于MRD的分层体系能否适用于接受CAR-T等新治疗手段的患者;
再次,AML患者的免疫细胞和/或自然杀伤细胞等在抗白血病方面发挥关键作用,那么能否将免疫状态的评估纳入AML预后分层体系等。
总之,AML诊断和预后分层规范化的不断完善将助力患者的精准/个体化治疗,使预后良好患者避免接受过度的治疗,从而获得长期生存的同时,减少治疗带来的不良反应、改善生活质量;
使预后不良患者提前得到干预或强化治疗,提升这部分患者的长期生存。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 急性 白血病 规范化 诊断 预后 分层 全文
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
