 届高三化学下学期考前仿真模拟考试试题Word文档下载推荐.docx
届高三化学下学期考前仿真模拟考试试题Word文档下载推荐.docx
- 文档编号:19555145
- 上传时间:2023-01-07
- 格式:DOCX
- 页数:11
- 大小:182.72KB
届高三化学下学期考前仿真模拟考试试题Word文档下载推荐.docx
《届高三化学下学期考前仿真模拟考试试题Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《届高三化学下学期考前仿真模拟考试试题Word文档下载推荐.docx(11页珍藏版)》请在冰豆网上搜索。
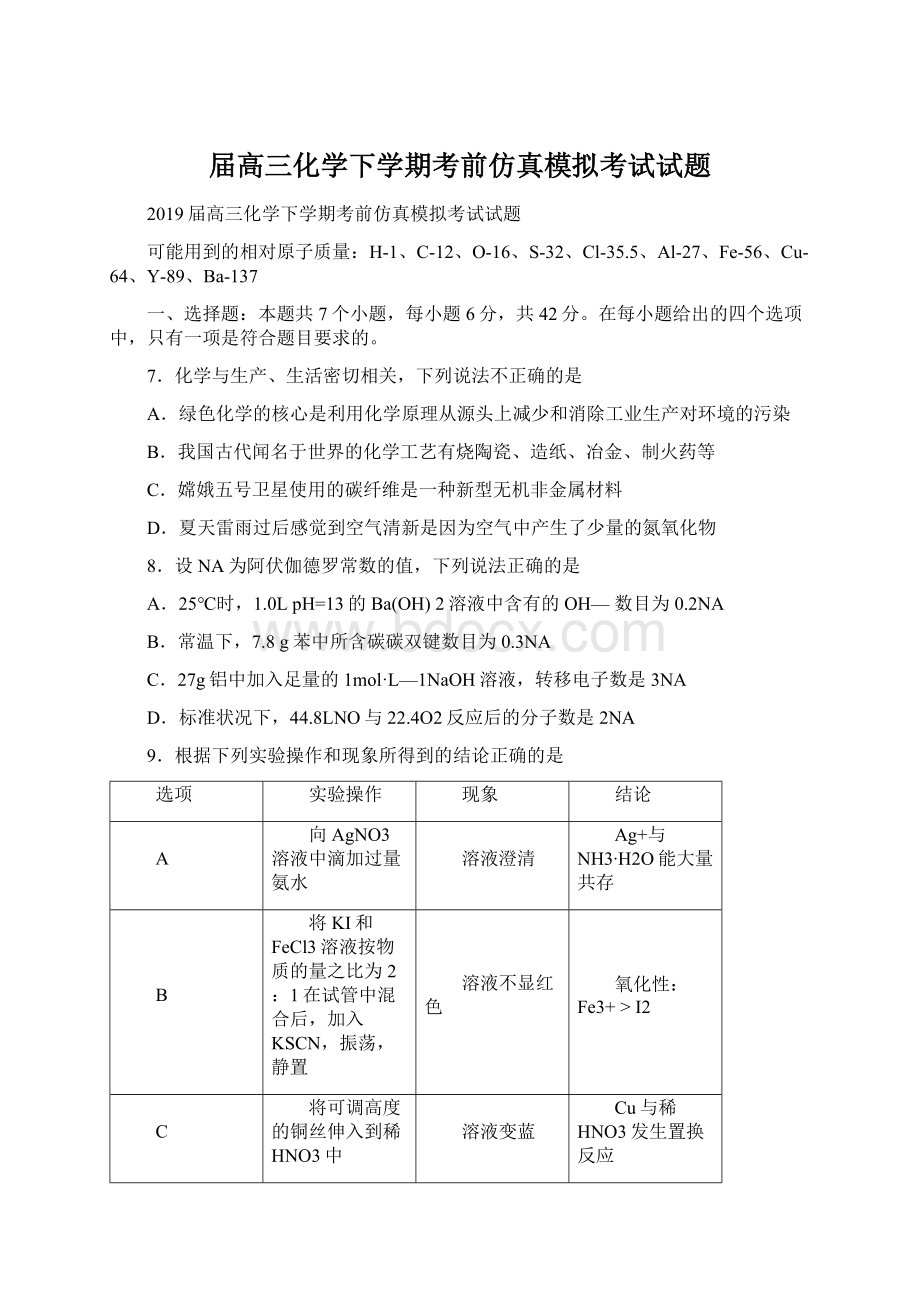
Ag+与NH3∙H2O能大量共存
B
将KI和FeCl3溶液按物质的量之比为2:
1在试管中混合后,加入KSCN,振荡,静置
溶液不显红色
氧化性:
Fe3+>
I2
C
将可调高度的铜丝伸入到稀HNO3中
溶液变蓝
Cu与稀HNO3发生置换反应
D
向稀HNO3中加入过量铁粉,再滴入少量KSCN溶液
溶液变红
稀HNO3将Fe氧化为Fe3+
10.有机物A、B均为合成某种抗支气管哮喘药物的中间体,A在一定条件下可转化为B(如图所示),下列说法正确的是
A.用FeCl3溶液可检验物质B中是否混有A
B.分子A中所有碳原子均位于同一平面
C.1molB最多可与5molH2发生加成反应
D.物质B既能发生银镜反应,又能发生水解反应
11.金属(M)—空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。
该类电池放电的总反应方程式为:
4M+nO2+2nH2O=4M(OH)n。
己知:
电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。
下列说法不正确的是
A.在M—空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
B.采用多孔电极的目的是提髙电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
C.M—空气电池放电过程的正极反应式:
4Mn++nO2+2nH2O+4ne—=4M(OH)n
D.比较Mg、Al、Zn三种金属—空气电池,Al—空气电池的理论比能量最高
12.X、Y、Z、W是原子序数依次增大的四种短周期元素,p、q、r、s是上述四种元素形成的二元化合物,其中r是一种中学常见的两性氧化物,s的水溶液是一种强酸溶液,与r反应生成P与q。
下列说法错误的是
A.简单离子半径:
W>
Y>
ZB.Y与W可以形成多种二元化合物
C.气态氢化物的沸点:
WD.p、q与r的化学键类型完全相同
13.常温下,向1L0.10mol/LCH3COONa溶液中,不断通入HCl气体(忽略溶液体积变化),得到c(CH3COO—)和c(CH3COOH)与pH的变化关系如下,则下列说法不正确的是
A.在溶液中加入一滴强酸或强碱,溶液pH变化最小的是y点
B.在y点再通入0.05molHCl气体后的溶液中:
c(Na+)=c(Cl—)>
c(CH3COO—)>
c(OH—)
C.该温度下,CH3COOH的Ka=10—4.75
D.溶液的pH比较:
x>
y>
z
三、非选择题:
共58分。
第26-28题为必考题,每个试题考生都必须作答。
第35、36题为选考题,考生根据要求作答。
(一)必考题(共43分)
26.(14分)某学习小组在实验室中利用下图装置(夹持装置略去)测定某铁硫化物(FexSy)的组成,并探究反应后D装置所得溶液中含硫化合物的组成。
(一)硫化物(FexSy)的组成
实验步骤:
步骤Ⅰ如图连接装置,检査装置气密性,装入药品;
步骤Ⅱ打开分液漏斗旋塞,缓缓滴入水,并点燃酒精喷灯;
步骤Ⅲ当硬质玻璃管中固体质量不再改变时,停止加热,继续通入—段时间的O2
步骤Ⅳ实验结束后,将D中所得溶液加水配制成250mL溶液;
……
请回答:
(1)简述检查该实验装置气密性的方法:
__________________________________________________。
(2)仪器a的作用为_________________________________。
(3)步骤Ⅲ中,停止加热后还需继续通入一段时间的O2,其目的为____________________________。
(4)步骤IV中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有____________________________。
(5)取25.00mL步骤IV中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66g。
则FexSy的化学式为___________________。
(6)问题讨论:
有同学认为可将装置D改为装有足量碱石灰的干燥管,通过测定反应前后干燥管的增重来计算硫元素的含量。
你认为此方案是否合理,为什么?
____________________________。
(二)探究反应后D装置所得溶液中含硫化合物的组成。
理论推测:
溶液中除含有Na2SO4外,还可能含有Na2SO3。
实验探究:
滴定法测定溶液中Na2SO3的含量。
可供选择的试剂:
①0.10mol•L—1KmnO4酸性溶液、②30%H2O2、③0.10mol•L—1KI淀粉溶液
(7)所选试剂为___________(填序号),所选试剂应装在____________(填“酸式”或“碱式”)滴定管中。
盛装试剂前应润洗滴定管,润洗方法是________________________________________________。
27.(14分)金属镉广泛用于合金制造及电池生产等,一种用铜镉废渣(含Cd、Zn、Cu、Fe及Co等单质)制取海绵镉的工艺流程如下:
∣
MnO、稀硫酸KMnO4溶液调pHZn粉→海绵镉
↓↓↓↓
铜镉废渣→破碎、粉磨→浸出―—→除铁—→过滤—―→沉镉——ⅥⅦ
Ⅰ↓ⅡⅢ↓ⅣⅤ→滤液――→过滤→ZnSO4溶液
Cu渣Fe(OH)3、MnO2↑↓
Zn粉、Sb盐Co渣
(1)步骤Ⅰ进行破碎和粉磨的目的是__________________________________________________。
(2)步骤Ⅱ需隔绝O2的原因_______________________________________(用文字和方程式说明)。
(3)步骤Ⅲ中除铁发生的离子反方程式为________________________________________________。
(4)步骤Ⅳ调节pH适宜的试剂是______________,应调整的范围为__________________________。
(已知部分氢氧化物开始沉淀和沉淀完全的pH如下表)
氢氧化物
Fe(OH)3
Cd(OH)2
Zn(OH)2
开始沉淀的pH
1.5
7.2
5.9
沉淀完全的pH
3.3
9.9
8.9
(5)步骤Ⅴ发生的反应为Zn+Co2+=Zn2++Co,(已知Sb的金属活动性介于Cu和Ag之间),加入少量锑盐能加快反应的进行,其原因是__________________________________________________。
(6)用石墨作阳极,纯锌作阴极电解ZnSO4溶液可得高纯锌,电解时总反应的离子方程式为__________________________________;
电解后的残液返回到步骤_________(填流程中数字)。
28.(15分)对温室气体二氧化碳的研究一直是科技界关注的重点。
I.在催化剂存在下用H2还原CO2是解决温室效应的重要手段之一,相关反应如下:
主反应:
CO2(g)+4H2(g)=CH4(g)+2H2O(g)△H1
副反应:
CO2(g)+H2(g)=CO(g)+H2O(g)△H2=+41.2kJ/mol
已知:
H2和CH4的燃烧热分别为-285.5kJ·
mol—1和-890.0kJ·
mol—1
H2O(l)=H2O(g)△H=+44kJ·
(1)△H1=___________kJ·
mol—1。
(2)有利于提高CH4平衡产率的反应条件是(至少写两条)_________________________________。
工业上提高甲烷反应选择性的关键因素是_____________________。
(3)T℃时,若在体积恒为2L的密闭容器中同时发生上述反应,将物质的量之和为5mol的H2和CO2以不同的投料比进行反应,结果如图所示。
若a、b表示反应物的转化率,则表示H2转化率的是_______________,c、d分别表示CH4(g)和CO(g)的体积分数,由图可知
=_____________时,甲烷产率最高。
若该条件下CO的产率趋于0,则T℃时①的平衡常数K=_____________________。
II.溶于海水中的CO2,95%以HCO3—形式存在。
在海洋中,通过下图钙化作用实现碳自净。
(4)写出钙化作用的离子方程式____________________________________________________。
(5)电解完成后,a(左)室的pH值________________(“变大”、“变小”或“几乎不变”);
其间b(中)室发生反应的离子方程式为___________________________________________________________。
(二)选考题(15)请考生从2道化学题任选一题作答。
如果多做,则按所做的第一题计分。
35.[化学——选修3:
物质结构与性质](15分)
Cu、Ni、V为制造合金及合成催化剂的重要元素。
(1)Cu元素位于元素周期表的__________区,其基态原子有___________种能量不同的电子。
(2)[Cu(NH3)4]SO4是一种重要的配合物。
与SO42—互为等电子体的分子的化学式为_______________(任写一种);
NH3分子的VSEPR模型为__________________。
(3)Ni(CO)4的熔点为-25℃,沸点为43℃。
其晶体类型为_______________。
晶体中σ键和π键的数目之比为_____________。
(4)Ni可作为
或
与H2加成的催化剂。
在相同压强下,
的沸点比
低,原因为______________________________________________________。
(5)有增强胰岛素和降糖作用,其中所含非金属元素的电负性由小到大的顺序为:
_______________(用元素符号表示);
氧原子的杂化轨道类型为____________。
(6)已知:
钇(Y)钡铜氧晶体的晶胞是一个长方体(如图所示),其晶胞参数分別为anm、bnm,阿伏加德罗常数的值为NA。
则该晶体的密度为___________________________g/cm3(列出计算式即可)。
36.[化学—选修5:
有机化学基础](15分)
以丙烯为原料合成抗炎药物D和机体免疫增强制剂Ⅰ的合成路线如下(部分反应条件和产物己经略去):
回答下列问题:
(1)由丙烯生成A的反应类型为_______________,由H生成I的反应类型为______________。
(2)F中含氧官能团的名称为_____________________。
(3)化合物G的化学式为C5H10O3N2,则其结构简式为________________________。
(4)A→B反应的化学方程式为________________________________________________________。
(5)A的同分异构体中属于苯的同系物的共有_____________种(不包含A),其中核磁共振氢谱有四组峰的是_________________________(写一种结构简式)。
。
结合上述流程中的信息,设计由制备
制备
的合成路线:
_____________________________________________。
郎溪中学2019届高考仿真模拟考试
化学参考答案及评分标准
一、选择题(共42分)
7、D8、C9、B10、A11、C12、D13、B
二、非选择题(共58分)
26.(14分)
(1)如图连接好装置,在D装置导管末端加接乳胶管并伸入盛水的烧杯中,再向分液漏斗中加入适量的水后,打开活塞观察到烧杯内水中乳胶管的管口处有气泡逸出,说明该装置的气密性良好(2分);
(2)防止倒吸(1分);
(3)使生成的SO2全部被NaOH溶液吸收(1分);
(4)250mL容量瓶、胶头滴管(2分);
(5)FeS2(2分);
(6)否;
部分SO2被氧化,且空气中的CO2和水蒸气可能使干燥管增重(2分);
(7)①(1分);
酸式(1分);
向用蒸馏水洗净的滴定管中加入适量的待测液或标准液,倾斜并转动滴定管洗涤内壁,最后将洗涤液经滴定管尖嘴放出。
重复上述操作2-3次即可。
(2分)。
27.(14分)
(1)加快浸取速率,提高原料浸取率(2分);
(2)防止发生2Cu+4H++O2=2Cu2++2H2O,导致铜被浸出(2分);
(3)3Fe2++MnO4-+4H+=MnO2↓+3Fe3++2H2O(2分);
(4)ZnO或Zn(OH)2(1分);
3.3≤pH<5.9(2分);
(5)形成原电池,Zn作负极,加快Co2+在锑正极表面得到电子析出(2分);
(6)2Zn2++2H2O
2Zn↓+O2↑+4H+(2分);
Ⅱ(1分)。
28.(15分)
(1)—164.0(2分);
(2)降低温度,增大压强(2分);
催化剂(1分);
(3)b(1分);
4(2分);
100(2分);
(4)2HCO3—+Ca2+=CaCO3↓+CO2↑+H2O(2分);
(5)几乎不变(1分);
H++HCO3—=CO2↑+H2O(2分)
35.(15分)
(1)ds(1分);
7(1分);
(2)CCl4(SiCl4、CBr4、SiF4)(1分);
四面体形(1分);
(3)分子晶体(1分);
1:
1(2分);
(4)
形成分子内氢键,而
形成分子间氢键(2分);
(5)H<C<N<O(2分);
sp3(1分)
(6)
(3分)
36.(15分)
(1)加成反应;
取代反应(2分);
(2)羰基(1分);
(3)
(2分);
(3分);
(5)21(3分);
(1分);
(6)
(3分)
命题人:
第8、10、12、26、28、36题—汪年庆;
第7、9、11、13、27、35题—李书建。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 届高三 化学 学期 考前 仿真 模拟考试 试题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
