 中考化学满分秘籍之专题训练质量守恒定律Word文件下载.docx
中考化学满分秘籍之专题训练质量守恒定律Word文件下载.docx
- 文档编号:19552561
- 上传时间:2023-01-07
- 格式:DOCX
- 页数:18
- 大小:104.15KB
中考化学满分秘籍之专题训练质量守恒定律Word文件下载.docx
《中考化学满分秘籍之专题训练质量守恒定律Word文件下载.docx》由会员分享,可在线阅读,更多相关《中考化学满分秘籍之专题训练质量守恒定律Word文件下载.docx(18页珍藏版)》请在冰豆网上搜索。
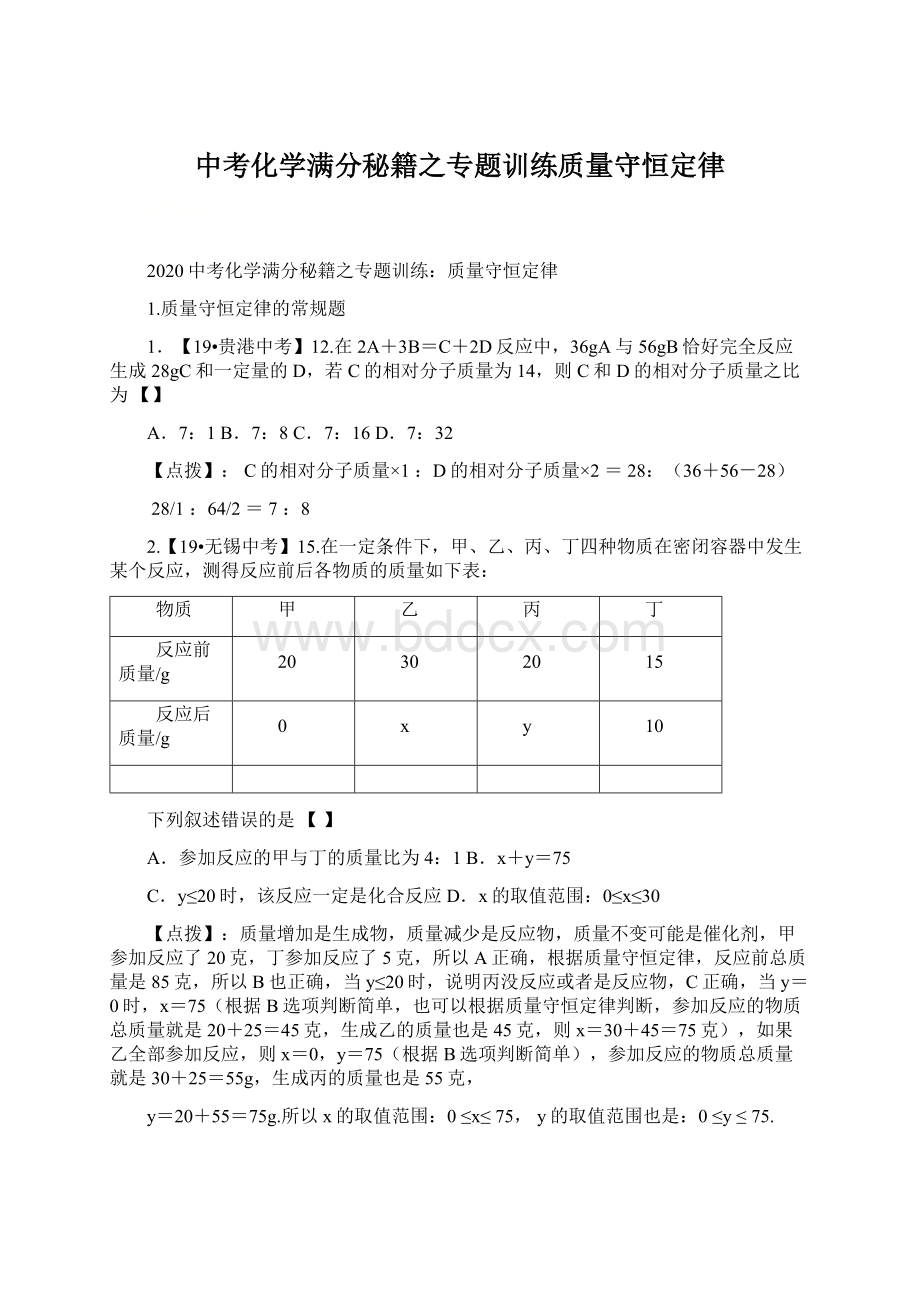
C.y≤20时,该反应一定是化合反应D.x的取值范围:
0≤x≤30
质量增加是生成物,质量减少是反应物,质量不变可能是催化剂,甲参加反应了20克,丁参加反应了5克,所以A正确,根据质量守恒定律,反应前总质量是85克,所以B也正确,当y≤20时,说明丙没反应或者是反应物,C正确,当y=0时,x=75(根据B选项判断简单,也可以根据质量守恒定律判断,参加反应的物质总质量就是20+25=45克,生成乙的质量也是45克,则x=30+45=75克),如果乙全部参加反应,则x=0,y=75(根据B选项判断简单),参加反应的物质总质量就是30+25=55g,生成丙的质量也是55克,
y=20+55=75g.所以x的取值范围:
0≤x≤75,y的取值范围也是:
0≤y≤75.
3.【19•濮阳模拟】11.小丽在化学实验室发现,硝酸银溶液存放在棕色瓶中。
小丽查阅资料得知,硝酸银见光易分解,产生一种有刺激性气味的气体。
该气体可能是【】
A.NO2B.NH3C.SO2D.N2
根据反应前后元素种类不变来判断
4.【19•郑州一模】11.将CO和CO2的混合气体共3.2g通过足量灼热的氧化铜粉末,充分反应后,将气体通入足量澄清石灰水中(气体全部被吸收),过滤,测得溶液质量减少5.6g,则原混合气体中碳元素的质量分数为A.21.0%B.27.3%C.33.3%D.37.5%【】
溶液质量减少5.6g,说明生成二氧化碳4.4g.混合气体含碳元素1.2g.
5.【19•十堰中考】20.将20.0g铜锌合金置于烧杯中,向其中逐渐加入稀硫酸。
当加入148.4g稀硫酸时,不再有气体生成,此时测得烧杯中混合物的质量为168.0g。
(1)反应中生成气体的质量是 g;
(2)求反应后烧杯溶液中溶质的质量分数。
(写出计算过程)
【答案】:
(1)0.4
(2)20%
根据质量守恒定律,生成氢气的质量为20.0g+148.4g-168.0g=0.4g
反应后烧杯中溶液的质量为13g(锌的质量)+148.4g-0.4g=161g
6.【19•西宁中考】22.小红同学将未知浓度的过氧化氢溶液34g,加入盛有0.5g二氧化锰的烧杯中,待完全反应后,称得烧杯中剩余物质的质量为33.7g。
计算该过氧化氢溶液中溶质的质量分数。
5%,根据质量守恒定律可得,生成的氧气的质量为34g+0.5g-33.7g=0.8g
7.【19•天津中考】10.在化学反应A+2B═C+2D中,已知16gA与64gB恰好完全反应,生成C和D的质量比为11:
9,又知B的相对分子质量为32,则D的相对分子质量为
A.9B.12C.18D.36【】
A+2B=C+2D(16+64)×
=36
642x
64g36x=18
8.【19•湘潭中考】14.在A+B→C+D的反应中,下列叙述错误的是【】
A.若C和D为盐和水,该反应不一定是中和反应
B.若A是氧化铜、C为铜,该反应不一定是置换反应
C.若将20gA和30gB混合,则生成C和D的总质量一定为50g
D.此反应可能是复分解反应
C.生成物的质量≤50g
9.【19•湖州中考】7.一定质量的某有机化合物X与8克氧气恰好完全反应,生成8.8克二氧化碳和1.8克水。
X中各元素的质量比为 ______
12:
1
10.【19•长沙中考】24.为了测量某石灰石矿中碳酸钙的含量,进行了如下实验:
称取10g石灰石样品,反复灼烧至质量不再改变,称量剩余固体质量为6.7g(假设杂质不参与反应),请计算:
(1)反应生成的CO2的质量为 _g。
(2)该石灰石样品中碳酸钙的质量分数.
(1)3.3
(2)75%【点拨】:
生成CO2的质量为:
10g-6.7g=3.3g
11.【19•衡阳中考】21.将一定量的丙醇(C3H8O)和氧气置于一个密封的容器中引燃,测得反应前后各物质的质量如表。
下列说法错误的是【】
丙醇
氧气
水
二氧化碳
X
6.0
14.8
0.4
2
7.2
9.2
a
A.表中a的值为2.8B.参加反应的氧气和生成二氧化碳的质量比为16:
11
C.X中一定含碳元素、氧元素D.该反应属于分解反应
燃烧不完全同时生成CO
根据反应前后各元素的种类不变,各元素的质量不变.X中含碳元素1.2g、氧元素1.6g
参加反应的物质的质量之和是18.8g,而生成物水和二氧化碳的质量之和16g,所以X是生成物,质量是18.8g-16g=2.8g,B.参加反应的氧气和生成二氧化碳的质量比为:
(14.8﹣2):
(9.2﹣0.4)=16:
11,该选项说法正确;
12.【19•说明与检测】某种催化剂可将二氧化碳转化成燃料甲醇,其反应的微观示意图如下:
乙甲丙丁
(1)参加反应的甲和乙的分子个数比为_________
(2)甲和丁化学性质不同的原因是_________________________
(1)1:
3
(2)分子的构成不同
13.【19•说明与检测】p59.某同学在做实验时发现:
铜片在空气中灼烧变黑后质量增大了。
请你根据质量守恒定律解释其原因.
铜与氧气发生化学反应生成了黑色的氧化铜。
即参加反应的铜片和氧气的质量之和等于生成的氧化铜的质量,所以生成的黑色固体的质量大于铜片的质量.
14.【19•说明与检测】p40.某种催化剂可将二氧化碳转化成燃料甲醇,其反应的微观示意图如下(图中的微粒恰好完全反应),请回答一下问题:
(1)丁的化学式为_________
(2)反应中甲和丙的质量比为__________
(3)请从微观角度解释该反应遵循质量守恒定律的原因___________________________
(1)H2O
(2)3:
16
(3)化学反应前后碳原子、氢原子、氧原子的种类、数目和质量均没有改变.
15.【19•说明与检测】p124.甲烷和水反应可以制备水煤气(混和气体),其反应的微观示意图如下所示:
根据以上微观示意图得出的结论中,正确的是【】
A.水煤气的成分是一氧化碳和氧气B.反应中含氢元素的化合物有三种
C.反应前后碳元素的化合价没有发生变化D.反应中甲和丁的质量之比为8:
3
16.【19•说明与检测】p90.取15g已部分变质的氢氧化钠固体,加入到50g稀盐酸中,恰好完全反应后,称量剩余物质的质量为60.6g,求该固体中氢氧化钠的质量.
4.4g
17.【19•说明与检测】p27.密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下
a
b
c
d
19.7
8.7
31.6
O.4
待测
17.4
0
3.6
下列说法不正确的是【】A.c一定是化合物,d可能是单质
B.c中元素种类等于a、b、d三种物质中元素的种类之和
C.反应过程中,b与d变化的质量之比为87:
36
D.若a与c的相对分子质量之比为197:
158,则反应中a与c的化学计量数之比为l:
质量增加是生成物,质量减少是反应物,质量不变可能是催化剂,
c→b+d+a
31.68.73.219.719.7/197:
31.6/158=1:
18.【19•攀枝花中考】15.用K2CO3溶液吸收CO2得到KHCO3,化学方程式为:
K2CO3+CO2+H2O=2KHCO3.向K2CO3溶液中通入CO2,至K2CO3恰好完全反应,
得到溶质的质量分数为20%的溶液50.0g。
则原K2CO3溶液中溶质的质量分数为【】
A.13.8%B.14.4%C.15.4%D.16.8%
K2CO3溶液的质量+CO2的质量=50.0g
19.【19•郑州一中】6.某物质在空气中完全燃烧时,生成质量比为11:
9的CO2和H2O,则该物质的化学式可能是A.COB.CH4C.C2H2D.C2H5OH【】
生成物二氧化碳11g含碳3g,水9克含氢1g,C:
H=3:
1,反应前后元素的质量不变,反应前反应物CH4符合C:
H=3:
生成物二氧化碳和水的分子个数比为11/44:
9/18=1:
2,碳和氢的原子个数比1:
4,反应前后原子的个数不变,反应前反应物中碳和氢的原子个数比也是1:
4
20.【19•郑外模拟】14.现有2.84g双氢青蒿素燃烧生成6.6gCO2和2.16gH2O,则双氢青蒿素中氧的质量与其燃烧消耗氧气的质量之比为【】
A.5:
62B.63:
5C.5:
36D.5:
37
6.6×
=1.82.1×
=0.24
或者用关系式计算CO2~CH2O~2H
4412182
6.6x=1.82.16x=0.24
(2.84-1.8-0.24):
(6.6+2.16-2.84)=5:
37
21.【18•青岛中考】25.随着科学的发展,新能源的开发不断取得突破。
清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如下图(图中的微粒恰好完全反应)所示。
请根据微观示意图回答以下问题.
(1)该反应的化学方程式为______
(2)下列说法正确的是______(填写字母序号).
A.反应前后原子数目发生改变B.该反应属于复分解反应
C.甲是单质,乙、丙、丁均为化合物
D.该反应体现了无机物在一定条件下可以转化为有机物
(1)3H2+CO2
CH4O+H2O(或3H2+CO2
CH3OH+H2O)
22.【18•新乡一模】14.某纯净物3g在氧气中完全燃烧,生成8.8g二氧化碳和5.4g水。
下列说法不正确的是【】
A.该纯净物中含有C、H元素,不含O元素B.该反应中O2和CO2的质量比为14:
11
C.该反应中O2和H2O的分子数之比为7:
6D.该纯净物中C、H原子的个数比为1:
4
2.4/12:
0.6/1=1:
3
23.【18•河南B卷】11.氢化钙与水反应的化学方程式为CaH2+2H2O=X+2H2↑.下列说法中不正确的是【】
A.氢化钙可用于干燥多种气体B.氢化钙是一种燃料提供剂
C.X的化学式为Ca(OH)2D.氢化钙需要密封保存
氢化钙只能干燥氢气
24.【18•开封一模】14.向盛有5g某黄铜(铜锌合金)样品的烧杯中加入100g稀硫酸,恰好完全反应,反应结束后,测得烧杯内物质的总质量为104.96g。
则该合金样品中锌的质量分数是A.26%B.36%C.63%D.74%【】
根据质量守恒定律,生成氢气的质量为5g+100g-104.96g=0.04g
25.【17•绵阳中考】9.120℃时,取3g有机物R在氧气中完全燃烧,产物只有CO2和H2O。
将
其燃烧产物依次通过足量的浓硫酸和足量的澄清石灰水中,最终浓硫酸增重1.8g;
澄清石灰水中产生10g沉淀。
下列判断正确的是【】
A.R的化学式一定是CH2O中B.6gR完全燃烧消耗氧气6.4g
C.R中碳元素的质量分数约为85.7﹪D.R仅由C、H两种元素组成,其质量比为6:
R的化学式中碳氢氧的原子个数比是1:
2:
26.【16•河南竞赛】20.向100克硝酸银溶液中加入稀盐酸恰好完全反应,过滤后所得溶液的质量等于原硝酸银溶液的质量,则所加稀盐酸中溶质的质量分数为【】
A.42.1%B.43.5%C.56.9%D.25.4【点拨】:
根据质量守恒定律,盐酸溶液的质量就等于氯化银沉淀的质量.
方法同无数据的化学方程式计算【19•河南中考】第14题.
27.【11•大连中考】现有一瓶无色、有特殊气味的液体,是甲醇(CH3OH)或乙醇(C2H5OH).通过测定该液体充分燃烧后生成的二氧化碳和水的质量可确定是哪种物质,解释原理.
【答案】:
根据质量守衡定律,化学反应前后元素的种类和质量不变,根据生成的二氧化碳和水的质量,可求出碳元素和氢元素的质量比,再与甲醇和乙醇中碳元素和氢元素的质量比对照,即可知道是哪种物质.
28.小丰为了探究一瓶CaCl2溶液的溶质质量分数,取该溶液50g,加入50gNa2CO3溶液,恰好完全反应,所得溶液质量95g,计算该CaCl2溶液的溶质质量分数?
11.1%
根据质量守恒定律,反应后减少的质量就是产生气体或生成沉淀的质量.
2.质量守恒定律的较难题
1.【19•哈尔滨中考】15.将炉甘石(碳酸锌和杂质)与木炭粉的混合物51.2g隔绝空气加热到约800℃,恰好完全反应后得到固体质量38g(杂质不含锌元素,也不反应,碳元素完全转化成二氧化碳),则炉甘石中锌元素的质量分数为【】
A.25.4%B.32.4%C.26%D.50%
二氧化碳的质量为51.2-38=3.2根据氧元素全部来自碳酸锌可得关系式为
2Zn~2ZnCO3~3CO2
130250132
x=13y=2513.2g
锌元素的质量分数为
×
100%=26%
2.【19•大连中考】25.氢氧化镁是一种固体阻燃剂,在加热条件下分解为氧化镁和水。
(2)现将5.8g氢氧化镁加热一段时间后,测得剩余干燥的固体中氧元素的质量为2.4g。
计算已反应的氢氧化镁的质量。
(2)2.9g
生成水中氧元素的质量为3.2g-2.4g=0.8g,已反应的氢氧化镁中氧元素的质量是生成水中氧元素质量的2倍.0.8×
32/58=2.9
Mg(OH)2~H2O~O
5816
x=2.90.8
3.【19•新乡二模】14.向氢氧化钠和碳酸钠固体混合物4.65g中加入50g质量分数为7.3%的稀盐酸,恰好完全反应得到中性溶液。
那么反应后所得溶液中溶质的质量为【】
A.5.85gB.11.7gC.17.55gD.160.3g
根据氯元素质量守恒HCl~NaCl50g×
7.3%=3.65g
36.558.5
3.65gx=5.85g
根据氯元素质量守恒50g×
7.3%=3.65g设氯化钠的质量为x
3.65
100%=x.
100%x=5.85
4.【19•盐城中考】15.工业上,高温煅烧石灰石可制取生石灰。
现有100gCaCO3样品,高温煅烧一段时间后,剩余固体的质量为67g。
下列推断不符合客观事实的是【】
A.生成
的质量是33gB.生成物中CaO的质量是42g
C.剩余固体中钙元素的质量分数大于
D.剩余固体中碳元素与氧元素的质量之比大于1:
碳酸钙中碳元素与氧元素的质量比为1:
4,反应过程中碳元素全部转化为二氧化碳,氧元素只有部分转化,所以剩余固体中碳元素与氧元素的质量之比小于1:
5.【19•天津中考】25.某金属粉末可能由镁、锌、铁、铝、银中的一种或几种组成。
取该样品2.4g,向其中加入100g一定溶质量分数的稀硫酸,恰好完全反应,生成0.2g氢气,得到无色溶液,固体无剩余。
下列说法正确的是【】
A.样品中一定含有镁B.样品中一定不含有银,可能含有铁
C.所得溶液中溶质总质量为12gD.加入的稀硫酸的溶质质量分数为19.6%
根据氢元素质量守恒,硫酸溶质的质量为9.8g,2.4+9.8-0.2=12
6.【19•湘潭中考】20.某同学取8gZnO、Al2O3、Cu的混合固体,与73g20%的稀盐酸混合后恰好完全反应,则该混合固体中金属元素的百分含量为【】
A.70%B.40%C.30%D.60%
根据关系式2HCl~H2O~O
7316
14.6x=3.2(8-3.2)
8=60%
7.【19•巴中中考】12.向10.7gMg、Al、Zn固体混合物中加入一定量的H2SO4恰好完全反应,反应后的溶液质量增加了10.1g,将反应后溶液蒸发结晶,干燥。
获得固体质量为【】
A.15.5gB.25.1gC.39.5gD.20.3g
溶液增加的质量=固体的质量-氢气的质量,氢气的质量0.6g,根据氢元素质量守恒,硫酸根的质量就是28.8g,28.8g+10.7g=39.5g.或10.7+29.4-0.6=39.5
8.【19•郑州一中】14.4.5g镁和铝的合金加入一定质量、一定质量分数的稀盐酸中,恰好完全反应,产生0.4g氢气。
向反应后的溶液中加入一定质量的NaOH溶液,恰好完全反应,则生成NaCl的质量为【】
A.23.4gB.29.25gC.11.7gD.5.85g
2HCl~H2~2NaCl
2117
0.4x=23.4
9.【19•烟台中考】22.取一定质量的CaCO3高温灼烧一定时间,测得反应后剩余固体质量为8.8g,其中钙元素质量分数为50%,则反应放出CO2的质量为【】
A.
B.
C.
D.5g
根据钙元素质量守恒,8.8g×
50%=4.4g4.4g÷
40%=11g11g-8.8g=2.2g
10.【19•河南二模】14.取一定量的氧化镁和氧化锌的固体混合物,加入100g溶质质量分数为9.8%稀硫酸中,恰好完全反应,原固体混合物中氧元素的质量是【】
A.1.8gB.1.5gC.2.0gD.1.6g
根据氢、氧质量守恒H2SO4~H2O~O
100g×
9.8%=9.8g9816
9.8gx=1.6g
11.【19•省实验一模】14.将3.0g表面有一层氧化物薄膜的镁带,放置于98g10%的稀硫酸中恰好完全反应,所得溶液中溶质的质量为【】
A.15.0gB.12.0gC.8.8gD.16.5g
H2SO4~MgSO4
98120
9.8gx=12g
12.【19•说明与检测】p132.取镁和氧化镁的混合物6.4g,与一定质量的稀硫酸恰好完全反应,所得溶液中溶质的质量24g,则原混合物中单质镁的质量分数为【】
A.37.5%B.60%C.75%D.80%
MgSO4~MgOMg→MgO△m
12040244016
24x=8y=2.4(8-6.4)2.4
6.4=37.5%
13.【19•说明与检测】p79.有CO、N2和CO2的混合气体50g,其中碳元素的质量分数为12%,使混合气体与足量灼热的氧化铜完全反应,再将气体通入过量的澄清石灰水中,充分反应后得到的白色沉淀质量为【】
A.30克B.50克C.80克D.100克
CO+CuO
Cu+CO2Ca(OH)2+CO2=CaCO3↓+H2O
根据碳元素质量守恒,50×
12%=x.12%x=50
14.【19•南阳一模】14.把40gCO和CO2的混合气体,通过足量灼热的氧化铜,充分反应后气体的质量为44g,则原混合气体中碳元素的质量分数为【】
A.30%B.42.9%C.72.7%D.90.1%
根据碳元素质量守恒,44gCO2所含碳元素质量12g就是混合气体碳元素的质量.
15.【19•河师大二模】14.一定的溶液中含有氢氧化钾和碳酸钾两种物质,向其中加人100g溶质质量分数3.65%的稀盐酸,恰好完全反应且溶液为中性,则原混合物中K元素的质量为A.3.9克B.7.8克C.5.6克D.13.8克
HCl~KCl~K
36.539
3.65x=3.9所得氯化钾质量也是根据关系式计算
16.【19•郑州模拟】14.现有25gKOH和K2CO3的固体混合物,已知K元素与C元素的质量比是13:
1,把固体全部加入到盛有100g的足量稀硫酸的烧杯中,充分反应后,烧杯里残留物质的质量是120.6g,则烧杯中硫酸钾的质量为【】
A.4.8gB.9.6gC.17.4gD.34.8g
先求出二氧化碳的质量,再根据碳元素的质量求出钾元素的质量,再根据钾元素质量守恒求出硫酸钾的质量.
17.【19•焦作一模】14.现有MgO和Mg(OH)2组成的固体混合物共5g,向其中加入100g7.3%的稀盐酸,恰好完全反应,得到105g不饱和溶液。
则原固体混合物中镁元素的质量为【】
A.1.2gB.12gC.4.8gD.2.4g
根据镁元素质量守恒,Mg~MgCl2~2HCl
2473
x=2.4g7.3g
18.【19•焦作二模】14.氧化钙和碳酸钙的固体混合物质量为120g,将其高温煅烧至碳酸钙完全分解,称得剩余固体的质量为84g,则原固体混合物中钙元素的质量分数为【】
A.70%B.20%C.40%D.50%
84g氧化钙含钙元素的质量是60g,根据钙元素质量守恒,60
120=50%
19.【19•唐河三模】14.由C2H2、CO、H2中的一种或几种组成的气体,完全燃烧后,生成的CO2和H2O的质量之比是44:
9,该气体的组成不可能是【】
A.C2H2和COB.只有C2H2C.C2H2、H2和COD.CO和H2
根据元素质量守恒,碳元素和氢元素的质量比是12:
1.
20.【19•濮阳模拟】20.镁和铝的混合粉末4g与100g19.6%的稀硫酸恰好完全反应,将所得溶液蒸干,得到硫酸盐固体的质量为 g
23.2
【点拨】:
根据氢元素质量守恒,求出产生氢气0.4g.4+19.6-0.4=23.2
或4+(19.6-0.4)硫酸根的质量=23.2
21.【18•郑州一中】某CaO和CaCO3的混合物中钙的质量分数为60%,将50g混合物高温煅烧至固体质量不再改变,下列说法正确的是【】
A.剩余固体是混合物B.生成CO2的质量是20g
C.剩余固体的质量是42gD.原混合物中CaCO3的质量是30g
50g
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 中考 化学 满分 秘籍 专题 训练 质量 守恒定律
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
