 高三化学工业流程题典题汇总文档格式.docx
高三化学工业流程题典题汇总文档格式.docx
- 文档编号:19524908
- 上传时间:2023-01-07
- 格式:DOCX
- 页数:15
- 大小:326.14KB
高三化学工业流程题典题汇总文档格式.docx
《高三化学工业流程题典题汇总文档格式.docx》由会员分享,可在线阅读,更多相关《高三化学工业流程题典题汇总文档格式.docx(15页珍藏版)》请在冰豆网上搜索。
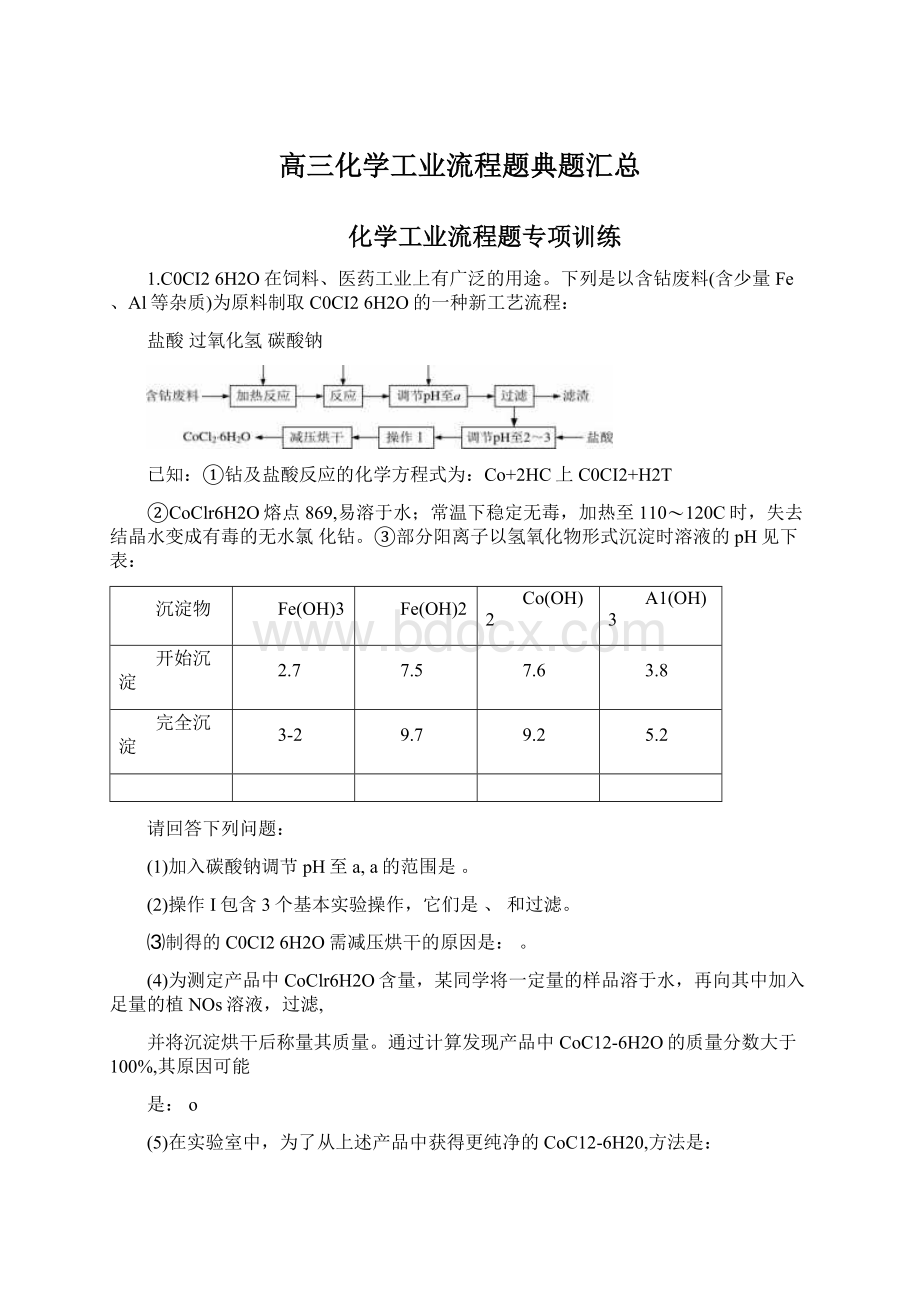
o原工艺较新工艺也有优点,其主要优点是o
2.某化学研究性学习小组通过査阅资料,设计了如下图所示的方法以含繚废催化剂为原料来制备NiSO4.7H2Oo已知某化工厂的含镰催化剂主要含有Ni,还含有AI(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。
碱液酸液H2O2
固体②
部分阳离子以氢氧化物形式完全沉淀时的pH如下:
Fe(OHb
Ni(OH)2
pH
3.2
回答下列问题:
⑴操作a、c中需使用的仪器除铁架台(带铁圈)、酒精灯、烧杯、玻璃棒外还需要的主要仪器为。
(2)“碱浸”过程中发生的离子方程式是o
(3)“酸浸”时所加入的酸是(填化学式)。
酸浸后,经操作a分离出固体①后,溶液中可能含有
的金属离子是o
(4)操作b为调节溶液的pH,你认为pH的最佳调控范围是:
(5)“调pH为2〜3”的目的是o
(6)产品晶体中有时会混有少量绿矶(FeSOy7H2O),其原因可能是。
3・高铁酸钾是一种高效的多功能的水处理剂。
工业上常采用NaClO氧化法生产,原理为:
3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4l+3NaCl+6NaNO3+5H2O
Na2FeO4+2KOH=K2FeO4+2NaOH
主要的生产流程如下:
(1)写出反应①的离子方程式
(2)
AsP(Na2FeO4)(填“〉”或“V”
流程图中“转化”是在某低温下进行的,说明此温度下^P(K2FeO4).或“=”)。
(3)反应的温度.原料的浓度和配比对高铁酸钾的产率都有影响。
图1为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;
图2为一定温度下,Fe(NO3)3质量浓度最佳时.NaClO浓度对K2FeO4生成率的影响。
■•
MaClO的质星浓度©
L/i
图1图2
1工业生产中最佳温度为9,此时Fe(NO3)3及NaClO两种溶液最佳质量浓度之比为
2若MaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:
若Fe(NO3)3加入过量,在碱性介质中K2FeO4及Fe"
发生氧化还原反应生成K3FeO4,此反应的离子方程式:
(4)K2FeO4在水溶液中易水解:
4FeO42-+10H2O^^4Fe(OH)3+8OH-+3O2f<
1在“提纯,K2Fe3中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液(填序号)。
A.H2OB.CH3COONa.异丙醇C・NH^Cl、异丙醇D.Fe(NO3)3.异丙醇
4.某铜矿石含氧化铜、氧化亚铜、三氧化二铁和脉石(SiO2),现采用酸浸法从矿石中提取铜,其工艺流程图如下。
其中铜的萃取(铜从水层进入有机层的过程)和反萃取(铜从有机层进入水层的过程)是现代湿法炼铜的重要工艺手段。
①Cu2O+2H+=Cu2++Cu+H2O;
②当矿石中三氧化二铁含量太低时,可用硫酸和硫酸铁的混合液浸出铜;
③反萃取后的水层2是硫酸铜溶液。
(1)矿石用稀硫酸处理过程中发生反应的离子方程式为:
Cu2O+2H+=Cu2++Cu+HzO
、(写其中2个)
(2)将有机层和水层分离的操作方法叫,实验室完成此操作所用到的一仪翠是。
(3)“循环I”经多次循环后的水层1不能继续循环使用,但可分离出一种匝要的硫酸盐晶体,该晶体的化学式
••
是O
(4)写出电解过程中(两电极都是惰性电极)阴极发生反应的电极反应
(5)“循环in”中反萃取剂的主要成分是
5.工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaCKh),其工艺流程如下:
1.NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。
2.高氯酸是至今为止人们已知酸
中的最强酸,沸点909。
请回答下列问题
(1)反应器I中发生反应的化学方程式为,冷却的目的
是,能用蒸馆法分离出高氯酸的原因是
(2)反应器II中发生反应的离子方程式为。
(3)通入反应器II中的SO2用另一物质H2O2代替同样能生成NaCKh,请简要说明双氧水在反应中能代
替SO2的原因是
(4)Ca(ClO)2.C1O2>
NaClO.NaCKh等含氯化合物都是常用的消毒剂和漂白剂是因为它们都具有
请写出工业上用氯气和NaOH溶液生产另一种消毒剂NaClO的离子方程式
6.钛合金是航天航空工业的亘要材料。
由钛铁矿(主要成分是TiO2和Fe的氧化物)制备TKh等产品的一种工艺流程示意如下:
fiTiOj
①TiO2+易水解,只能存在于强酸性溶液中
®
TiCh的熔点一25.0-C,沸点136.4-C;
SiCh的熔点一68.8'
C,沸点57.6C
(1)写出钛铁矿酸浸时,主要成分TiO2反应的离子方程式
加入铁屑的作用是。
(2)操作II包含的具体操作方法有。
(3)向“富含TKJ2+溶液”中加入N^COs粉末得到固体TiO2nH2O,请用恰当的原理和化学用语解释其原
因,废液中溶质的主要成分是(填化学式)。
(4)
用金红石(主要含TiO2)为原料,采用亨特(Huntei*)法生产钛的流程如下:
电解过程中阳极电极上会有气体生成,
写出沸腾氯化炉中发生反应的化学方程式,制得的TiCh液
体中常含有少«
SiC14杂质,可釆用方法除去。
(5)TiO2直接电解法生产金属钛是一种较先进的方法,电解质为某种可以传导02离子的熔融盐,原理如右
图所示,则其阴极电极反应为:
该气体可能含有
7.炼锌厂产生的工业废渣——锌渣(除了含Zn外,还含有Fe、ARCd和SKh等杂质,利用锌渣制取并回收ZnSO4-7H2O和金属镉是一个有益的尝试,其流程如下:
已知:
Fe3\Al叭Zn2\Cd2\Fe“以氢氧化物完全沉淀时的pH分别为:
3.2,4.7,6.5,9.4,9.7;
锌的
金属活动性比镉强。
试回答下列问题:
(1)“浸出”时用到的“试剂X”为(填名称)。
(2)写出“氧化”过程的离子方程式o
(3“调pH”过程可以选用o(从以下选项选择,填序号)
A.H2SO4B・ZnOC.NaOH
“滤渣2”的主要成分是(填化学式,下同)。
(4)“试剂Y”;
“滤渣3”的成分为。
(5)“操作1”的方法是;
在“操作1"
时,必须采取的实验措施是o
8•从粗产品硫酸锌固体除去铁.铜.镉等可溶性硫酸盐,从而得到较纯净的硫酸锌,实验流程如下:
Zn(OH)2
Cu(OH)2
Cd(OH)2
Mn(OH)2
pH值
8.0
6.7
9.4
10.4
部分阳离子以氢氧化物形式完全沉淀时溶液的PH参见上表,请回答下列问题:
(1)"
酸浸”步骤中,为提高锌的浸出率,可采取的措施有。
“酸浸”时适当补充少量水的原因是。
(2)滤液I加入酸性KMMh所发生反应的离子方程式,请完成剩余产物,并配平相关系数,若系数为1,
也需写上Fe2++MnO4+H+=Fe3++Mn2++
加入ZnO的原因是(写出相关方程式以及对应的文字说明)。
(3)滤渣III的成份主要是(化学式)o
(4)从滤液III得到晶体的操作过程为、冷却结晶、过滤冼涤、小心干燥。
9.工业上利用硫酸渣(含Fe2+、F0的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3)和回收(NH4)2SO4,具体生产流程如下:
(1)在废渣溶解操作时,应选用溶解(填字母人
A、氨水B、氢氧化钠C、盐酸D、硫酸
(2)物质A是一种氧化剂,工业上最好选用供选择使用的有:
空气、6、MnOz),其理由
是。
(3)
根据下图有关数据,你认为工业上氧化操作时应控制的条件是:
⑷“结晶”生成钱黄铁矶的反应化学方程式为—
(5)简述检验“滤液”中含有NH?
的实验方法:
10.高纯碳酸链广泛应用于电子工业,是制造高性能磁性材料的主要原料。
新工艺采用工业
冶铜后的废气SO2进行湿法浸取软猛矿(主要含MnOz,同时含有少量SiO2、Fe2O3>
AI2O3)来制备。
(已知亚硫酸酸性强于碳酸)
1将过量的SO2气体通入软镭矿浆中进行“浸镭”操作,并控制温度加热反应;
2向浸镭结束后的滤液中加入MnO2s同时通入空气,再用Na2CO3溶液调节pH为3.7后
过滤分离;
3调节滤液pH值为6.5〜7.2,然后加入NH4HCO3,有浅红色的沉淀生成,过滤洗涤干燥后就可以得到高纯碳酸猛。
工业流程图如下:
泓度/C
fflI通度对盘浸出率的影列
已知生成氢氧化物的pH如下表:
物质
开始沉淀pH
8.3
完全沉淀pH
3.7
9.6
9.8
请根据题中有关信息回答问题:
(1)“浸链"
后所得混合液中主要存在的金属阳离子有。
(2)由图可知,副反应MnSO4+SO2=F^MnS2O6的AH0(填>
、V或=),为减少MnS2O6的
生成,“浸镭”的适宜温度是。
(3)步骤②中加入MnO2和通入空气的作用o
(4)③中控制温度为60~70・C,温度不宜太高的原因是。
(5)及传统的电解法制MnCO3工艺相比较,新工艺的优点是
(写两点)。
11.氟碳饰矿主要化学成分为CeFCOs,它是提取饰族稀土元素的重要矿物原料。
氛碳钟矿的冶炼处理工艺已经发展到十数种,其中一种提取钟的工艺流程如下:
NaClO
焙烧后烧渣中含+4价的肺及+3价的其它稀土氟氧化物;
酸浸I的浸出液中含少就的+3价的饰
请回答下列问题
(1)焙烧前将矿石粉碎成细颗粒的目的是•
(2)酸浸II后,四价饰转化为三价,为了避免三价饰以四氟硼酸盐形式损失,用可溶性钾盐将四氟硼酸根
沉淀除去,该反应的离子方程式为:
(3)在生产过程中,酸浸I中会产生大量黄绿色气体,污染环境、腐蚀设备,写出产生黄绿色气体的离子方程
式:
,提出一种解决的方案:
•
(4)实验室中进行操作I所用玻璃仪器名称:
;
在操作I后的溶液中加入NaOH溶液是为了调节
溶液pH值获得Ce(OH)3,测定该溶液pH值的操作是•
(5)写出氧化步骤的化学方程式:
,其中还原产物是
12.2011年8月12日,网上传云南曲靖市越州镇有总量5000余吨的重毒化工废料辂渣由于非法丢放,毒水
被直接排放南盘江中。
I:
某工厂对制革工业污泥中Cr(III)回收及再利用工艺如下(硫酸浸取液中金属离子主要是CE,其次是Fe^、Al3\Ca\Mg2+):
,-4.8mol-L'
1
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
阳离子
Fe3+
Fe2+
Mg2+
Al,
Cu2+
Cr3+
开始沉淀时的pH
1.9
7.0
4.7
沉淀完全时的pH
9.0
1L1
8
909溶解)
n:
工业废水中常含有一定量的CnOY一和CrOFS它们会对人类及生态系统产生很大损害,必须进行处理。
其中一种处理方法为电解法:
该法用Fe做电极,电解含CdCV一的酸性废水,随着电解进行,阴极附近溶液pH升高,产生Cr(OH)j沉淀。
阳极的电极反应式为。
在阴极附近溶液pH
升高的原因是(用电极反应方程式解释)o
13.工业上需要利用一批回收的含铜废料制造胆矶(CuSO4-5H2O)0该废料中各种成份含量如下:
Cu和CuO约占87%,其它为M像AkFe、Si及其氧化物,还有少量的难溶物质。
工艺流程为:
部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH如下表:
Al(OH)
3
Fe(OH)
Cu(OH)
2
Mg(OH)2
3.1
回答:
(1)步骤①中为什么要将含铜废料研磨成粉状?
(2)步骤②中的离子方程式(写出2个即可):
(4)加稀硫酸酸化(2分〉(5)冷却结晶(2分)
3.
(1)MnCO3+2HCl=MnC12+CO2T+H2O(2分)
⑵图中反映浸取时间为60.分伊时漫取率岀现第一个峰值,此后吋间延攻对漫岀率汶有明曇影响,从提高生产效率角度选择浸出时间为60分钟较为合理。
(2分)
(3)碳酸链(其它碳酸盐也可)(2分)(4)MgSO4(或答硫酸镁晶体)(2分)
(5)若水分太少可能导致得到的晶体是失去部分结晶水的产物。
4.
(1)改变高岭土的结构,使其能溶于酸。
(2)230;
量筒。
(3)AI203+6H+==2Ar+3H2OFe2O3+6H+==2Fe3++3H2O(4)除去溶液中的铁离子;
(5)pH计(或精密pH试纸);
水浴加热。
5.
(1)8LiCoO,+Na2S2O3+11H2SO4=4Li2SO4+8COSQ,+Na2SO4+11H2O
LiCoO、
■
(2)将正二价铁元素氧化成正三价A1(OH)3和Fe(OH)3
(3)Co2+4-20H=Co(OH)212Li++CO32=Li2CO3|(4)Na2SO4
6.
(1)5.2〜7.6⑵蒸发浓缩、冷却结晶
⑶降低烘干温度,防止产品分解生成有毒的无水氯化钻。
⑷样品中含有NaCl杂质;
烘干时失去了部分结晶水⑸重结晶
⑹减少有毒气体的排放,防止大气污染;
防止产品中混有硝酸盐硝酸替代新工艺中的盐酸和过氧化氢,比新工艺流程少,节约成本
7.
(1)漏斗、蒸发皿⑵2A1+2OH-+2H2O=2A1O2-+3H2T>
AI2O3+2OH-=2A1O2-+3H2O
⑶H2SO4Ni2+、Fe2+⑷3.2—9.2(5)防止在浓缩结晶过程中水解
⑹H2O2的用量不足(或H2O2失效)、保温时间不足导致Fe2+未被完全氧化造成的
8.
(1)C12+2OH-=C1-+C1O-+H2O(2分)
(2)V(2分)(3)①26(1分)1.2(1分)
3ClO-+Fe3++3H2O=Fe(OH)31+3HClO(2分)2FeO42-4-Fe3++8OH~=3FeO43-+4H2O(2分)
(4)B(2分)9.
(1)CuO+2H==Cu2++H2O^Fc2O3+6H4==2Fc3++3H2OsCu+2Fe3+=2Fe2++Cu2+
(任写出其中两个即给分,每空3分,共6分)
(2)分液分液漏斗(各2分,共4分)(3)
FeSO4-7H2O(2分,只写FeSO4得1分)(4)C1P++2e-=Cu(2分)(5)H2SO4(2分)
10.(13分)
(1)3NaClOj4-3H2SO4=HClO4+2ClO2+3NaHSO4+H2O;
(2分)
降低NaHSO4的溶解度,使NaHSO4结晶析出(2分)高氯酸的沸点低(1分)
(2)2C1O2+SO2+4OIT=2C1O2~+SO广+2H2O;
(3)HiOi有还原性也能把CIO2还原为NaClOz(2分)
(4)强氧化性(2分)Cl2+2OH"
=CIO-+CF+H2O;
11.(16分)
(1)TiO2+2H+=TiO2++H2O(2分),使Fe"
还原为Fe?
+(1分)。
(2)蒸发浓缩,冷却结晶,过滤(洗涤)(2分);
(3)溶液中存在水解平衡TQ2++(n+1)H2O—TiOynH2O+2H+,加入的Na2CO3粉末及H+
反应,降低了溶液中c(H+),促进水解平衡向生成TiO2nH2O的方向移动;
(3分)Nj^SOa(1分)
(4)TiO2+2C+2Cb茎为TiCh+2CO(2分);
蒸馆(或分馅)(1分)
(5)TiO2+4e~=Ti+2O2-(2分);
O2,CO,CO2(2分)
12.(16分,每空2分)
(1)硫酸溶液
(2)2H++H2O2+2Fe2+=2Fe^+2H2O(3)B;
Fe(OH)3A1(OH)3
(4)Zn;
Cd和Zn(5)加热浓缩、蒸发结晶、过滤(洗涤);
保持溶液一定的酸度
13.(11分)
(1)增大硫酸浓度或加热升高温度或边加硫酸边搅拌或增加浸出时间(2分)(要求写出一条即可)。
防止硫酸锌中从溶液中析出。
(1分)
(2)5Fe2++MnO4+8H+=5Fe5++Mn2++4H2O(2分,不配平扣1分)
因为Fe3++3H2O=sFe(OHh+3H+,ZnO+2H+=Zn2++H2O,加入ZnO能促进Fe"
水解生成Fe(OH)3而除去。
(3)Zn、Cd、Cu(2分,漏写扣1分)(4)蒸发浓缩(2分)
14.(16分)
(1)D(2分)
(2)空气(2分)
原料来源容易,成本低,不产生污染,不引入杂质。
(2分,答其中两点即可)
(3)溶液温度控制在80・C(1分),pH控制在1.5(1分),氧化时间为4小时左右(2分)
(4)3Fe2(SO4)3+12NHyH2O=(NH4)2Fe6(SO4)4(OH)12l+5(NH4)2SO4(3分)
(5)取少量滤液于试管中,向试管中加入足量的浓氢氧化钠溶液,加热。
用湿润的红色石蕊试纸放在试管口处,红色石蕊试纸变蓝色,说明滤液中含有NHf。
(3分)
15.
(1)Mn2\F0、Al3+(2分)
(2)<
1509(各2分)
(3)加入MnO2是为了除去过量的SO2;
通入空气将Fe2+氧化成Fe"
便于后来加碳酸钠除去(4分)
(4)防止NHUHC03受热分解(3分)
(5)综合利用了尾气SO?
有利于环境保护,同时节约能源。
16.
(1)增大固体及空气的接触面积,增大反应速率;
提高原料的利用率
(2)K++BF4=KBF4I
(3)2Ce4+2C1=2Ce3++Ch:
用H2SO4酸浸
(4)漏斗烧杯玻璃棒;
撕下一小片pH试纸放在干燥洁净的表面皿上,用玻璃棒談取该溶液点在pH试纸的中央,然后及标准比色卡对比。
(5)2Ce(OH)j+NaCIO+HzO=2Ce(OH)4+NaClNaCl
17.(16分)
(1)250mL容量瓶(1分)、胶头滴管(1分)
(2)①升高反应温度,②搅拌,③过滤后再向滤浹中加入硫酸(多次浸取),④适当延长浸取时间(只
要答出任意一点即可,可从反应温度、溶液的pH、搅拌速度、溶剂的配比等角度)(2分)
(3)氧化+3价Cr使之转变成+6价Cr(或Cr2O72),以便于及杂质离子分离(2分);
FB和AP*(2分,各1分)
(4)Ca2\Mg2+(2分,各1分)(5)1,3,UH2O,2,1(2分),
Fe-2e~=Fe2+(2分),2H++2e-=H2f(2分)
18.(16分)
(1)增大固体反应物的表面积,增大化学反应的速率。
(2)2Al+2OH~+2H2O=2AIO2~+3H2T:
Si+2NaOH+H2O=Na2SiO3+2H2f;
AI2O3+2OH-=2AIO2_+HzO;
SiO2+2NaOH=Na2SiO3+H2O。
(每写出其中1个给2分,共4分,没气体符号扣1分,未配平0分)
2Fe2++H2O2+2H+=2Fe3++2H2O(2分)
(3)C、D(2分)Fe(OH)j(1分)
(4)加热蒸发浓缩时会导致Ch发生水解生成Cu(OH)2,用硫酸调节pH=2〜3是为了抑制Ch的水解,
也不会引入杂质。
(2分)蒸发浓缩,冷却结晶,过滤。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 化学工业 流程 题典题 汇总
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
