 河南省罗山高中高二化学下学期暑假自主学习考点自检测Word文件下载.docx
河南省罗山高中高二化学下学期暑假自主学习考点自检测Word文件下载.docx
- 文档编号:19415558
- 上传时间:2023-01-06
- 格式:DOCX
- 页数:17
- 大小:96.80KB
河南省罗山高中高二化学下学期暑假自主学习考点自检测Word文件下载.docx
《河南省罗山高中高二化学下学期暑假自主学习考点自检测Word文件下载.docx》由会员分享,可在线阅读,更多相关《河南省罗山高中高二化学下学期暑假自主学习考点自检测Word文件下载.docx(17页珍藏版)》请在冰豆网上搜索。
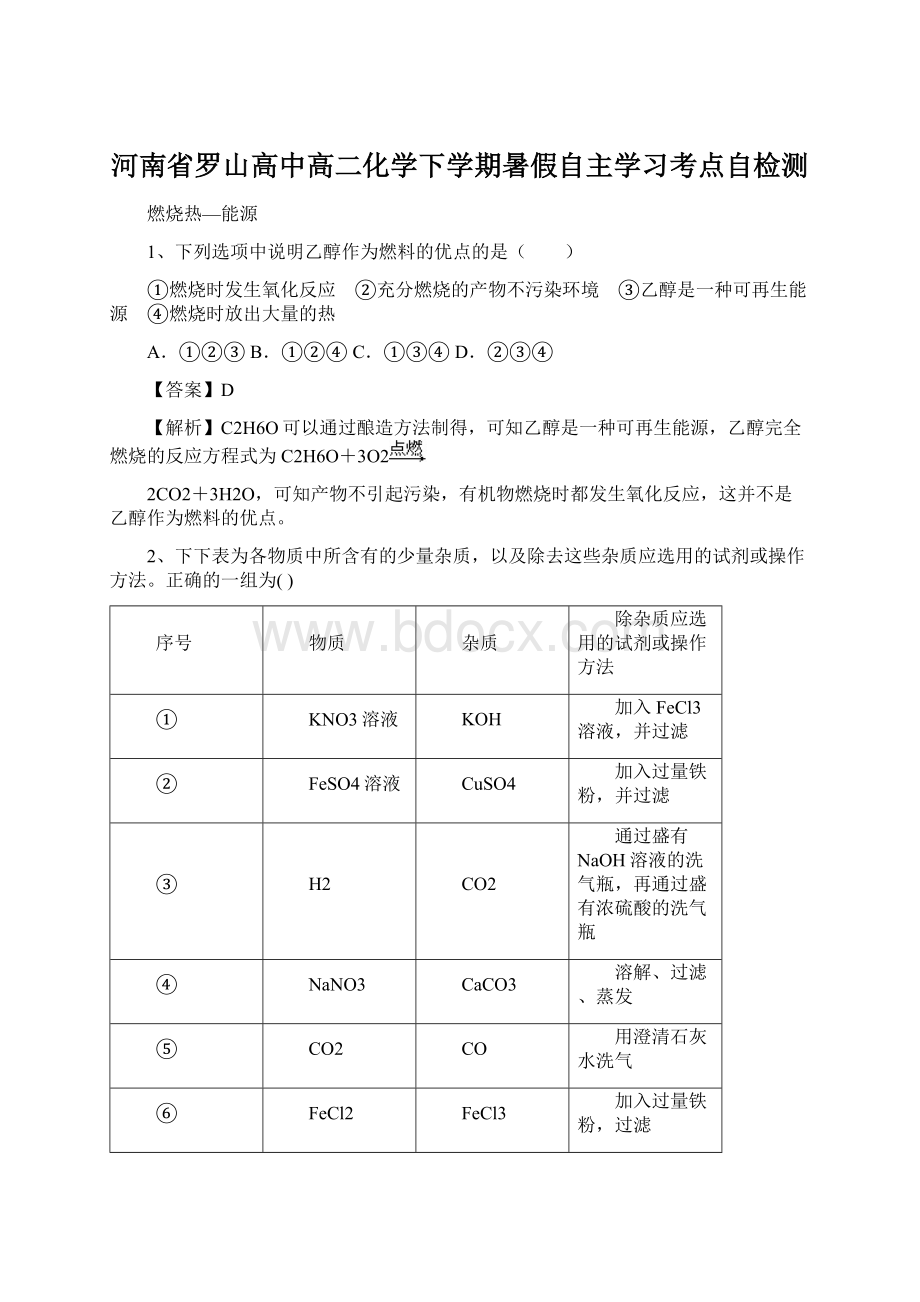
FeCl3
加入过量铁粉,过滤
⑦
Cu
CuO
加适量稀硝酸后,过滤、洗涤
⑧
BaCO3
BaSO4
加过量盐酸后,过滤、洗涤
A.①②③④⑤B.③④⑤C.②③④⑥D.①②③⑤⑧
【答案】C
【解析】
3、某溶液中仅含Na+、H+、OH-、CH3COO-四种离子,下列说法错误的是()
A.溶液中四种粒子之间可能满足:
c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
B.若溶液中部分粒子间满足:
c(CH3COO-)=c(Na+)则该溶液一定呈中性
C.若溶液中溶质仅为CH3COONa,则粒子间一定满足:
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.若溶液中的溶质为CH3COONa和CH3COOH,则溶液中粒子间一定满足:
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
【答案】D
【解析】
4、某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42-的物质的量浓度为6mol/L,则此溶液最多可溶解铁粉的质量为()
A.5.6gB.11.2gC.22.4gD.33.6g
【答案】C
5、[2014·
鹰潭市高一期末]在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是( )
A.H+、Mg2+、Al3+B.Mg2+、Al3+、Fe2+
C.H+、Ba2+、Al3+D.只有Mg2+、Al3+
【答案】A
【解析】首先由溶液为无色可排除B项;
一开始加入NaOH无沉淀生成,证明溶液中有H+存在,排除D项;
C项加过量NaOH后无沉淀生成;
故答案为A。
6、在0.1mol/L的NaHSO3溶液中有如下关系:
c(Na+)>
c(HSO3-)>
c(SO32-)>
c(H2SO3),向NaHSO3溶液中慢慢地加入少量的NaOH溶液,发生的主要反应的离子方程式为
A.SO32-+H2O
HSO3-十OH—B.HSO3-十H2O
H2SO3十OH-
C.HSO3-十OH—
SO32—十H2OD.H2SO3+OH-
HSO3-十H2O
7、常温下,下列溶液中可能大量共存的离子组是( )
A.加入金属镁能产生H2的溶液中:
Na+、Fe3+、SO
、NO
B.含有大量Fe2+的溶液中:
K+、Mg2+、ClO-、SO
C.能使Al3+生成沉淀的溶液中:
NH
、Na+、SiO
、HCO
D.水电离产生的c(OH-)=1×
10-10mol/L的溶液中:
Al3+、SO
、Cl-
8、下列关于热化学反应的描述中正确的是( )
A.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+2×
283.0kJ/mol
B.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×
(-57.3)kJ/mol
C.用等体积的0.50mol·
L-1盐酸、0.55mol·
L-1NaOH溶液进行中和热测定的实验,会使测得的值偏大
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
【解析】试题分析:
燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,据此可知选项A是正确的;
中和热是在一定条件下,稀溶液中,强酸和强碱反应生成1mol水时所放出的热量,所以选项B是错误的,H2SO4和Ca(OH)2反应的中和热ΔH=-57.3kJ/mol;
同样根据中和热的概念可知,选项C也是错误,中和热不变,与盐酸和氢氧化钠的用量没有关系。
D不正确,生成物应该是液态水,答案选A。
考点:
考查燃烧热、中和热以及热化学方程式的判断
点评:
该题是高考中的常见题型和考点,属于基础性试题的考查。
旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和应试能力。
该题的关键是明确燃烧热和中和热的含义,然后结合题意灵活运用即可。
9、已知:
CH4(g)+2O2(g)===CO2(g)+2H2O(l)ΔH=-Q1kJ·
mol-1
2H2(g)+O2(g)===2H2O(g) ΔH=-Q2kJ·
2H2(g)+O2(g)===2H2O(l) ΔH=-Q3kJ·
常温下,取体积比为4∶1的甲烷和氢气的混合气体11.2L(标准状况),经完全燃烧后恢复到常温,放出的热量为( )
A.0.4Q1+0.05Q3B.0.4Q1+0.05Q2C.0.4Q1+0.1Q3D.0.4Q1+0.2Q3
【解析】标准状况下的混合气体11.2L,其物质的量是0.5mol。
其中甲烷0.4mol,氢气0.1mol。
又知在常温下,水是液态。
所以0.4mol甲烷完全燃烧放出热量:
0.4mol×
Q1kJ·
mol-1=0.4Q1kJ;
0.1mol氢气完全燃烧放出热量:
0.1mol×
1/2Q3kJ·
mol-1=0.05Q3kJ,所以标准状况下11.2L混合气体燃烧共放出热量:
(0.4Q1+0.05Q3)kJ。
10、已知两个方程式:
2CO(g)+O2(g)===2CO2(g) ΔH=-566kJ/mol
Na2O2(s)+CO2(g)===Na2CO3(s)+
O2(g) ΔH=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的燃烧热为283kJ
B.下图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g)ΔH>
-452kJ/mol
D.CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数为6.02×
1023
【解析】A选项中燃烧热单位错误,应为kJ/mol;
B项中图中没有表示出ΔH=-566kJ/mol时对应的反应物与生成物的量的关系,B项错误;
由于2Na2O2(s)+2CO2(g)===2Na2CO3(s)+O2(g) ΔH=-452kJ/mol,所以2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g) ΔH>
-452kJ/mol,C正确;
由盖斯定律得:
CO(g)+Na2O2(s)===Na2CO3(s) ΔH=-509kJ/mol,可知当放出509kJ热量时,消耗1molCO,电子转移数为2×
6.02×
1023,D错误。
11、下列说法不正确的是( )
A.已知冰的熔化热为6.0kJ/mol,冰中氢键键能为20kJ/mol。
假设每摩尔冰中有2mol氢键,且熔化热完全用于打破冰的氢键,则最多只能破坏冰中15%的氢键
B.已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,
Ka=(cα)2/[c(1—α)]。
若加入少量CH3COONa固体,则电离平衡CH3COOH
CH3COO——+H+向左移动,α减小,Ka减小
C.实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为—3916kJ/mol、—3747kJ/mol和—3265kJ/mol,可以证明在苯分子中不存在独立的碳碳双键
D.已知:
Fe2O(s)+3C(石墨)==2Fe(s)+3CO(g)△H=489.0kJ/mol
CO(g)+1/2O2(g)==CO2(g)△H=—283.0kJ/mol
C(石墨)+O2(g)==CO2(g)△H=—393.05kJ/mol
则4Fe(s)+3O2(g)==2Fe2O3(s)△H=—1641.0kJ/mol
【答案】B
【解析】A选项:
每摩冰中氢键的键能为2mol×
20kJ/mol==40kJ,每摩最多只能破坏冰中6.0kJ/40kJ==0.15的氢键。
B选项:
醋酸的电离平衡:
CH3COOH
CH3COO—+H+
平衡时浓度(mol/L)c(1—α)cαcα
Ka=(cα)2/[c(1—α)]
Ka只受温度的影响,与平衡时的浓度无关,若加入少量CH3COONa固体,醋酸的电离平衡向左移动,α减小,但Ka不受其影响。
C选项:
环己烷(l)比环己烯(l)和苯(l)的标准燃烧热多放出169kJ/mol热,环己烷(l)比苯(l)的标准燃烧热多放出651kJ/mol热,小于3×
169kJ/mol=507kJ/mol,说明苯分子更稳定,苯分子中不存在单独碳碳单键和碳碳双键。
D选项:
根据题给的化学方程式:
4Fe(s)+3O2(g)==2Fe2O3(s),要求将其3个热化学方程式作适当的整合:
2Fe(s)+3CO(g)==Fe2O(s)+3C(石墨)△H=—489.0kJ/mol×
2
CO2(g)==CO(g)+1/2O2(g)△H=283.0kJ/mol×
6
+)C(石墨)+O2(g)==CO2(g)△H=—393.05kJ/mol×
4Fe(s)+3O2(g)==2Fe2O3(s)△H=—3282.0kJ/mol
【点评】A、B、C、D4个选项都涉及了简单的计算,但只要有“Ka只受温度的影响,不受浓度影响”知识,就能做好本题。
12、关于反应:
①2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣2600kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=﹣566kJ/mol
③CO2(g)+3H2(g)
CH3OH(g)+H2O(g)△H=﹣49.0kJ·
mol﹣1
下列叙述正确的是( )
A.CO的燃烧热为﹣566kJ/mol
B.在③反应时,若加入催化剂,可以使△H减小
C.若投入1molCO2和3molH2在一定条件下充分反应,则放出热量49kJ
D.若生成相同质量的CO2,则放出的热量C2H2大于CO
【解析】解:
A.燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,由2CO(g)+O2(g)═2CO2(g)△H=﹣566kJ/mol知,CO的燃烧热为283kJ/mol,故A错误;
B.焓变=反应物断裂化学键吸收的能量﹣生成物形成化学键放出的能量,在反应体系中加入催化剂,催化剂改变反应速率,不改变化学平衡,反应热不变,故B错误;
C.投入1molCO2和3molH2在一定条件下充分反应,则放出小于热量49kJ,故C错误;
D.假设都生成2molCO2,C2H2燃烧放出1300KJ热量,CO燃烧放出566kJ,前者大于后者,故D正确;
故选D.
13、下列推论正确的是( )
A.S(g)+O2(g)═SO2(g)△H1;
S(s)+O2═SO2(g)△H2,则△H1>△H2
B.C(石墨,s)═C(金刚石,s)△H=+1.9kJ·
mol﹣1,则金刚石比石墨稳定
C.OH﹣(aq)+H+(aq)=H2O(l)△H=﹣57.4kJ·
mol﹣1,则:
含20gNaOH的稀溶液与过量稀醋酸完全反应,放出的热量为28.7kJ
D.2C(s)+O2(g)═2CO(g)△H=﹣221kJ·
mol﹣1,则碳的燃烧热大于110.5kJ·
A.固体硫燃烧时要先变为气态硫,过程吸热,气体与气体反应生成气体比固体和气体反应生成气体产生热量多,但反应热为负值,所以△H1<△H2;
故A错误;
B.C(石墨,S)=C(金刚石,S)△H=+l.9kJ/mol,则由石墨制取金刚石的反应是吸热反应,金刚石的能量比石墨高,则石墨比金刚石稳定,故B错误;
mol﹣1,但由于稀醋酸电离要吸热,所以含20gNaOH的稀溶液与过量稀醋酸完全反应,放出的热量小于28.7kJ,故C错误;
D.2C(s)+O2(g)=2CO(g)△H=﹣221kJ/mol,该反应方程式中C的物质的量为2mol,生成的氧化物为CO不是稳定氧化物,还会继续燃烧放热,所以碳的燃烧热大于110.5kJ·
mol﹣1,故D正确.
14、肼(N2H4)是火箭发动机的燃料,它与N2O4反应时,N2O4为氧化剂,生成氮气和水蒸气.已知:
N2(g)+2O2(g)===N2O4(g) ΔH=+8.7kJ/mol,N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=-534.0kJ/mol,下列表示肼跟N2O4反应的热化学方程式,正确的是( )
A.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g);
ΔH=-542.7kJ/mol
B.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g);
ΔH=-1059.3kJ/mol
C.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g);
ΔH=-1076.7kJ/mol
D.N2H4(g)+
N2O4(g)===
N2(g)+2H2O(g);
【解析】N2(g)+2O2(g)===N2O4(g) ΔH=+8.7kJ/mol①,N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=-534.0kJ/mol②,将热化学方程式②×
2-①就可以得到肼与N2O4反应的热化学方程式,则ΔH=-534.0kJ/mol×
2-8.7kJ/mol=-1076.7kJ/mol,选项C正确.
15、下列关于化学反应的描述中正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.反应4Fe(OH)2(s)+02(g)+2H20(l)=4Fe(OH)3(S)的△H>
O
C.已知①
则a<b
D.CO(g)的标准燃烧是283.0kJ·
mol-1,则2CO2(g)=2CO(g)+O2(g)△H=+566.0kJ·
mol-1
【解析】反应是放热反应还是吸热反应,与反应条件无关,A不正确;
B不正确,该反应是放热反应,△H小于0;
由于液态水的能量高于气态水的能量,所以氢气燃烧生成液态水放出的热量多,但放热越多,△H越小,即选项C中a大于b,所以正确的答案选D。
16、根据从草木灰中提取钾盐的实验,填写下列空白:
(1)此实验操作顺序如下:
①称量样品,②溶解、沉降,③________,④________,⑤冷却、结晶。
(2)用托盘天平(指针向上的)称量样品时,若指针偏向右边,则表示________(填下列正确选项的代码)。
A.左盘重,样品轻 B.左盘轻,砝码重
C.右盘重,砝码轻D.右盘轻,样品重
(3)在进行第③步操作时,有可能要重复进行,这是由于____________________。
(4)在进行第④步操作时,要用玻璃棒不断小心地搅动液体,目的是防止________________。
(5)所得产物中主要的钾盐有________等。
【答案】
(1)③过滤 ④蒸发浓缩
(2)B (3)滤液浑浊 (4)液体飞溅 (5)K2CO3、K2SO4、KCl
(1)由于草木灰中含有不溶性的灰尘和可溶性的碳酸钾等物质,所以应首先进行溶解,之后过滤可得到主要含碳酸钾的滤液,而碳酸钾的溶解度受温度的影响变化较大,则可采用冷却热的饱和溶液的方法得到晶体。
(2)考查托盘天平的使用,只要记住左物右码的规则即可选出正确答案。
(3)对于玻璃棒的作用在溶解、过滤、蒸发的操作中使用比较普遍,此处的作用是防止液体局部过热引起液体飞溅出来。
17、实验室用碳酸钠晶体配制1.00mol·
L-1的Na2CO3溶液100mL,完成下列问题:
(1)所需主要仪器有:
药匙、________、________、________、________、________和________。
(2)本实验需称量碳酸钠晶体(Na2CO3·
10H2O)________g。
(3)容量瓶上标有________、________、________。
(4)某同学将称量好的碳酸钠晶体用适量的蒸馏水在烧杯中溶解,冷却后直接倒进所选的且经检查不漏水的容量瓶中,洗涤烧杯2~3次,洗涤液也移至容量瓶中,然后加水至离刻度线2cm处,用滴管加水至刻度线。
请指出上述操作中的3处错误:
①_______________________________________________________________________;
②_______________________________________________________________________;
③_____________________________________________________________________。
(1)托盘天平 烧杯 量筒 玻璃棒 100mL容量瓶 胶头滴管
(2)28.6 (3)容量 温度 刻度线
(4)①不应直接倒入容量瓶中,而应用玻璃棒引流
②洗涤液注入容量瓶之后、向容量瓶中加蒸馏水之前,应将溶液振荡摇匀
③定容后应将容量瓶倒转摇匀
(1)用固体物质配制100mL一定物质的量浓度的溶液所用仪器除药匙外,还需要天平、烧杯、量筒、玻璃棒、胶头滴管和100mL容量瓶。
(2)m=n·
M=c·
V·
M=1.00mol·
L-1×
0.100L×
286g·
=28.6g
18、现有25mL盐酸和硫酸混合溶液,加入1mol·
L-1的NaOH溶液25mL恰好中和,在中和后的溶液中加过量的Ba(OH)2溶液,所得沉淀质量为1.7475g。
求混合溶液中盐酸和硫酸的物质的量浓度各是多少?
【答案】解:
设原混合溶液中含硫酸的物质的量为x,由反应:
H2SO4+2NaOH===Na2SO4+2H2O,
Na2SO4+Ba(OH)2===BaSO4↓+2NaOH
则有关系式:
H2SO4~BaSO4
1mol1mol
x1.7475g/233g·
x=[1.7475g/233g·
mol-1]×
1mol/1mol
=0.0075mol
所以混合液中c(H2SO4)=0.0075mol/0.025L=0.3mol·
L-1。
根据NaOH溶液与混合酸中和,可知混合酸中含H+的总量与NaOH溶液中NaOH的物质的量相等,即1mol·
0.025L=0.025mol。
混合溶液中由硫酸提供的H+物质的量为:
x=2×
0.0075mol=0.015mol。
则余下部分为盐酸提供的H+物质的量为0.025mol-0.015mol=0.01mol。
所以c(HCl)=0.01mol/0.025L=0.4mol·
L-1
即:
c(H2SO4)=0.3mol·
L-1,c(HCl)=0.4mol·
L-1。
【解析】根据题中所给出的信息,结合已经学习过的知识分析,由m(BaSO4)→n(BaSO4)→n(H2SO4)
求出n(HCl)→c(H2SO4)和c(HCl)
19、A、B、C是单质,其中A是金属,各种物质间的转化关系如图:
根据图示转化关系回答:
(1)写出下列物质的化学式.
A________________,B________________,
乙________________,丁________________.
(2)写出下列变化的化学方程式.
①A与NaOH溶液反应的化学方程式________________________________________________________________________________________________________________.
②甲与NaOH溶液反应的离子方程式_____________________________________________________________________________________________________________.
(3)将一定量的A加入到NaOH溶液中,产生的C在标准状况下的体积为3.36L,则消耗的A的物质的量为______________,转移电子的物质的量为__________.
(1)Al O2 NaAlO2 Al(OH)3
(2)①2Al+2NaOH+2H2O===2NaAlO2+3H2↑②Al2O3+2OH-==2AlO2—+H2O(3)0.1mol 0.3mol
【解析】常见金属单质中能与NaOH溶液反应产生气体的只有Al,所以A是Al,乙是NaAlO2,C是H2,甲是Al的化合物,可和NaOH溶液反应产生NaAlO2,可能是Al2O3,则丙是H2O,B即是O2.根据NaAlO2+CO2+2H2O===NaHCO3+Al(OH)3↓得丁是Al(OH)3.
20、A—J是中学化学常见的物质,它们之间的转化关系如下图所示(部分产物已略去)。
已知A是一种高熔点物质,D是一种红棕色固体。
请回答下列问题:
(1)固体A的晶体类型为___________,K的化学式为。
(2)C与D在高温下的反应在冶金工业上称为反应,引发该反应的实验操作是___________。
(3)G→J的化学方程式为____________。
(4)A→H的离子方程式为。
(5)I的水溶液pH_____7(填“>
”、“<
”或“=”),原因是____(用离子方程式表示)。
(1)离子晶体Al(OH)3
(2)铝热反应,在混合粉末上插上镁条,周围撒上少量KClO3,然后点燃镁条(3)4Fe(OH)2+O2+2H2O=4Fe(OH)3(4)Al2O3+2OH—=2AlO2—+H2O
(5)<(1分)Al3++3H2O
Al(OH)3+3H+
【解析】本题属于无机框图题,关键是找准突破点。
D是一种红棕色固体,所以D是氧化铁,则J是氢氧化铁。
又因为A是一种高熔点物质,所以A是氧化铝,B是氧气,C是Al,E是铁,F是氯化亚铁,G是氢氧化亚铁,H是偏铝酸钠,I是氯化铝,K是氢氧化铝。
氯化铝由于是强酸弱碱盐,水解显酸性,方程式为Al3++3H2O
Al(OH)3+3H+。
21、A、B、C、D、E五种短周期元素(A、B、C、D、E分别代表元素符号),它
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 河南省 罗山 高中 化学 下学 暑假 自主 学习 考点 检测
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
