 学年高二化学下学期期末学霸挑战卷人教版选修301解析版Word下载.docx
学年高二化学下学期期末学霸挑战卷人教版选修301解析版Word下载.docx
- 文档编号:19209852
- 上传时间:2023-01-04
- 格式:DOCX
- 页数:20
- 大小:342.79KB
学年高二化学下学期期末学霸挑战卷人教版选修301解析版Word下载.docx
《学年高二化学下学期期末学霸挑战卷人教版选修301解析版Word下载.docx》由会员分享,可在线阅读,更多相关《学年高二化学下学期期末学霸挑战卷人教版选修301解析版Word下载.docx(20页珍藏版)》请在冰豆网上搜索。
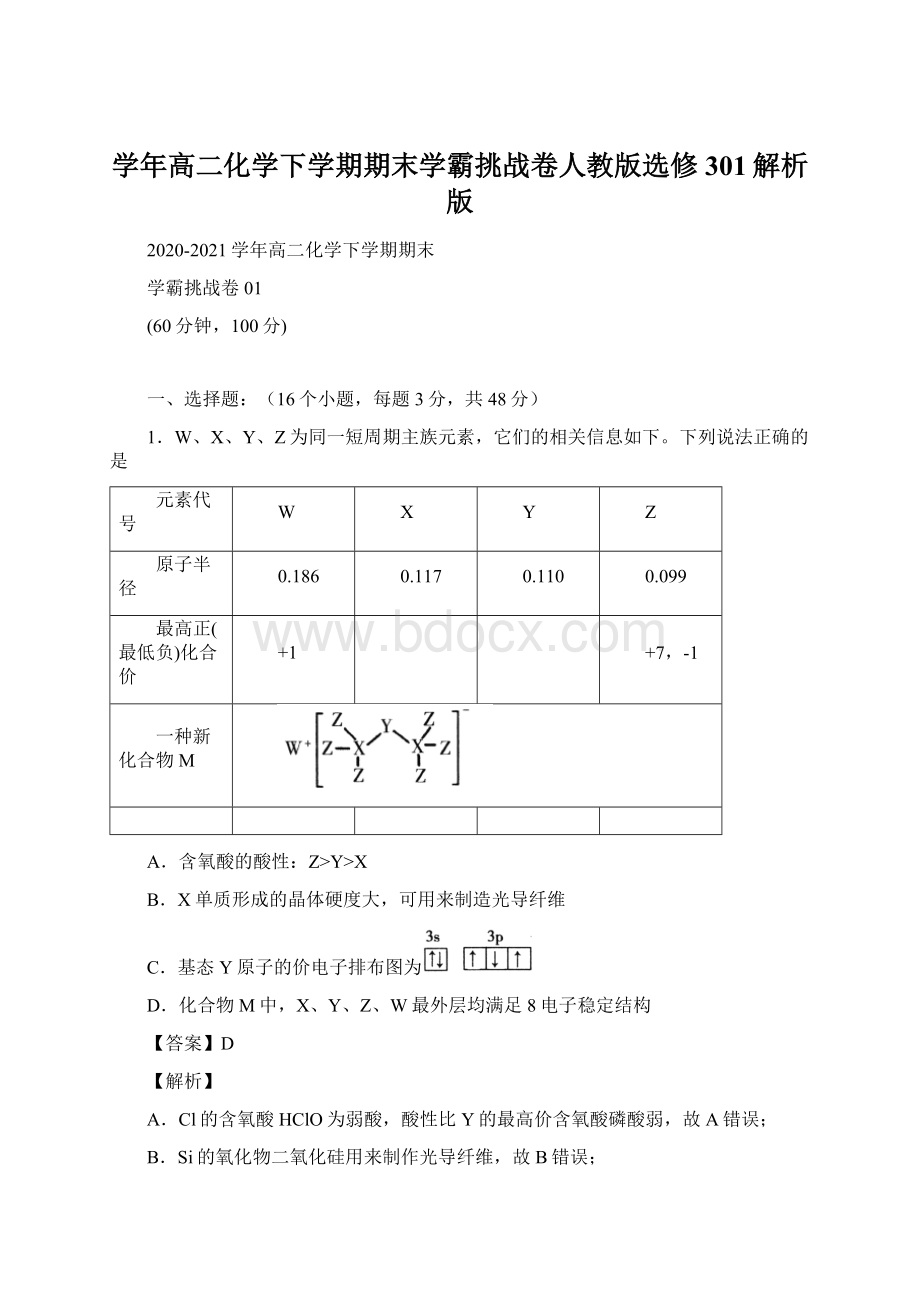
D.由结构图可知M中,X、Y、Z、W所有原子均达到最大成键数量,都满足8电子稳定结构,故D正确;
故选:
D。
2.X、Y、Z、R、W为原子序数依次增大前20号主族元素,X元素原子失去一个电子后是“裸露”质子;
R原子最外层电子数是其内层电子总数的一半;
X、Y、Z、R形成化合物表示为[YX4]+[X2RZ4]-;
W是前20号元素中金属性最强的。
下列正确的是
A.离子半径:
W+<
Z2-
B.键能:
Y—X>
R—X
C.第一电离能:
D.
该物质中,冠醚和W+之间配位键是离子键
【答案】B
【分析】
X元素原子失去一个电子后是“裸露”质子,X是H,R原子最外层电子数是其内层电子总数的一半;
则R为第三周期元素,是15号元素,R为P,由[YX4]+[X2RZ4]-可知Y是N、Z是O;
W是前20号元素中金属性最强的,W为K。
分析知,X、Y、Z、R、W分别为H、N、O、P、K;
A.K+有三层电子层,O2-有两层电子层,则离子半径:
W+>
Z2-,A错误;
B.非金属性越强,气态氢化物越稳定,则NH3比PH3稳定,则NH3的能量越低,N-H的键能比P-H的大,B正确;
C.同一周期从左到右,第一电离能逐渐增大,N原子的2p3是半充满结构,第一电离能变大,C、N、H的第一电离能大小顺序为N>O>H,即Y>
X,C错误;
D.冠醚和K+之间配位键是共价键,D错误;
B。
3.X、Y、Z、W、R属于周期表中前20号主族元素,且原子序数依次增大。
X的简单氢化物水溶液显碱性,Z是元素周期表中电负性最大的元素,Z和W同主族,R的基态原子只有一个未成对电子。
A.简单离子半径:
r(R)>
r(W)>
r(Z)B.第一电离能:
I1(X)>
I1(Y)>
I1(Z)
C.Z的最高价氧化物的水化物是强酸D.X的简单氢化物分子属于极性分子
X、Y、Z、W、R为周期表前20号元素,原子序数依次增大,X的简单氢化物的水溶液为碱性,为NH3,X为N元素,Z是元素周期表中电负性最大的元素,Z为F元素,Z和W同主族,W为Cl元素,Y为O元素,R的基态原子只有一个未成对电子,R为K元素。
A.简单离子半径,K+与Cl-核外电子层相同,原子序数越大,离子半径越小,F-核外电子层结构较K+与Cl-少,离子半径小,故r(W)>
r(Z),A错误;
B.同周期元素,第一电离能从左往右依次增大,第ⅤA族大于第ⅣA族,故F>
N>
O,即I1(Z)>
I1(Y),B错误;
C.Z为F元素,F元素没有正价,故无最高价氧化物对应的水化物,C错误;
D.X为N元素,简单氢化物分子为NH3,NH3为三角锥形分子,为不对称结构,故属于极性分子,D正确。
答案选D。
4.短周期元素W、X、Y、Z的原子序数依次增加。
m、n、p是前三种元素组成的二元化合物,0.01mol·
L-1q溶液的pH为1.86,上述物质的转化关系如图所示。
下列说法不正确的是
Y>ZB.最简单氢化物稳定性:
X>Y
C.键角:
p>nD.沸点:
m>r
【答案】C
0.01mol·
L-1q溶液的pH为1.86,则q为多元强酸,m、n化合可以得到q,说明q也是由W、X、Y元素组成,则应为H2SO4,所以W为H、X为O、Y为S,Z为原子序数大于S的短周期元素,则为Cl,n与p和Cl2反应可得H2SO4,n与m也可以反应生成H2SO4,则n应为SO2、p为H2O、m为H2O2,r为HCl。
A.电子层数相同核电荷越小半径越大,所以离子半径:
S2->Cl-,A正确;
B.非金属性O>S,则最简单氢化物稳定性O>S,B正确;
C.H2O的VSEPR模型为正四面体,且有两对孤电子对,所以键角小于109°
28′,SO2的VSEPR模型为平面三角形,含一对孤电子对,键角略小于120°
,所以键角H2O<SO2,C错误;
D.H2O2分子间存在氢键,沸点较高,常温下为液态,HCl常温为气态,所以沸点H2O2>HCl,D正确;
综上所述答案为C。
5.F-与Al3+可以形成非常稳定的
(结构见图),试剂乙二胺四乙酸(简称EDTA)能与Al3+和Zn2+发生配位反应。
现欲用EDTA试剂来滴定某溶液中Zn2+(只含Al3+杂质),可加入NH4F溶液,在pH=5.5左右以二甲酚橙作指示剂可以滴定测量Zn2+的浓度。
A.
离子构型为正八面体
B.Al(OH)3不能溶于浓的氢氟酸溶液
C.F-与Al3+发生反应方程式:
,该反应平衡常数非常大
D.NH4F的作用是作为遮掩剂,利用F-和Al3+形成
,以防止Al3+和EDTA试剂发生配位反应
A.F-与Al3+可以形成非常稳定的
,其中4个F-与Al3+在同一平面上,另外2个F-在平面两侧等距离的位置,6个F-构成正八面体结构,A正确;
B.Al(OH)3难溶于水,在溶液中存在电离平衡:
Al(OH)3
Al3++3OH-,电离产生的Al3+与HF电离产生的F-结合形成
离子,促进氢氧化铝电离、故氢氧化铝可溶于氢氟酸,B错误;
C.由于F-与Al3+反应形成的
非常稳定,因此F-与Al3+发生反应方程式:
正向进行的程度很大,因此该反应平衡常数非常大,C正确;
D.EDTA能与Al3+和Zn2+都发生配位反应,向溶液中加入NH4F溶液,NH4F的作用是作为遮掩剂,利用F-和Al3+形成
,就可以防止Al3+和EDTA试剂发生配位反应,以便滴定测量Zn2+的浓度,D正确;
故合理选项是B。
6.NA为阿伏加德罗常数的值。
A.1molH2S分子中,S原子的价层电子对数目为4NA,VSEPR模型为四面体形
B.34g
中含有的极性键数目为2NA
C.1L0.01mol·
L-1
溶液中,
和
的离子数目之和为0.01NA
D.电极反应LiFePO4-xe-=xLi++Li1-xFePO4,每转移1mol电子释放2NA个Li+
【答案】A
A.价层电子对数等于σ键+孤电子对数=2+(6−2×
1)/2=4,所以1molH2S分子中,S原子的价层电子对数目为4NA,H2S分子的VSEPR模型为正四面体形,故A正确;
B.1个
中含有4个C-H,2个C-O,共6个极性共价键,因此含有极性键数目为34g÷
68g/mol×
6×
NAmol-1=3NA,故B错误;
C.依据物料守恒可知:
1L0.01mol•L-1
的总物质的量为0.01mol,所以
的离子数目之和小于0.01NA,故C错误;
D.据电极反应式可知,转移xe-释放x个Li+,则每转移1mol电子释放NA个Li+,故D错误;
A。
7.在照片底片冲洗的过程中会发生如下反应:
AgBr+2S2O
[Ag(S2O3)2]3-+Br-,有关说法正确的是
A.S2O
酸性条件下不能稳定存在,会与酸反应生成S和SO
B.向平衡体系中加AgBr,平衡将向正反应方向移动
C.已知S2O
做配体时是硫原子提供孤电子对,则配合物[Ag(S2O3)2]3-中银离子的配位数是2
D.加水稀释时平衡向正反应方向移动,平衡常数会变大
酸性条件下不能稳定存在,会与酸反应生成S、SO2和水:
S2O
+2H+=S↓+SO2↑+H2O,故A错误;
B.增加固体的量,对平衡无影响,故B错误;
做配体时是硫原子提供孤电子对,在S2O
中,只有1个S有孤电子对,则配合物[Ag(S2O3)2]3-中银离子的配位数是2,故C正确;
D.平衡常数只和温度有关,加水稀释时平衡常数不变,故D错误;
故选C。
8.下列说法错误的是
A.水分子间存在氢键,故H2O比H2S的稳定性强
B.原子最外层电子为ns1的元素可以形成离子化合物,也可形成共价化合物
C.N、O、S的第一电离能逐渐减小,其氢化物分子中键角逐渐减小
D.铟(49In)是第五周期第ⅢA族元素,位于元素周期表p区
A.氢键是分子间的作用力,决定物质的物理性质,不会影响分子稳定性,分子稳定性是其被破坏的难易程度,和化学键有关,A项错误;
B.最外层电子为ns1的元素有:
H、Li、Na、K、Rb、Cs等,可以形成离子化合物(如NaCl)也可形成共价化合物(如HCl),B项正确;
C.根据同周期同主族元素性质递变规律判断,同一周期由左向右元素原子的第一电离能呈递增趋势,但氮原子2p轨道为半充满状态,第一电离能比相邻的元素都大,同主族由上到下元素原子的第一电离能逐渐减小,则N、O、S三种元素的第一电离能从大到小的顺序为N>O>S;
N、O、S的氢化物分子都是有孤对电子的角锥形分子。
水和硫化氢有两对孤对电子,但是氧原子的电负性比硫原子大,氧原子对其携带的两对孤对电子的吸引比硫原子大,相应的孤对电子斥力增大使键角也相应比硫化氢大,氨分子只有一对孤对电子,排斥力比有两对孤对电子的情况小,所以键角比水和硫化氢都大,即键角大小氨>
水>
硫化氢,C项正确;
D.铟(49In)是一种金属元素,元素符号为In,原子序数为49,位于元素周期表第五周期ⅢA族,p区包括第三主族到第七主族加上零族的元素,因此它位于p区,D项正确;
答案选A。
9.我国科学家合成的某种离子化合物结构如下图,该物质由两种阳离子和两种阴离子构成,其中有两种10电子离子和一种18电子离子。
X、Y、Z、M均为短周期元素,且均不在同一族;
X是半径最小的元素,Z是空气中含量最多的元素,Y的电负性大于Z。
A.X与Y形成的化合物沸点高于Y同族元素与X形成化合物的沸点主要原因是容易形成分子间氢键
B.Z的最高价氧化物对应水化物的阴离子中Z的杂化方式为sp2杂化
C.元素第一电离能:
Y<
D.该盐中,存在离子键、极性共价键、非极性共价键、配位键和氢键等化学键
X、Y、Z、M均为短周期元素,且均不在同一族,X是半径最小的元素,则X为H元素,Z是空气中含量最多的元素,则Z为N元素;
离子化合物由两种阳离子和两种阴离子构成,其中有两种10电子离子和一种18电子离子,由化合物的结构和Y的电负性大于Z可知,Y为O元素、M为Cl元素,化合物中的阳离子为H3O+和NH
、阴离子为Cl—和N
。
A.水分子间能形成氢键,而与氧元素同主族的元素的氢化物分子间不能形成氢键,则水分子间的作用力强于同主族的元素的氢化物,沸点高于同主族的元素的氢化物,故A正确;
B.硝酸根离子中氮原子的价层电子对数为3,则氮原子的杂化方式为sp2杂化,故B正确;
C.同周期元素,从左到右元素第一电离能有增大的趋势,氮原子的2p轨道为稳定的半充满结构,元素第一电离能大于相邻元素,则氧元素的元素第一电离能小于氮元素,故C正确;
D.氢键是一种作用力较强的分子间作用力,比化学键弱很多,不是化学键,故D错误;
故选D。
10.磷及其化合物在电池、催化等领域有重要应用。
黑磷与石墨类似,也具有层状结构,单层黑磷叫黑磷烯,其结构如图1所示。
为大幅度提高锂电池的充电速率,科学家最近研发了黑磷——石墨复合负极材料,其单层结构俯视图如图2所示。
A.黑磷烯中最小的环为六元环,每个环平均含有2个P原子
B.黑磷区中P-P键的键能不完全相同
C.复合材料单层中,P原子与C原子之间的作用力属范德华力
D.石墨与黑磷的交界结合区域中,P原子与C原子共平面
A.由图可知,黑磷烯中最小的环为六元环,每个P原子为3个环所共有,则每个环中P原子的个数为6×
=2个,故A正确;
B.由图可知,石墨与黑磷的交界结合区域中P原子与C原子形成P—C键,导致黑磷区中P—P键的键长、键能不完全相同,故B错误;
C.由石墨与黑磷制备该复合材料的过程中会形成P—C键,则复合材料单层中,P原子与C原子之间的作用力是共价键,故C错误;
D.石碳原子为sp2杂化,与六元环中碳原子相连的原子与六元环共面,则墨与黑磷的交界结合区域中,磷原子与碳原子共平面,故D正确;
11.石墨烯可转化为富勒烯(C60),某金属M与C60可制备一种低温超导材料,晶胞结构如图所示,晶胞边长为a,M原子位于晶胞的棱上与内部。
A.C60和石墨烯是同分异构体
B.C60周围等距且最近的C60的个数为4个
C.该材料的化学式为M3C60
D.C60与C60的最短距离是
a
A.C60和石墨烯是C元素的两种不同性质的单质,二者互为同素异形体,A错误;
B.由晶胞结构可知:
在一个晶胞中距离顶点的C60最近的C60有3个,分别位于通过该顶点的三个面心上。
通过该顶点可形成8个晶胞,每个面心C60被重复了二次,故C60周围等距且最近的C60的个数为
,B错误;
C.该晶胞中C60个数为:
8×
+6×
=4,含有M数目为:
12×
+8+1=12,M:
C60=12:
4=3:
1,所以该材料的化学式为M3C60,C正确;
D.由图可知在晶胞中C60与C60的最短距离是面对角线的一半。
晶胞边长为a,晶胞面对角线为
,则晶胞面对角线的一半为
,D错误;
故合理选项是C。
12.如图,X、Y、Z、W四种短周期元素的原子最外层电子数之和为21.下列说法正确的是
T
A.原子半径(r):
r(Z)>r(Y)>r(X)
B.X的氢化物一定比Y的氢化物的沸点要低
C.WY2、WZ4、WX均有熔点高、硬度大的特性
D.某病毒DNA链中有T元素,可能是T取代了普通DNA链中的P元素
设X的最外层电子数为a,则Y、W、Z的最外层电子数分别为(a+2)、a、(a+3),从而得出a+(a+2)+a+(a+3)=21,a=4,故X、Y、W、Z分别为C、O、Si、Cl,则T为As元素。
A.X、Y、Z分别为C、O、Cl,C、O为同周期元素,C在O的左边,则原子半径(r):
r(C)>r(O),故A错误;
B.X、Y分别为C、O,若X的氢化物中碳原子数比较多(如石蜡),常温下呈固态,则其沸点可能比Y的氢化物(H2O)的沸点要高,故B错误;
C.SiCl4在固态时形成分子晶体,其熔点较低、硬度较小,故C错误;
D.某病毒DNA链中有As元素,As与P属于同主族元素,可能是As取代了普通DNA链中的P元素生成的,故D正确;
13.下面有关氮化硼(BN)两种晶体说法正确的是
A.两种晶体均为原子晶体
B.两种晶体的化学式相同所以属于同种物质
C.两种晶体中均含有极性键和非极性键
D.根据立方相氮化硼的晶体结构推测其可用作超硬材料,有优异的耐磨性
A.六方相氮化硼为混合型晶体,立方相氮化硼为原子晶体,A错误;
B.二者结构不同,不属于同种物质,B错误;
C.两种晶体均只含有B-N键,属于极性共价键,C错误;
D.立方相氮化硼为空间网状立体构型,原子间以共价键相结合,难以形变,所以硬度大,可用作超硬材料,有优异的耐磨性,D正确;
14.元素周期表中第四周期某些过渡元素(如Ti、Mn等)在生产生活中有着广泛的应用。
如钛的应用越来越受到人们的关注,锰及其化合物的应用研究是前沿科学之一,下列有关说法错误的是
A.钛比钢轻、比铝硬,是一种新的结构材料。
钛硬度比铝大的原因是Ti的相对原子质量大,分子间作用更强
B.第四周期元素中,基态原子的未成对电子数与钛相同的有Ni、Ge、Se
C.已知三醋酸锰[(CH3COO)3Mn]是一种很好的有机反应氧化剂。
三醋酸锰[(CH3COO)3Mn]中阳离子的价层电子排布式中电子的自旋状态相同
D.比较Fe和Mn的第三电离能,可得I(3Fe)小于I3(Mn),原因是Mn2+的3d能级是半充满的相对稳定结构,较难失去电子
A.钛硬度比铝大的原因是Ti原子的价电子数比Al多,金属键更强,A错误;
B.Ti是22号元素,有2个未成对电子,在第四周期元素中,基态原子的未成对电子数与钛相同的有28号的Ni,32号Ge,34号Se元素三种元素,B正确;
C.在Mn是25号元素,三醋酸锰[(CH3COO)3Mn]中阳离子Mn3+的价层电子排布式是3d4。
3d轨道有5个,原子核外电子总是尽可能成单排列,而且自旋方向相同,这种排布使原子的能量低,比较稳定,故Mn3+的4个价电子的自旋状态相同,C正确;
D.Fe3+的价电子排布式是3d5,处于轨道的半充满的稳定状态;
而Mn2+的3d能级是半充满的相对稳定结构,再失去1个电子变为Mn3+时是3d4的不稳定状态,因此Mn2+较难失去电子,故第三电离能:
I(3Fe)小于I3(Mn),D正确;
故合理选项是A。
15.TiO2的“纳米材料”有广泛的应用,工业上可利用TiCl4制取。
TiCl4熔点为-25℃,沸点为136.4℃。
制取TiO2的反应为①2FeTiO3+7Cl2+3C=2TiCl4+2FeCl3+3CO2、②TiCl4+O2=TiO2+2Cl2。
A.基态Ti原子核外价电子排布式为3d24s2
B.Cl2、CO2都是含有非极性键的非极性分子
C.TiCl4晶体是离子晶体,配位数为4
D.生成1molFeCl3转移电子的物质的量为14mol
A.Ti的原子序数为22,Ti原子核外有22个电子,基态Ti原子的核外电子排布式为1s22s22p63s23p63d24s2,价电子排布式为3d24s2,A正确;
B.Cl2和CO2都是非极性分子,Cl2中含Cl—Cl非极性键,CO2中含C=O极性键、不含非极性键,B错误;
C.TiCl4的熔点为-25℃,沸点为136.4℃,熔、沸点较低,TiCl4晶体是分子晶体,C错误;
D.反应①中Fe元素的化合价由+2价升至+3价,C元素的化合价由0价升至+4价,Cl元素的化合价由0价降至-1价,生成2molFeCl3转移14mol电子,则生成1molFeCl3转移电子物质的量为7mol,D错误;
16.下列关于Be、Mg及其化合物结构与性质的论述错误的是
A.Mg的两种激发态[Ne]3s13p1和[Ne]3p2中,前者第二电离能更大
B.F-半径小,MgF2晶格能更高,故MgF2熔点高于BeCl2
C.BeH2、Be(OH)
中心原子的杂化方式分别为sp1、sp3
D.BeCl2在一定条件下可通过配位键形成多聚分子,结构如图所示
A.Mg的激发态[Ne]3s13p1第二电离能失去3s1,激发态[Ne]3p2中第二电离能失去3p1,3p能量高,需要能量少,则前者第二电离能更大,A正确;
B.MgF2是离子晶体,熔沸点和晶格能有关,BeCl2为分子晶体,熔沸点和范德华力有关,即与F-半径无关,B错误;
C.BeH2中价电子对数为2+0=2,sp杂化,Be(OH)
价电子对数为4+0=4,sp3杂化,C正确;
D.Be周围的四个键中有2个配位键,如图
,Be提供两个空轨道参与配位键,D正确;
二、填空题:
(4个小题,共52分)
17.(16分)硅铝合金广泛应用于航空、交通、建筑、汽车等行业。
完成下列填空:
(1)硅原子的结构示意图为___________;
比较硅铝的原子半径:
r(Si)___________r(Al)(选填:
“>
”、“<”或“=”)。
硅铝合金中的铝与氢氧化钠溶液反应的化学方程式为___________。
(2)氟化铝和氯化铝的熔点分别为1040
和194
,它们熔点差异大的原因可能是___________。
(3)门捷列夫准确预测了铝、硅下一周期的同主族元素(当时并未被发现)的性质,并将他们分别命名为“类铝”和“类硅”。
你据此推断类铝的最外层电子排布式为___________,推断的依据是___________。
(4)制备硅铝合金时,在高温真空炉中发生如下反应:
;
上述反应的最终还原产物为___________;
当有1molC参加反应时,转移的电子数目为___________。
【答案】
(每空2分)
(1)
<
(2)氟化铝为离子晶体,氯化铝为分子晶体,离子晶体的熔沸点比分子晶体高(3)
类铝与铝同主族,故最外层为3个电子,在铝下一周期,故为第四周期,电子层数为4层(4)Al、Si2NA
(1)硅为14号元素,故硅原子的结构示意图为
硅和铝为同一周期元素,从左往右半径依次减小,故r(Si)<r(Al),铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,故铝与氢氧化钠溶液反应的化学方程式为:
,故答案为:
<;
(2)由于F的电负性比Cl的大,故氟化铝中存在离子键,而氯化铝中存在的是共价键,它们熔点差异大的原因可能是氟化铝是离子晶体,氯化铝是分子晶体,故答案为:
氟化铝为离子晶体,氯化铝为分子晶体,离子晶体的熔沸点比分子晶体高;
(3)类铝与铝同主族,故最外层为3个电子,在铝下一周期,故为第四周期,电子层数为4层,故类铝的最外层电子排布式为
类铝与铝同主族,故最外层为3个电子,在铝下一周期,故为第四周期,电子层数为4层;
(4)还原产物是指元素的化合价降低被还原而成的产物,根据上述反应可知,最终还原产物为Al、Si;
反应中C的化合价由0价升高为CO中的+2价,故当有1molC参加反应时,转移的电子数目为:
2NA个,故答案为:
Al、Si;
2NA。
18.(12分)工业上常利用FeSO4还原酸浸软锰矿(主要成分MnO2,杂质为Si、Fe和Al等元素的化合物)制备MnSO4·
H2O。
(1)①FeSO4还原MnO2生成MnSO4反应的离子方程式为___。
②Fe2+基态核外电子排布式为___。
(2)在一定温度下,软锰矿与FeSO4、硫酸、蒸馏水按照一定比例混合搅拌反应。
混合体系液固比(g·
mL-1)对锰浸取率(%)的影响如图所示。
反应需要控制液固比=4:
1:
当液固比<4:
1时,锰浸取率随液固比增大而迅速上升的原因是___。
(3)浸取液经氧化、中和等系列操作后,可得到MnSO4·
H2O粗产品。
通过下列方法测定产品纯度:
准确称取3.000g样品,加适量ZnO及H2O煮沸、冷却,转移至锥形瓶中,用0.5000mol·
L-1KMnO4,标准
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 学年 化学 学期 期末 挑战 卷人教版 选修 301 解析
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
