 北京顺义 高中化学中总复习一轮复习氮及其化合物专题训练Word文件下载.docx
北京顺义 高中化学中总复习一轮复习氮及其化合物专题训练Word文件下载.docx
- 文档编号:19178656
- 上传时间:2023-01-04
- 格式:DOCX
- 页数:11
- 大小:303.63KB
北京顺义 高中化学中总复习一轮复习氮及其化合物专题训练Word文件下载.docx
《北京顺义 高中化学中总复习一轮复习氮及其化合物专题训练Word文件下载.docx》由会员分享,可在线阅读,更多相关《北京顺义 高中化学中总复习一轮复习氮及其化合物专题训练Word文件下载.docx(11页珍藏版)》请在冰豆网上搜索。
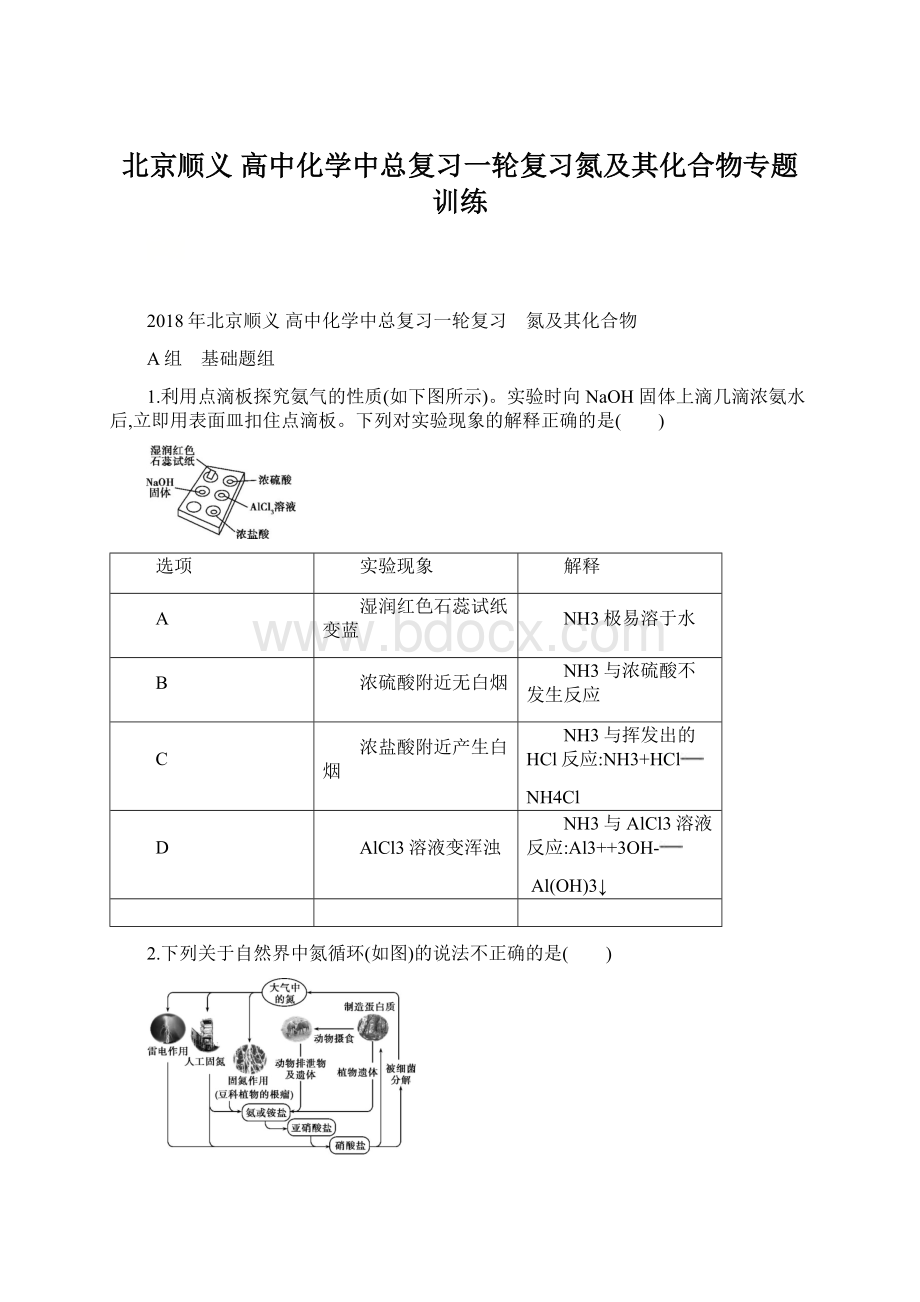
D.碳、氢、氧三种元素也参与了氮循环
3.将氨水分别滴加到下列4种溶液中,下列说法不正确的是( )
A.试管a中产生白烟
B.试管b中溶液由红色变为蓝色
C.试管c中能发生氧化还原反应
D.试管d中先有沉淀,后沉淀溶解
4.下列解释物质用途或现象的反应方程式不正确的是( )
A.汽车尾气中发生的催化转化反应:
2NO+2CO
N2+2CO2
B.铝热反应用于焊接钢轨:
2Al+Fe2O3
Al2O3+2Fe
C.燃煤时加入石灰石减少SO2排放:
2CaCO3+2SO2+O2
2CaSO3+2CO2
D.用Na2CO3溶液处理水垢中的不溶物CaSO4:
CaSO4+C
CaCO3+S
5.下列关于浓硫酸和浓硝酸的叙述不正确的是( )
A.加热条件下均能与碳反应
B.长期露置在空气中浓度均会降低
C.常温下均不能用铁制容器贮存
D.一定条件下均可与铜片反应
6.某同学将光亮的镁条放入盛有NH4Cl溶液的试管中,有大量气泡产生。
为探究该反应原理,该同学做了以下实验并观察到相关现象,由此得出的结论不合理的是( )
实验及现象
结论
将湿润的红色石蕊试纸放在试管口,试纸变蓝
反应中有NH3产生
收集产生的气体并点燃,火焰呈淡蓝色
反应中有H2产生
收集气体的同时测得溶液的pH为8.6
弱碱性溶液中Mg也可被氧化
将光亮的镁条放入pH为8.6的NaHCO3溶液中,有气泡产生
弱碱性溶液中OH-氧化了Mg
7.NH3是一种重要的化工产品,是制造铵盐的原料。
(1)NH3的电子式为 。
(2)实验室用图1所示装置制备氨气,该反应的化学方程式为 。
检验氨气的方法是 。
(3)实验室也常用图2所示的简易装置制备氨气,下列说法正确的是 (填字母序号)。
a.锥形瓶中加入的固体物质可以是碱石灰
b.制得的氨气可用碱石灰来干燥
c.可用图3装置和试剂对氨气进行尾气处理
(4)氯化铵常用作除锈剂,用化学用语表达其水溶液呈酸性的原因是 。
(5)工业上用活性炭作催化剂,在280~450℃条件下氯化铵与甲醇反应制取一氯甲烷,该反应的化学方程式为 。
(6)工业合成氨的反应为N2+3H2
2NH3。
已知断开1mol化学键所需的能量见下表。
H—H
N—H
键能/kJ·
mol-1
945
436
391
则运用键能数据计算,该反应的ΔH约为 kJ·
mol-1。
B组 提升题组
8.在通风橱中进行下列实验:
步骤
现象
Fe表面产生大量无色气泡,液面上方变为红棕色
Fe表面产生少量红棕色气泡后,迅速停止
Fe、Cu接触后,其表面均产生红棕色气泡
下列说法不正确的是( )
A.Ⅰ中气体由无色变红棕色的化学方程式:
2NO+O2
2NO2
B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
9.2.8gFe全部溶于一定浓度的200mLHNO3溶液中,得到标准状况下的气体1.12L,测得反应后溶液的pH为1。
若反应前后溶液体积变化忽略不计,则下列有关判断不正确的是( )
A.反应后溶液中铁元素一定只以Fe3+形式存在
B.1.12L气体可能是NO、NO2的混合气体
C.反应后溶液中c(N
)=0.85mol/L
D.反应后的溶液最多还能溶解1.82gFe
10.为了避免NO、NO2、N2O4对大气的污染,常采用氢氧化钠溶液进行吸收处理(反应方程式:
3NO2+2NaOH
2NaNO3+NO+H2O;
NO2+NO+2NaOH
2NaNO2+H2O)。
现有由amolNO、bmolNO2、cmolN2O4组成的混合气体恰好被VL氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液中溶质的物质的量浓度为( )
A.
mol·
L-1B.
L-1
C.
L-1D.
11.(2016北京海淀期中,19)Na2O2和NO2都是中学化学常见的物质,某实验小组对它们之间的反应进行了探究。
(1)小组同学对NO2与Na2O2的反应提出以下假设。
假设一:
生成NaNO3,反应的化学方程式为2NO2+Na2O2
2NaNO3
假设二:
生成NaNO2,反应的化学方程式为 。
(2)小组同学在通风橱中制备并收集干燥的NO2后进行如下实验:
序号
操作步骤
实验1
①按下图组装仪器。
打开K,将气球中的Na2O2粉末倒入试管中,振荡,充分反应
试管内红棕色消失,气球变瘪
②试管冷却后,打开胶塞,加入5mL蒸馏水
未见红棕色气体,试管底部固体全部溶解得澄清溶液
①实验室常利用铜与浓硝酸反应制备NO2,反应的化学方程式为 。
②有同学根据实验1中“气球变瘪”的现象推断假设一成立,你认为是否合理并简述理由:
。
(3)小组同学进一步对产物进行检验。
查阅资料:
ⅰ.Na2O2与水反应会生成H2O2;
ⅱ.N
具有还原性,可用酸性KMnO4溶液进行检验;
ⅲ.含N
的溶液遇FeSO4和浓硫酸生成棕色物质[Fe(NO)]2+。
进行实验:
实验2
取实验1所得清液, ,再调节此溶液pH至7左右
实验3
取实验2后的清液2mL,加入2滴0.1%的酸性KMnO4溶液
——
实验4
①向试管中加入2mL新制FeSO4溶液,再加入10滴0.1mol·
L-1NaNO3溶液,振荡,再向试管中加入0.5mL98%的浓硫酸
滴入NaNO3溶液,无明显变化;
加入浓硫酸后,溶液变棕色
②向试管中加入2mL新制FeSO4溶液,再加入10滴0.1mol·
L-1NaNO2溶液,振荡,再向试管中加入0.5mL98%的浓硫酸
加入NaNO2溶液,立即变棕色;
加入浓硫酸后,溶液无明显变化
③向试管中加入2mL新制FeSO4溶液,加10滴实验2后的清液,振荡,再加0.5mL98%的浓硫酸
滴加实验2得到的清液后,溶液立即变浅棕色;
加入浓硫酸后,溶液变深棕色
①实验2的主要目的是排除溶液中H2O2对后续实验的干扰,请补全实验2的操作
。
②根据实验3的现象可得出结论“产物含N
”,则该实验的现象是 。
③实验4中进行步骤②的目的是 。
(4)该小组同学由以上全部实验可得出结论:
。
答案全解全析
1.C A项,氨气极易溶于水且氨水显碱性,故氨气能使湿润的红色石蕊试纸变蓝;
B项,氨气可与浓硫酸反应,但因浓硫酸难挥发,所以观察不到白烟;
C项,浓盐酸易挥发,氨气与浓盐酸反应可看到大量白烟;
D项,氨气与水反应生成一水合氨,一水合氨能与氯化铝反应生成氢氧化铝白色沉淀,离子方程式为Al3++3NH3·
H2O
Al(OH)3↓+3N
。
2.A A项,人工固氮时,N2+3H2
2NH3,氮元素被还原;
B项,把游离态的氮元素转化为含氮化合物的过程是氮的固定,工业合成氨属于人工固氮;
C项,硝酸盐可转化为蛋白质,动植物遗体可转化为氨或铵盐,则含氮有机物和含氮无机物可相互转化;
D项,在自然界氮循环过程中,碳、氢、氧三种元素也参与了循环。
3.D A项,浓盐酸挥发出的氯化氢气体与氨水挥发出的氨气反应生成氯化铵固体,产生白烟;
B项,氨气溶于水生成弱碱,红色石蕊遇碱变蓝;
C项,氨水能与硫酸亚铁溶液反应生成氢氧化亚铁白色沉淀,氢氧化亚铁易被空气氧化;
D项,Al(OH)3不溶于氨水。
4.C C项,反应生成CaSO4,正确的反应方程式为2CaCO3+2SO2+O2
2CaSO4+2CO2。
5.C A项,加热条件下,浓硫酸和浓硝酸都能与碳发生氧化还原反应。
B项,浓硫酸具有吸水性,能吸收空气中的水蒸气;
浓硝酸具有挥发性,所以长期露置在空气中浓度均会降低。
C项,常温下,浓硫酸和浓硝酸都能使铁发生钝化,所以常温下均能用铁制容器贮存。
D项,加热条件下,铜和浓硫酸发生氧化还原反应生成二氧化硫;
常温下,铜和浓硝酸反应生成二氧化氮。
6.D NH4Cl溶液中存在平衡:
N
+H2O
H++NH3·
H2O,镁条与H+反应生成H2,同时平衡正向移动,溶液由弱酸性逐渐变为弱碱性,NH3·
H2O浓度变大,分解产生NH3,A、B、C项均合理;
pH=8.6的NaHCO3溶液中存在HC
+H+,Mg与H+仍可反应产生H2,D项不合理。
7.
答案
(1)
(2)2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
方法1:
用湿润的红色石蕊试纸靠近气体,试纸变蓝,说明气体是氨气
方法2:
用一根玻璃棒蘸取浓盐酸,靠近气体,有大量白烟,说明气体是氨气
(填一种方法即可)
(3)ab
(4)N
NH3·
H2O+H+
(5)NH4Cl+CH3OH(g)
CH3Cl+NH3+H2O
(6)-93
解析
(1)NH3是共价化合物,电子式为
(2)实验室用加热氯化铵和消石灰的方法制备氨气,反应的化学方程式为2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;
检验氨气可用湿润的红色石蕊试纸,若试纸变蓝,说明气体是氨气或者用一根玻璃棒蘸取浓盐酸,靠近气体,有大量白烟,说明气体是氨气。
(3)把浓氨水滴加到碱石灰上可产生氨气;
氨气是碱性气体,可用碱石灰干燥;
吸收氨气要注意防止倒吸,a、b正确,c错误。
(4)氯化铵是强酸弱碱盐,水解显酸性,N
H++NH3·
H2O。
(5)氯化铵与甲醇反应制取一氯甲烷的化学方程式为NH4Cl+CH3OH(g)
CH3Cl+NH3+H2O。
(6)ΔH=945kJ·
mol-1+3×
436kJ·
mol-1-6×
391kJ·
mol-1=-93kJ·
8.C A项,Fe与稀HNO3反应生成NO,无色的NO易被空气中的O2氧化为红棕色的NO2,化学方程式为2NO+O2
2NO2;
B项,Ⅱ中现象说明Fe遇到浓HNO3发生钝化,表面形成致密的氧化层,阻止Fe进一步反应;
C项,浓HNO3的氧化性强于稀HNO3;
D项,Fe、Cu、浓HNO3可构成原电池,连接电流计可以判断Fe是否被氧化。
9.B A项,反应后溶液的pH为1,即HNO3过量,Fe只能转化为Fe3+,故A正确;
B项,2.8gFe的物质的量为
=0.05mol,设还原产物中N元素的化合价为x,由得失电子守恒可得0.05×
3=(5-x)×
解得x=2,即还原产物为NO,B错误;
C项,反应后溶液为硝酸铁、硝酸的混合溶液,根据电荷守恒可得c(H+)+3c(Fe3+)
=c(N
)+c(OH-),因溶液呈强酸性,c(OH-)可忽略不计,故c(N
)=3c(Fe3+)+c(H+)=
×
3+0.1mol/L=
0.85mol/L,故C正确;
D项,由氮原子守恒可知n原来(HNO3)=3n[Fe(NO3)3]+n剩余(HNO3)+n(NO)=0.05mol×
3+
0.1mol/L×
0.2L+0.05mol=0.22mol,生成Fe(NO3)2时原硝酸溶解的铁最多,由3Fe+8HNO3
3Fe(NO3)2+
2NO↑+4H2O可知,0.22molHNO3最多溶解铁
0.22mol,质量为
0.22mol×
56g/mol=4.62g,故还能溶解铁4.62g-2.8g=1.82g,故D正确。
10.B 根据题意可知最终所得溶液中的溶质为NaNO2或NaNO3、NaNO2,根据物料守恒可知n(NaOH)=n(NO)+n(NO2)+2n(N2O4)=(a+b+2c)mol,故此氢氧化钠溶液中溶质的物质的量浓度为
=
L-1。
11.
答案
(1)2NO2+Na2O2
2NaNO2+O2
(2)①Cu+4HNO3(浓)
Cu(NO3)2+2NO2↑+2H2O
②不合理,理由是:
根据方程式可以发现无论是按假设一还是假设二发生反应,体系的压强都要减小,都能观察到“气球变瘪”的现象
(3)①向其中加入少量MnO2粉末,待不再产生气泡后,静置,取上层清液
②KMnO4溶液褪色
③通过和实验4步骤①进行对比,排除N
的存在对N
检验的干扰
(4)Na2O2和NO2反应既能生成NaNO3也能生成NaNO2(或答“假设一和假设二都成立”,或答“Na2O2和NO2反应的产物中既含N
又含N
”)
解析
(1)NO2与Na2O2反应生成NaNO2的化学方程式为2NO2+Na2O2
2NaNO2+O2。
(2)①铜与浓硝酸反应制备NO2的化学方程式为Cu+4HNO3(浓)
Cu(NO3)2+2NO2↑+2H2O。
②根据方程式可以发现无论是按假设一还是假设二发生反应,体系的压强都要减小,都能观察到“气球变瘪”的现象,故不能根据“气球变瘪”的现象推断假设一成立。
(3)①MnO2可以加快H2O2的分解。
②N
具有还原性,能使酸性KMnO4溶液褪色。
③实验4中进行步骤②的目的是通过和实验4步骤①进行对比,排除N
检验的干扰。
(4)由全部实验可得出结论:
Na2O2和NO2反应既能生成NaNO3也能生成NaNO2。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 北京顺义 高中化学中总复习一轮复习氮及其化合物专题训练 北京 顺义 高中化学 复习 一轮 及其 化合物 专题 训练
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
