 五年制预防医学专业《基础化学》课程教学大纲Word文档下载推荐.docx
五年制预防医学专业《基础化学》课程教学大纲Word文档下载推荐.docx
- 文档编号:19140097
- 上传时间:2023-01-04
- 格式:DOCX
- 页数:10
- 大小:19.16KB
五年制预防医学专业《基础化学》课程教学大纲Word文档下载推荐.docx
《五年制预防医学专业《基础化学》课程教学大纲Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《五年制预防医学专业《基础化学》课程教学大纲Word文档下载推荐.docx(10页珍藏版)》请在冰豆网上搜索。
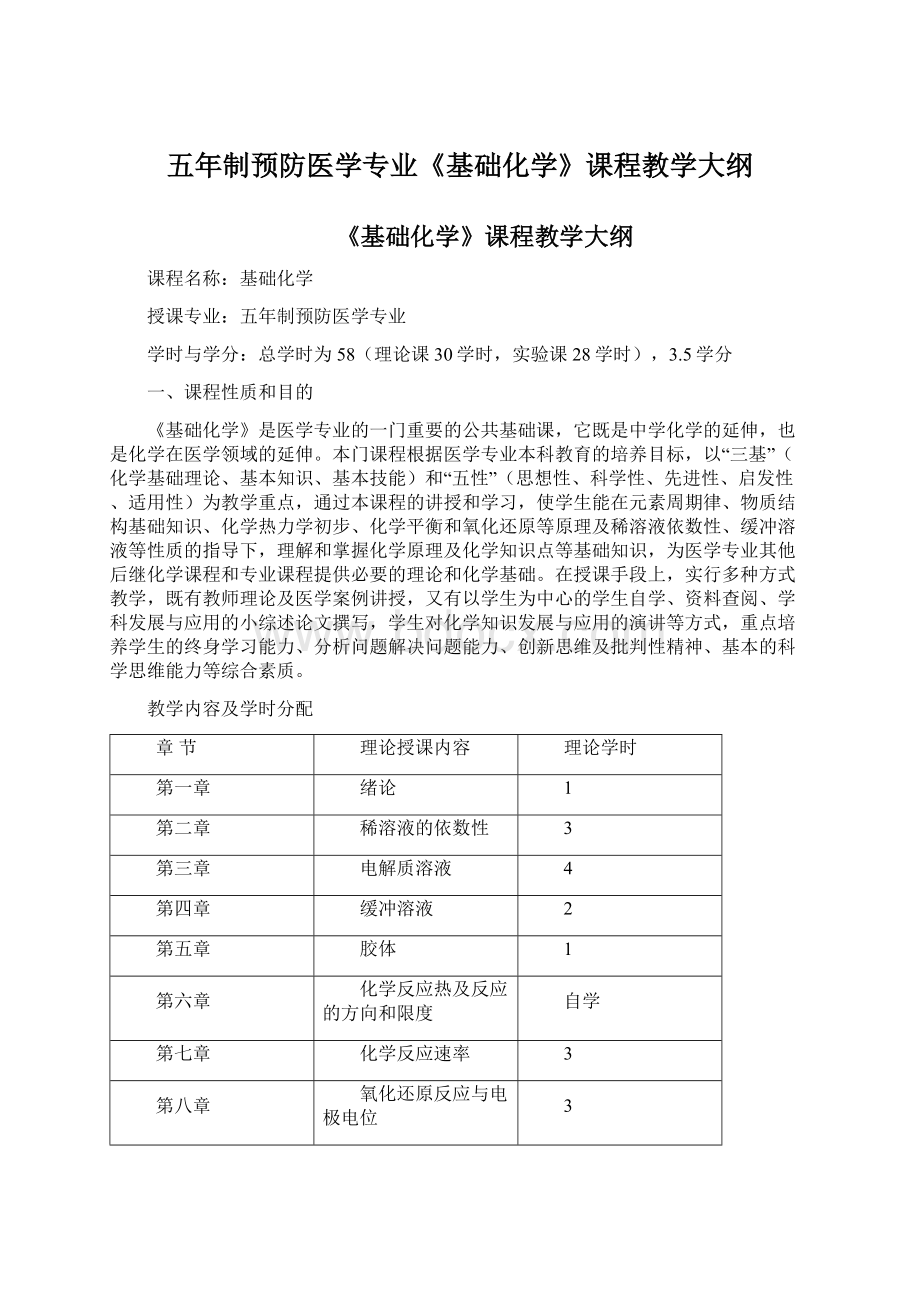
第五章
胶体
第六章
化学反应热及反应的方向和限度
自学
第七章
化学反应速率
第八章
氧化还原反应与电极电位
第九章
原子结构和元素周期律
第十章
共价键与分子间力
第十一章
配位化合物
第十二章
滴定分析
第十三章
可见分光光度法和紫外分光光度法
第十四章
现代仪器分析简介
合计
30
二、理论课教学内容及基本要求
第一章绪论
【目的要求】
一、掌握:
溶液的组成标度:
物质的量、物质的量浓度、摩尔分数、质量摩尔浓度的基本概念及有关计算。
有效数字和运算规则。
二、熟悉:
质量浓度、质量分数的基本概念及有关计算。
三、了解:
基础化学的学习方法和法定计量单位。
【教学内容】
一、基础化学课程的地位和作用
二、我国的法定计量单位
三、溶液的组成标度
【教学方法】
课堂讲授、多媒体教学
【教学时数】
1学时
第二章稀溶液的依数性
稀溶液的依数性(溶液的蒸气压下降、溶液的沸点升高、凝固点降低、溶液的渗透压)的概念、性质、影响因素及其有关计算;
临床上等渗、高渗、低渗的概念及判断,渗透浓度的计算。
强电解质溶液的依数性,渗透压在医学中的意义;
胶体渗透压、晶体渗透压的概念。
胶体渗透压、晶体渗透压在体液交换中的主要作用及其应用。
一、溶液的蒸气压下降
二、溶液的沸点升高和凝固点降低
三、溶液的渗透压力
3学时
第三章电解质溶液
酸碱质子理论:
酸碱定义、共轭酸碱间的基本关系、酸碱反应的本质、酸碱强度的相对性;
水的质子自递作用及水的离子积;
水溶液的pH值;
一元弱酸弱碱质子转移平衡及相关计算、酸碱的强度及平衡常数;
同离子效应和盐效应。
强电解质和弱电解质的概念;
强电解质溶液理论的基本要点;
离子的活度和活度因子概念;
离子强度的计算。
多元弱酸、弱碱溶液、两性物质溶液有关离子浓度的计算;
难溶电解质溶液的溶度积及溶度积规则;
分级沉淀及相关计算。
一、强电解质溶液
二、酸碱质子理论
三、酸碱溶液pH值的计算
四、难溶电解质的沉淀溶解平衡
课堂讲授、多媒体教学
4学时
第四章缓冲溶液
缓冲溶液的概念、缓冲溶液组成和缓冲作用机制;
缓冲溶液pH值的计算(Henderson-HasselbalchEquation);
缓冲容量的概念及影响因素;
缓冲作用范围。
配制缓冲溶液的原则、方法及计算。
缓冲溶液pH值的计算公式的校正;
标准缓冲溶液;
人体血液中的主要缓冲对及其缓冲作用机制。
一、缓冲溶液及缓冲机制
二、缓冲溶液的pH
三、缓冲容量和缓冲范围
四、缓冲溶液的配制
五、血液中的缓冲系
2学时
第五章胶体
分散系的概念及分类方法;
溶胶的基本特征;
胶粒带电原因、胶粒的双电层结构、溶胶的稳定因素、溶胶的聚沉和保护。
溶胶的光学性质、动力学性质;
电泳、电渗的概念
高分子化合物结构特点及其溶液形成、性质;
表面活性剂的结构及其吸附作用。
一、分散系统和胶体分散系
二、溶胶
三、高分子溶液
四、表面活性剂和乳状液
五、胶体与医药学
课堂讲授、多媒体教学、自学
第六章化学反应热及反应的方向和限度
状态函数、热、功、内能、焓、熵、Gibbs自由能概念;
热力学第一定律的基本内容;
化学反应的热效应和焓变;
Hess定律和反应热的计算;
自发反应的推动力;
运用Gibbs自由能判断化学反应的可能性和方向;
化学反应等温方程式;
化学平衡的概念及化学平衡常数的计算;
Gibbs自由能与化学平衡常数的关系。
热力学系统与过程;
熵增原理;
Gibbs自由能的计算;
标准平衡常数与化学反应限度及判断自发反应方向;
浓度、压力、温度对化学平衡的影响;
LeChatelier规律。
等压反应热和等容反应热;
自发过程。
一、热力学系统和状态函数
二、能量守恒和化学反应热
三、熵和Gibbs自由能
四、化学反应的限度和平衡常数
第七章化学反应速率
化学反应速率的概念及表示法;
质量作用定律与化学反应速率方程;
速率常数;
元反应与反应分子数;
简单反应和复杂反应,反应级数,一级反应的特征及计算。
碰撞理论基本要点;
有效碰撞、活化能、活化分子的概念;
活化能与反应速率的关系;
浓度、温度、催化剂对化学反应速率的影响。
二级反应、零级反应的特征及计算。
过渡态理论的基本要点;
均相催化作用的特点。
一、化学反应速率的表示方法
二、反应机制和元反应
三、具有简单级数的反应及其特点
四、化学反应速率理论简介
五、温度对化学反应速率的影响
六、催化剂对化学反应速率的影响
第八章氧化还原反应与电极电位
氧化值;
原电池的正负极、正负极反应、电池组成式书写方式;
电极电位的影响因素;
掌握Nernst方程式在计算电极电位、电池电动势、判断氧化还原反应的方向、计算化学平衡常数等方面的应用。
标准电极电位测定及其应用;
电位法测定溶液pH值。
电极电位的产生;
电极类型及其特点;
常用参比电极和指示电极。
一、氧化还原反应
二、原电池与电极电位
三、电池电动势与化学反应Gibbs自由能
四、电极电位的Nernst方程式及影响电极电位的因素
五、电位法测定溶液的pH值
第九章原子结构和元素周期律
四个量子数的概念及意义,用四个量子数表示核外电子的运动状态。
s、p、d原子轨道角度分布图;
原子核外电子的排布规律:
Pauli不相容原理、能量最低原理、Hund规则;
原子的电子组态与元素周期表,元素周期表的意义;
元素性质的周期性变化规律:
原子半径、电负性。
原子轨道(波函数)、概率密度、电子云的概念;
屏蔽作用,钻穿效应、多电子原子的能级;
过渡元素概念。
氢原子结构;
电子的波粒二象性;
测不准原理;
原子轨道径向分布图、径向分布函数图表示的意义。
一、氢原子的结构
二、量子数和原子轨道
三、电子组态和元素周期表
四、元素性质的周期性变化规律
五、元素和人体健康
第十章共价键与分子间力
现代价键理论中共价键的本质、特征:
方向性和饱和性;
形成条件、类型(σ键和π键);
杂化轨道类型及其在解释分子空间构型中的应用;
分子的极性;
VanderWaals力、氢键的概念及其对物质物理性质的影响。
共价键的键参数的基本概念:
键能、键角、键长、键的极性;
配位键的特点;
分子轨道理论要点及其在简单双原子分子中的应用。
分子轨道形成的条件,自由基的概念;
分子的极化。
价层电子互斥理论(自学)
一、现代价键理论
二、杂化轨道理论
三、分子轨道理论简介
四、分子间作用力
第十一章配位化合物
配位化合物的定义、组成、命名;
螯合物中螯合剂的特点及螯合效应;
影响螯合物稳定性的因素。
配位平衡常数;
配位平衡移动及影响因素。
配位化合物的价键理论(sp、sp3、dsp2、d2sp3、sp3d2的杂化类型;
内轨型配合物;
外轨型配合物;
配合物的磁性判断);
配位平衡移动的有关计算。
生物配体;
配位化合物在医学中的应用及意义。
一、配位化合物的基本概念
二、配合物的化学键理论
三、配位平衡
四、螯合物和螯合滴定
第十二章滴定分析
滴定分析的一般过程;
滴定分析的计算;
酸碱指示剂的变色原理、变色范围确定、在滴定分析中指示剂的选择原则;
常见酸碱指示剂:
甲基红、甲基橙、酚酞的变色范围。
滴定分析中的常用术语;
滴定分析反应的基本条件;
滴定分析的类型;
滴定曲线:
强酸与强碱间滴定的突跃范围、强碱与一元弱酸间的滴定突跃范围、强酸与一元弱碱间的滴定突跃范围;
滴定突跃范围与酸碱强度、浓度的关系。
滴定分析过程误差的产生原因;
分析结果的误差;
常用酸碱标准溶液。
氧化还原滴定法;
沉淀滴定法;
配位滴定法。
一、滴定分析法概述
二、酸碱滴定法
第十三章可见分光光度法和紫外分光光度法
透光率和吸光度概念及相互关系;
Lambert-Beer定律。
分光光度法影响因素、使用范围及使用条件;
分光光度法中的标准曲线法、标准对照法。
物质的吸收光谱及其意义。
一、物质的吸收光谱
二、分光光度法基本原理
三、可见分光光度法
四、提高测量灵敏度和准确度的方法
第十四章现代仪器分析简介
一、熟悉:
原子吸收光谱法、荧光分析法、色谱法的基本原理。
灵敏度和检出限的概念。
二、了解:
原子吸收分光光度计的基本结构和定量分析方法;
荧光光度计的基本结构和定量分析方法;
色谱分析的塔板理论、定性与定量分析的基本方法
一、原子吸收光谱法
二、荧光分析法
三、色谱法
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 基础化学 五年制 预防 医学专业 基础 化学 课程 教学大纲
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
