 北京各区初三一模化学分类汇编生产实际分析11区含答案Word格式文档下载.docx
北京各区初三一模化学分类汇编生产实际分析11区含答案Word格式文档下载.docx
- 文档编号:19086746
- 上传时间:2023-01-03
- 格式:DOCX
- 页数:12
- 大小:445.25KB
北京各区初三一模化学分类汇编生产实际分析11区含答案Word格式文档下载.docx
《北京各区初三一模化学分类汇编生产实际分析11区含答案Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《北京各区初三一模化学分类汇编生产实际分析11区含答案Word格式文档下载.docx(12页珍藏版)》请在冰豆网上搜索。
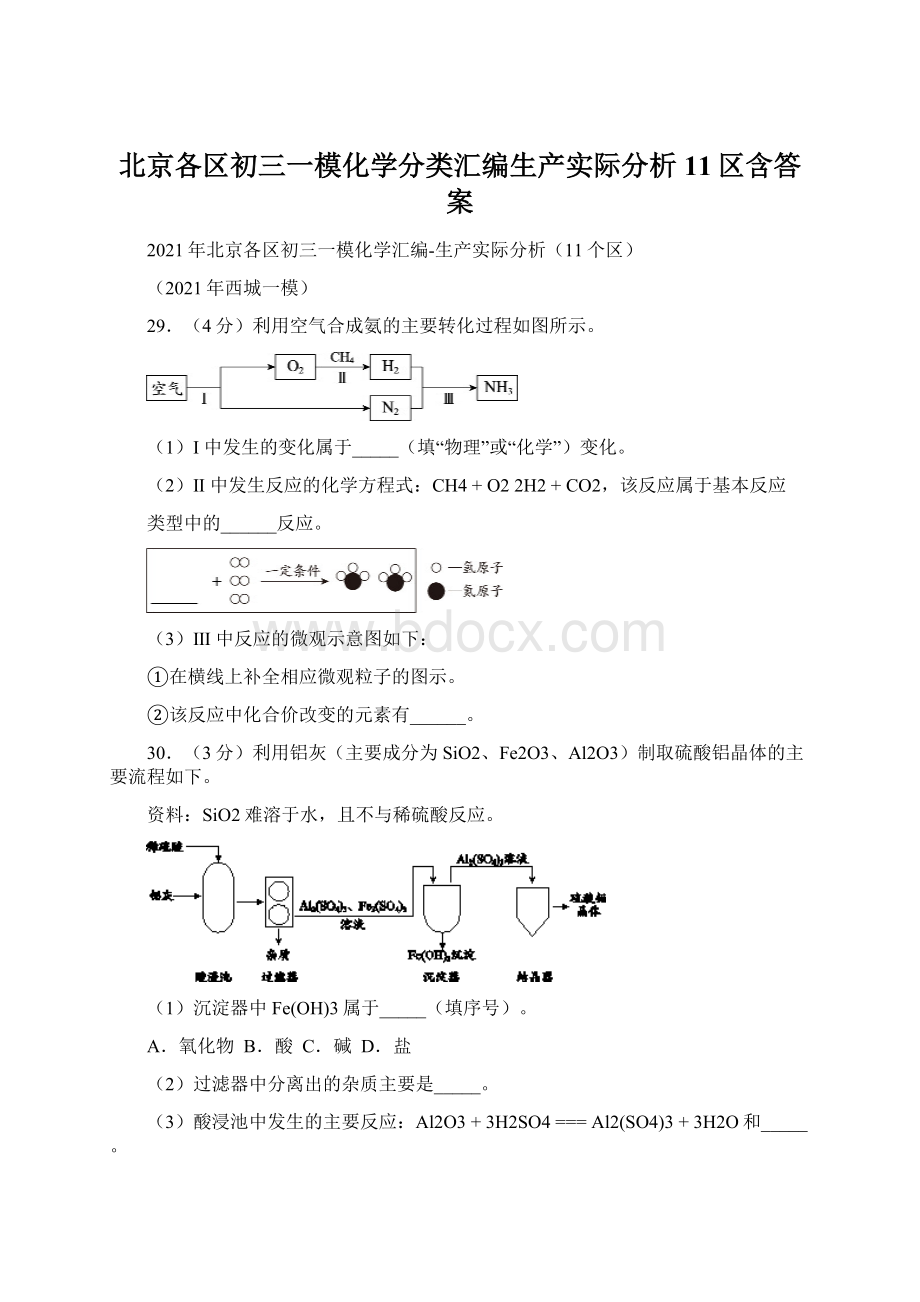
已知:
燃烧器中发生的反应为Mg+CO2=====MgO+CO
(1)燃烧器中,Mg与CO2反应后,镁元素的化合价(填“升高”或“降低”)。
(2)热气中一定含有的物质有。
31.(3分)工业上常以CH4为原料生产工业原料气H2,其部分工艺流程如下:
(1)高温下,转化炉中发生反应的化学方程式为。
(2)变换塔中,H2O变成H2发生的是(填“物理”或“化学”)变化。
(3)洗涤塔中,除去混合气中的CO2利用的CO2性质有(写出1条即可)。
32.(3分)过氧化钙(CaO2)与H2O反应会释放出O2,常用作鱼塘供氧剂。
制备CaO2的部分流程如下:
(1)I中,反应的化学方程式为。
(2)II中,H2O2溶液的溶质质量分数为3%,则100gH2O2溶液中,H2O2的质量为g。
(3)已知:
CaO2·
8H2O加热至130℃时开始分解,变为CaO2;
加热至315℃时,CaO2逐步分解为CaO。
III中,烘干时可选用的温度范围是(填序号)。
a.100~120℃b.150~200℃c.280~350℃
(2021年朝阳一模)
30.(3分)波尔多液是农业上常用的杀菌剂,生产波尔多液的流程如下:
(1)“煅烧”的化学方程式为CaCO3高温CaO+CO2↑,该反应属于基本反应类型中
的反应
(2)“混合”时不能用铁制容器,原因是(用化学方程式解释)。
(3)“混合”时需不断搅拌,目的是。
31.(4分)钛(Ti)被称为“航空金属”。
由钛铁矿(主要成分是钛酸亚铁,化学式为FeTiO3)制备钛的流程如下:
(1)钛酸亚铁中钛元素的化合价为。
(2)电解厂参加反应的物质为。
(3)制钛厂中,在氩气环境下发生置换反应的化学方程式为。
(4)合成厂中,参加反应的CO和H2的分子个数比为。
(2021年丰台一模)
30.(3分)利用工业废碱渣(主要成分为Na2CO3)可吸收烟气中的SO2,同时生产Na2SO3。
(1)SO2中S元素的化合价为_________。
(2)补全过程Ⅰ中发生主要反应的化学方程式:
Na2CO3+2SO2+H2O=====2NaHSO3+_______
(3)溶液X中一定含有的溶质是________。
31.(4分)工业制造高纯度氧化钙(CaO)的流程如下:
(1)反应器1中先加入一定量水。
气体从底部缓慢通入的原因是_______。
(2)反应器2中发生复分解反应的化学方程式为_______。
(3)过滤器中分离出的固体是_______。
(4)上述流程中可循环利用的物质是_______。
(2021年石景山一模)
硝酸钠(NaNO3)是一种重要的化工原料和农用肥料。
根据制取工艺,回答30和31题。
30.(2分)利用硝酸(HNO3)和Na2CO3制NaNO3的主要工艺流程如下。
(1)反应槽中反应的化学方程式为2HNO3+Na2CO3===2NaNO3+H2O+CO2↑,该反应属于基本反应类型中的______反应。
(2)将溶液pH调到6.5,加入的x是______。
A.盐酸B.氢氧化钠C.氢氧化钙
31.(3分)利用Na2CO3溶液吸收硝酸生产中排出的NO和NO2尾气制取NaNO3,可实现综合利用资源,减少环境污染,其主要工艺流程如下。
(1)吸收时,发生的反应有:
①Na2CO3+2NO2===NaNO3+NaNO2+CO2;
②NO+NO2+Na2CO3===2NaNO2+CO2。
反应①的物质中,属于氧化物是______;
反应②中,氮元素有______种不同的化合价。
(2)转化时,加入HNO3的作用是______。
(2021年门头沟一模)
31.(4分)2019年诺贝尔化学奖授予对锂离子电池研究作出贡献的三位科学家。
下图是从钴酸锂废极片[主要成分为钴酸锂(LiCoO2)]中回收得到Co2O3和Li2CO3的一种工艺流程。
(1)操作1中,粉碎废极片的目的是_______________;
(2)在实验室中完成操作2时,需要用到的玻璃仪器是____________(填一种即可);
(3)操作4中,在高温条件下,CoC2O4在空气中反应,生成Co2O3和二氧化碳,化学方程式为_________;
(4)操作5中,Li2CO3晶体用热水洗涤比用冷水洗涤损耗更少,说明Li2CO3的溶解度随温度升高而______(填“增大、不变或减小”)。
32.(2分)工业上用石灰石为原料制备纳米CaCO3的一种流程如下图所示。
SiO2不与盐酸反应
(1)设备Ⅰ中发生反应的化学方程式为_____________________。
(2)设备Ⅲ中参加反应的物质除水外,还有______________________。
(2021年顺义一模)
32.载人航天器中的水气整合系统如下图所示。
(1)CO2再利用反应器中装有特定催化剂,反应的化学方程式是____________。
(2)整个循环系统中未被利用的物质是__________。
33.丙酸钙[(C2H5COO)2Ca]可作食品防霉剂,国家标准规定了其最大使用量。
丙酸钙的工业生产过程如下图所示。
(1)石灰窑中的反应在高温下进行,生成两种氧化物,反应的化学方程式为______________。
(2)过筛的目的是除去未分解的石灰石等杂质,检验滤渣中含有石灰石所加的试剂是__________。
(3)制备丙酸钙时需要调节反应锅中的pH,调节操作中加入的物质可以是__________。
(4)已知反应锅中发生中和反应。
上述流程中,不涉及的基本反应类型是__________。
(2021年大兴一模)
31.以空气等为原料合成氨(NH3)、尿素[CO(NH2)2]R的简易生产流程如下图所示。
(1)
中发生的变化属于(填“物理变化”或“化学变化”)。
一定条件
(2)补全
中反应的化学方程式:
2NH3+CO2=====CO(NH2)2+。
32.氟化工产品生产过程中产生的副产品盐酸可制备氯化钙,其主要工艺流程如下图所示。
(1)化灰池中发生反应的基本反应类型为。
(2)中和锅中发生反应的化学方程式为。
(3)上述流程中,用于分离提纯的设备有______。
(2021年房山一模)
32.(3分)磷酸铁(FePO4)是制备磷酸铁锂电池的材料之一,用工业级硫酸亚铁(含有钛、镁、锰等杂质)制备磷酸铁的转化过程如下:
(1)步骤Ⅰ和Ⅲ都需要进行的操作是。
(2)步骤Ⅱ中发生的化学反应为:
2FeSO4+H2SO4+X=Fe2(SO4)3+2H2O,则X的化学式为。
(3)上述流程中产生的(NH4)2SO4属于化学肥料中的肥。
33.(3分)对工业湿法炼锌残留的铜镉渣(主要成分为Zn、Cu和Cd)进行处理,可
回收金属铜,其主要工艺流程如下:
(1)酸浸槽中搅拌的目的是。
(2)酸浸槽中发生的主要反应为:
Cd+2HCl=CdCl2+H2↑和。
(3)过滤器和干燥器中发生的是(填“物理”或“化学”)变化。
(2021年通州一模)
33.(2分)嫦娥五号带回的月球土壤中含有大量甲烷和钛铁矿(主要成分FeTiO3)。
科学家设想的有关人类利用月球土壤资源的流程图如下:
Ⅰ
Ⅱ
Ⅲ
(1)该流程中获得的金属单质有Ti和________。
(2)Ⅱ中发生的反应化学方程式为CO+3H2CH4+H2O,该反应前后化合价发生
改变的元素有C和______。
34.(4分)碳酸锂(Li2CO3)是制备锂电池的重要原料。
工业上以锂辉石精矿(主要成分为Li2O)为原料制取碳酸锂(注:
Li2CO3溶解度随温度升高而减小),其主要工艺流程如下图所示:
(1)酸浸槽中发生反应的化学方程式为________。
(2)反应器中搅拌的目的是_____。
(3)滤渣主要成分是Li2CO3、Na2CO3、Na2SO4。
洗涤时使用热水的作用是 。
(4)上述流程中,用于分离提纯的设备有洗涤槽和_______。
(2021年延庆一模)
30.(2分)海水中的资源丰富,可以制备金属镁,转化过程如下:
流程图涉及的含镁化合物中,镁元素的质量分数最大的是________。
(填化学式)
HCl能与Mg(OH)2发生了复分解反应,该反应的化学方程式为_________。
31.(3分)立德粉(ZnS·
BaSO4)是一种常用白色颜料,以重晶石(BaSO4)为原料生产立德粉的主要工艺流程如下:
BaS可溶于水,ZnS和BaSO4均难溶于水。
(1)原料进入回转炉之前先进行粉碎的目的。
(2)回转炉中,重晶石(BaSO4)与焦炭在高温下焙烧制得BaS,其中一个化学反应为BaSO4+2C
2CO2↑+BaS,这个反应中,化合价发生变化的元素有______。
(3)上述流程中,主要用于分离、提纯的设备有______、过滤器和洗涤槽。
2021年北京各区初三一模化学汇编-生产实际分析(11区)答案
29.(4分)
(1)物理
(2)置换(3)
N、H
30.(3分)
(1)C
(2)SiO2(3)Fe2O3+3H2SO4===Fe2(SO4)3+3H2O
30.(2分)
(1)升高
(2)CO
高温
31.(3分)
(1)CH4+H2O======CO+3H2
(2)化学
(3)能溶于水(或能与水反应)
32.(3分)
(1)CaCO3+2HCl====CaCl2+CO2↑+H2O
(2)3
(3)b
30.(3分)
(1)分解
(2)Fe+CuSO4=Cu+FeSO4
(3)使反应物充分接触,加快反应速率
31.(4分)
(1)+4
(2)NaCl和H2O
(3)2Mg+TiCl4Ar/800℃2MgCl2+Ti
(4)1:
2
30、
(1)+4
(2)CO2(3)Na2SO3
31、
(1)使反应物充分接触,充分反应
(2)CaCl2+(NH4)2CO3=====2NH4Cl+CaCO3↓
(3)CaCO3(4)CO2
30.
(1)复分解
(2)B
31.
(1)NO2CO2三
(2)把NaNO2转化为NaNO3
MnO2
32-A
(1)A2KMnO4△K2MnO4+MnO2+O2↑
(2)剧烈燃烧,火星四射,放出热量,生成黑色固体
31.(4分)
(1)增大反应物间接触面积,使反应更充分
(2)烧杯(或漏斗、玻璃棒)
(3)4CoC2O4+3O2=====2Co2O3+8CO2(4)减小
32.(2分)
(1)CaCO3+2HCl===CaCl2+H2O+CO2↑
(2)CO2、NH3、CaCl2
32.(2分)
(1)CO2+4H2催化剂CH4+2H2O
(2)CH4
33.(4分)
(1)CaCO3高温CaO+CO2↑
(2)稀盐酸(和澄清石灰水)
(3)C2H5COOH或Ca(OH)2
(4)置换反应
31.
(1)物理变化
(2)H2O
32.
(1)化合反应
(2)Ca(OH)2+2HCl====CaCl2+2H2O
(3)过滤器、蒸发浓缩锅
32.
(1)过滤
(2)H2O2
(3)氮
33.
(1)使反应物充分接触,反应更充分
(2)Zn+2HClZnCl2+H2↑
33.
(1)铁
△
(2)H
34.
(1)Li2O+H2SO4Li2SO4+H2O
(2)使液体充分接触,充分反应
(3)除去Na2CO3和Na2SO4
(4)沉锂池
30.(2分)
(1)Mg(OH)2
(2)Mg(OH)2+2HCl=MgCl2+2H2O
31.(3分)
(1)增大反应物的接触面积,使反应更充分
(2)C和S(碳和硫)
(3)浸出槽
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 北京 各区 初三 化学 分类 汇编 生产 实际 分析 11 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
 冶金资源与环境.ppt
冶金资源与环境.ppt
