 金属及其化合物提纲和练习题文档格式.docx
金属及其化合物提纲和练习题文档格式.docx
- 文档编号:19059559
- 上传时间:2023-01-03
- 格式:DOCX
- 页数:57
- 大小:706.69KB
金属及其化合物提纲和练习题文档格式.docx
《金属及其化合物提纲和练习题文档格式.docx》由会员分享,可在线阅读,更多相关《金属及其化合物提纲和练习题文档格式.docx(57页珍藏版)》请在冰豆网上搜索。
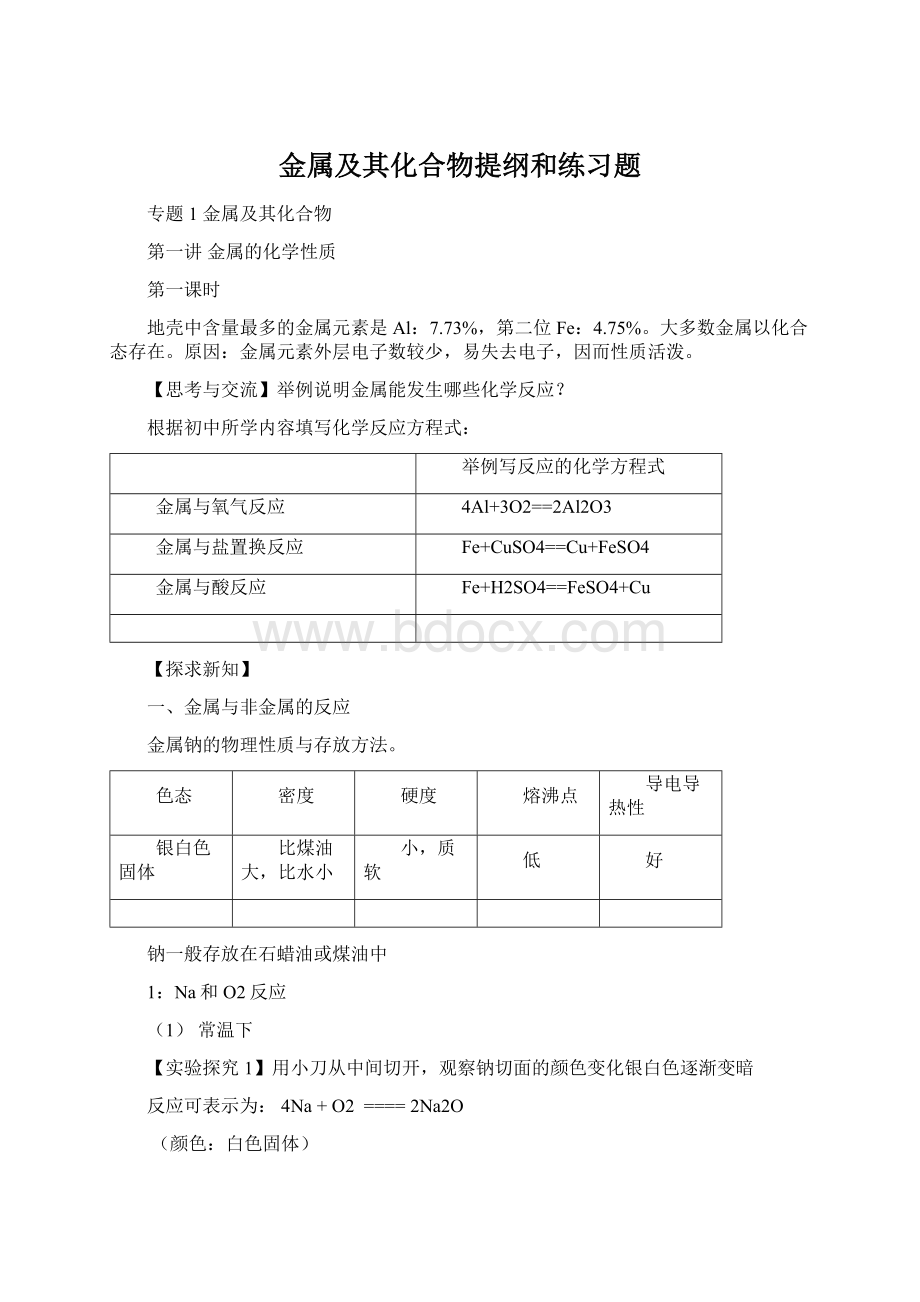
白色固体)
(2)钠的燃烧。
【实验探究2】用小刀切下绿豆粒大小的钠块,用滤纸吸干煤油后放入坩埚中,点燃酒精灯进行加热。
Δ
描述实验现象:
金属先熔化,在空气中燃烧,火焰呈黄色,生成淡黄色固体
2Na+O2Na2O2
淡黄色固体)
注意:
①用镊子夹取存放在煤油中的金属钠,②用滤纸吸干表面的煤油防止干扰观察现象,③未用完的钠块全部放回原试剂瓶中。
2、铝与氧气的反应
4Al+3O2点燃2Al2O3
【实验探究1】用坩埚钳钳住一块铝片在酒精灯上加热至熔化,轻轻晃动
实验现象逐渐熔化,失去光泽,但不滴落
铝的熔点为665℃氧化铝的熔点为2050℃,铝表面的致密氧化膜包在铝的外面,所以熔化了的液态铝不会落下。
【实验探究2】用坩埚钳钳住一块用砂纸打磨过的铝片在酒精灯上加热至熔化,轻轻晃动
实验现象:
熔化的铝仍不滴落
磨去氧化膜的铝片在空气中很快又形成一层新的氧化膜
【归纳小结】①金属的活动性越强,与氧气反应就越易进行(如钠露置空气中就氧化);
金属活动性越弱,与氧气发生反应时反应条件较高(如铁在空气中不能被点燃),俗语说“真金不怕火炼”就说明金在加热条件下不与氧气反应。
②金属和氧气反应一般生成普通氧化物,例MgOAl2O3CuO,但钠在氧气中燃烧生成Na2O2,铁在氧气中燃烧生成Fe3O4。
③金属表面的氧化物有的疏松,不能保存内层金属,如铁;
金属表面的氧化物有的致密,可以保存内层金属镁、铝。
巩固练习
1.金属钠是_______色固体,质地__________,将钠放在空气中一会儿,会发现金属钠的表面变暗,原因是(用化学方程式表示)___________________________;
将钠放在空气中燃烧,其反应的化学方程式是_____________________,生成物的颜色是___________色。
2.保存金属钠时,应放在( )
A、水中 B、煤油中 C、棕色瓶中 D、酒精中
3.以下说法错误的是( )
A、钠在常温下就容易被氧化B、钠受热后能够着火燃烧
C、钠在空气中缓慢氧化能自燃D、钠在氧气中燃烧更为激烈
4.关于Na2O与Na2O2的叙述正确的是( )
A、都是白色的固体B、都是碱性氧化物
C、都能和水反应形成强碱溶液D、都是强氧化剂
5.当钠着火时,应选用灭火的是( )
A、煤油 B、水 C、沙土 D、泡沫灭火器
6.下列物质放置在空气中,因发生氧化还原反应而变质的是( )
A、NaB、NaClC、NaOHD、Na2O2
7.2.3g纯净金属钠在干燥空气中被氧化后得到3.5g固体,由此可判断其氧化物是( )
A、只有Na2O B、只有Na2O2 C、Na2O和Na2O2 D、无法确定
8.钠离子的性质是( )
A、有强还原性 B、有弱氧化性 C、有碱性 D、比钠原子稳定
9.取一小块钠放在玻璃燃烧匙里加热,下列实验现象正确的是( )
①金属先熔化②在空气中燃烧火焰呈黄色③燃烧时火星四射④燃烧后生成淡黄色固体⑤燃烧后生成白色固体
A、①②③B、①②④C、①②⑤D、①③⑤
10.下列叙述正确的是( )
①Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
②Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成O2
③Na2O主要起氧化剂,Na2O2主要起还原剂
④Na2O2可作供氧剂,而Na2O不行
⑤Na2O2是强氧化剂,Na2O是一种碱性氧化物
A、都正确 B、②③④⑤ C、②③⑤ D、④⑤
11.将一小块金属钠久置于空气中,有下列现象:
①生成白色粉末;
②变暗;
③生成白色固体;
④发生潮解变为液体,这些现象的先后顺序是()
A.①②③④ B.④③②① C.②③④① D.①③④②
参考答案 1、银白 柔软 4Na+O2=2Na2O 2Na+O2=Na2O2 淡黄
2、B 3、C 4、C 5、C 6、AD 7、C 8、BD 9、B 10、D11、C
第二课时
二、金属和水的反应
1.钠与水反应
【实验探究】Na和烧杯里的水作用:
现象:
反应剧烈,钠浮在水面上,熔成小球,迅速游动,嘶嘶作响,溶液变红。
(2)现象分析
现象
原因
浮
密度比水小
熔
钠和水反应放热,使钠熔成闪亮的小球
游
钠和水反应生成气体,推动钠游动
响
钠和水反应放出热量使水局部蒸发为气体
红
钠和水反应生成了碱
化学反应方程式:
2Na+2H2O=2NaOH+H2↑离子方程式:
2Na+2H2O=2Na++OH-+H2↑
【思考讨论】
①金属钠着火,能否用水灭?
为什么?
应该如何处理?
(不能,因能和水反应。
应用细砂)
②为什么能将钠保存在煤油中?
能否保存在汽油或CCl4中?
(钠容易被氧气氧化而变质,必须将钠隔绝空气保存;
钠不与煤油发生化学反应;
钠的密度比煤油大,能够有效隔绝空气。
不能保存在汽油中,因汽油易挥发,使钠暴露在空气中,发生火灾。
不能保存在CCl4中因钠的密度小于CCl4的密度)
③将一小块金属钠投入CuSO4溶液中,可观察到什么现象?
写出发生的化学方程式。
(观察到现象:
反应剧烈,钠熔成小球,浮在水面上,迅速游动,嘶嘶作响,溶液中同时出现蓝色沉淀。
2Na+2H2O=2NaOH+H2↑,CuSO4+2NaOH=Cu(OH)2↓+Na2SO4)
2、铁和水反应
铁不能和冷水、热水反应但能和水蒸气反应
铁与水蒸气反应的实验装置见课本P50(引导学生从水蒸气的产生,水蒸气与铁粉反应,反应产物的检验设计装置。
还可设计成以下二种实验装置)
【实验探究】铁粉与水蒸气的反应:
3Fe+4H2O(g)==Fe3O4+4H2↑
点燃肥皂泡可听到爆鸣声
三、铝与盐酸、氢氧化钠溶液的反应
【实验探究】
(1)取2支小试管分别加入5mL盐酸和5mLNaOH溶液,再分别放入一小段铝片,观察现象。
(2)将点燃的木条分别放在两支试管口,观察现象。
铝既能与盐酸反应,又能与氢氧化钠溶液反应,都能产生一种可燃性气体H2
铝与盐酸反应的化学方程式:
2Al+6HCl=2AlCl3+3H2↑离子方程式:
2Al+6H+=2Al3++3H2↑
铝与氢氧化钠溶液反应的化学方程式:
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
离子方程式:
2Al+2OH-+2H2O=2AlO2-+3H2↑
1、在上述实验中,为什么铝片放入盐酸和NaOH溶液中,不立即产生气泡?
2、由上述实验还能得出哪种物质既能与盐酸反应,又能与NaOH溶液反应?
(1)、原因:
铝片表面上的Al2O3先和盐酸和NaOH溶液中,所以不立即产生气泡
(2)、物质名称:
Al2O3
1、在进行钠和水的反应实验中,有如下操作和实验现象,请根据钠的性质解释说明。
(1)刚用小刀切开的金属钠断面呈_______色,在空气中放置几分钟后发生的变化为______________。
(2)切下来的金属钠块要用滤纸擦净后方可放入水中实验,这是因为_______________。
(3)金属钠块必须用_______夹取,而不能用手拿取,理由是______________________。
(4)金属钠块投入水中后,钠很快熔成一个闪亮的小球并浮于水面上,这是因为_____。
(5)钠小球在水面上迅速游动,这是因为_____________________________________,反应容器的上方弥漫着“白色物”,它的主要成分是___________________________________。
(6)如果水中在未加钠之前已滴入酚酞试溶,反应后溶液由无色变为_______________色,理由是____________________________。
2、红热的铁能与水蒸气反应,有氢气生成,根据下图所示装置进行铁在高温下与水蒸气反应的实验,并用简单的方法收集,检验生成氢气。
请回答下列问题:
(1)写出铁在高温下与水蒸气反应的化学方程式______________________________。
(2)干燥管C内盛放的药品是_______或______。
干燥管的________(m或n)端与g导管相连接。
(3)在D处画出用简单方法用试管来收集氢气的装置图(所需其他仪器自己选择)。
(4)怎样用简单的方法检验收集到的气体是氢气,简述实验操作步骤和现象___________________。
3、将一小块Na投入足量的CuSO4溶液中,现象是( )
A、置换出金属铜 B、产生气体,置换出金属铜
C、生成蓝色沉淀 D、产生气体,生成蓝色沉淀
4、下列物质中不能与NaOH溶液反应的是( )
A.NaB.FeC.AlD.Cu
5、铝与氢氧化钠溶液反应的离子方程式正确的是( )
A、2Al+2Na++2OH-+2H2O=2NaAlO2+3H2↑B、Al+OH-+H2O=AlO2-+3H2↑
C、2Al+2OH-+2H2O=2AlO2-+3H2↑D、Al+2OH-+H2O=AlO2-+2H2↑
6、在实验室里做钠跟水反应的实验时,用到的仪器是( )
a.试管夹 b.镊子 c.小刀 d.冷凝管 e.滤纸 f.研钵 g.烧杯
h.坩埚 i.石棉网 j.玻璃片 k.药匙 l.燃烧匙
A.abdiB.ecfkC.fghlD.bcegj
7、往烧杯内注入煤油和水各100mL,静置后将一小块钠投入烧杯内。
(已知钠的密度介于煤油和水之间,且水和煤油互不相溶)发生的现象是
A、钠沉到液柱1/2处,钠块下部有许多气泡放出,附有气泡的钠块徐徐上升到液体表面,一会儿又沉到液柱1/2处,如此反复多次,最后消失
B、钠块一直沉到烧杯底部,并停留在杯底,放出气泡,最后消失
C、钠块浮在液柱表面上,很快熔成一个光亮的小球,小球四处浮动,最后消失
D、钠块沉到液柱1/2处,很快熔成一个闪亮的小球,小球在液柱1/2处沿水平方向迅速游来游去,最后消失
8、用铝箔包装0.1mol金属钠,用针扎一些小孔,放入水中,完全反应后,用排水取气法收集产生的气体,则收集到气体的为( )
A.O2和H2的混合气体 B.0.05molH2
C.大于0.05molH2 D.小于0.05molH2气体
9、等质量的钠、镁、铝分别与足量的盐酸反应,产生H2的质量由大到小排列顺序正确的是
A、Al、Mg、Na B、Mg、Al、Na C、Na、Mg、Al D、Na、Al、Mg
10、相同质量的两块铝,分别和足量的稀H2SO4和NaOH溶液反应,产生气体的物质的量之比是( )
A、2:
3 B、3:
2 C、2:
1 D、1:
1
11、将2.3g金属钠投入100g水中,反应结束后,溶液中溶质的质量分数计算式表示正确的是( )
A.2.3/100×
100%B.4/(100+2.3-0.1)×
100%
C.4/(100+2.3)×
100%D.4/(4+100-1.8)×
100%
12、将2.3g金属钠放入多少克水中,反应完全后,溶液中Na+与H2O分子的个数比为1:
50,最后溶液中水的质量为多少?
13、天平两边各放一个烧杯,烧杯分别盛放同体积同浓度的盐酸(足量),调节天平达到平衡。
将12g镁和12g铝分别放入两烧杯中,反应完毕后,哪一端还要放入多少克同种金属,反应完毕后天平才能平衡?
14、一块表面已部分被氧化成氧化钠的钠块质量为1.08g,投入到100g水中,完全反应后收集到0.02gH2。
求:
(1)未被氧化的金属钠的质量是多少?
(2)被氧化的金属钠的质量是多少?
参考答案:
1、
(1)银白 变暗 这是因为钠与氧气反应,在钠的表面生成了一薄层氧化物所致
(2)用滤纸吸干钠块表面煤油,防止钠与水反应放热,引起煤油燃烧
(3)镊子 手指表面有水份,能跟钠块反应生成强碱NaOH腐蚀皮肤
(4)钠的密度比水小,与水反应,放热,使钠熔化形成银白色小球
(5)钠与水反应放出氢气,推动钠球在水面上运动 钠与水反应放热使与钠球接触的水蒸发,在容器上方凝聚而形成白雾。
(6)使酚酞变红,钠与水反应生成NaOH。
2、
(1)3Fe+4H2O(g)=Fe3O4+4H2↑
(2)CaCl2碱石灰 n
(3)向下排空气法、导管口伸入试管底部
(4)用拇指堵住试管口,移近火焰,松开,能燃烧或发出爆鸣声,说明收集的是H2
3、B 4、BD 5、C 6、D 7、A 8、C 9、A 10、D11、B12、90g 13、Al0.4g14、0.46g0.46g
第三课时
物质的量在化学方程式计算中的运用
一、回忆以物质的量为中心的计算公式
二、理解方程式中化学计量数之比与物质的量之比的含义
我们知道:
物质是由原子、分子、离子等粒子构成的,物质之间的化学反应也是这些粒子按一定的数目关系进行的,比如在下面的那个反应中,Na和H2O以及产物NaOH、H2是按2:
2:
1的比例进行的,也就是说它们的分子数之比为:
2Na+2H2O==2NaOH+H2
化学计量数之比2221
扩大NA倍1.204×
10241.204×
10246.02×
1023
物质的量之比2mol2mol2mol1mol
质量之比4g32g36g
从上面一系列的比例中我们可以得出一些什么结论呢?
结论:
化学方程式中各物质的化学计量数之比,等于组成各物质的粒子数之比,因而也等于各物质的物质的量之比,还等于在相同条件下各气体的体积之比。
计算时同种物质各种量(物质的量、质量、体积)的单位要统一。
即上下单位要一致
三、物质的量在方程式中的运用
例题讲解
例1见课本P52页
例2实验室用60g含CaCO380%的大理石与足量12mol/l浓盐酸完全反应(杂质不参加反应)求:
①参加反应浓盐酸的体积。
②生成CO2的体积(标况下)。
分析思路:
把参加反应CaCO3转化为物质的量,再根据化学方程式中的化学计量数,求题目所求。
(注意解题格式)
解
CaCO3(S)+2HCl==CaCl2+H2O
+CO2
1mol2mol22.4L
0.48mol12mol/L×
V[HCl(aq)]V(CO2)
V[HCL(aq)]=0.08LVV(CO2)=10.752L
答:
参加反应浓盐酸体积为0.08L,生成CO2的体积在标况下10.75L。
例3.用8.7gMnO2与100g36.5﹪的浓盐酸反应,消耗盐酸的物质的量是多少?
产生Cl2在标况下的体积是多少?
未参加反应的HCl的质量是多少?
被氧化的HCl物质的量是多少?
根据化学方程式进行计算,当两种反应物的量均为已知时,首先须判断何者过量,然后根据不过量的物质来进行计算。
解:
△
MnO2+4HCl(浓)======MnCl2+Cl2↑+2H2O
1mol4mol22.4L
V(Cl2)
因为:
1mol×
0.1mol<4mol×
1mol
所以,反应物HCl过量,应根据MnO2的物质的量0.1mol计算:
消耗HCl为:
n1(HCl)=
剩余HCl为:
n2(HCl)=1mol-0.4mol=0.6mol
剩余HCl的质量为:
m(HCl)=n2(HCl)·
M(HCl)
=0.6mol×
36.5 g·
mol-1=21.9g
V(Cl2)=
被氧化的HCl物质的量:
因参加反应的盐酸一半被氧化所以n(被氧化HCl)=0.4mol/2=0.2mol
消耗HCl0.4mol,产生Cl22.24L,未参加反应的HCl为21.9g,被氧化的HCl物质的量是0.2mol。
1.在250mL0.1mol·
L-1的Ca(OH)2溶液中通入CO2,生成1g白色沉淀.则通入的CO2可能是()
A.0.44gB.0.04mol C.0.112L D.4.4g
2.将H2和CO在相同条件下按2∶1的体积比混合成AL混合气,当完全燃烧时,所需O2的体积为()
A.AL B.0.5AL C.1.5AL D.2AL
3.用CO还原1.0g某种赤铁矿石(主要成分为Fe2O3,杂质不参加反应)样品,生成的CO2跟足量的石灰水反应,得到1.36g沉淀.此赤铁矿石中Fe2O3的质量分数为()
A.72.5% B.44.8% C.25.6% D.80.0%
4.称取14g铁放入100mL,0.1mol·
L-1的CuSO4溶液中,反应后析出铜的质量为()
A.0.32g B.0.64g C.16g D.32g
5.把200gH2和O2混合气体,点燃爆炸后生成液态水,还剩余20g气体,则原混合气体中H2的质量分数为()
A.40% B.30% C.20% D.10%
6.用1L、1.0mol·
L-1NaOH溶液吸收0.8molCO2,所得溶液中CO32-和HCO3-的物质的量之比是()
A.3∶1 B.1∶3 C.3∶2 D.2∶3
7.在密闭容器中盛有H2、O2、Cl2的混合气体,通过电火花点燃,3种气体恰好完全反应,冷却至室温后所得溶液中溶质的质量分数为25.26%,则容器中原有H2、O2、Cl2的分子个数比是()
A.9∶4∶1 B.13∶6∶1C.10∶6∶1 D.8∶5∶2
8.下列说法正确的是()
A.5gO2与5gH2化合可生成10g水 B.8gO2与2gH2化合可生成10g水
C.2gO2与8gH2化合可得10g水 D.16gO2与2gH2化合可生成18g水
9.用AgNO3溶液和NaCl、MgCl2、AlCl3三种溶液分别反应时,若把同体积、同物质的量浓度的三种溶液中的Cl-全部沉淀下来,所需AgNO3溶液的体积比是___________;
若把同体积的三种溶液中的Cl-全部沉淀下来,所用AgNO3溶液体积相同,则此三种溶液中溶质的物质的量浓度之比为________。
生成沉淀的质量比为____________。
(1∶2∶36∶3∶21∶1∶1)
10.在含有35.8gNa2CO3和NaHCO3的溶液内,加入700mL1mol·
L-1的盐酸,反应完全后可以生成8.96LCO2(标准状况).
(1)其中物质是过量的.
(2)溶液中含有Na2CO3g.
11.将0.65g锌加到50mL1mol·
L-1盐酸中,计算:
(1)标准状况下,生成H2的体积。
(2)若反应完成后,溶液体积仍为50mL,这时溶液中的Zn2+和H+的物质的量浓度是多少?
12.取50.0mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51g白色沉淀,用过量稀硝酸处理后沉淀量减少到4.66g,并有气体放出。
试计算:
(1)原混合溶液中Na2CO3和Na2SO4的物质的量浓度;
(2)产生的气体在标准状况下的体积。
1、AB2、B3、A4、B5、CD6、B7、B8、D
9、1∶2∶36∶3∶21∶1∶110、
(1)HCl
(2)10.6g(3)7.84L
11:
Zn+2HCl======ZnCl2+H2↑
1mol2mol1mol22.4L
0.05×
1mol·
L-10.05L×
c(ZnCl2)V(H2)
经分析,HCl过量,应按不过量的Zn的物质的量来进行计算。
反应消耗HCl为:
n1(HCl)=
n2(HCl)=0.05L×
1 mol·
L-1-0.02 mol=0.03 mol
剩余HCl的浓度:
c(HCl)=
c(H+)=c(HCl)=0.6mol·
L-1
V(H2)=
c(ZnCl2)=
c(Zn2+)=c(ZnCl2)=0.2mol·
L-1
(1)标准状况下,生成H20.224 L。
(2)反应后溶液中Zn2+与H+的物质的量浓度分别为0.2mol·
L-1和0.6mol·
L-1。
12:
Na2CO3+BaCl2====BaCO3↓+2NaClNa2SO4+BaCl2====BaSO4↓+2NaCl
BaCO3+2HNO3====Ba(NO3)2+CO2↑+H2O
(1)n(Na2SO4)=n(BaSO4)=
=0.02mol
m(BaCO3)=14.51g-4.66g=9.85g
n(Na2CO3)=n(BaCO3)=
=0.05mol
c(Na2SO4)=
=0.40mol·
c(Na2CO3)=
=1.0mol·
(2)n(CO2)=n(Na2CO3)=0.05mol
V(CO2)=0.05mol×
22.4L·
mol-1=1.12L
第一节金属的化学性质
一、选择题(12*4=48分)
1.下列有关钠的物理性质的叙述中正确的是( )
①银白色金属②质软,可以用小刀切割 ③熔点低于100℃④密度比水小 ⑤热和电的良导体
A.①②④ B.①②③④ C.①③④ D.①②③④⑤
2.关于Na2O和Na2O2的叙述正确的是( )
A.都是白色的固体 B.都是碱性氧化物
C.都能和水反应形成强碱溶液 D.都是强氧化剂
3.下列说法正确的是( )
A.钠在溶液中可置换出铁 B.铁在溶液中可置换出铜
C.Fe不与H2O反应 D.Fe比Al活泼
4.下列关于金属的叙述中正确的是()
A.所有的金属都是固态的
B.金属具有导电性、导热性和延展性
C.活泼的金属、或较活泼的金属能与酸反应,但不能与碱反应
D.金属元素在自然界中都是以化合态存在的
5.通过你的观察和推理,判断下列实验室中对于少量Na的保存方法正确的是()
A.保存在水中B.密封,保存在广口瓶中
C.用铝箔包裹,密封在广口瓶中D.密封,保存在煤油中
6.从生活常识角度考虑,试推断钠元素在自然界中存在的主要形式是()
A.NaB.NaCl
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 金属 及其 化合物 提纲 练习题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
