 高中化学第二册wordWord文件下载.docx
高中化学第二册wordWord文件下载.docx
- 文档编号:18973403
- 上传时间:2023-01-02
- 格式:DOCX
- 页数:98
- 大小:464.08KB
高中化学第二册wordWord文件下载.docx
《高中化学第二册wordWord文件下载.docx》由会员分享,可在线阅读,更多相关《高中化学第二册wordWord文件下载.docx(98页珍藏版)》请在冰豆网上搜索。
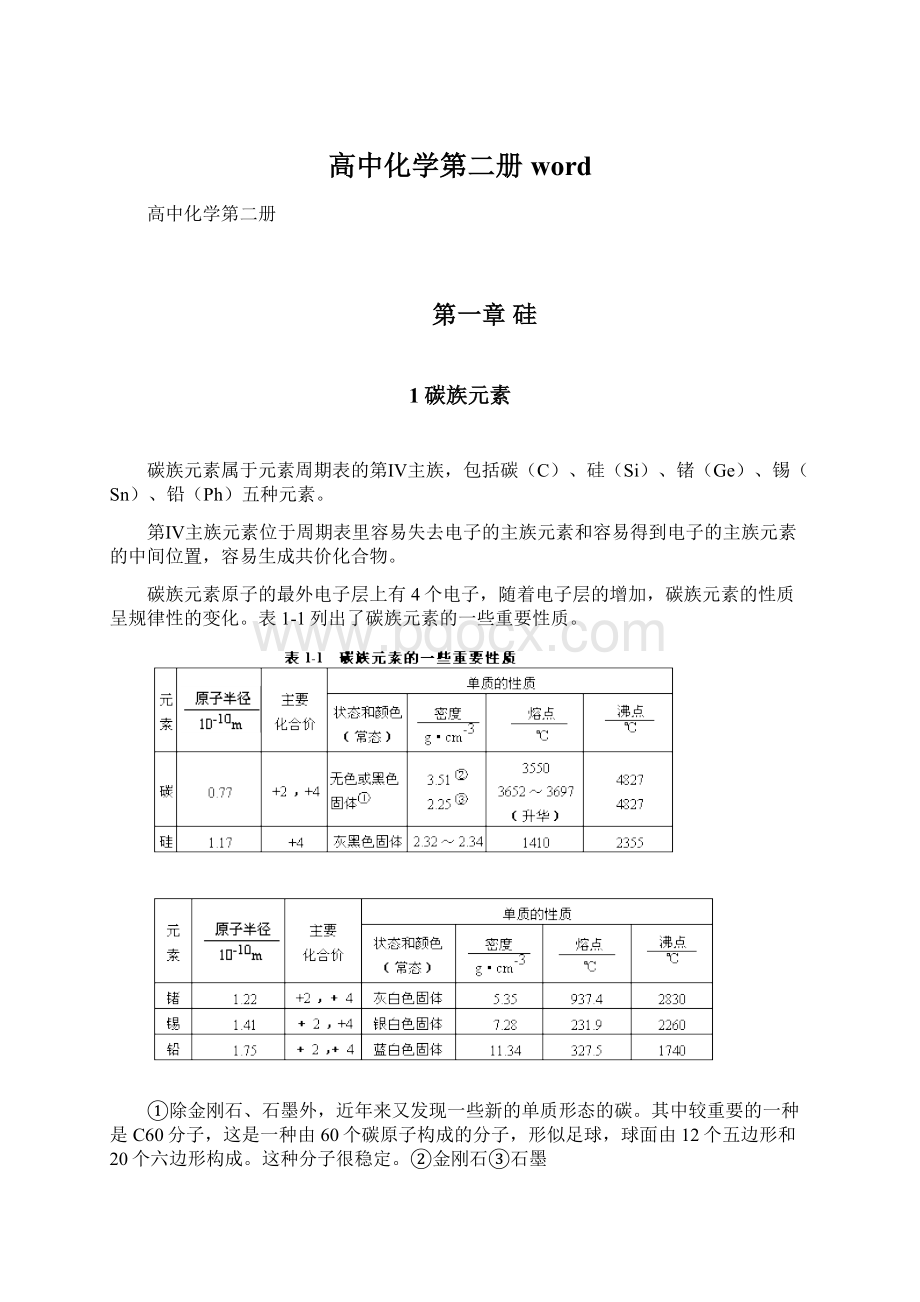
硅是良好的半导体材料,可用来制造半导体器件,如硅整流器、晶体管和集成电路等。
锗和硅相似,也是重要的半导体材料。
2.化学性质
硅是非金属元素,硅的许多化学性质和碳相似,它跟其它元素化合时形成共价键。
硅的化学性质不活泼。
在常温下,除氟气、氢氟酸和强碱溶液外,其它物质如氧气、氯气、硫酸和硝酸等都不跟硅起反应。
在加热条件下,硅能跟一些非金属起反应。
例如,把硅研细后加热,它就燃烧生成二氧化硅,同时放出大量的热。
Si+O2
SiO2
硅只有在高温下才能跟氢气起反应。
硅的氢化物常用间接的方法制得。
硅可以用来制造合金。
含硅4%的钢有导磁性,可以用来制造变压器的铁芯;
含硅15%左右的钢有耐酸性,可以用来制造耐酸设备。
工业上,硅是在电炉里用碳还原二氧化硅而制得的。
这样制得的硅是含少量杂质的粗硅。
粗硅提纯后,可制得作为半导体材料的高纯硅。
二、二氧化硅
二氧化硅(SiO2)是一种坚硬难熔的固体,它同其它矿物构成了多种岩石,广泛地分布在自然界里。
天然的二氧化硅分为晶体和无定形两大类。
石英的主要成分就是二氧化硅。
自然界透明的六方柱状石英晶体,就是我们常说的水晶。
硅藻土含有无定形二氧化硅,它是死去的硅藻[1]及其它微小生物的遗体经沉积胶结而成的多孔、质轻、松软的固体物质。
它的表面积很大,吸附能力较强,可作吸附剂和催化剂的载体②,以及保温材料等。
二氧化硅和二氧化碳在物理性质上有很大差别。
例如,二氧化硅的熔点高、硬度大;
而二氧化碳在通常状况下是气体,固体二氧化碳的熔点很低,等等。
二氧化硅和二氧化碳的这些差别是由它们的不同结构决定的。
我们已经知道固体二氧化碳是一种分子晶体。
分子间只有较小的分子间引力,所以,它的熔点很低。
但是二氧化硅却不是由单个的“SiO2”的分子所组成的分子晶体,而是一种原子晶体。
如图1-1③所示,1个Si原子跟4个O原子形成了4个共价键,这样,每1个Si原子周围结合4个O原子;
同时,每个O原子跟两个Si原子相结合。
实际上,二氧化硅晶体是由硅原子和氧原子按1∶2的比率所组成的立体网状的原子晶体,我们通常用“SiO2”的式子表示二氧化硅的组成。
在二氧化硅的晶体里,Si-O键的键长为1.62×
10-10m,键能为369kJ/mol。
由于二氧化硅晶体里Si—O键的键能很高,并形成了一种立体网状的原子晶体,所以,要使它熔融,也就是说要破坏二氧化硅的晶体,必须消耗较多的能量,因此,二氧化硅的熔点很高,硬度也很大。
2.化学性质
由于二氧化硅的Si—O键能很大,因而它的化学性质十分稳定,不能跟酸(除氢氟酸外)发生反应。
二氧化硅是一种酸性氧化物。
但是,二氧化硅不溶于水,它不能跟水起反应生成酸。
二氧化硅能跟碱性氧化物或强碱反应生成盐。
SiO2+CaO
CaSiO3
SiO2+2NaOH=Na2SiO3+H2O
玻璃中含有SiO2,因而它能够被碱溶液腐蚀。
实验室里盛放碱溶液的试剂瓶常用橡皮塞,而不用玻璃塞,就是为了防止玻璃受碱溶液腐蚀生成Na2SiO3,而使瓶口和塞子粘结在一起。
3.用途
二氧化硅的用途很广。
自然界里比较稀少的水晶可用以制造电子工业的重要部件、光学仪器和工艺品。
二氧化硅是制造光导纤维的重要原料。
一般较纯净的石英,可用来制造石英玻璃。
石英玻璃膨胀系数很小,相当于普通玻璃的1/18,能经受温度的剧变,耐酸性能好(除HF外),因此,石英玻璃常用来制造耐高温的化学仪器。
石英砂常用作玻璃原料和建筑材料。
三、硅酸硅酸盐
1.硅酸
虽然二氧化硅是酸性氧化物,但不能用二氧化硅跟水直接作用制得硅酸,而只能用相应的可溶性的硅酸盐跟酸作用来制硅酸。
硅酸钠(Na2SiO3)的水溶液跟盐酸起反应生成白色胶状沉淀。
这种白色胶状沉淀叫做原硅酸,通常用H4SiO4来表示它的组成。
原硅酸几乎不溶于水,是一种弱酸,很不稳定。
这种白色胶状物在空气里干燥,失去一部分水后,变成白色粉末。
这种物质是硅酸,通常用H2SiO3来表示它的组成(可以认为是H4SiO4=H2SiO3+H2O)。
硅酸不溶于水,也是一种弱酸,它的酸性比碳酸还弱。
2.硅酸盐
硅酸、原硅酸和由它们缩水结合而成的各种酸所对应的盐,统称硅酸盐,如硅酸钠(Na2SiO3)、镁橄榄石(Mg2SiO4)、高岭石[Al2(Si2O5)(OH)4]等都是硅酸盐。
硅酸盐种类很多,结构也很复杂,它是构成地壳岩石的最主要成分。
我们可以用二氧化硅和金属氧化物的形式表示硅酸盐的组成。
例如:
硅酸钠Na2SiO3(Na2O·
SiO2)
镁橄榄石Mg2SiO4(2MgO·
高岭石Al2(Si2O5)(OH)4(Al2O3·
2SiO2·
2H2O)
许多硅酸盐都是难溶于水的。
可溶性硅酸盐中,最常见的是Na2SiO3,它的水溶液俗名水玻璃。
水玻璃是无色粘稠的液体,是一种矿物胶,它既不能燃烧又不受腐蚀,在建筑工业上可用作粘合剂等。
木材、织物浸过水玻璃后,具有防腐性能,且不易着火。
水玻璃还可用作耐火材料。
粘土的成分也是硅酸盐。
花岗岩里的正长石(KAlSi3O8)长时间在二氧化碳和水的作用下,分解而生成粘土等物质。
粘土的种类很多,成分也很复杂(主要是高岭石),它是土壤里矿物质的主要部分。
常见的有高岭土①和一般粘土,前者含杂质较少,后者含杂质较多。
[1]①硅藻是单细胞的低等水生植物。
②
为了增加催化剂的有效面积,一般使催化剂附着于多孔的物体表面,这种多孔物体叫做载体。
③
图1-1是一个简化的平面示意图,实际上二氧化硅晶体是立体的网状结构。
①
高岭土又叫瓷土,主要由高岭石的微细晶体组成,因盛产于我国江西景德镇的高岭而得名。
3硅酸盐工业简述
以含硅物质为原料,经过加热制成硅酸盐产品的工业,如制造水泥、玻璃、陶瓷等产品的工业,叫做硅酸盐工业。
它在国民经济中占有重要的地位。
一、水泥
水泥是一种重要的建筑材料,主要以石灰石和粘土为原料。
生产时,把石灰石、粘土及其它辅助原料按一定比率混合,磨细成生料。
将生料装入水泥窑中烧至部分熔化,冷却后成为硬块,叫做熟料。
再加入适量的石膏(调节水泥硬化速度),磨成细粉,这就是制得的水泥。
这种水泥叫做普通硅酸盐水泥。
它的主要成分有:
硅酸三钙3CaO·
硅酸二钙2CaO·
铝酸三钙3CaO·
Al2O3
水泥实际上是上述主要成分的混合物,水泥的组成和结晶形态的不同直接影响到它的各种主要性能。
水泥具有水硬性。
水泥跟水拌和后,发生作用,生成不同的水合物,同时放出一定的热量。
生成的水合物逐步形成胶状物,并开始凝聚,最后,有些胶状物转变为晶体,使胶状物和晶体交错地结合起来,成为强度很大的固体。
这个过程叫做水泥的硬化。
水泥不论在空气中还是在水中都能硬化,所以,它不仅是一般的建筑材料,而且是水下工程必不可少的建筑材料。
为了改善水泥的性能,扩大水泥的使用范围,可在硅酸盐水泥熟料里,掺入适当比率的混合材料,制成各种水泥。
例如,矿渣硅酸盐水泥就是在硅酸盐水泥熟料里加入一定量的高炉矿渣(主要成分是CaSiO3);
沸石岩水泥就是在水泥熟料里掺入一定量的沸石岩。
水泥、沙子和水的混合物叫做水泥沙浆,在建筑上用作粘合剂,能把砖、石等物粘结起来。
水泥、沙子和碎石按一定比率的混合物硬化后,叫做混凝土,常用来建造桥梁、厂房等巨大建筑物。
水泥的热膨胀系数几乎跟铁一样,所以用混凝土建造建筑物常用钢筋作结构,使建筑物更加坚固,这叫做钢筋混凝土。
二、玻璃
制造普通玻璃的主要原料是纯碱(Na2CO3)、石灰石(CaCO3)和石英(SiO2)。
有些特种玻璃原料中还包含氧化铅(PbO)和硼砂(Na2B4O7·
10H2O)。
生产玻璃时,把原料粉碎,按适当比率混合以后,放入玻璃熔炉里,加强热。
原料熔融后发生了比较复杂的物理、化学变化,其中主要的反应是二氧化硅跟碳酸钠和碳酸钙起反应生成硅酸盐和二氧化碳:
Na2CO3+SiO2
Na2SiO3+CO2↑
CaCO3+SiO2
CaSiO3+CO2↑
在原料里,石英的用量较多,所以,普通玻璃是Na2SiO3、CaSiO3和SiO2熔化在一起所得到的物质。
这种物质不是晶体,称作玻璃态物质,它没有一定的熔点,而是在某一温度范围内逐渐软化。
在软化状态时,玻璃可以制成任何形状的制品。
玻璃的种类很多,除上述普通玻璃外,还有硼酸盐玻璃,它的膨胀系数小,能够耐骤冷、骤热,化学稳定性好,能耐酸、碱的腐蚀,可用于制造化学仪器。
铅玻璃折光率强,常用于制作光学仪器等。
制造有色玻璃,一般是在原料里加入某些金属氧化物,金属氧化物均匀地分散到玻璃态的物质里,使玻璃呈现出特征颜色。
例如,加氧化钴(CO2O3)呈蓝色,加氧化亚铜(Cu2O)呈红色,等等。
把普通玻璃放入电炉里加热,使它软化,然后急速冷却,得到钢化玻璃。
钢化玻璃的机械强度比普通玻璃大4~6倍,不易破碎。
破碎时碎块没有尖锐的棱角,不易伤人,可用来制造汽车或火车的车窗等。
4内容提要
一、碳族元素
碳族元素属于元素周期表的第Ⅳ主族,包括碳、硅、锗、锡、铅五种元素。
碳族元素的最外电子层都有4个电子。
碳族元素位于元素周期表里容易失去电子的主族元素和容易得到电子的主族元素的中间位置。
碳族元素除+4价外,还有+2价。
二、硅及其重要化合物
1.硅
硅的原子序数为14,原子结构示意图为硅原子有4个价电子,能够形成4个共价键。
硅的晶体结构跟金刚石的结构相似,也是一种原子晶体。
硅和锗是良好的半导体。
硅的化学性质不活泼,在常温下,除氟气、氢氟酸和强碱溶液外,其它物质如氧气、氯气、硫酸和硝酸等都不跟硅起反应。
但在加热条件下,硅能跟氧气起反应。
2.二氧化硅
二氧化硅的晶体是由硅原子和氧原子组成的原子晶体,可用“SiO2”来表示它的组成。
二氧化硅不溶于水,是一种酸性氧化物,能跟碱性氧化物或碱起反应生成盐。
3.硅酸和硅酸盐
硅酸有原硅酸(H4SiO4)、硅酸(H2SiO3)等。
它们都是弱酸,它们的酸性比碳酸还要弱。
可用硅酸钠跟盐酸起反应制得硅酸。
硅酸、原硅酸以及由它们缩水而成的各种酸所对应的盐,统称硅酸盐。
如硅酸钠(Na2SiO3)、高岭石[Al2(Si2O5)(OH)4]等。
可溶性硅酸盐中,最常见的是硅酸钠,其水溶液俗名水玻璃。
4.硅酸盐工业
用石灰石和粘土作主要原料可制造水泥。
用纯碱、石灰石和石英作原料可制造普通玻璃。
5单元小结
硅及其重要化合物的性质与碳及其重要化合物的性质既有相似之处又有不同的地方,两者还有密切的联系,这可以用图1-1概括。
6教材分析
本章内容由两部分组成。
第一部分包括第一、二节,主要是运用所学的物质结构和元素周期律等理论,讨论碳族元素的通性和性质的递变规律,然后分别介绍单质硅、二氧化硅、硅酸和硅酸盐的性质等知识。
第二部分包括第三节,主要是简要地介绍了水泥、玻璃等硅酸盐工业知识。
本章安排在物质结构、元素周期律等理论和卤族、碱金属、氧族、氮族之后。
通过本章教学,可以进一步发挥理论对学习元素及其化合物知识的指导作用,也有利于复习巩固学生所学的理论知识,发展学生智力,培养自学能力。
碳族是中学化学学习的最后一个非金属元素族。
在元素周期表中,碳族处在从活泼金属向活泼非金属过渡的中间位置。
碳族包括两种非金属、两种金属、一种介于金属和非金属之间的元素锗(有人称锗为半金属)。
碳族元素从非金属性向金属性变化的规律相当典型,这对复习巩固元素周期律和物质结构理论有重要作用。
硅是重要的半导体材料,硅及其化合物在电子工业和冶金工业上有广泛的用途,而硅酸盐工业在国民经济中占有重要地位。
SiO2具有酸性氧化物的共性,能与碱、碱性氧化物起反应;
SiO2又有其特性,如它不能直接与水化合生成硅酸,一般要在高温条件下才能与碱性氧化物发生反应等。
学习这些知识有助于扩大学生对非金属和酸性氧化物的认识。
由于硅酸盐工业的生产原理较复杂,教材只简单介绍了生产玻璃的原料和化学反应原理,对水泥则只讲了原料、成分及简单的生产过程和水泥的硬化。
本章重点:
硅及其化合物的性质。
第二章镁
铝
在已发现的一百多种元素里,大约有五分之四是金属元素。
金属有不同的分类方法。
在冶金工业上,人们常把金属分为黑色金属(包括铁、铬、锰)和有色金属(铁、铬、锰以外的金属)两大类。
人们也常按照密度大小来把金属分类,把密度小于4.5g/cm3的叫做轻金属(如钾、钠、钙、镁、铝等);
把密度大于4.5g/cm3的叫做重金属(如铜、镍、锡、铅等)。
此外,还可把金属分为常见金属(如铁、铝等)和稀有金属(如钴、铪、铌、钼等)。
这一章主要学习两种重要的轻金属镁和铝。
7金属的物理性质
金属有许多共同性质,像有金属光泽、不透明、容易导电、导热、有延展性等。
怎样解释金属的这些共同性质呢?
金属(除汞外)在常温下一般都是晶体。
用X射线进行研究发现,在晶体中,金属原子好像硬球,一层一层地紧密堆积着。
金属原子的价电子比较少,容易失去价电子变成金属离子。
这些释出的价电子在整个晶体里可以自由地运动,这些电子叫做自由电子。
金属离子跟自由电子之间存在着较强的作用,因而使许多金属离子相互结合在一起形成晶体。
在通常情况下,金属里自由电子的运动是没有一定方向的。
但在外加电场的条件下,自由电子在金属里就会发生走向运动,因而形成电流。
这就是金属容易导电的原因。
金属的导热性也跟自由电子的运动有关。
自由电子在运动时经常跟金属离子相碰撞,从而引起两者能量的交换。
当金属某一部分受热时,在那个区域里的自由电子的能量增加,运动速率也随之加快,于是,通过碰撞,自由电子就能把能量传给其他金属离子。
金属就是借着自由电子的运动把能量从温度高的部分传到温度低的部分,从而使整块金属达到同样的温度。
金属的延展性也可以从金属的结构特点加以说明。
当金属受外力作用时,各层之间就发生了相对的滑动(图2-2),但是由于金属离子跟自由电子之间的较强作用仍然存在,因此金属虽然发生了形变,但不致断裂,所以金属一般地说有不同程度的延展性。
8镁和铝的性质
镁和铝都是第三周期的金属元素,它们原子的价电子数都比较少,因而性质有类似的地方。
但是由于结构不同,所以它们的性质又有许多差异。
为了便于比较,我们把镁和铝的性质并列介绍。
一、物理性质
表2-1表示了镁和铝的原子和单质的一些性质。
从表2-1可以知道,镁和铝都是密度较小、熔点较低、硬度较小的银白色金属。
但镁和铝比较,铝的硬度比镁的稍大,熔点和沸点都比镁的高。
纯铝的导电性很好,在电力工业上它可以代替部分铜作导线和电缆。
铝有很大的延展性,能够抽成细丝,也能压成薄片成为铝箔,铝箔可以用来包装胶卷、糖果等。
铝粉跟某些油料混合,可以制银白色防锈油漆。
铝的更重要的用途是可以跟许多元素形成合金。
所谓合金就是两种或两种以上的金属(或金属跟非金属)熔合而成的具有金属特性的物质。
合金比它的成分金属具有许多良好的物理的、化学的或机械的等方面的性能,一般地说,合金的熔点比它的各成分金属的熔点都低。
例如,铝硅合金(含Si质量分数为13.5%)的熔点为564℃,比纯铝或硅的熔点低,而且它在凝固时收缩率又很小。
因而,这种合金适合铸造。
又如,硬铝(含Cu4%、Mg0.5%、Mn0.5%、Si0.7%)(均为质量分数)的强度和硬度都比纯铝大,几乎相当于钢材,且密度较小。
铝合金的种类很多,它们在汽车、船舶、飞机等制造业上以及在日常生活里的用途很广。
镁的主要用途也是制造各种轻合金。
例如,镁跟铝、铜、锡、锰、钛、铍等金属元素形成的多种合金(约含镁质量分数为80%),密度只有1.8g/cm3左右,但硬度和强度都较大。
因此,镁合金也是汽车、飞机制造业的重要材料。
二、化学性质
镁或铝原子的最外层分别有2个或3个电子,它们都容易失去最外层电子成为阳离子。
Mg-2e→Mg2+
Al-3e→Al3+
镁和铝是比较活泼的金属,能跟非金属、酸等起反应。
1.跟非金属的反应
在常温下,镁和铝在空气里都能跟氧气起反应,生成一层致密而坚固的氧化物薄膜,从而使金属失去光泽。
但是,这层氧化物薄膜能够阻止金属的继续氧化,所以镁和铝都有抗腐蚀的性能。
镁在空气里点燃可以燃烧,放出大量的热并发出耀眼的白光。
我们利用镁的这种性质来制造照明弹等。
2Mg+O2
2MgO+热量
铝跟氧气起反应没有镁那样容易,可是把铝粉或铝箔放在氧气里加热,铝也能燃烧,放出大量的热,同时发出耀眼的白光。
但是,在空气里,只是在高温下,铝才能发生这样剧烈的变化。
4Al+3O2
2Al2O3+热量
镁、铝除能跟氧气起反应外,还能跟其他非金属如硫、卤素等起反应。
2.跟酸的反应
镁和铝都能跟稀盐酸或稀硫酸起反应生成氢气。
在常温下,铝在浓硝酸里表面被钝化,生成坚固的氧化膜,能阻止反应继续进行,因此,可以用铝制的容器来贮运浓硝酸。
3.跟碱的反应
镁不能跟碱起反应,但铝能跟强碱溶液起反应,生成氢气和偏铝酸盐。
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
4.跟某些氧化物的反应
镁不仅能跟空气中的氧气起反应,而且能够跟二氧化碳起反应,夺取其中的氧,析出游离态的碳。
[实验2-1]
如图2-3所示,点燃镁条,放入盛有二氧化碳的集气瓶里,镁条剧烈燃烧,生成氧化镁,析出的碳附着在集气瓶内壁上。
反应的化学方程式如下:
2Mg+CO2
2MgO+C
铝在一定条件下能跟氧化铁发生氧化还原反应。
[实验2-2]
用两张圆形滤纸分别折叠成漏斗状,套在一起使四周都有四层。
把内层的纸漏斗取出,在底部剪一个孔,用水润湿,再跟另一纸漏斗套在一起,架在铁圈上(如图2-4),下面放置盛沙的蒸发皿。
把5g炒干的氧化铁粉末和5g铝粉混合均匀,放在纸漏斗中,上面加少量氯酸钾并在混合物中间插一根镁条,用小木条点燃镁条,观察发生的现象。
从实验我们看到,镁条剧烈燃烧,放出一定的热量,使氧化铁粉末和铝粉在较高的温度下发生了剧烈的反应,放出大量的热,发出耀眼的光芒。
我们还可以看到纸漏斗下部被烧穿,有熔融物落入沙中。
冷却后除去外层熔渣,仔细观察,可以发现落下的是铁珠。
这个反应叫铝热反应。
在反应中放出大量的热,可达很高的温度,生成了氧化铝和液态铁。
2Al+Fe2O3=2Fe+Al2O3+热量
通常把铝粉和氧化铁的混合物叫铝热剂。
铝热反应原理可以应用在生产上,例如焊接钢轨等。
往铝热剂里加入一定量的铁合金和铁钉屑,把这种混合物放到特制的坩埚里,点燃后,立即发生剧烈的复杂的化学反应①,产生了高温的钢水和熔渣。
随即把高温钢水浇入扣在两根钢轨缝上的沙型中,这样可以把两根钢轨焊接起来(图2-5)。
这种焊接不用电源,而且焊接的速度快,设备简易,适合在野外作业。
用这种焊接方法可以把比较短的钢轨(12.5~25m)焊接成较长的钢轨(约1000m),这在建设铁道的无缝线路上有着重要的意义。
此外,在工业上,也用铝热剂的焊接法焊接大截面的钢材部件。
不仅用铝粉和氧化铁粉可以做铝热剂,用某些金属氧化物(如V2O5、Cr2O3、MnO2等)代替氧化铁也可以做铝热剂。
当铝粉跟某些金属氧化物反应时,产生足够的热量,使被还原的金属在较高的温度下,呈熔融状态并跟形成的熔渣分离开来,从而获得较纯的金属。
在工业上常用这种方法冶炼难熔的金属,如钒、铬、锰等。
除发生铝热反应外,还有炼钢和造渣等反应。
9镁和铝的重要化合物
镁和铝在自然界的分布都很广。
铝是地壳里存在最多的金属元素,约占地壳总质量的7.7%。
镁的储量也很丰富,约占地壳总质量的2.0%。
由于它们都是较活泼的金属,所以都以化合态存在于自然界中。
含镁的主要矿物有光卤石、白云石、菱镁矿、硫酸镁、滑石和石棉等。
此外,海水中也含有大量的镁盐。
含铝的主要矿物有长石、云母、铝土矿、明矾石等。
一、镁的重要化合物
1.氧化镁(MgO)
镁在空气里燃烧可以生成氧化镁。
工业上通常由煅烧菱镁矿(主要成分是MgCO3)来制取氧化镁:
MgCO3
MgO+CO2↑
氧化镁是密度很小的白色粉末,它的熔点高达2800℃,是优良的耐火材料,常用来制造耐火砖、耐火管和坩埚等。
氧化镁是一种碱性氧化物,可以跟水缓慢地反应生成氢氧化镁:
MgO+H2O=Mg(OH)2
2.氯化镁(MgCl2)
从光卤石(KCl·
MgCl2·
6H2O)溶液里把KCl提出以后,把溶液浓缩,就得到六水合氯化镁(MgCl2·
6H2O)晶体。
氯化镁也存在于海水里,它是制取食盐的副产品。
在制盐剩下的苦卤里加入熟石灰,或直接把海水引入水渠中加入熟石灰,氢氧化镁就沉淀析出。
MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓
然后用盐酸溶解氢氧化镁,再将溶液浓缩,就得到氯化镁晶体。
氯化镁是一种无色、苦味、易溶的晶体,极易吸收空气中的水分而潮解,粗制食盐在潮湿的空气中容易吸湿变潮,就是由于里面含有少量氯化镁杂质的缘故。
氯化镁是制取镁的重要原料,工业上采用通电分解熔融的氯化镁的方法制取镁。
二、铝的重要化合物
1.氧化铝(Al2O3)
自然界存在的铝的矿物主要有铝土矿。
铝土矿又称矾土,它是由一水合氧化铝(Al2O3·
H2O)、三水合氧化铝(Al2O3·
3H2O)以及少量氧化铁和石英等杂质组成的。
铝土矿可用来提取纯氧化铝。
氧化铝是一种白色难熔的物质,工业上,主要是以氧化铝为原料,采用通电分解的方法制得铝的。
氧化铝也是一种比较好的耐火材料,它可以用来制造耐火坩埚、耐火管和耐高温的实验仪器等。
刚玉是天然产的无色氧化铝晶体。
刚玉的硬度很大,仅次于金刚石。
因此,它常被用来制成砂轮、研磨纸或研磨石等,用以加工光学仪器和某些金属制品。
通常所说的蓝宝石和红宝石是混有少量不同氧化物杂质的刚玉。
它们可以用做精密仪器和手表的轴承。
氧化铝是典型的两性氧化物,
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 第二 word
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
