 高中化学钠元素及其化合物讲义1Word下载.docx
高中化学钠元素及其化合物讲义1Word下载.docx
- 文档编号:18893460
- 上传时间:2023-01-02
- 格式:DOCX
- 页数:13
- 大小:90.96KB
高中化学钠元素及其化合物讲义1Word下载.docx
《高中化学钠元素及其化合物讲义1Word下载.docx》由会员分享,可在线阅读,更多相关《高中化学钠元素及其化合物讲义1Word下载.docx(13页珍藏版)》请在冰豆网上搜索。
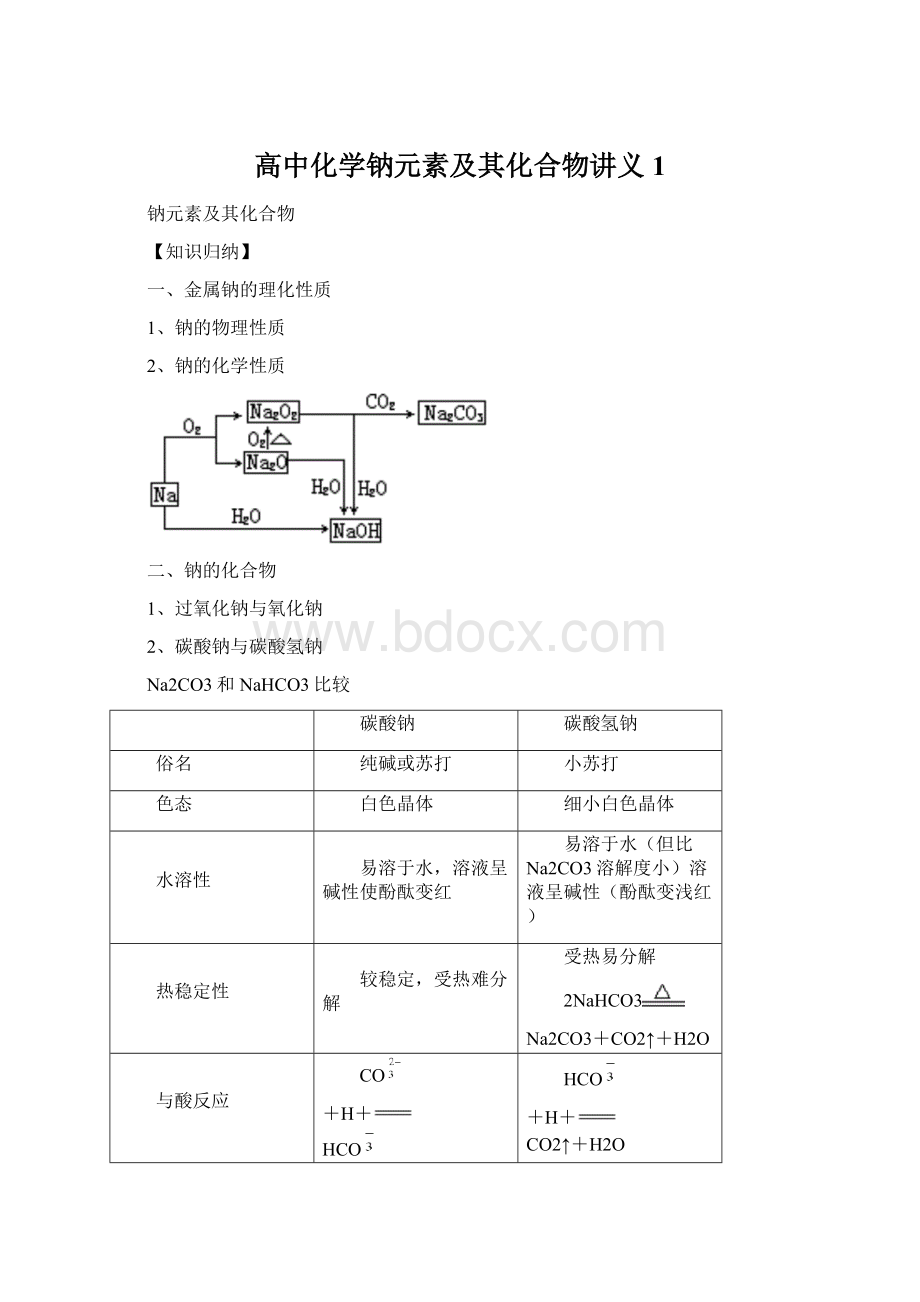
相同条件下放出CO2的速度NaHCO3比Na2CO3快
与碱反应
Na2CO3+Ca(OH)2
CaCO3↓+2NaOH
反应实质:
与金属阳离子的复分解反应
NaHCO3+NaOH
Na2CO3+H2O
+OH-
H2O+CO
与H2O和CO2的反应
Na2CO3+CO2+H2O
+H2O+CO2
不反应
与盐反应
CaCl2+Na2CO3
CaCO3↓+2NaCl
Ca2++CO
CaCO3↓
主要用途
玻璃、造纸、制皂、洗涤
发酵、医药、灭火器
转化关系
典型例题
1.一小块金属钠长时间置于空气中,可能有下列现象,这些现象出现的先后顺序是( )
①变成白色粉末 ②变暗 ③变成白色固体 ④变成液体
A.①②③④ B.②③④①
C.②③①④D.③②④①
解析:
钠在空气中发生如下变化:
Na→Na2O→NaOH→Na2CO3·
10H2O→Na2CO3。
反应现象为:
钠由银白色变暗,之后变成白色固体(NaOH),白色固体潮解变成液体,与空气中的CO2、H2O结合形成白色晶体(Na2CO3·
10H2O),最后晶体风化,变成白色粉末(Na2CO3)。
答案:
B
2.在烧杯中加入水和苯(苯的密度为0.88g/cm3,与水互不相溶,且不与钠反应)各50mL,将一小粒金属钠(密度为0.97g/cm3)投入烧杯中,观察到的现象可能为( )
A.钠在水层中反应并四处游动
B.钠停留在苯层中不发生反应
C.钠在苯的液面上反应并四处游动
D.钠在苯与水的界面处反应并可能上浮下沉
苯与水互不相溶,且钠的密度介于苯和水之间;
加入钠后,钠处在苯与水的中间。
由于钠能与水反应,生成氢气,氢气附着在钠的周围,浮力增大,钠上浮进入苯层,氢气放出后,浮力减小,钠又回到水层,这样上浮下沉至反应完全。
D
3.在一定条件下,将钠与氧气反应的生成物1.5g溶于水,所得溶液恰好能被80ml浓度为0.50mol·
L-1的HCl溶液中和,则该生成物的成分是()
A.Na2OB.Na2O2C.Na2ONa2O2D.Na2O2NaO2
3、C
4.向紫色石蕊试液中加入过量Na2O2粉末振荡,可观察到的现象是()
A.溶液仍为紫色B.最终溶液褪色,而无其它现象
C.溶液最终变蓝色D.溶液中有气泡产生,溶液最终变为无色
5.设阿伏加德罗常数的值为NA,下列说法正确的是()
A.1mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA
B.1molNa2O2与足量CO2反应时,转移2NA个电子
C.1mol·
L-1的NaOH溶液中含Na+数目为NA
D.1molNa2O2中含有的阴离子数目为2NA
6.(双选)过氧化钠可做为氧气的来源,常温常压下为二氧化碳与过氧化钠反应,若固体质量增加了28克,反应中有关质量的物理量正确的是()
A.二氧化碳44克,氧气16克
B.二氧化碳88克,氧气32克
C.碳酸钠106克,氧气16克
D.碳酸钠106克,氧气32克
4、D5、A6、AB
7.除去括号内的杂质,所选用的试剂或方法不正确的是()
A.Na2CO3溶液(NaHCO3),选用适量的NaOH溶液
B.NaHCO3溶液(Na2CO3),应通入过量的CO2气体
C.Na2O2粉末(Na2O),将混合物在氧气中加热
D.Na2CO3溶液(Na2SO4),加入适量Ba(OH)2溶液,过滤
8.将过量CO2通入NaOH溶液中反应,然后将得到的溶液蒸干并灼烧最后剩余固体成分为()
A.Na2CO3B.Na2CO3和NaOHC.NaHCO3D.NaHCO3和Na2CO3
A
巩固训练
1.2.3g纯净的金属钠在干燥的空气中被氧化后得到3.5g固体,由此判断其产物是( )
A.只有Na2OB.只有Na2O2
C.Na2O和Na2O2D.无法确定
若2.3g钠全部生成Na2O,质量为3.1g;
若2.3g钠全部生成Na2O2,质量为3.9g,因为3.1g<
3.5g<
3.9g,故氧化产物应为Na2O和Na2O2的混合物。
C
2.将金属钠分别投入下列物质的稀水溶液中,能生成白色沉淀的是( )
A.HClB.K2SO4
C.MgCl2D.CuCl2
在考虑钠与碱、盐水溶液反应的问题时,注意钠与水反应的同时,还要考虑生成的NaOH与溶液中溶质的反应。
钠与四种溶液反应都生成氢气;
CuCl2溶液中会有蓝色沉淀生成,只有氯化镁溶液中可生成白色沉淀。
3.下列关于钠的性质叙述中,不正确的是( )
A.切下一小块钠,投入水中,钠熔成小球,说明钠与水反应有热量放出
B.从钠能与水反应可推知钠也能与盐酸反应
C.钠在空气中燃烧生成氧化钠
D.切开一块钠,呈银白色,很快变暗,说明钠常温下能与氧气反应
钠在空气中燃烧时发生反应:
2Na+O2
Na2O2,故C选项错误。
4.[双选题]关于Na2O2与CO2、H2O反应的叙述正确的是( )
A.Na2O2与CO2反应中,Na2O2只作还原剂,CO2作氧化剂
B.Na2O2与H2O反应中,Na2O2既作氧化剂又作还原剂
C.Na2O2与CO2反应中,1molNa2O2转移2mol电子
D.Na2O2与水反应中,1molNa2O2转移1mol电子
Na2O2与CO2、H2O反应中,既作氧化剂又作还原剂,且1molNa2O2反应均转移1mol电子。
故选B、D。
BD
5.1mol过氧化钠与2mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是( )
A.Na2CO3 B.Na2O2 Na2CO3
C.NaOH Na2CO3D.Na2O2 NaOH Na2CO3
由题意可知,首先发生反应:
Na2CO3+H2O+CO2↑,生成H2O和CO2各1mol;
然后H2O和CO2与Na2O2反应:
2Na2O2+2H2O===4NaOH+O2↑,2Na2O2+2CO2===2Na2CO3+O2,CO2和H2O完全反应需消耗2molNa2O2,但题中只有1molNa2O2,应优先考虑与CO2的反应:
1molNa2O2先与1molCO2反应,生成1molNa2CO3和0.5molO2。
最后残留的固体是Na2CO3。
6.下列叙述中正确的是( )
A.向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液,又有CaCO3沉淀生成
B.向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1∶2
C.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同
D.向Na2CO3饱和溶液中通入CO2,有NaHCO3结晶析出
A项,CaCO3+CO2+H2O===Ca(HCO3)2,产物与NaHCO3不反应。
B项,发生反应:
+H+===HCO
,不生成CO2。
C项,等质量的NaHCO3和Na2CO3分别与足量盐酸反应时,NaHCO3产生的CO2多。
D项,向饱和Na2CO3溶液中通入CO2时发生反应:
Na2CO3+CO2+H2O===2NaHCO3↓,反应中消耗H2O,且生成的NaHCO3溶解度小、质量多,故NaHCO3会结晶析出。
7.[双选题]有两个无标签的试剂瓶,分别装有Na2CO3和NaHCO3固体,有四位同学为鉴别它们采用以下不同方法,其中可行的是( )
A.分别将它们配制成溶液,再加入澄清石灰水
B.分别将它们配制成溶液,再加入NaOH溶液
C.分别将它们配制成溶液,再加入CaCl2溶液
D.分别加热,再用石灰水检验是否有CO2产生
A项中发生的反应分别为:
Na2CO3+Ca(OH)2===CaCO3↓+2NaOH,2NaHCO3+Ca(OH)2===CaCO3↓+Na2CO3+2H2O,两者现象相同(产生白色沉淀);
B项中只发生反应:
NaHCO3+NaOH===Na2CO3+H2O,但无明显现象;
C项Na2CO3与CaCl2发生反应:
Na2CO3+CaCl2===CaCO3↓+2NaCl,产生白色沉淀,NaHCO3与CaCl2不反应,可以鉴别;
D项将固体物质分别加热后,只发生反应:
Na2CO3+H2O+CO2↑,产生的CO2能使澄清石灰水变浑浊。
CD
8.下列对于过氧化钠的叙述中,正确的是( )
A.过氧化钠能与酸反应生成盐和水,所以过氧化钠是碱性氧化物
B.过氧化钠能与水反应,所以过氧化钠可以作很多气体的干燥剂
C.过氧化钠与水反应时,过氧化钠是氧化剂,水是还原剂
D.过氧化钠与二氧化碳反应时,过氧化钠既是氧化剂又是还原剂
A项:
产物中还有O2生成,故不是碱性氧化物,B项,Na2O2与H2O反应产生O2,故不能作干燥剂,Na2O2与水、CO2的反应中,Na2O2既是氧化剂又是还原剂。
D项正确。
9.用光洁的铂丝蘸取某无色溶液在无色火焰上灼烧,直接观察时看到火焰呈黄色,下列判断正确的是( )
A.只含Na+
B.一定含Na+,可能含有K+
C.既含有Na+,又含有K+
D.可能含有Na+,可能还含有K+
钠的焰色是黄色,K的焰色是紫色,观察K的焰色时需要透过蓝色钴玻璃,以滤去黄色光的干扰,该实验中没有通过蓝色钴玻璃观察说明一定含Na+,不能确定是否含K+。
10.将一小块钠投入到FeCl3溶液中,此时观察到的现象是__________________________________________________________,有关的化学方程式是__________________________________________________________。
钠与盐溶液反应分两个过程,一是钠与水反应,二是NaOH与盐的反应。
钠浮于液面上,熔成闪亮的小球,四处游动,发出嘶嘶的响声,溶液中有红褐色沉淀析出 2Na+2H2O===2NaOH+H2↑,3NaOH+FeCl3===Fe(OH)3↓+3NaCl或2FeCl3+3H2O+6Na===2Fe(OH)3↓+3H2↑+6NaCl
11.(10分)下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。
填写下列空白:
(1)写出化学式:
A______________,B______________,D______________。
(2)以上反应中属于氧化还原反应的有______________(填序号)。
(3)写出反应⑤的离子方程式:
____________________________________。
写出反应⑥的化学方程式:
___________________________________。
由题给条件知A为单质钠,再由图示关系可以看出,B是A与O2在点燃条件下生成且焰色反应为黄色,故B为Na2O2,C为NaOH,D为Na2CO3,E为NaHCO3。
(1)Na Na2O2 Na2CO3
(2)①②③④
(3)OH-+CO2===HCO
12.A、B、C、D、F五种物质的焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃性气体。
而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变浑浊。
D和A可反应生成C,F和H也可反应生成C和另一种无色无味气体。
请回答下列问题:
(1)写出A、C、F的化学式
A________;
C________;
F________。
(2)写出F和H反应的化学方程式____________________________________。
(3)写出下列反应的离子方程式:
①D+盐酸_________________________________;
②B+水___________________________________。
由焰色反应为黄色,且A、B、C、D均与盐酸反应生成E,知E为NaCl,B还生成一种可燃性气体知B为Na,C、D还生成气体H使澄清石灰水变浑浊,知C、D为Na2CO3或NaHCO3,F和H(CO2)反应生成C和另一种气体,则F为Na2O2、C为Na2CO3,因而D为NaHCO3,D和A反应可生成Na2CO3,则A为NaOH。
(1)NaOH Na2CO3 Na2O2
(2)2Na2O2+2CO2===2Na2CO3+O2
(3)①HCO
+H+===H2O+CO2↑
②2Na+2H2O===2Na++2OH-+H2↑
提升训练
1.①纯净的碳酸钠ag;
②碳酸钠与碳酸氢钠的混合物ag,两者相比下列各种情况的描述正确的是( )
A.分别和盐酸完全反应时,混合物的耗酸量大
B.分别和盐酸完全反应时,纯净的碳酸钠放出的CO2多
C.分别溶于水,再加入足量澄清石灰水,混合物得到的沉淀质量大
D.分别配成等体积溶液,混合物溶液中的Na+的物质的量浓度大
同质量的Na2CO3比NaHCO3耗酸量要多,但是产生的CO2要少,故A、B项均错误;
同质量的两组物质,混合物含的碳元素较多,故最终转化成CaCO3沉淀的质量就大,C项正确;
同质量的Na2CO3比NaHCO3所含Na+物质的量大,故配成等体积溶液后纯净的碳酸钠溶液中的Na+物质的量浓度大,故D项错误。
2.把2.3gNa投入到97.7g水中,所得溶液中溶质的质量分数为()
A.2.3%B.4%C.大于4%D.小于4%
3.将金属钠投入下列溶液中,既有气体又有沉淀析出的是()
A.BaCl2B.(NH4)2SO4C.Fe2(SO4)3D.NH4HSO4
2、C3、C
4.为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1g样品加热,其质量变为w2g,则该样品的纯度(质量分数)是( )
A.
B.
C.
D.
依据NaHCO3受热分解的化学方程式,结合反应前后固体质量差可列式求解:
Na2CO3+H2O↑+CO2↑ Δm
2×
84 106 18 44 62
m(NaHCO3) (w1-w2)g
m(NaHCO3)=
g,
m(Na2CO3)=w1-m(NaHCO3)=
g。
5.“绿色化学实验”进课堂,某化学教师为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验。
实验操作:
钠与氯气反应的装置可作如图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。
先给钠预热,到钠熔融成小球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。
以下叙述错误的是
A.反应生成的大量白烟是氯化钠晶体
B.浸有NaOH溶液的棉球用于吸收未反应的氯气,以免污染空气
C.用淀粉碘化钾溶液滴在管外的棉球,可以判断氯气是否被完全吸收
D.钠着火燃烧产生苍白色火焰
6.等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气(常温)中充分反应,则
下列说法正确的是()
A.第一块钠失去电子多
B.两块钠失去电子一样多
C.第二块钠的反应产物质量最大
D.两块钠的反应产物质量一样大
答案:
5、D6、B
7.1mol过氧化钠与2mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体是()
A.Na2CO3B.Na2O2、Na2CO3
C.NaOH、Na2CO3D.Na2O2、NaOH、Na2CO3
A
8.CO与H2的混合气体3g在足量氧气中燃烧后,在150℃时将混合气体通过足量的Na2O2后,Na2O2增重的质量为()
A.1.5gB.3gC.6gD.无法计算
9.将O2、CH4、Na2O2放入密闭容器中,在150℃条件下电火花引发恰好完全反应后,容器中的压强为零。
原O2、CH4、Na2O2物质的量之比为()
A.1∶2∶6B.2∶1∶6C.1∶2∶8D.2∶1∶4
10.将一定质量的钠、氧化钠、过氧化钠的混合物与足量的水反应,得到0.36g混合气体,通过放电完全反应,则混合物中钠、氧化钠、过氧化钠的质量比可能为()
A.23∶62∶7B.92∶93∶156C.23∶124∶78D.46∶93∶78
11.取ag某物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体增加的质量大于ag。
下列物质中满足以上结果的是:
( )
①H2②CO③C6H12O6④C2H5OH⑤HCOOCH3⑥C12H22O11
A.①②③④⑤⑥B.①②③⑤C.③④⑤⑥D.④⑥
12.在一定条件下,使CO和O2的混合气体26g充分反应,所得混合物在常温下跟足量的Na2O2固体反应,结果固体增重14g,则原混合气体中O2和CO的质量比可能是( )。
A.9∶4B.1∶1
C.7∶6D.6∶7
13.某溶液中含有HCO
、CO
、SO
、Na+、NO
五种离子。
若向其中加入Na2O2粉末充分反应后(溶液体积变化忽略不计),溶液中离子浓度保持不变的是( )
A.NO
B.CO
、NO
C.SO
D.CO
、Na+
14.下列叙述中正确的是()
A.向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液,又有CaCO3沉淀生成
B.向Na2CO3溶液中加入含等物质的量的HCl的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1∶2
D.向Na2CO3饱和溶液中通入足量CO2,有NaHCO3结晶析出
15.(10分)某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图所示。
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是________(填装置序号)。
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式:
________________________________________________________________________;
与实验Ⅲ相比,实验Ⅳ的优点是__________(填选项序号)。
A.Ⅳ比Ⅲ复杂
B.Ⅳ比Ⅲ安全
C.Ⅳ比Ⅲ操作简便
D.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是________(填化学式)。
(1)Na2CO3、NaHCO3均能与盐酸反应生成使澄清石灰水变浑浊的CO2气体,但等质量的Na2CO3与NaHCO3跟过量盐酸反应时,NaHCO3与盐酸反应更剧烈且产生气体的量多,故实验Ⅰ不能鉴别Na2CO3与NaHCO3,而实验Ⅱ可以。
(2)NaHCO3受热易分解:
Na2CO3+CO2↑+H2O,Na2CO3受热不分解,可用加热方法鉴别,对比实验Ⅲ,实验Ⅳ可以同时进行两个对比实验,现象明显。
(3)将NaHCO3置于小试管B,Na2CO3置于大试管A,加热时D中澄清石灰水不变浑浊,C中变浑浊,说明Na2CO3比NaHCO3稳定。
(1)Ⅱ
(2)2NaHCO3
Na2CO3+CO2↑+H2O D (3)NaHCO3
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 元素 及其 化合物 讲义
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
