 高中化学专题:电化学计算.doc
高中化学专题:电化学计算.doc
- 文档编号:1870691
- 上传时间:2022-10-24
- 格式:DOC
- 页数:5
- 大小:108.40KB
高中化学专题:电化学计算.doc
《高中化学专题:电化学计算.doc》由会员分享,可在线阅读,更多相关《高中化学专题:电化学计算.doc(5页珍藏版)》请在冰豆网上搜索。
电化学计算
一.选择题(共1小题)
1.用铂作电极电解1000mL0.1mol/LAgNO3溶液,通电一段时间后关闭电源,测得溶液的质量减少了13.4g.下列有关叙述正确的是(NA代表阿伏加德罗常数的值)( )
A.电解过程中流经外电路的电子数目为0.1NA
B.在标准状况下,两极共产生3.92L气体
C.电解后溶液的pH为2(假设溶液体积不变)
D.加入13.8gAg2CO3可将溶液彻底复原
二.解答题(共3小题)
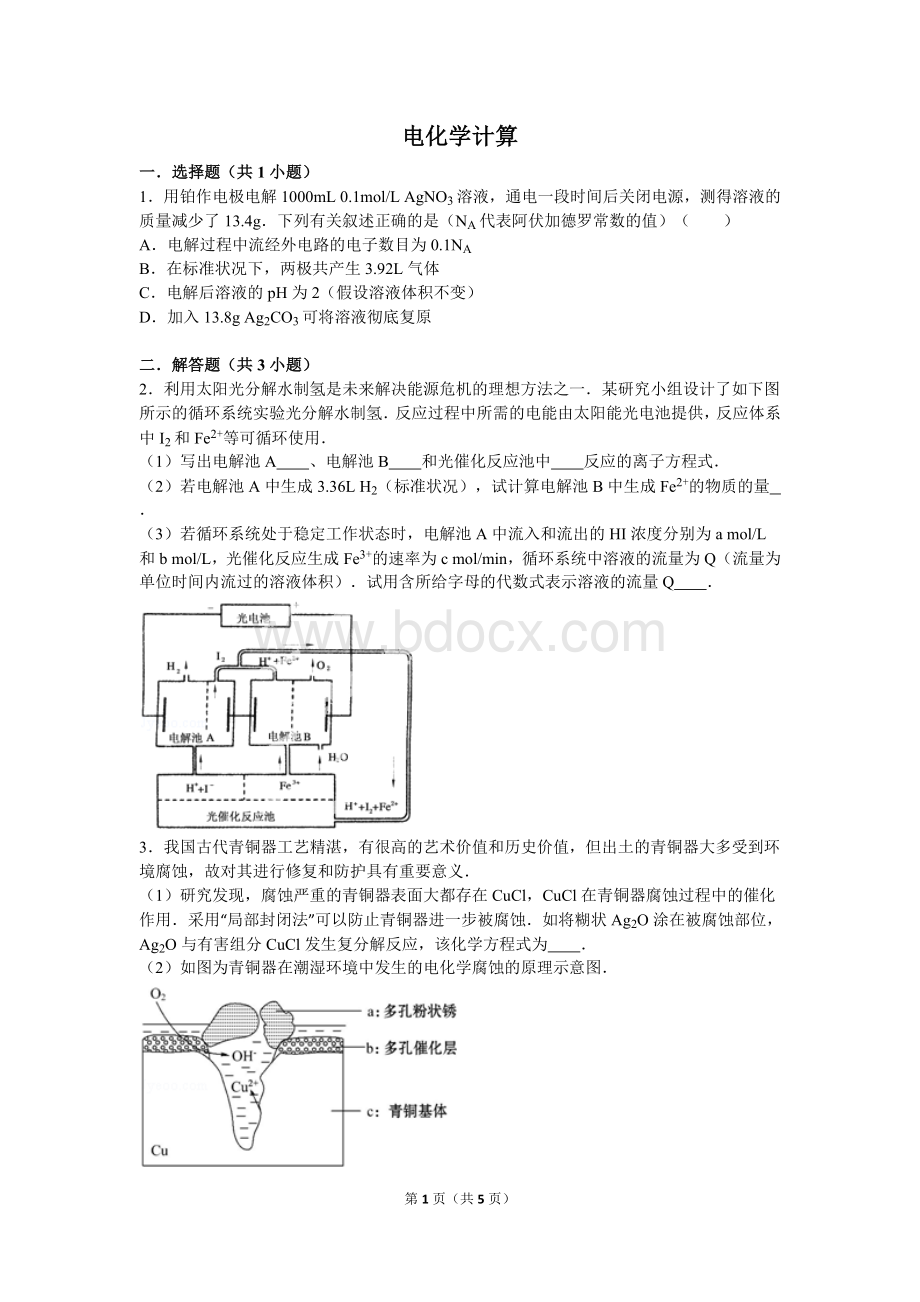
2.利用太阳光分解水制氢是未来解决能源危机的理想方法之一.某研究小组设计了如下图所示的循环系统实验光分解水制氢.反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe2+等可循环使用.
(1)写出电解池A 、电解池B 和光催化反应池中 反应的离子方程式.
(2)若电解池A中生成3.36LH2(标准状况),试计算电解池B中生成Fe2+的物质的量 .
(3)若循环系统处于稳定工作状态时,电解池A中流入和流出的HI浓度分别为amol/L和bmol/L,光催化反应生成Fe3+的速率为cmol/min,循环系统中溶液的流量为Q(流量为单位时间内流过的溶液体积).试用含所给字母的代数式表示溶液的流量Q .
3.我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义.
(1)研究发现,腐蚀严重的青铜器表面大都存在CuCl,CuCl在青铜器腐蚀过程中的催化作用.采用“局部封闭法”可以防止青铜器进一步被腐蚀.如将糊状Ag2O涂在被腐蚀部位,Ag2O与有害组分CuCl发生复分解反应,该化学方程式为 .
(2)如图为青铜器在潮湿环境中发生的电化学腐蚀的原理示意图.
①腐蚀过程中,负极是 (填图中字母“a”或“b”或“c”);
②环境中的Cl﹣扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈
Cu2(OH)3Cl,其离子方程式为 ;
③若生成4.29gCu2(OH)3Cl(M=214.5g•mol﹣1),则理论上耗氧体积为 L(标准状况).
(3)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(如图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生.
0~t1时,原电池的负极是Al片,此时,正极的电极反应式是 ,溶液中的H+向 极移动.t1时,原电池中电子流动方向发生改变,其原因是 .
4.甲醇是一种重要的化工原料和新型燃料.如图1是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.
(1)甲中负极的电极反应式为 .
(2)乙中A极析出的气体在标准状况下的体积为 .
(3)丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2,则图中②线表示的是 的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要 mL5.0mol•L﹣1NaOH溶液.
电化学计算
参考答案与试题解析
一.选择题(共1小题)
1.【解答】解:
A.用石墨作电极电解1000mL0.1mol/LAgNO3溶液的阴极反应首先是Ag++e﹣=Ag,假设所有的银离子0.1mol全部放电,转移电子的物质的量为0.1mol,则析出金属银的质量为:
0.1mol×108g/mol=10.8g,此时阳极放电的电极反应为:
4OH﹣=O2↑+H2O+4e﹣,转移0.1mol电子时生成的氧气的质量是:
0.025mol×32g/mol=0.8g,所以溶液质量减少总量为10.8g+0.8g=11.6g<13.4g,接下来阴极放电的是氢离子,阳极仍是氢氧根放电,相当于此阶段电解水,还要电解掉水的质量为13.4g﹣11.6g=1.8g,电解这些水转移电子的物质的量为0.2mol,所以整个过程转移电子的总量为0.3mol,个数为0.3NA,故A错误;
B.阳极放电的电极反应为:
4OH﹣=O2↑+H2O+4e﹣,当转移0.3mol电子时,产生的氧气物质的量为0.075mol,即1.68L,阴极上产生氢气,2H++2e﹣=H2↑,当转移0.2mol电子时,产生的氢气物质的量为0.1mol,即2.24L,所以在标准状况下,两极共产生3.92L气体,故B正确;
C.电解过程中溶液中的氢离子减少了0.2mol,而氢氧根总共减少了0.3mol,所以最后溶液中c(H+)=0.1mol/1L=0.1mol/l,其pH=1,故C错误;
D.溶液相当于减少了氧化银和水,只加入Ag2CO3不能将溶液彻底复原,故D错误;
故选:
B.
二.解答题(共3小题)
2.【解答】解:
(1)由图可知,电解池A中,电解HI生成氢气与I2,电解池中总反应的离子方程式为:
2H++2I﹣H2↑+I2,
电解池B中为电解铁盐溶液,生成Fe2+、O2、H+,电解池中总反应的离子方程式为:
4Fe3++2H2O4Fe2++O2↑+4H+,
光催化反应池中为Fe2+、I2、H+,生成Fe3+、I﹣、H+,光催化反应池中总反应的离子方程式为:
2Fe2++I22Fe3++2I﹣,
故答案为:
2H++2I﹣H2↑+I2;4Fe3++2H2O4Fe2++O2↑+4H+;2Fe2++I22Fe3++2I﹣;
(2)若电解池A中生成3.36LH2(标准状况),氢气的物质的量==0.15mol,转移电子物质的量=0.15mol×2=0.3mol,根据电子转移守恒,电解池B中生成Fe2+的物质的量为=0.3mol,
故答案为:
0.3mol;
(3)若电解池A中流入和流出的HI浓度分别为amol/L和bmol/L,则单位时间内消耗的HI的物质的量为(a﹣b)×Qmol/L,根据反应方程式得失电子守恒,光催化反应池中单位时间内生成Fe3+的物质的量为cmol/min,则有(a﹣b)×Qmol/L=cmol/min,故答案为:
Q=.
3.【解答】解:
(1)Ag2O与有害组分CuCl发生复分解反应,则二者相互交换成分生成另外的两种化合物,反应方程式为Ag2O+2CuCl=2AgCl+Cu2O,
故答案为:
Ag2O+2CuCl=2AgCl+Cu2O;
(2)①根据图知,氧气得电子生成氢氧根离子、Cu失电子生成铜离子,发生吸氧腐蚀,则Cu作负极,即c是负极,故答案为:
c;
②Cl﹣扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,负极上生成铜离子、正极上生成氢氧根离子,所以该离子反应为氯离子、铜离子和氢氧根离子反应生成Cu2(OH)3Cl沉淀,离子方程式为2Cu2++3OH﹣+Cl﹣=Cu2(OH)3Cl↓,
故答案为:
2Cu2++3OH﹣+Cl﹣=Cu2(OH)3Cl↓;
③n[Cu2(OH)3Cl]==0.02mol,根据转移电子得n(O2)==0.02mol,V(O2)=0.02mol×22.4L/mol=0.448L,
故答案为:
0.448;
(3)0~t1时,原电池的负极是Al片,溶液中产生红棕色气体是二氧化氮,故正极反应方程式为:
2H++NO3﹣+e﹣=NO2↑+H2O,此时溶液中的氢离子移向正极,一段时间后,由于Al与浓硝酸发生钝化,导致原电池中Al作正极,Cu作负极,
故答案为:
2H++e﹣+NO3﹣=NO2↑+H2O;正;铝在浓硝酸中发生钝化,表面生成了氧化膜阻止了Al的进一步反应.
4.【解答】解:
(1)甲醇燃料电池是原电池反应,甲醇在负极失电子发生氧化反应,电极反应为:
CH3OH﹣6e﹣+8OH﹣=CO32﹣+6H2O,
故答案为:
CH3OH﹣6e﹣+8OH﹣=CO32﹣+6H2O;
(2)工作一段时间后,断开K,此时A、B两极上产生的气体体积相同,分析电极反应,B为阴极,溶液中铜离子析出,氢离子得到电子生成氢气,设生成气体物质的量为X,溶液中铜离子物质的量为0.1mol,电极反应为:
Cu2++2e﹣=Cu,
0.1mol0.2mol
2H++2e﹣=H2↑,
2xx
A电极为阳极,溶液中的氢氧根离子失电子生成氧气,电极反应为:
4OH﹣﹣4e﹣=2H2O+O2↑,
4xx
根据得失电子守恒得到0.2+2x=4x,
x=0.1mol
乙中A极析出的气体是氧气,物质的量为0.1mol,在标准状况下的体积为2.24L,
故答案为:
2.24L;
(3)根据转移电子的物质的量和金属阳离子的物质的量的变化,可知,铜离子从无增多,铁离子物质的量减小,亚铁离子增加,故①为Fe3+,②为Fe2+,③为Cu2+,
由图可知电子转移为0.4mol,生成Cu2+物质的量为0.2mol,阴极电极反应Fe3++e﹣=Fe2+,反应结束后,溶液中有Fe2+为0.5mol,Cu2+为0.2mol,所以需要加入NaOH溶液0.5×2+0.2×2=1.4mol,所以所需NaOH溶液的体积为=0.28L=280mL,
故答案为:
Fe2+;280.
第5页(共5页)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 专题 电化学 计算
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 保育笔记.doc
保育笔记.doc
 幼儿园日常安全检查记录表.xls
幼儿园日常安全检查记录表.xls
