 高中化学必修二知识框架.doc
高中化学必修二知识框架.doc
- 文档编号:1870097
- 上传时间:2022-10-24
- 格式:DOC
- 页数:8
- 大小:1.67MB
高中化学必修二知识框架.doc
《高中化学必修二知识框架.doc》由会员分享,可在线阅读,更多相关《高中化学必修二知识框架.doc(8页珍藏版)》请在冰豆网上搜索。
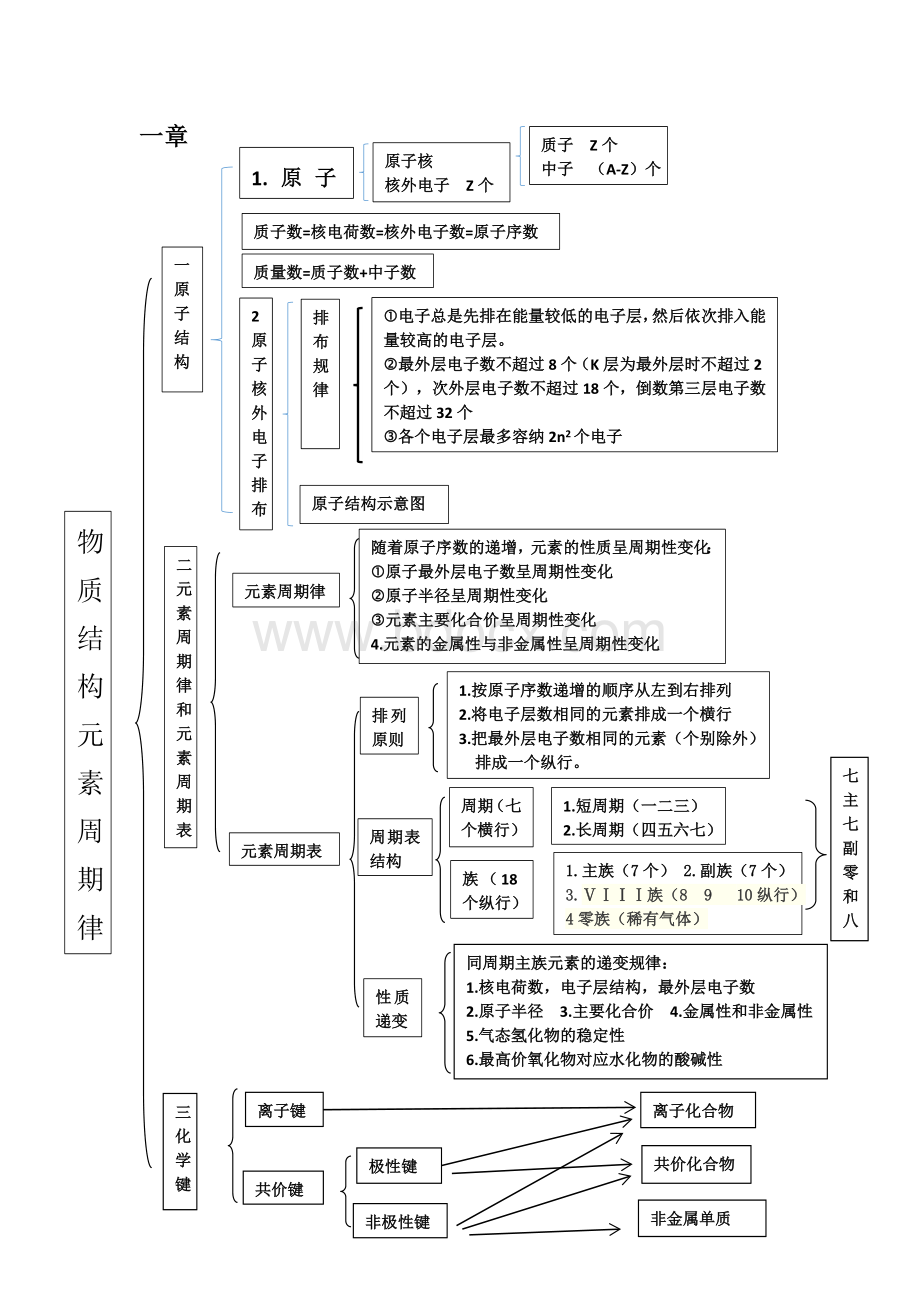
物质结构元素周期律
共价化合物
非金属单质
非极性键
极性键
离子化合物
共价键
离子键
三化学键
元素周期表
同周期主族元素的递变规律:
1.核电荷数,电子层结构,最外层电子数
2.原子半径3.主要化合价4.金属性和非金属性
5.气态氢化物的稳定性
6.最高价氧化物对应水化物的酸碱性
七主七副零和八
性质递变
1.按原子序数递增的顺序从左到右排列
2.将电子层数相同的元素排成一个横行
3.把最外层电子数相同的元素(个别除外)
排成一个纵行。
周期表结构
1.主族(7个)2.副族(7个)
3.ⅤⅠⅠⅠ族(8910纵行)
4零族(稀有气体)
1.短周期(一二三)
2.长周期(四五六七)
族(18个纵行)
周期(七个横行)
排列原则
随着原子序数的递增,元素的性质呈周期性变化:
原子最外层电子数呈周期性变化
原子半径呈周期性变化
元素主要化合价呈周期性变化
4.元素的金属性与非金属性呈周期性变化
元素周期律
二元素周期律和元素周期表
原子结构示意图
一原子结构
电子总是先排在能量较低的电子层,然后依次排入能量较高的电子层。
最外层电子数不超过8个(K层为最外层时不超过2个),次外层电子数不超过18个,倒数第三层电子数不超过32个
各个电子层最多容纳2n2个电子
排布规律
2原子核外电子排布
质量数=质子数+中子数
质子数=核电荷数=核外电子数=原子序数
质子Z个
中子(A-Z)个
原子核
核外电子Z个
1.原子AZX
一章
二章1.化学反应的本质
反应物化学键的断裂(吸收能量)
生成物化学键的形成(放出能量)
化学能与热能
2.化学键:
共价键/离子键
3.化学反应中的能量变化
三章
四章
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 必修 知识 框架
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 保育笔记.doc
保育笔记.doc
 幼儿园日常安全检查记录表.xls
幼儿园日常安全检查记录表.xls
