 高中化学必修一第四章测试卷.doc
高中化学必修一第四章测试卷.doc
- 文档编号:1864473
- 上传时间:2022-10-24
- 格式:DOC
- 页数:6
- 大小:197.50KB
高中化学必修一第四章测试卷.doc
《高中化学必修一第四章测试卷.doc》由会员分享,可在线阅读,更多相关《高中化学必修一第四章测试卷.doc(6页珍藏版)》请在冰豆网上搜索。
第四章非金属及其化合物测试题
一、选择题
1.2007年世界环境日中国主题是:
“污染减排和环境友好型社会”,下列有关环境问题说法不正确的是()
A.正常雨水的pH为7.0,酸雨的pH小于7.0
B.严格执行机动车尾气排放标准有利于防止大气污染
C.使用二氧化硫和某些含硫化合物进行增白食品对人体健康产生损害
D.使用氯气对自来水消毒过程中,生成的有机氯化物可能对人体有害
2.下列叙述正确的是()
A.硅在自然界中能够以单质形式存在
B.SiO2是酸性氧化物,所以不与任何酸反应
C.可用Na2SiO3溶液和CO2反应来制备H2SiO3
D.NaOH溶液可以盛装在带玻璃塞的磨口试剂瓶中
3.美国“9·11”恐怖袭击给纽约带来了一场严重的环境灾害-石棉污染,易使吸入石棉纤维者患肺癌。
已知石棉是硅酸盐矿物,某种石棉的化学式可表示为Ca2MgxSiyO22(OH)2,x、y的值可能分别为()
A.8、3B.5、8C.3、8D.9、6
4.下列关于SO2的说法中,不正确的是()
A.SO2是硫及某些含硫化合物在空气中燃烧的产物
B.SO2具有漂白性,可以使品红溶液褪色
C.SO2溶于水后生成H2SO4
D.SO2是一种大气污染物
5.下列实验中能证明某气体为SO2的是()
①使澄清石灰水变浑浊
②使湿润的蓝色石蕊试纸变红
③使品红溶液褪色
④通入足量NaOH溶液中,再滴加BaC12溶液,有白色沉淀生成,该沉淀溶液于稀盐酸
⑤通入溴水中,能使溴水退色,再滴加Ba(NO 3)2溶液有白色沉淀产生
A.都能证明 B.都不能证明 C.③④⑤均能证明D.只有⑤能证明
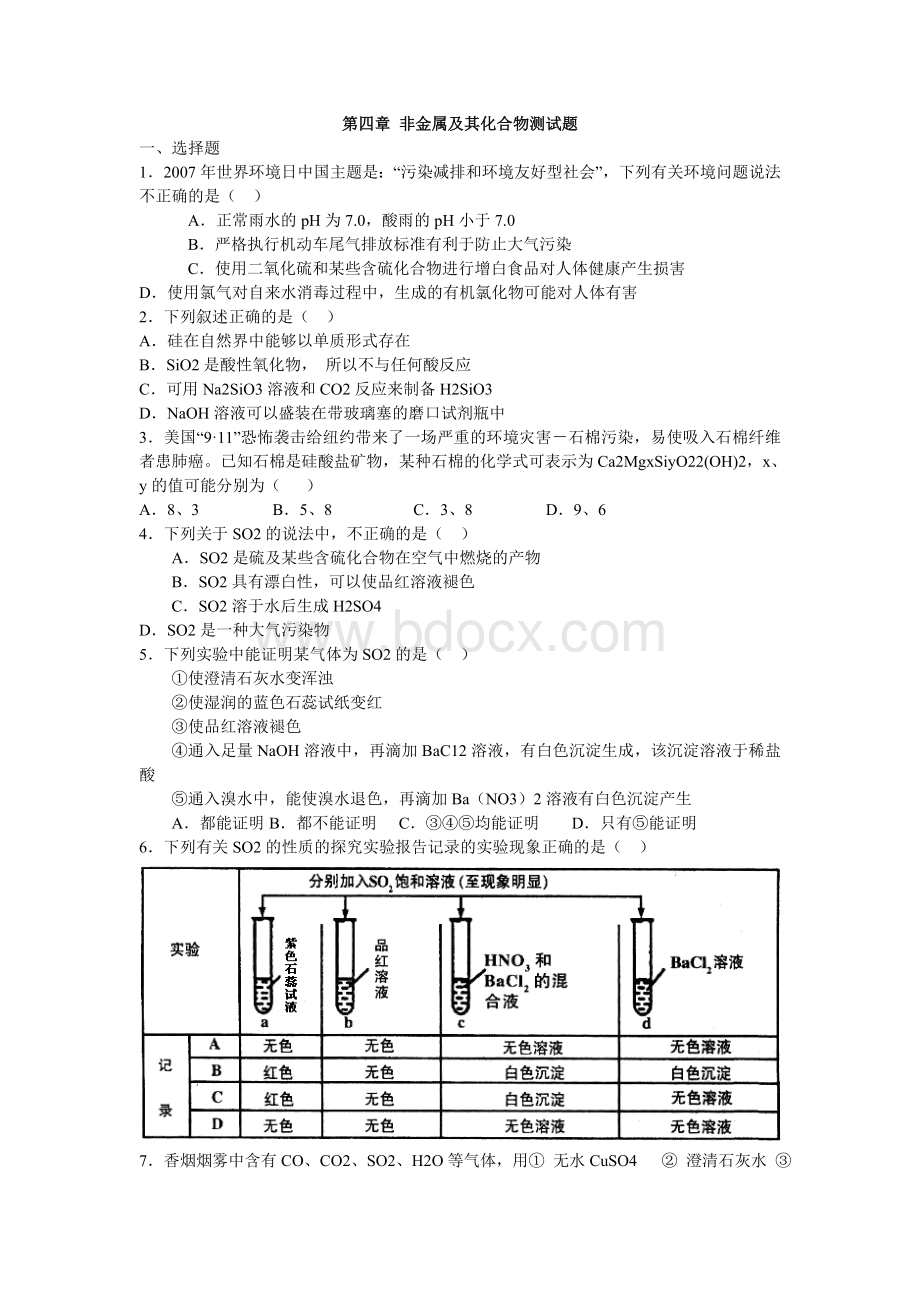
6.下列有关SO2的性质的探究实验报告记录的实验现象正确的是()
7.香烟烟雾中含有CO、CO2、SO2、H2O等气体,用①无水CuSO4 ②澄清石灰水③红热CuO④生石灰⑤品红溶液⑥酸性高锰酸钾溶液等药品可将其一一检出,检测时香烟烟雾通入药品的正确顺序是()
A.①——⑤——②——⑥——④——③
B.①——⑤——⑥——②——④——③
C.③——④——②——⑥——⑤——①
D.②——⑤——①——④——③——⑥
8.为了防止储存氯气的钢瓶被腐蚀,钢瓶在装入氯气前必须()
A.在钢瓶中充入稀有气体B.彻底干燥钢瓶内壁
C.用盐酸彻底清洁钢瓶 D.除去钢瓶表层的铁锈
9.某城市以“液氯泄漏”作为应急预警演习的项目,演习时下列防护措施合理的是()
①及时向上风口和地势较高处转移疏散人群;②及时戴上用浓烧碱溶液湿润过的口罩;③用高压水枪向泄露口附近喷洒稀碱液并设法控制氯气泄漏;④及时戴上用稀纯碱溶液湿润过的口罩;⑤就近向地下商场转移。
A.②③④⑤ B.①②④⑤ C.①③④⑤ D.①③④
10.实验室为了使用方便,通常将氯气溶解于水形成氯水或将其降温加压形成液氯来使用。
下列有关这两种液体的实验描述正确的是()
A.两种液体都可以使干燥的红布条褪色
B.两种液体都可以使干燥的蓝色石蕊试纸变红
C.用这两种液体都可以给自来水消毒
D.分别向这两种液体中投入几颗金属锌粒均有气泡产生
11.下列关于浓HNO3与浓H2SO4的叙述正确的是()
A.常温下都不可用铁制容器贮存 B.常温下都能与铜较快反应
C.露置于空气中,溶液质量都增重减轻D.露置于空气中,溶液浓度均降低
12.关于氮的变化关系图如下:
则下列说法不正确的是()
A.路线①②③是工业生产硝酸的主要途径
B.路线ⅠⅡⅢ是雷电固氮生成硝酸的主要途径
C.上述所有反应都是氧化还原反应
D.氮气可在足量的氧气中通过一步反应生成NO2
13.有一瓶Na2SO3溶液,由于它可能部分被氧化,某同学进行如下实验:
取少量溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加足量稀硝酸,充分振荡后,仍有白色沉淀,对此实验下述结论正确的是( )
A.Na2SO3已部分被氧化
B.加入Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4
C.加硝酸后的不溶沉淀一定是BaSO4和BaSO3
D.此实验不能确定Na2SO3是否部分被氧化
14.1.28g铜投入一定量浓HNO3中,铜完全溶解,生成气体颜色越来越浅,共收集到672mL气体(标况)。
将盛有此气体的容器倒扣在水中,通入标况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积是()
A.504mL B.168mL C.336mL D.224mL
二、填空题
15.A、B、C、D均为中学化学所学的常见物质,且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其它产物已略去):
请填写下列空白:
(1)若A、D的水溶液均能使湿润的蓝色石蕊试纸变红,则D为(填写化学式)
。
(2)若A为气体,其水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使湿润的蓝
色石蕊试纸变红。
则工业上合成A的化学方程式为。
(3)若A为短周期元素的形成的非金属单质,则A可能是
(填3种不同单质的化学式)。
16.据广西广播网:
2006年5月30日凌晨5时许,一辆装有27.8吨浓硝酸的罐车,在辽宁省葫芦岛市绥中县102国道前所镇至高岭镇路段处突然发生泄漏,硝酸流到轮胎上引发火灾。
辽宁省绥中消防大队官兵接到报警后迅速投入事故抢险,并协助消防人员进行扑救工作。
阅读上述信息后解答下列问题:
(1)硝酸是一种强酸,并且具有强的氧化性,一般在运输浓硝酸时采用的储藏罐材料是
(填序号),原因是。
①铁②铜③铝④陶瓷
(2)对于硝酸的泄漏事故,必须采取正确的处理方法,由于泄漏的硝酸与其他物质发生反应,会放出大量的热,可能会导致轮胎等着火,甚至可能会引发罐车爆炸,故要及时地用水降温,另外可以在地面铺撒(选填①氯化钙②熟石灰③生石灰④石灰石粉末⑤氯化钠)目的是。
用铁粉可以吗?
,原因
是。
(3)硝酸本来无色,但有挥发性,挥发出来的硝酸遇空气中的水蒸气形成白雾,白雾的成分是。
而实际情况并非如此,从硝酸泄漏现场可以看到大量的红棕色气体弥漫,该红棕色气体的成分是;用化学方程式表示产生这种现象的原因
。
三、实验题
17.某学生做浓硫酸性质的实验:
实验一:
在一个白色的点滴板的孔穴中分别放入小纸片、
少量CuSO4·5H2O。
然后如图所示,分别滴入几滴浓硫酸,
观察现象。
回答下列问题:
(1)浓硫酸滴在小纸片上,小纸片变(填实验现象),说明浓硫酸具有性。
(2)浓硫酸滴入CuSO4·5H2O中,胆矾(填实验现象),说明浓硫酸具有性。
实验二:
用如右图装置进行铜与一定体积已知浓度的浓硫酸反应的实验研究。
(1)写出试管B中的实验现象。
(2)写出A处反应的化学方程式,并用双线桥
标明电子转移的方向和数目:
。
(3)充分反应后,该学生发现铜和硫酸都有剩余。
在不补充浓硫酸的前提下,若要使剩余的铜片溶解,可再加入(要求填写一种与硫酸不同类别的物质)。
(4)B试管口的棉花应沾有的试剂是,其作用是,离子方程式为。
18.某学习小组设计以下四个实验探究氯水中的成份,请根据下表回答问题。
实验序号
实验方法
实验现象
结论
①
生成白色沉淀
氯水中含有Cl-
②
将氯水滴加到含有酚酞的NaOH溶液中
氯水中含有HClO
③
试纸变蓝色
氯水中含有Cl2
④
将氯水滴加到Na2CO3溶液中
氯水中含有H+
(1)实验室如何保存饱和氯水?
(2)指出实验①和实验③中的实验方法:
①;③;
(3)指出实验②和实验④中的实验现象:
②;④。
(4)有同学认为实验②现象产生的原因可能有两种:
(简要文字说明)①是由于氯水中的HClO将酚酞氧化而褪色;②是由于
(5)以下实验可以验证实验②产生的原因:
将NaOH溶液滴入含酚酞的氯水中,若观察到,证明红色褪去的原因是①;若观察到
,证明红色褪去的原因是②。
四、计算题
19.有一瓶(约100mL)硫酸和硝酸的混合溶液,取出10.00mL该混合溶液,加入足量氯化钡溶液,充分反应后过滤、洗涤、烘干,可得4.66g沉淀。
滤液跟2.00mol/LNaOH溶液反应,共用去35.00mL碱液时恰好中和。
试完成下列填空:
(1)则混合溶液中硝酸的物质的量浓度c(HNO3)=______________
(2)另取10.00mL原混酸溶液,加入1.92g铜粉共热,在标准状况产生的气体体积为________mL。
(写出必要的计算过程)
参考答案和解析
1.A解析:
正常雨水由于溶有空气中的二氧化碳略显酸性,其pH为5.6,酸雨的pH小于5.6。
2.D解析:
硅在自然界中以氧化物和硅酸盐形式存在,A错;SiO2能够与氢氟酸反应,B错;NaOH能与SiO2生成胶状的Na2SiO3,应盛放在橡皮塞的玻璃瓶中,D错。
3.B解析:
根据化学式中正负化合价的代数和为0,则2×2+2x+4y-22×2-1×2=0,则2x+4y=42。
4.C解析:
硫磺及含硫化合物燃烧生成SO2,A对;SO2能使品红溶液褪色,B对;SO2溶于水后生成H2SO3,C错;SO2容易造成酸雨,D对。
5.D解析:
CO2也能使澄清石灰水变浑浊,①错;HCl等酸性气体也能使蓝色石蕊试纸变红,②错;氯气也能使品红溶液褪色,③错;二氧化碳通入足量NaOH溶液中,再滴加BaC12溶液,生成的白色沉淀也能溶解于稀盐酸,④错。
6.C解析:
本题考查SO2的漂白性和还原性等。
SO2通入酚酞试液,由于溶液显酸性故紫色石蕊试液变红;SO2通入品红溶液,由于SO2具有漂白性,故品红褪色;SO2通入HNO3和BaCl2的混合溶液,2HNO3+3H2SO3=3H2SO4+2NO↑、H2SO4+BaCl2=BaSO4↓+2HCl,有白色沉淀产生;SO2通入BaCl2溶液,无明显现象。
7.B解析:
首先利用无水硫酸铜检验水蒸气,由于SO2对CO2的检验产生干扰,因此通过品红溶液检验S
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 必修 第四 测试
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 保育笔记.doc
保育笔记.doc
 幼儿园日常安全检查记录表.xls
幼儿园日常安全检查记录表.xls
