 药源性兴奋剂专项治理情况汇总表模板文档格式.docx
药源性兴奋剂专项治理情况汇总表模板文档格式.docx
- 文档编号:18635268
- 上传时间:2022-12-30
- 格式:DOCX
- 页数:19
- 大小:17.52KB
药源性兴奋剂专项治理情况汇总表模板文档格式.docx
《药源性兴奋剂专项治理情况汇总表模板文档格式.docx》由会员分享,可在线阅读,更多相关《药源性兴奋剂专项治理情况汇总表模板文档格式.docx(19页珍藏版)》请在冰豆网上搜索。
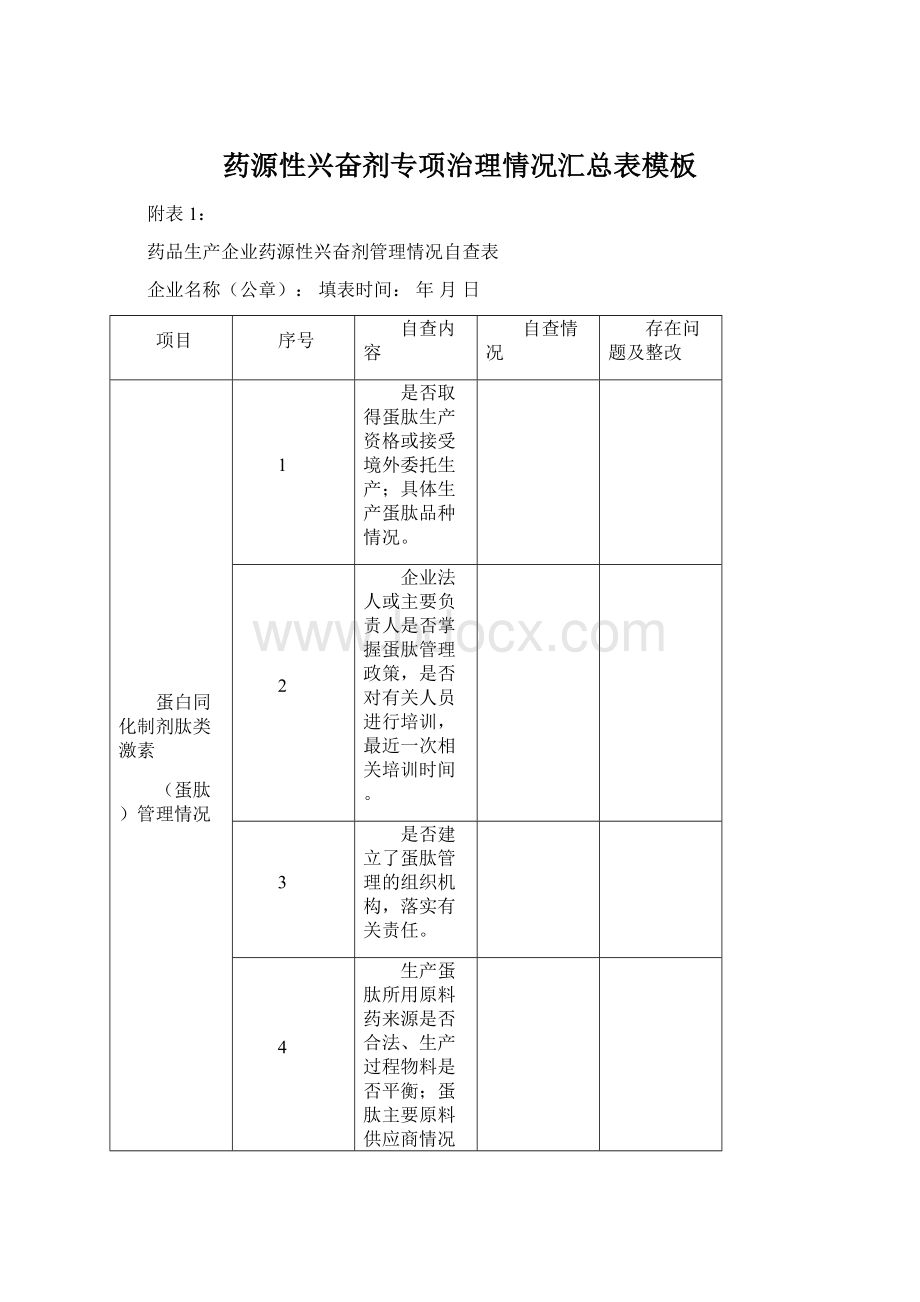
具体生产蛋肽品种情况。
2
企业法人或主要负责人是否掌握蛋肽管理政策,是否对有关人员进行培训,最近一次相关培训时间。
3
是否建立了蛋肽管理的组织机构,落实有关责任。
4
生产蛋肽所用原料药来源是否合法、生产过程物料是否平衡;
蛋肽主要原料供应商情况。
(可另附表格)
5
近两年购进蛋肽原料药情况,蛋肽验收、入库出库情况(手续是否齐全,记录内容是否完整、清晰,记录是否及时、准确)。
6
蛋肽是否单独储存保管,帐物是否相符。
7
是否有严格的蛋肽销售管理制度,是否对购买方资格进行审核。
8
是否按规定渠道销售蛋肽。
(原料购买方是否为取得制剂批准文号的药品生产企业,有蛋肽资格批发企业或出口企业,制剂购买方是否为有蛋肽资格的批发企业、医疗机构或出口企业;
销售单位名称请附表)。
9
蛋肽购买方档案是否齐全,是否有药品注册证、定点批发资格证明文件、医疗机构执业许可证等。
10
是否存在通过互联网宣传、销售蛋肽。
兴奋剂药品“运动员慎用”标识标注情况
企业法人或主要负责人是否了解含兴奋剂药品加注标识规定。
是否有含兴奋剂药品,有多少含兴奋剂药品,分别是哪些品种。
是否按规定办理加注标识备案。
出厂药品是否按规定加注标识。
如果有含《2014年兴奋剂目录》新列品种药品,2014年7月1日后生产的是否按规定加注标识。
如果有含《2014年兴奋剂目录》新列品种药品,2014年7月1日前生产的,未加注标识药品是否有销往本省市场的,如有,是否按规定召回或采取必要的补救措施。
填表人签字:
企业负责人签字:
附表2:
药品批发企业药源性兴奋剂管理情况自查表
年月日
是否取得蛋肽经营资格。
是否擅自经营蛋肽。
企业法人或主要负责人是否掌握蛋肽管理政策,是否对有关人员进行培训。
是否对蛋肽的购、销、存实行计算机管理。
采购蛋肽的渠道是否符合规定。
蛋肽验收、入库出库手续是否齐全,记录内容是否完整、清晰,记录及时、准确。
原料购买方是否为取得制剂批准文号的药品生产企业,有蛋肽资格批发企业或出口企业,制剂购买方是否为有蛋肽资格的批发企业、医疗机构或出口企业。
11
12
是否经营含兴奋剂药品,经营多少含兴奋剂药品。
所经营含兴奋剂药品是否按规定加注标识。
如果经营含《2014年兴奋剂目录》新列品种药品,2014年7月1日后生产的是否按规定加注标识
如果经营含《2014年兴奋剂目录》新列品种药品,且有2014年7月1日前生产未加注标识药品,是否按规定召回或采取必要的补救措施。
附表3:
药品零售企业药源性兴奋剂管理情况自查表
填表时间:
检查内容
检查方法
检查记录
蛋白同化制剂肽类激素管理
是否擅自经营蛋肽(胰岛素除外)。
查货架及销售记录。
询问相关人员,查培训档案。
询问。
对照《2014年兴奋剂目录公告》,了解企业含兴奋剂药品经营情况。
抽查10个品种,看药品看所附标签或说明书
抽查2个品种,看药品所附标签或说明书
抽查2个品种,看是否采取召回或补救措施的记录及证明材料。
附表4:
药品生产企业药源性兴奋剂管理情况检查表
检查企业:
检查时间年月日
是否取得蛋肽生产资格或接受境外委托生产。
询问并查看车间、仓库及出入库记录。
核对《生产许可证》、《药品注册证》等。
询问相关人员,查培训档案,看是否了解有关管理规定。
查看组织机构图和管理文件。
生产蛋肽所用原料药来源是否合法、生产过程物料是否平衡。
查看供应商资质、批生产、检验记录等。
查仓库记录,并与出入库手续核对。
查仓库及记录。
查销售制度,查购买方资格审核流程。
查销售记录及销售手续。
查销售记录所收载购买方档案情况。
查企业网站及销售记录。
询问,看是否了解有关管理规定。
是否有含兴奋剂药品,有多少含兴奋剂药品。
对照《2014年兴奋剂目录公告》,了解企业含兴奋剂药品生产情况。
查《药品注册证》及药品说明书或标签加注“运动员慎用”字样备案证明。
查所有品种批生产记录,看所附标签或说明书
如果有含《2014年兴奋剂目录》新列品种药品,2014年7月1日后生产的是否按规定加注标识
查涉及品种批生产记录,看所附标签或说明书
查销售记录,看对所有售出产品采取召回或补救措施的记录及证明材料。
检查人员签字:
附表5:
药品批发企业药源性兴奋剂管理情况检查表
核对蛋肽经营资格证明。
查仓库及出入库记录。
查组织机构图和管理文件。
查蛋肽销售开票情况。
查供应商资质。
企业负责人签字:
附表6:
药品零售企业药源性兴奋剂管理情况检查表
附表7:
药源性兴奋剂专项治理情况汇总表
填报单位:
(盖章)年月日
单位
检查数
一、检查药品生产经营企业情况
家
出动执法人员
人次
药品
生产
企业
蛋白同化制剂、肽类激素企业数量
检查情况
检查企业数
发现违规生产销售企业数
含兴奋剂药品企业数
含兴奋剂药品品种数
个
检查含兴奋剂药品企业数
检查含兴奋剂药品品种数
发现未加注标识品种数
批发
药品批发企业数
具有蛋肽经营资质企业数
检查企业总数
检查蛋肽经营企业数
发现违规销售企业数
检查含兴奋剂药品批发企业数
抽查含兴奋剂药品品种数
零售
药品零售企业数
家
发现擅自经营蛋肽企业数
二、互联网治理情况
违规发布蛋白同化制剂、肽类激素信息网站处理数
违规进行蛋白同化制剂、肽类激素互联网交易处理数
填表人:
填报日期:
年月日
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 药源性 兴奋剂 专项 治理 情况 汇总表 模板
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
