 消毒产品生产企业卫生许可申报资料范本.docx
消毒产品生产企业卫生许可申报资料范本.docx
- 文档编号:1855916
- 上传时间:2022-10-24
- 格式:DOCX
- 页数:40
- 大小:63.31KB
消毒产品生产企业卫生许可申报资料范本.docx
《消毒产品生产企业卫生许可申报资料范本.docx》由会员分享,可在线阅读,更多相关《消毒产品生产企业卫生许可申报资料范本.docx(40页珍藏版)》请在冰豆网上搜索。
消毒产品生产企业卫生许可申报资料范本
消毒产品生产企业卫生许可申报资料范本
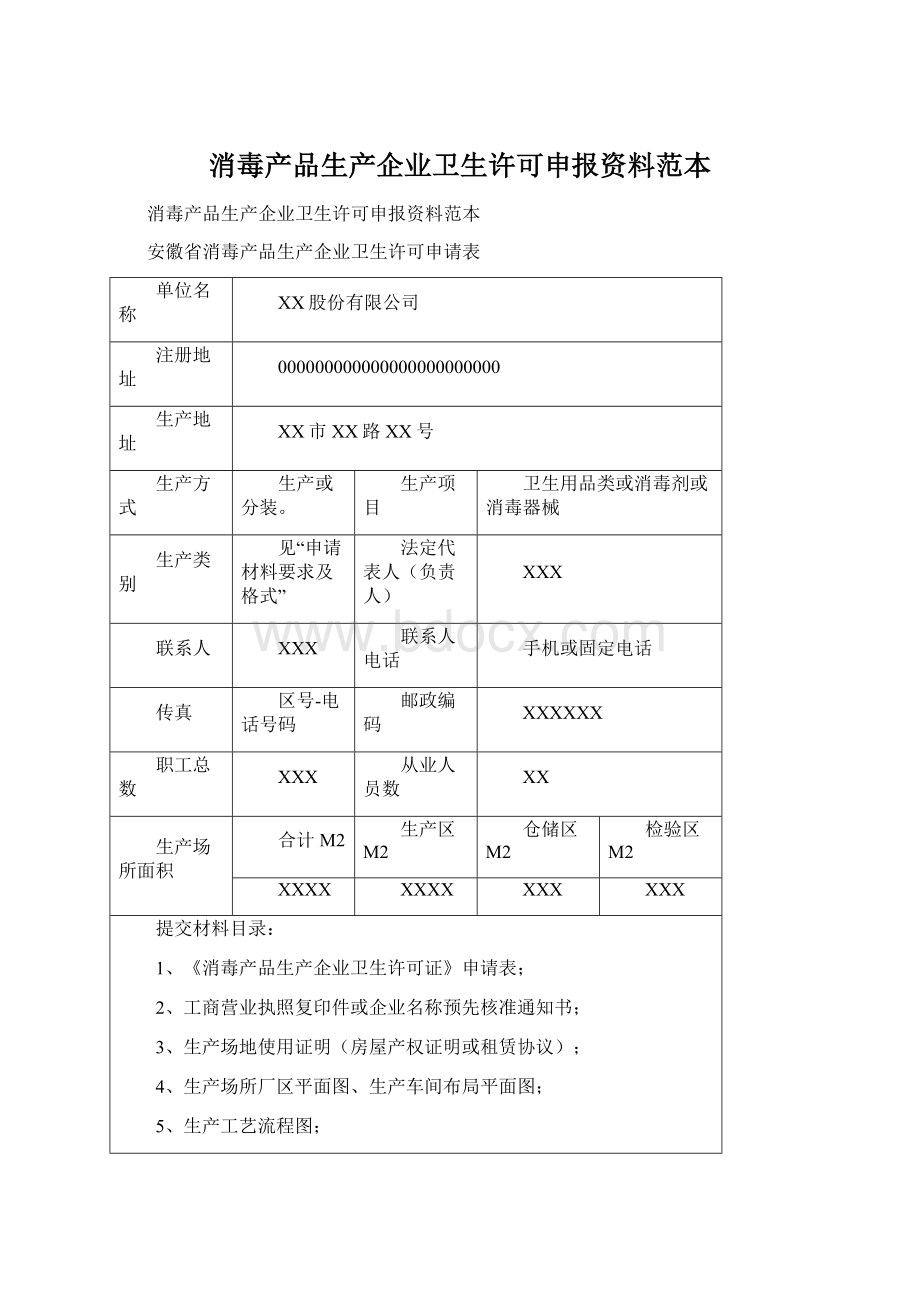
安徽省消毒产品生产企业卫生许可申请表
单位名称
XX股份有限公司
注册地址
000000000000000000000000
生产地址
XX市XX路XX号
生产方式
生产或分装。
生产项目
卫生用品类或消毒剂或消毒器械
生产类别
见“申请材料要求及格式”
法定代表人(负责人)
XXX
联系人
XXX
联系人电话
手机或固定电话
传真
区号-电话号码
邮政编码
XXXXXX
职工总数
XXX
从业人员数
XX
生产场所面积
合计M2
生产区M2
仓储区M2
检验区M2
XXXX
XXXX
XXX
XXX
提交材料目录:
1、《消毒产品生产企业卫生许可证》申请表;
2、工商营业执照复印件或企业名称预先核准通知书;
3、生产场地使用证明(房屋产权证明或租赁协议);
4、生产场所厂区平面图、生产车间布局平面图;
5、生产工艺流程图;
6、生产和检验设备清单;
7、质量保证体系文件;
8、产品目录;
9、生产环境检测报告;
10、生产用水检测报告(限隐形眼镜护理用品、抗(抑)菌制剂、灭菌剂、皮肤粘膜消毒剂的生产用水);
11、委托检测协议书(限允许委托检验的项目)。
对于一次性使用卫生用品、首次上市前需要进行卫生安全评价的消毒剂和消毒器械的生产企业还应提供以下材料:
1、产品的标签说明书;
2、产品配方/原材料;
3、产品检验报告(由卫生监督机构现场采样,经省级卫生行政部门认定的检验机构检验)。
申请材料按照附件“申请材料要求及格式”的要求和格式提供。
本申请表中所申报的内容和所附资料均真实、合法,符合国家有关规范、标准和规定,如有不实之处,我单位愿负相应法律责任,并承担由此造成的一切后果。
法定代表人(签字):
申报单位(公章)
年月日
附件1
申请材料要求及格式
一、申请材料的形式审查要求
(一)申请材料为A4规格纸打印,中文使用宋体小4号字,英文使用12号字,申请表用钢笔(水笔)填写或打印。
(二)申请材料内容完整、清楚,无涂改,申请材料中同一项目的填写一致,无前后矛盾。
(三)申请材料中的复印件清晰并与原件完全一致。
(四)申请材料中所有外文译为规范的中文,并有译文附在相应的外文材料之后。
(五)申请材料一份,每页加盖单位公章或盖骑缝章。
(六)申请材料根据目录顺序装订成册。
二、申请材料标准格式
(一)“安徽省消毒产品生产企业卫生许可申请表”填写要求
1、单位名称、法定代表人(负责人)、注册地址应与工商部门核准的一致。
2、生产方式填写生产、分装。
3、生产项目填写卫生用品、消毒剂、消毒器械。
4、生产类别按照《消毒产品生产企业卫生许可规定》中《生产类别分类目录》填写,不得注明具体产品的名称。
5、职工总数:
指全体职工总数。
6、从业人员指直接从事消毒产品生产的操作人员。
(二)生产工艺及流程图:
每一种产品均需列出;
(三)生产场所厂区平面图:
指行政、生活、生产车间、质检用房、物料和成品仓储用房等总体布局;
(四)生产车间布局平面图:
需标各功能间(区)、更衣室的位置及面积、紫外线灯数量、分布;
(五)生产设备清单。
××××单位生产设备清单
设备编号
设备名称
型号规格
数量
用途
制造商
(六)检验设备清单。
××××单位检验设备清单
设备编号
设备、仪器名称
型号规格
数量
用途
制造商
(七)拟生产产品目录。
××××单位产品目录
序号
产品名称
使用对象或范围
剂型/型号
(八)质量保证体系文件。
1、消毒产品生产标准操作规程。
2、人员岗位责任制度。
3、生产人员个人卫生制度。
4、设备采购和维护制度。
5、卫生质量检验制度。
6、留样制度。
7、物料采购制度。
8、原材料和成品仓储管理制度。
9、销售登记制度。
10、产品投诉与处理制度。
11、不合格产品召回及其处理制度。
三、检测报告要求
生产企业应提供1年内的生产环境和生产用水检测报告,检测报告应由经过计量认证的检验机构出具。
(一)卫生用品生产企业检验项目。
1、生产车间环境:
(1)有净化要求的生产车间:
隐形眼镜护理用品生产(包装除外)、分装应在10万级空气洁净度以上净化车间进行。
皮肤粘膜抗(抑)菌制剂(用于洗手的抗(抑)菌制剂除外)等产品配料、混料、分装工序应在30万级空气洁净度以上净化车间进行。
检测净化车间的温度、相对湿度、进风口风速、室内外压差、空气中≥0.5μm和≥5μm尘埃粒子数,车间空气、工作台表面细菌菌落总数,工人手表面细菌菌落总数和致病菌。
(2)无净化要求的生产车间:
检测生产车间工作台表面、车间空气细菌菌落总数,工人手表面细菌菌落总数和致病菌。
2、紫外线灯辐射强度:
采用紫外线对车间空气消毒的生产企业。
3、消毒灭菌效果验证:
自备消毒灭菌器对生产的消毒产品进行消毒灭菌处理的生产企业。
4、生产用水:
隐形眼镜护理用品和抗(抑)菌制剂的生产用水按照《中华人民共和国药典》二部纯化水检测全项目,隐形眼镜护理用品的生产用水还应做无菌试验。
(二)消毒剂生产企业检验项目。
1、有净化要求的生产车间:
检测净化车间的温度、相对湿度、进风口风速、室内外压差、空气中≥0.5μm和≥5μm尘埃粒子数,工作台表面细菌菌落总数。
2、紫外线灯辐射强度:
采用紫外线进行车间空气消毒的生产企业。
3、生产用水:
灭菌剂、皮肤粘膜消毒剂的生产用水按照《中华人民共和国药典》二部纯化水检测全项目。
四、消毒产品分装生产企业还需提供以下材料
(一)大包装产品生产企业保证其生产的半成品符合相关卫生质量标准的承诺书。
(二)大包装产品生产企业与分装生产企业的合同协议书。
(三)大包装产品生产企业的消毒产品生产企业卫生许可证复印件。
(四)大包装产品若为须经过卫生部许可的消毒产品,还应提供该产品的卫生许可批件复印件。
五、产品检验报告
(一)申请卫生许可证
仅限于不需要取得产品卫生许可的消毒产品,包括需要进行卫生安全评价的产品、一次性使用卫生用品等。
需要进行卫生安全评价的产品包括:
1、紫外线杀菌灯;2、食具消毒柜(限于符合GB17988《食具消毒柜安全和卫生要求》的产品);3、压力蒸汽灭菌器;4、75%单方乙醇消毒液;5、符合《次氯酸钠类消毒剂卫生质量技术规范》和《戊二醛类消毒剂卫生质量技术规范》的产品;6、抗(抑)菌制剂。
(二)延续卫生许可证
包括需要取得产品卫生许可、需要进行卫生安全评价的消毒产品及一次性使用卫生用品。
检验项目与《消毒产品生产企业管理规范》中的要求企业自检的化学和微生物指标一致。
XX股份有限公司申报资料2
工商营业执照复印件或企业名称预先
核准通知书
XX股份有限公司申报资料3
生产场地使用证明
(房屋产权证明或租赁协议)
XX股份有限公司申报资料4
厂区平面总图:
指行政、生活、生产车间、质检用房、物料和成品仓储用房等总体布局
XX股份有限公司申报资料4
车间布局平面图:
需标注更衣室位置、生产车间面积、紫外线灯数量、分布、人流物流路线等
XX股份有限公司申报资料5
生产工艺及流程图
生产工艺及流程图
1、生产工艺:
文字描述,需明确涉及到的主要参数如:
温度、压力等。
2、流程图:
用图标识(根据不同产品分别描述)例如:
XX股份有限公司申报资料6
主要生产设备清单、检验仪器清单
按序号、名称、型号、产地、数量、状态列表;基本设备要求见《消毒产品生产企业管理规范(2009年版)》附件1“消毒产品生产企业基本生产设备清单(试行)”
主要生产设备清单
设备
编号
设备名称
型号规格
数量
用途
制造商
----
2
1
1
1
2
3
4
1
1
1
1
1
1
主要检验仪器清单
设备编号
设备名称
型号规格
数量
用途
制造商
XX股份有限公司申报资料7
质量保证体系文件
以下仅供参考,申报时不可照抄,企业应根据生产类别的不同,结合企业自身实际情况,制定切实可行的质量保证体系文件。
1、XX抗菌洗液生产标准操作过程
2、人员岗位责任制度
3、生产人员个人卫生制度
4、设备采购和维护制度
5、卫生质量检验制度
6、留样制度
7、物料采购制度
8、原材料和成品仓储管理制度
9、销售登记制度
10、产品投诉与处理制度
11、不合格产品召回及其处理制度
XX股份有限公司申报资料7
XX抗菌洗液生产标准操作规程
一、目的:
建立XX抗菌洗液生产标准操作规程,确保生产操作按规范进行。
二、范围:
适用于公司所有产品生产过程的管理。
三、责任:
操作人员、生产车间负责人、生产部门和质量部门负责人。
四、内容:
1、生产计划:
1.1、企业的生产计划必须按照市场情况、库存情况,制订企业的年、季、月生产计划。
按照计划制订原辅料、包装材料采购计划,生产部按计划组织生产。
2、工艺规程的管理:
2.1、凡正式生产的产品均须制定工艺规程,否则不许生产,当新的工艺规程执行时应收回旧的工艺规程。
2.2、凡从事生产管理人员和操作人员必须严格遵守工艺规程,任何人不得违反和擅自改动。
2.3、工艺规程是编写岗位SOP、组织和指导生产的主要依据,是公司技术管理的基础,具有技术法规的作用,操作人员必须经培训、考核合格后方可上岗。
2.4、生产部门和质量部门负责监督工艺规程的执行,不定期抽查工艺的执行情况。
2.5、工艺规程属内部技术资料,应归档保存,严防失密。
3、批记录的管理:
3.1、各岗位操作人员必须按每批岗位要求做批生产记录;
3.2、必须将记录内容与生产指令和SOP对照审核;
3.3、上、下工序记录中产品数量、质量、批号、桶号必须一致、正确;
3.4、对生产记录中不符合要求的填写方法,必须有填写人更正并签字。
3.5、每批生产结束后,岗位操作记录由班组长根据原编号按批整理,做好生产操作记录的收集和保管。
4、称量、复核的管理
4.1、所使用的衡器应校验合格并在校验有效期内,称量前对所用衡器清洁并归零。
4.2、称量必须在专门称量间进行,原辅料必须在洁净区称量。
4.3、所称取物料总量应与生产指令下达的处方计算出的投料量一致,物料的称量
XX股份有限公司申报资料7
精密度应高于处方精度要求。
4.4、称量时,一人称量,另一人复核或复称,并再次核对品名、含量、投料量是否有误,发现有误及时纠正。
4.5、边称量边记录、填写原辅料称量记录,并在原包装外标明该次称取量、称取日期、称取人等内容。
4.6、余料要扎紧口,定置于暂存室,明示状态标志。
5、投料管理
5.1、核对生产品种所需原辅料的品名、编号、规格、剂型、批号、生产日期等。
5.2、生产过程中的各项卫生管理及清场管理,如核对设备、工作地点、文件、前次生产遗留物、生产所不需物料的清场及清洁程序等。
5.3、生产过程中的全
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 消毒 产品 生产 企业 卫生 许可 申报 资料 范本
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
