 江苏省第一类医疗器械生产备案申请表Word格式.docx
江苏省第一类医疗器械生产备案申请表Word格式.docx
- 文档编号:18503980
- 上传时间:2022-12-18
- 格式:DOCX
- 页数:11
- 大小:18.38KB
江苏省第一类医疗器械生产备案申请表Word格式.docx
《江苏省第一类医疗器械生产备案申请表Word格式.docx》由会员分享,可在线阅读,更多相关《江苏省第一类医疗器械生产备案申请表Word格式.docx(11页珍藏版)》请在冰豆网上搜索。
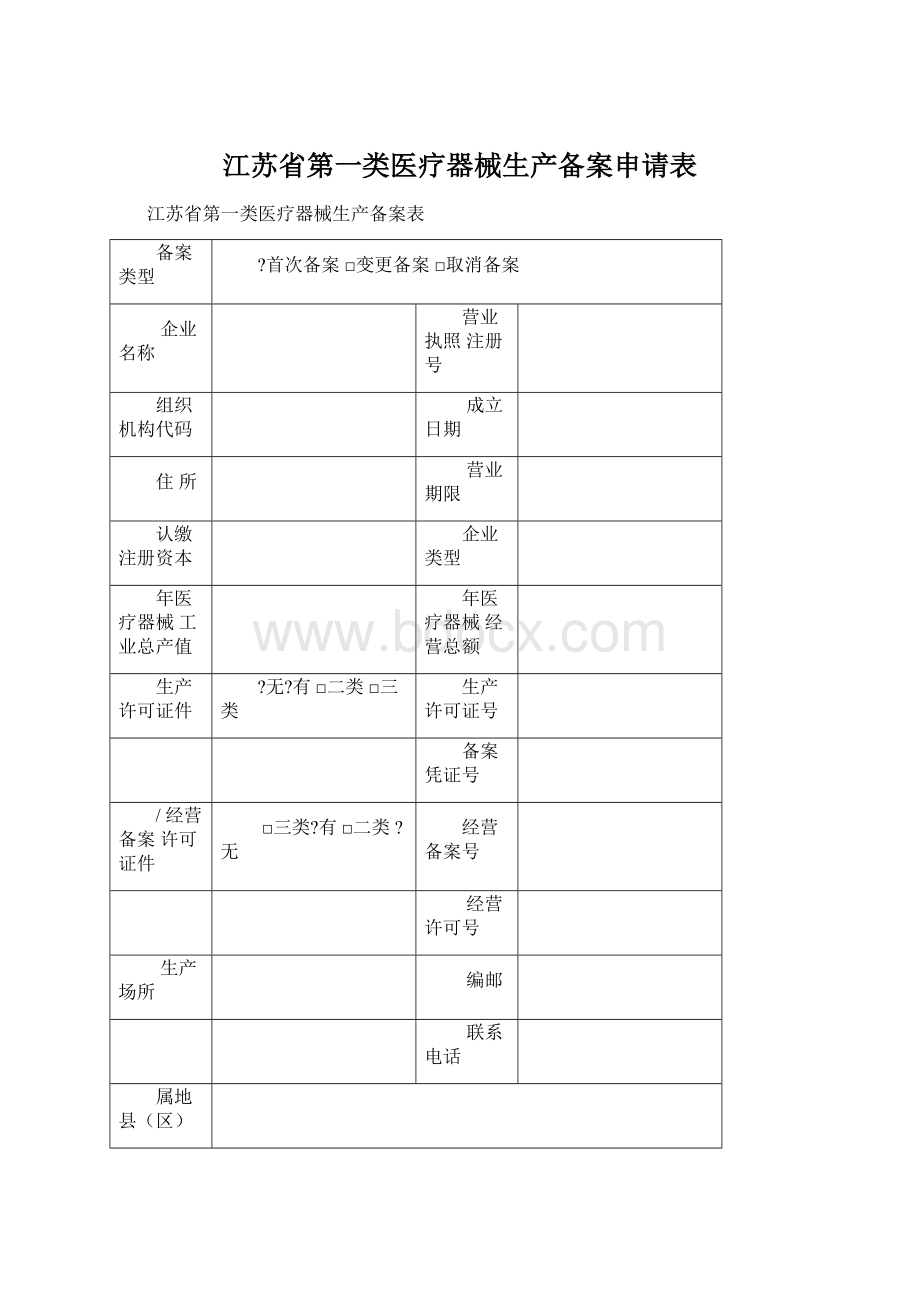
生产许可证件
无?
有□二类□三类
生产许可证号
备案凭证号
/经营备案许可证件
□三类?
有□二类?
无
经营备案号
经营许可号
生产场所
编邮
联系电话
属地县(区)
人员情况
姓名
身份证号
职务
学历
职称
法定代表人或投资人
企业负责人
联系人
姓名
联系电话
传真
电子邮件
企业人员况情
人员总数(人)
生产管理人员(人)
质量管理人员(人)
专业技术人员(人)
占地面积(㎡)
建筑面积(㎡)
生产场所
情况
建筑面积生产面积(㎡)(㎡)
净化面积(㎡)
检验面积(㎡)
仓储面积(㎡)
检验机构状况
总人数
技术人员数
委托生产
备案人信息1
企业名称
联系人姓名:
座机:
手机:
委托生产2备案人信息
企业名称
是否开展互联网销售
销售网址
备案事项
生产范围
生产第一类医疗器械列表
序号
产品名称
产品备案号
是否受托生产
备案日期
两年内质量管理体系检查情况(如有):
无
两年内省级以上质量抽验结果(如有):
用户投诉处理情况:
不良事件处理监测及处理情况:
主要管理人员情况一览表
性别
年龄
专业
生产管理、质量检验岗位从业人员情况一览表
部门
质量管理体系内审员情况一览表.
内审员证书编号
企业主要生产检验设备清单:
设备名称申备案产品基本情况(按产品逐一填写)
生产厂家
规格型号
数量
用途
使用部门
注册产品标准号或产品技术要求备案号
产品类别
体外诊断试剂?
无源医疗器械?
□有源医疗器械
产品作用机理及组成:
产品生产工艺流程图:
关键和特殊控制点名称:
主要原材料/部件名称
供方(含加工)名称
注册产品标准或成品检验规程规定的出厂检验项目
条款号
检验项目
检测设备/器具
申备案产品基本情况(按产品逐一填写)
注册产品标准号或产品技术要求备案号
□无源医疗器械□有源医疗器械□体外诊断试剂
产品作用机理及组成:
企业质量管理体系程序文件和第三层次文件目录(可加页)
文件编号
文件名称
第一类医疗器械生产备案提交资料清单:
1.第一类医疗器械生产备案表;
2.所生产产品的注册证/医疗器械备案凭证复印件;
(产品仅供出口的,提供拟出口第一类医疗器械产品清单)
3.经核准的注册产品标准/备案的产品技术要求复印件;
(产品仅供出口的,提供出口第一类医疗器械产品技术要求或详细技术合同复印件)
4.营业执照和组织机构代码证复印件;
5.法定代表人、企业负责人身份证明复印件;
6.生产、质量和技术负责人的身份、学历职称证明复印件;
7.生产场地的证明文件(有特殊生产环境要求的,还应提交设施、环境的证明文件)复印件;
8.质量手册和程序文件;
□9.《医疗器械生产质量管理规范自查表》(发文实施后提交)
10.经办人授权证明;
□11.其他证明材料(如境内企业之间委托生产合同复印件,境外企业委托境内企业生产仅供出口合同复印件、质量管理体系建设承诺书、门牌号码文字性改变证明等)。
□12.变更/取消备案说明及其证明材料
首次备案:
1-11
□变更/取消备案:
1,12,2-11相关内容以及备案凭证原件
备案材料应完整、清晰,使用A4纸打印装订并附有目录,复印件加盖公章后与电子版(以上文件的WORD或PDF格式,含《第一类医疗器械生产备案凭证》样稿)一并提交,上传邮箱为各市局指定生产备案邮箱,压缩文件名为公司名+备案类型+提交日期,例:
A公司生产备案或变更备案20140606。
我公司已知悉以下内容:
1、已学习了《医疗器械监督管理条例》及医疗器械生产相关法律法规,相关工作人员已经过培训,取得上岗证;
2、第一类医疗器械生产企业也需符合《医疗器械生产质量管理规范》要求;
3、已知监管部门在生产备案后将对企业进行日常监管,包括对现场进行检查,不符合要求会被依法处理;
4、已知悉企业需按规定履行年度质量管理报告义务;
5、已知悉监管部门将按规定把企业违法违规行为向社会公示,这将影响企业的的信用记录和信用评级;
6、已知悉此备案表中所有信息发生变更或取消备案需及时到药监部门办理变更备案或取消备案;
7、已知提交《第一类医疗器械生产备案凭证》样稿电子版将加快备案速度。
本企业承诺所提交的全部备案材料真实有效,并承担因失实引发的一切法律责任。
同时,保证按照法律法规的要求从事医疗器械生产活动。
法定代表人(签字)(企业盖章)
年月日
填表说明:
一、本表按照实际内容填写,不涉及的可缺项。
其中,企业名称、营业执照注册号、住所、法定代表人或投资人、注册资本、成立日期、营业期限等按照营业执照内容填写。
若为合伙企业,法定代表人或投资人栏填写“-”;
企业负责人指法人资格企业的法定代表人或其授权的最高管理者;
个人独资企业的投资人或授权的经营者;
合伙企业指执行事务合伙人。
二、本表生产范围应当按照国家食品药品监督管理总局颁布的医疗器械分类目录中规定的管理类别、分类目录类代号和类代号名称填写。
三、本表应使用A4纸双面打印,不得手写。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 江苏省 一类 医疗器械 生产 备案 申请表
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《雷雨》中的蘩漪人物形象分析 1.docx
《雷雨》中的蘩漪人物形象分析 1.docx
