 物质的量Word文档格式.docx
物质的量Word文档格式.docx
- 文档编号:18323102
- 上传时间:2022-12-15
- 格式:DOCX
- 页数:13
- 大小:105.12KB
物质的量Word文档格式.docx
《物质的量Word文档格式.docx》由会员分享,可在线阅读,更多相关《物质的量Word文档格式.docx(13页珍藏版)》请在冰豆网上搜索。
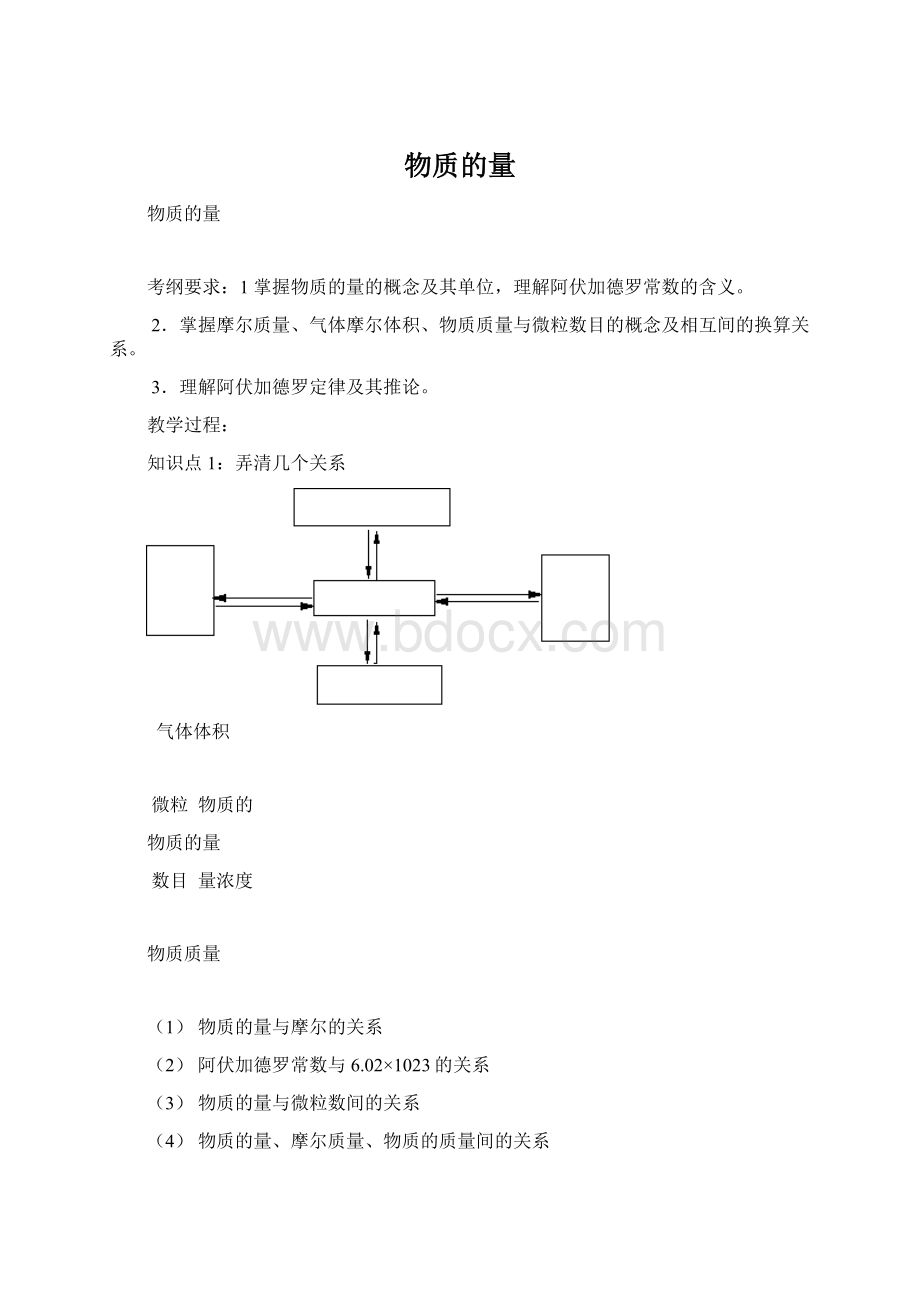
B.1:
4
C.11:
14
D.11:
28
2.
273K、1.01×
105Pa下,NA个H2分子所占体积约为____________,2.3g金属钠变成离子时失去的电子数目为____________,1L1mol·
L-1的CH3COONa溶液中,CH3COO—离子数目为____________,常温常压下,16g臭氧所含的氧原子数目为
____________。
3.下列两种气体的分子数一定相等的是()
A.质量相等、密度不等的N2和C2H4B.等温等压的CO和C2H4
C.等温等体积的O2和N2D.等压等体积的N2和CO2
4.已知Q与R的摩尔质量之比为9:
22,在反应X+2Y=2Q+R中,当1.6gX与Y完全反应后,生成4.4gR,则参与反应的Y和生成物Q的质量之比为()
A.46:
9B.32:
9C.23:
9D.16:
9
5.已知过量氨气跟氯气可迅速反应生成氯化铵和氮气。
当转移的电子总数为a个时,生成的氮气的物质的量bmol。
①写出该反应配平的化学方程式:
②该反应中参加氧化还原反应的氧化剂和还原剂的物质的量之比为
③阿伏加德罗数常数为(用含a、b的代数式表示)
知识点2:
关于阿伏加德罗常数的考查
近年来关于用NA表示阿伏加德罗常数的考查点有以下几个方面:
(1)特殊物质的摩尔质量例如H2O、D2O、T2O;
H3PO4、H2SO4;
C7H8、C3H8O3等。
(2)考查晶体的知识:
NaHSO4、Na2O2等晶体中阴阳离子数目。
(3)特殊物质中共价键数目、共用电子对数目的考查:
如一定物质的量的白磷、SiO2、金刚石、石墨晶体中的共价键数目,一定物质的量的CnH2n+2、CnH2n、CnH2n-2、CnH2n-6中共用电子对数目。
(4)反应中得失电子数目的考查如Cl2与水或碱的反应;
Na2O2与H2O或CO2;
Cu与S;
Fe与Cl2的反应。
(5)一些微粒中电子数、质子数、中子数的考查如—CH3、—CHO、D2O、NH4+等。
(6)弱电解质的电离或弱酸弱碱离子的水解导致微粒数目减少。
(7)有关气体摩尔体积的问题,在用22.4L/mol计算时要注意条件是标况,是否为气体如SO3、CCl4、C6H6、氯仿、辛烷等。
(8)有关电解时析出金属(或放出气体)的量与转移电子的关系。
(9)关于阿伏加德罗定律的三同→一同的考查。
例1、用NA表示阿伏加德罗常数,下列叙述中正确的是()
A、12g的金刚石晶体中含有碳碳键的数目为4NA
B、46g四氧化二氮含有的原子总数一定为3NA
C、500mL1.0mol/L的乙酸溶液中含有的H+数为0.5NA
D、1molFeCl3制成胶体,所得胶体的粒子数为NA
答案:
B
例2、设NA表示阿伏加德罗常数,下列说法中正确的是()
A、1molI-被氧化时失去的电子数目为2NA
B、标准状况下,2.24LNH3和CH4混合气体所含电子数目为2NA
C、1LpH=1的水溶液中含有氢离子数为NA
D、1molOH-在电解过程中被氧化时提供电子数目为NA
D
例3、设NA为阿伏加德罗常数,下列说法中正确的是()
A、11.2LCO2所含的原子个数为1.5NA
B、mg
中所含电子总数为(Z-n)m
C、1mol十七烷分子中共价键总数为34NA
D、25℃时,1g水中含有H+约为
例4.设NA、表示阿伏加德罗常数值,下列说法正确的是()
A.500mL0.1mol·
L-1的Al2(SO4)3溶液中,含Al3+0.1NA
B.36g重氧(18O2)气体所含分子数为NA,占体积为22.4L
C.7.8gNa2O2与足量CO2反应,转移电子数为0.1NA
D.15g甲基中含有的电子数为8NA
C
练习Ⅱ
1、设NA表示阿伏加德罗常数,下列说法中正确的是()
A、11.2L乙烷中所含的碳氢单键数为3NA
B、NA个碳原子燃烧时所放出的热量就是碳的燃烧热
C、在1mol甲基中,原子核外存在的电子数为10NA
D、1mol氧气分别与足量的Mg、Al反应,Mg、Al失去的电子数都是4NA
2、设NA表示阿伏加德罗常数,下列叙述中正确的是()
A、标准状况下,22.4LN2含有共用电子对数为NA
B、常温常压下,1mol氢气含共价键个数为NA
C、1mol氢氧化铁胶体粒子所含电荷数为3NA
D、1molCH3CH2CH(CH3)2所含甲基个数为2NA
3、设NA表示阿伏加德罗常数的值,下列说法中正确的是()
A、室温时,4g氦气所含原子数目为2NA
B、常温常压下,1mol氯气与足量的铁粉反应,转移的电子数为3NA
C、标准状况下,22.4LSO3所含电子数为24NA
D、500mL0.5mol/LBa(NO3)2溶液中,NO3-的数目为0.5NA
4、设NA表示阿伏加德罗常数的值,下列说法中正确的是()
A、1.8g铵根离子所含的电子数为1.1NA
B、1mol白磷分子中所含共价键数为4NA
C、标准状况下,22.4L乙醇所含的分子数必定为NA
D、在电解食盐水的实验中,测得电解后溶液的pH为14,又知电解后溶液总体积为1L,则阴极析出气体的分子数为0.5NA
5、设NA为阿伏加德罗常数,下列说法正确的是()
A、28g乙烯与28g丙烯中均含有6NA对共用电子对
B、1molH2O2完全分解时转移电子2NA个
C、常温常压下,3.5g35Cl2所含中子数为0.1NA
D、常温常压下,22.4LO3气体中含有3NA个原子
6、设NA为阿伏加德罗常数,下列叙述中正确的是()
A、等物质的量的丁酸和戊醇所含分子个数均为NA
B、等质量的丁酸和戊醇所含分子个数均为NA
C、分子数均为NA的丁酸和戊醇质量相等
D、分子数均为NA的丁酸和戊醇的蒸气体积相等
7、设NA表示阿伏加德罗常数,下列说法中正确的是()
A、标准状况下,17g氨气的体积恰好是22.4L
B、标准状况下,1molNa2O2与水反应时转移电子2NA
C、2g重氢在标准状况下所含原子个数为2NA
D、常温常压下,32g氧气与34g硫化氢分子数之比为1:
1
8、NA代表阿伏加德罗常数,以下说法正确的是()
A.在100mL0.1mol/LFeCl3溶液中含有的Fe3+0.01NA
B.常温常压下46gNO2和N2O4的混合气体与水反应生成
个
离子
C.标准状况下,11.2L三氧化硫溶于水,可生成0.5NA个硫酸分子
D.7.8gNa2O2溶于水时转移的电子数为0.1NA
9、
为阿伏加德罗常数,下列说法正确的是()
A、1摩尔氯化铁制成氢氧化铁胶体,胶体微粒数目为NA
B、常温常压下,4g氦气所含有的中子数目为4NA
C、标准状况下,22.4L单质溴所含有的原子数目为2NA
D、电解食盐水若产生1g氢气,则转移的电子数目为NA
10.设NA为阿伏加德罗常数,下列说法中正确的是()
A.lmolO2-含有的电子数为17NA
B.足量Na2O2和11.2LCO2反应,转移电子数目为0.5NA
C.常温常压下,32g
中所含的中子数为20NA
D.27g金属Al与足量的稀硫酸反应时生成的H233.6L
知识点3:
气体摩尔体积与阿伏加德罗定律
(1)气体摩尔体积定义及计算式
(2)阿伏加德罗定律及推论据PV=nRT推出
同温同压下V1:
V2=n1:
n2
同温同体积:
P1:
P2=n1:
n2
同温同压下:
ρ1:
ρ2=M1:
M2
(3)气体相对分子质量计算
a.已知标况下气体密度ρ,M=ρ×
22.4
b.已知气体A对气体B的相对密度D,MA=D×
MB
c.混合气体的平均相对分子质量:
M=MAΦA+MBΦB+……(ΦA、ΦB为A、B的体积分数)
M=总质量/总物质的量
例1.体积为1L的干燥容器中充人HCl气体后,测得容器中气体对氧气的相对密度为1.082。
将此气体倒扣在水中,进入容器中液体的体积是()
A.0.25LB.0.5LC.0.75LD.1L
解析:
Mr.=D*Mr(O2)=1.082×
32=34.6<
Mr(HCl),故混合气体中必有空气。
进入容器中的液体体积等于HCl气体体积。
HCl36.55.6
34.6
空气291.9约为3:
1所以HCl的体积为0.75L
例2.在某温度时,一定量的元素A的氢化物AH3,在一定体积的密闭容器中可以完全分解成两种气态单质,此时压强增加了75%,则A单质的一个分子中有____个A原子,分解反应的化学方程式是______________________。
依据阿伏加德罗定律,同温同体积时,气态物质的压强与物质的量成正比,设反应物为1mol.P1:
P2=n1:
n2则反应后的物质的量为1.75mol
?
AH3=?
AX+?
H2
10.251.5
据原子守恒可知A单质的一个分子中有4个原子。
方程式为4AH3=A4+6H2
练习Ⅲ
1.(2005年高考江苏理综)在一定条件下,l体积气体A2和3体积气体B2完全反应生成了2体积气体(体积在相同条件下测定),则X的化学式是()
A.ABB.A2B3C.AB2D.AB3,
2.(2005年全国理综卷III)在273K和10kPa的条件下,将2.00g氦气、1.40g氮气和1.60g氧气混合,该混合气体的体积是()
A.6.72LB.7.84LC.10.08LD.13.44L
3.混合气体由N2和CH4组成,测得混合气体在标准状况下的密度为0.821g/L,则混合气体中N2和CH4的体积比为()
A.1︰1B.1︰4C.4︰1D.1︰2
4.在两个容积相同的容器中,一个盛有HCl气体,另一个盛有
和
的混合气体。
在同温同压下,两容器内的气体一定具有相同的()
A.原子数B.密度C.质量D.质子数
5.某气体的摩尔质量为Mg·
,NA表示阿伏加德罗常数,在一定的温度和压强下,体积为VL的该气体所含有的分子数为X.则1L该气体的质量(以g为单位)
6.将乙烯(C2H4),一氧化碳、氮气三种气体分别盛放在三个容器中,并保持三个容器内气体的温度和质量均相等,这三种气体对容器壁所施压强的大小关系是()
A.C2H4>CO>N2B.C2H4=CO=N2C.CO>C2H4>N2D.N2>C2H4>CO
溶液的浓度
1.理解物质的量浓度
2.掌握物质的量浓度溶液质量分数之间的换算
3.掌握一定物质的量浓度溶液的配制
知识点:
(1)溶解度概念、溶液质量分数及计算ω%=m溶质/m溶液×
100%
(2)物质的量浓度概念及计算
C=n/V
已知溶液密度、质量分数:
C=1000ρa%/M
(3)一定物质的量溶液的配制及误差分析
例1、若20g密度为dg·
cm-3的硝酸钙溶液里含1gCa2+,则NO3-离子的浓度是()
A、
mol·
L-1 B、
L-1
C、1.25dmol·
L-1 D、2.5dmol·
L-1
D
例2、将溶质的质量分数为a%,物质的量浓度为c1mol·
L-1的H2SO4溶液蒸发掉一定量的水,使其溶质的质量分数为2a%,此时物质的量浓度为c2mol·
L-1。
则c1和c2的关系是
A、c2=2c1 B、c2<2c1 C、c2>2c1 D、c1=2c2
答案:
例3.20℃时饱和KCl溶液的密度为1.174g/cm3,物质的量浓度为4.0mol/L。
则下列说法中不正确的是()
A.25℃时,饱和KCl溶液的浓度大于4.0mol/L
B.此溶液中KCl的质量分数为
C.20℃时,密度小于1.174g/cm3的KCl溶液是不饱和溶液
D.将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174g/cm3
D25℃时,KCl的溶解度比20℃的大,饱和KCl溶液的浓度也比20℃时高,选项A正确;
根据质量分数的含义可知选项B正确;
KCl溶液的密度越大,其溶液的浓度越大,密度小于1.174g/cm3的KCl溶液是不饱和溶液,选项C正确;
将20℃的饱和KCl溶液蒸发部分水后,再恢复到20℃溶液仍是饱和溶液,其密度应等于1.174g/cm3,选项D错误。
例4
(1)实验室里需用480mL1.0mol/L的NaOH溶液,下图是某学生在实验室配制该NaOH溶液的过程示意图。
请你回答有关问题。
①用已知质量为25.6g的表面皿,准确称取NaOH固体。
则应在托盘天平的右盘上放置砝码的质量是(最小的砝码质量为1.0g),然后将,在左盘的表面皿中加入NaOH固体,这时指针偏向右边,下面他的操作应该是;
②观察配制NaOH溶液的过程示意图,指出其中有错误的是(填操作序号)。
如果配制过程中没有等到溶液冷却到室温,则配制所得溶液的浓度将(填“偏高”、“偏低”、“不变”);
③在上述实验过程中,用到的容量瓶的规格是;
①45.0g游码移至标尺的0.6g处
向左盘中继续小心加NaOH至天平平衡
②①⑤偏高③500mL
练习
1、将ag无水Na2CO3溶于t℃的饱和Na2CO3溶液中,析出bg晶体,则(b-a)g表示的是
A、饱和溶液失去水的质量 B、饱和溶液失去溶质Na2CO3的质量
C、析出Na2CO3·
10H2O的质量 D、减少的饱和溶液的质量
2、Ca(OH)2在80℃时的溶解度为xg,20℃的溶解度为yg。
取80℃时的Ca(OH)2饱和溶液Ag,蒸发掉wg水后再恢复至20℃,滤去析出的固体,滤液中Ca(OH)2的质量分数为z%,则x、y、z的关系正确的是
A、x>y>z B、y<z<x C、z<y D、y<z
3、在一定温度下,向足量的饱和Cu(NO3)2溶液中加入1.88g无水Cu(NO3)2,搅拌后静置,最终析出Cu(NO3)2·
6H2O晶体质量为
A、等于2.96g B、大于2.96g
C、小于2.96g D、大于1.88g而小于2.96g
4、t℃时,CuSO4在水中的溶解度为25g,将32gCuSO4白色粉末加入ng水中形成CuSO4溶液并有CuSO4·
5H2O晶体析出,则n的取值范围是
A、18g<n<128g B、36g<n<180g
C、18g≤n≤128g D、36g≤n≤180g
5、某温度下碳酸钠饱和溶液的质量分数为a%,向其中加入mmol五水碳酸钠或nmol无水碳酸钠,可析出相同质量的十水碳酸钠,下列判断正确的是
A、a可能为40,m>n B、a可能为40,m=n
C、a可能为30,m>n D、a可能为30,m<n
6、在一定温度下向某饱和硫酸铜溶液中(过量)投入Wg无水CuSO4粉末,下列说法错误的是
A、析出的胆矾的质量与原硫酸铜溶液的质量有关
B、所得溶液中Cu2+的数目较原溶液中的少
C、析出胆矾的质量一定大于Wg
D、所得溶液的质量减少,但SO42-的浓度不变
7、60℃时mgKNO3的饱和溶液,恒温下蒸发部分溶剂,然后再使溶液逐渐
冷却至40℃。
能够正确表示此过程中溶液浓度a%与时间t关系的示意图是
8、在60℃恒温条件下,取200gA物质的溶液蒸发掉20g水后,析出10gA的无水晶体,再蒸发掉20g水后,又析出20gA的无水晶体,则原溶液中溶质的质量分数为
A、64.4% B、50.0% C、47.5% D、33.3%
9、欲使ag10%盐酸溶液的质量分数增大至20%,下列方法正确的是
A、加入0.1ag盐酸 B、加热蒸发掉一半的水
C、蒸发溶剂至溶液质量为0.4ag D、加入2ag25%的盐酸
10、一定温度下,石灰乳悬浊液中存在下列平衡:
Ca(OH)2(s)
Ca2+(aq)+2OH-(aq),当向一定量的石灰乳悬浊液中加入少量生石灰时,下列说法中正确的是
A、溶液中Ca2+数目减少 B、溶液中c(Ca2+)增大
C、溶液的pH增大 D、溶液中溶质的质量分数增大
11、若以w1和w2表示浓度为amol/L和bmol/L氨水的质量分数,且知2a=b,则下列推断正确的是
A、2w1=w2 B、2w2=w1 C、w2>2w1 D、w1<w2<2w1
12.相对分子质量为a的某物质在室温下的溶解度为6g,此时测得饱和溶液的密度为cg·
cm-3,则该饱和溶液的物质的x量浓度是()
A.
mol·
L-1B.
L-1
C.
L-1D.
L-16.实
13.实验室里需用
的硫酸铜溶液,现选取500mL容量瓶进行配制,以下操作正确的是()
A.称取7.68g硫酸铜,加入500mL水
B.称取12.0g胆矾配成500mL溶液
C.称取8.0g硫酸铜,加入500mL水
D.称取12.5g胆矾配成500mL溶液
14.用固体NaOH配制物质的量浓度溶液时,下列操作会导致溶液浓度偏高的是()
A.在烧杯中溶解时,有少量液体溅出B.样品中含有少量Na2O杂质
C.容量瓶使用前未干燥D.定容时仰视容量瓶刻度线
15.某种胃药片的制酸剂为碳酸钙,其中所含的制酸剂质量的测定如下:
①需配制0.1mol·
L-1的HCl溶液和0.1mol·
L-1的NaOH溶液②每次取一粒(药片质量均相同)0.2g的此胃药片,磨碎后加入20mL蒸馏水③以酚酞为指示剂,用0.1mol·
L-1的NaOH溶液滴定,需用去VxmL达滴定终点④加入25mL0.1mol·
L-1的HCl溶液
(1)写出全部实验过程的步骤_________。
(写编号顺序)
(2)如图所示的仪器中配制0.1mol·
L-1的NaOH溶液肯定不需要的仪器是_________(填序号),配制上述溶液还需用到的玻璃仪器是_________(填仪器名称)。
(3)配制上述溶液应选用的容量瓶规格分别为_________(填字母)。
A.50mL,50mLB.100mL,100mL
C.100mL,150mLD.250mL,250mL
(4)写出相关的化学反应方程式:
___________________________________。
(5)胃药中含碳酸钙的质量为:
_________g(写出计算式并加以文字说明)。
参考答案:
2
3
4
5
6
7
8
10
A
11
12
13
14
15
16
17
18
19
20
22.Ac=
23.D24B
26.
(1)①②④③②④③或②①④③②④③(3分)
(2)A、C(1分)烧杯、玻璃棒(1分)
(3)B(1分)
(4)CaCO3+2HCl=CaCl2+CO2↑+H2OHCl+NaOH=NaCl+H2O(2分)
(5)0.125-
或0.125-
(3分)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 物质
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
