 高考化学 考点汇总 考点7 电解质溶液Word文件下载.docx
高考化学 考点汇总 考点7 电解质溶液Word文件下载.docx
- 文档编号:17943926
- 上传时间:2022-12-12
- 格式:DOCX
- 页数:16
- 大小:176.79KB
高考化学 考点汇总 考点7 电解质溶液Word文件下载.docx
《高考化学 考点汇总 考点7 电解质溶液Word文件下载.docx》由会员分享,可在线阅读,更多相关《高考化学 考点汇总 考点7 电解质溶液Word文件下载.docx(16页珍藏版)》请在冰豆网上搜索。
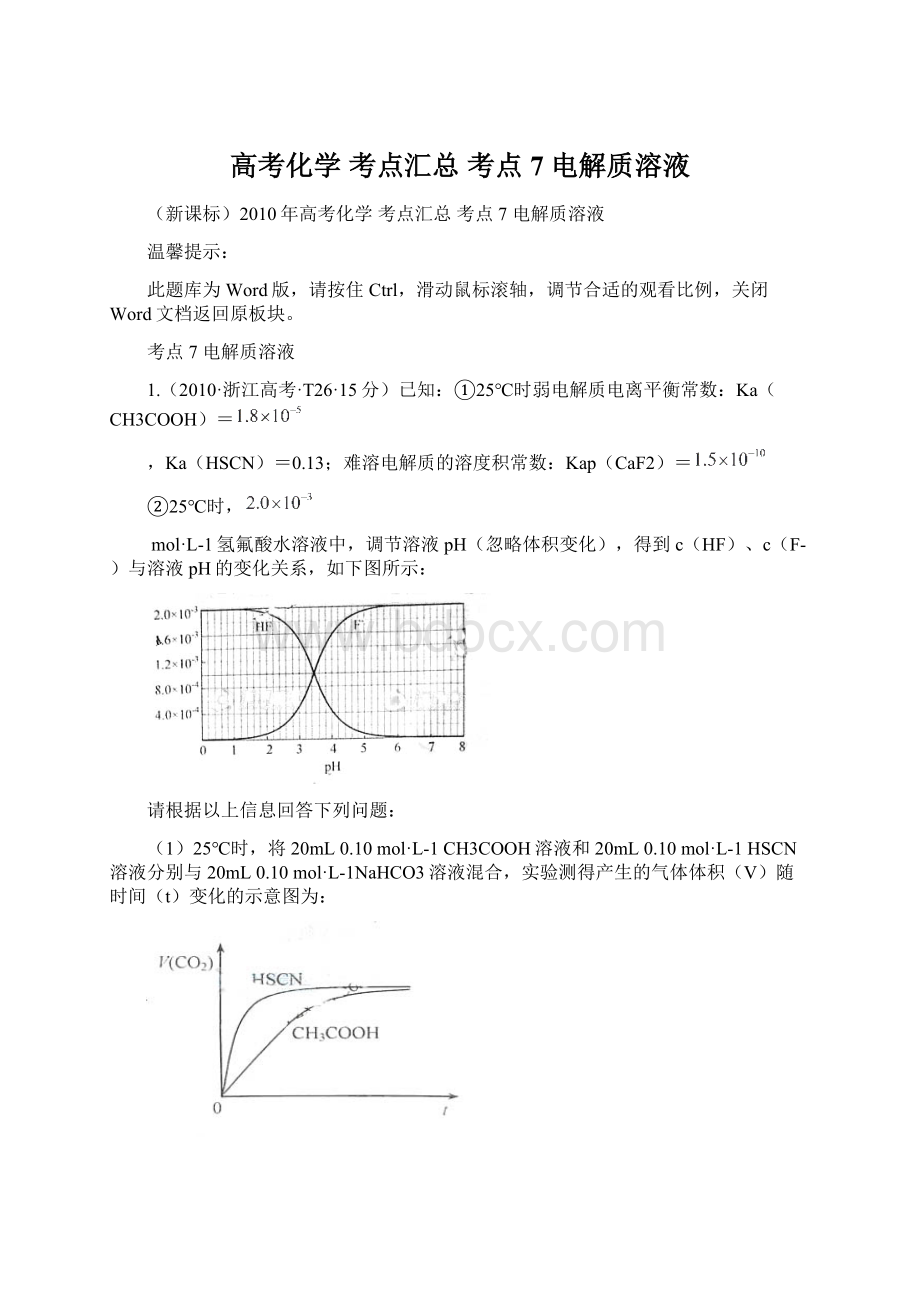
(F-)=5.1×
10-10>Kap(CaF2),故有沉淀产生。
答案:
(1)HSCN的酸性比CH3COOH强,其溶液中c(H+)大,故其溶液与NaHCO3溶液反应的速率较快<
(2)10-3.45(或3.5×
10-4)Ka(HF)=
,当c(F-)=c(HF)时,Ka(HF)=c(H+),查图中交点处即c(F-)=c(HF),故所对应的pH即为Ka的负对数,所以Ka(HF)=10-3.45。
(3)查图知,当pH=4.0时,溶液中的c(F-)=1.6×
L-1,溶液中
c(Ca2+)=2.0×
10-10>Kap(CaF2),故有少量沉淀产生。
【类题拓展】
沉淀的溶解与生成
(1)沉淀的溶解
在难溶电解质的溶液中当Q<Ksp时,就会使沉淀溶解。
①酸碱溶解法
加入酸或碱与平衡体系中的相应离子反应,降低离子浓度,使溶解平衡向溶解的方向移动。
如难溶于水的碳酸钙可以溶解于酸中等。
②发生氧化还原反应使沉淀溶解
如难溶于水的硫化铜等可以溶解于硝酸中。
③生成络合物使沉淀溶解
如难溶于水的氯化银可以溶解于氨水中。
(2)沉淀的生成
在难溶电解质的溶液中当Q>Ksp时,就会有沉淀生成。
在溶解平衡体系中加入与体系中相同的一种离子,就会使另一种离子沉淀出来;
在有多种离子的溶液中,当加入一种与它们都生成沉淀的离子时,生成的哪种沉淀的溶解度最小,就优先生成哪种沉淀。
2.(2010·
北京高考·
T10·
6分)下列解释实验事实的方程式不正确的是
A.0.1
/L
溶液的pH>1:
CH3COOH
CH3COO-+H+
B.“
球”浸泡在冷水中,颜色变浅2NO2(g)
N2O4(g)ΔH<0
(红棕色)(无色)
C.铁溶于稀硝酸,溶液变黄:
3Fe+8H++
3Fe2++2NO↑+4H2O
D.向Na2CO3溶液中滴入酚酞溶液,溶液变红:
CO32-+H2O
HCO3-+OH-
【命题立意】本题以常见实验为呈现形式,主要考查对反应原理的正确理解和化学用语的准确使用。
【思路点拨】对实验反应原理的正确理解和准确使用化学用语。
【规范解答】选C。
若
是强酸,则0.1
溶液的PH=1,现在PH>1,说明
是弱酸,因此A正确。
“
球”浸泡在冷水中,温度降低,颜色变浅,说明
2NO2(g)
N2O4(g)平衡正向移动,ΔH<0,故B正确。
铁溶于稀硝酸,溶液变黄,是因为生成了Fe3+,方程式为Fe+NO3-+4H+====Fe3+
+NO↑+2H2O,故C错误。
向Na2CO3溶液中滴入酚酞溶液,溶液变红,说明溶液呈碱性,CO32-+H2O
HCO3-+OH-,故D正确。
3.(2010·
T11·
6分)自然界地表层原生铜的硫化物经氧化、淋滤
作用后变成CuSO4溶液,向地下层渗透,遇到难溶的ZnS或PbS,慢慢转变为铜
蓝(CuS)。
下列分析正确的是
A.CuS的溶解度大于PbS的溶解度
B.原生铜的硫化物具有还原性,而铜蓝没有还原性
C.CuSO4与ZnS反应的离子方程式是
CuS↓
D.整个过程涉及的反应类型有氧化还原反应和复分解反应
【命题立意】本题以自然界中铜的转化为体现形式,主要考查沉淀溶解平衡的相关知识。
【思路点拨】考虑沉淀转化的实质。
【规范解答】选D。
沉淀转化的实质是溶解度小的沉淀转化成溶解度更小的沉淀,PbS转变为铜蓝
(CuS),说明CuS的溶解度小于PbS的溶解度;
原生铜的硫化物具有还原性,
而铜蓝也应该具有还原性,因为硫元素处于最低价态—2价;
CuSO4与ZnS反应
的离子方程式应该是Cu2++ZnS=CuS+Zn2+,这是一个复分解反应;
自然界地表
层原生铜的硫化物被氧化的过程是氧化还原反应,故只有D正确。
4.(2010·
福建理综·
6分)下列关于电解质溶液的正确判断是
A.在pH=12的溶液中,
、Cl-、
、
可以大量共存
B.在pH=0的溶液中,
C.由0.1mol·
一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH=
D.由0.1mol·
一元酸HA溶液的pH=3,可推知NaA溶液存在A-+H2O
HA+OH-
【命题立意】本题主要考查考生对电解质溶液中的离子共存、弱电解质的电离以及盐的水解的掌握情况,这部分内容的考查形式一般是将盐类水解与弱电解质的电离、pH等知识融合在一起进行综合考查。
【思路点拨】解答本题应注意以下几个问题:
(1)做离子共存问题要特别注意题设条件,同时要注意把握能反应的离子。
(2)注意弱电解质的电离特点(3)注意判断pH与盐水解的关系。
选项A:
pH=12的溶液呈碱性含有比较多的OH-,不能与HCO3-共存,A是错误选项;
选项B:
pH=0的溶液呈酸性含有较多的H+,在NO3-存在的情况下,亚硫酸根离子容易被氧化成硫酸根离子,无法共存,B是错误选项。
选项C:
0.1mol/L的一元碱的pH=10表明该一元碱在溶液中不能完全电离,是弱碱、弱电解质,电离方程式应该用可逆号。
C是错误选项。
选项D:
由题意可得该酸是弱酸,在NaA溶液中A-会发生水解而使溶液呈碱性,D项正确,选D。
【类题拓展】判断离子共存的规律方法:
1.若题目限定了颜色,如限定溶液无色,则有颜色的离子不能存在。
2.在强酸性溶液中,OH-及弱酸根离子均不能大量共存;
在强碱性溶液中,H+及弱碱阳离子均不能大量共存;
而酸式弱酸根离子在以上两种溶液中均不能大量共存。
3.能发生复分解反应、氧化还原反应、络合反应以及双水解完全的离子均不能共存。
4.做离子共存问题时,应该注意隐含条件的挖掘,如“在无色透明溶液中”、“在强碱性溶液中”、“因发生氧化还原反应而不能大量共存的”等等。
5.(2010·
广东高考·
T12·
4分)HA为酸性略强于醋酸的一元弱酸,在0.1mol·
L-1
NaA溶液中,离子浓度关系正确的是
A.c(Na+)>c(A-)>c(H+)>c(OH-)
B.c(Na+)>c(OH-)>c(A-)>c(H+)
C.c(Na+)+c(OH-)=c(A-)+c(H+)
D.c(Na+)+c(H+)=c(A-)+c(OH-)
【命题立意】本题主要考查离子浓度的关系,是最近几年高考常考试题,属于拔高题,同学们要进行专题训练才可以熟练掌握其解题技巧。
【思路点拨】看到不等式想到盐类水解、弱电解质电离
分析题干中酸性强弱→看选项→
看到等式想到三守恒(物料守恒、电荷守恒、质子守恒)
A明显错误,因为阳离子浓度都大于阴离子浓度,电荷不守恒;
D是电荷守恒,正确。
NaA的水解是微弱的,故c(A-)>c(OH-),B错;
C的等式不符合任何一个守恒关系,是错误的;
【类题拓展】比较盐溶液中离子浓度间的大小关系.
1.一种盐溶液中各种离子浓度的相对大小
①当盐溶液中阴、阳离子等价时
[不水解离子]>[水解的离子]>[水解后呈某性的离子(如H+或OH-)]>[显性对应离子如OH—或H+]
实例:
a.CH3COONa溶液b.NH4Cl溶液
a.[Na+]>[CH3COO-]>[OH-]>[H+]
b.[Cl-]>[NH4+]>[H+]>[OH-]
②当盐中阴、阳离子不等价时。
要考虑是否水解,水解分几步,如多元弱酸根的水解,则是“几价分几步,为主第一步”,实例:
Na2S水解分两步
S2—+H2OHS—+OH—(主要)
HS—+H2OH2S+OH—(次要)
各种离子浓度大小顺序为:
[Na+]>[S2—]>[OH—]>[HS—]>[H+]
2.两种电解质溶液混合后各种离子浓度的相对大小:
①若酸与碱恰好完全反应,则相当于一种盐溶液。
②若酸与碱反应后尚有弱酸或弱碱剩余,则一般弱电解质的电离程度>盐的水解程度。
3.溶液中各种微粒浓度之间的关系
以Na2S水溶液为例来研究
(1)写出溶液中的各种微粒
阳离子:
Na+、H+
阴离子:
S2-、HS-、OH-
分子:
H2S
(2)利用守恒原理列出相关方程
①电荷守恒:
[Na+]+[H+]=2[S2-]+[HS-]+[OH-]
②物料守恒:
Na2S====2Na++S2-
若S2—已发生部分水解,S原子以三种微粒存在于溶液中,[S2-]、[HS-]、[H2S],根据S原子守恒及与Na+的关系可得.
[Na+]=2[S2-]+2[HS-]+2[H2S]
③质子守恒
H2OH++OH-
由H2O电离出的[H+]=[OH—],水电离出的H+部分被S2—结合成为HS—、H2S,根据H+(质子)守恒,可得方程:
[OH-]=[H+]+[HS-]+2[H2S]
小结:
溶液中的几个守恒关系
(1)电荷守恒:
电解质溶液呈电中性,即所有阳离子所带的正电荷总数与所有阴离子所带的负电荷总数代数和为零。
(2)物料守恒(原子守恒):
即某种原子在变化过程(水解、电离)中数目不变。
(3)质子守恒:
即在纯水中加入电解质,最后溶液中[H+]与其他微粒浓度之间的关系式(由电荷守恒及质子守恒推出)
6.(2010·
安徽高考·
T13·
6分)将0.01mol下列物质分别加入100mL蒸馏水
中,恢复至室温,所得溶液中阴离子浓度的大小顺序是(溶液体积变化忽略不
计)
①Na2O2②Na2O③Na2CO3④NaCl
A.①>
②>
③>
④B.①>
④>
③
C.①=②>
④D.①=②>
③=④
【命题立意】本题考查了溶液中离子浓度大小的比较。
【思路点拨】注意Na2O2、Na2O与水反应产物;
同时考虑CO32-水解。
①②溶于水,溶质都是NaOH,且物质的量都为0.02moL,且二者与水反应时消耗的水的物质的量相同。
故反应后溶液体积相同,故①=②;
③中CO32-水解,溶液中出现了OH-、HCO3-,故溶液中阴离子浓度稍大于④;
故C正确。
7.(2010·
海南高考·
T2·
2分)常温下,将0.1mol·
L-1氢氧化钠溶液与
0.06mol·
L-1硫酸溶液等体积混合,该混合溶液的pH等于
A.1.7B.2.0C.12.0D.12.4
【命题立意】本题以酸、碱混合时溶液pH的计算为载体,考查溶液pH的计算方法和计算能力。
【思路点拨】酸、碱混合时溶液pH计算的步骤:
(1)首先判断混合后溶液的酸碱性。
(2)若为酸性,计算剩余H+的浓度,再求出pH。
(3)若为碱性,先计算剩余OH-的浓度,再通过Kw求出c(H+),最后求pH。
【规范解答】选B。
设两溶液的体积均为1L,OH-的物质的量为0.1mol·
L-1×
1L=0.1mol,因H+的浓度是硫酸浓度的2倍,即0.06mol·
2=0.12mol·
L-1,故H+的物质的量为0.12mol·
1L=0.12mol,H+的物质的量大于OH-的物质的量,混合后,溶液呈酸性;
混合反应后剩余H+的物质的量浓度为(0.12mol-0.1mol)÷
(1L+1L)=0.01mol·
L-1,溶液的pH=-lgc(H+)=2。
【类题拓展】两两混合溶液的pH的计算方法
(1)强酸与强酸混合:
先求出混合后的c(H+)混,c(H+)混=
,再根据公式计算pH。
(2)强碱与强碱混合:
先求出混合后c(OH-),c(OH-)混=
,再通过Kw求出c(H+),再计算pH。
(3)强酸与强碱混合:
强酸与强碱混合实质为中和反应,可以有以下三种情况:
①若恰好中和,pH=7。
②若酸剩余,先求出中和后剩余的c(H+),再计算pH。
③若碱剩余,先求出中和后剩余的c(OH-),再通过Kw求出c(H+),最后计算
pH。
8.(2010·
T5·
2分)已知:
Ksp(AgCl)=1.8×
10—10,Ksp(AgI)=1.5×
10—16,
Ksp(Ag2CrO4)=2.0×
10—12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的
是
A.AgCl>
AgI>
Ag2CrO4 B.AgCl>
Ag2CrO4>
AgI
C.Ag2CrO4>
AgCl>
AgI D.Ag2CrO4>
AgCl
【命题立意】本题考查了难溶电解质的溶解平衡,Ksp的概念及计算。
【思路点拨】解答此题注意两点:
(1)首先书写出3种难溶电解质Ksp的表达式。
(2)找出每种难溶电解质电离出的阴、阳离子浓度间的关系。
Ag++Cl—,AgCl饱和溶液中Ag+和Cl—的浓度相等,Ksp(AgCl)=c(Ag+)×
c(Cl—)=c2(Ag+),故AgCl饱和溶液中c(Ag+)=
=
×
10—5mol·
L-1;
同理AgI饱和溶液中c(Ag+)=
10—8mol·
Ag2CrO4
2Ag++CrO42-,Ag2CrO4饱和溶液中2c(CrO42—)=c(Ag+),Ksp(Ag2CrO4)=c2(Ag+)×
c(CrO42-)=c3(Ag+)/2,故Ag2CrO4饱和溶液中c(Ag+)=
10-4mol·
Ag+浓度大小顺序是Ag2CrO4>
AgI。
9.(2010·
T6·
2分)光谱研究表明,易溶于水的SO2所形成的溶液中存在着下列平衡:
据此,下列判断中正确的是
A.该溶液中存在着SO2分子
B.该溶液中H+浓度是SO2-3浓度的2倍
C.向该溶液中加入足量的酸都能放出SO2气体
D.向该溶液中加入过量NaOH可得到Na2SO3、NaHSO3和NaOH的混合溶液
【命题立意】本题考查化学反应平衡及弱电解质的电离平衡的理解和应用,考查的知识点有:
平衡的特点、外界因素对平衡的影响。
【思路点拨】在平衡体系中,所有物质均同时共存,外部条件改变,平衡发生移动,判断平衡移动的方向。
【规范解答】选A。
因上述变化均为可逆反应,故均不能反应完全,所以溶液中存在着SO2、SO2·
xH2O、H+、HSO3—、SO32—等微粒,A正确C错误。
SO2·
xH2O
H++HSO3—+(x-1)H2O、HSO3—
H++SO32—均为可逆反应,所以SO2·
xH2O电离出的HSO3—没有完全电离成H+和SO32—,故H+浓度不是SO2-3浓度的2倍,B错误;
向该溶液中加入过量NaOH,NaOH消耗H+,使平衡HSO3—
H++SO32—向右移动,HSO3—几乎完全电离,故不存在NaHSO3,D错误。
10.(2010·
江苏高考·
4分)常温下,用0.1000mol·
L-1NaOH溶液滴
定20.00mL0.1000mol·
L-1CH3COOH溶液,滴定曲线如图。
下列说法正确的是
A.点①所示溶液中:
c(CH3COO—)+c(OH—)=c(CH3COOH)+c(H+)
B.点②所示溶液中:
c(Na+)=c(CH3COOH)+c(CH3COO—)
C.点③所示溶液中:
c(Na+)>
c(OH—)>
c(CH3COO—)>
c(H+)
D.滴定过程中可能出现:
c(CH3COOH)>
c(H+)>
c(OH—)
【命题立意】本题以NaOH溶液滴定CH3COOH溶液滴定曲线图为背景,考查滴定过程中不同阶段离子浓度的大小关系,体现化学的真实性。
【思路点拨】注意滴定过程的阶段性,针对不同阶段对应的溶液,分析离子浓
度大小关系。
A项,点①时加入的NaOH溶液为10.00mL,所得溶液相当于等物质的量浓度的CH3COOH与CH3COONa的混合溶液,此时溶液中电荷守恒关系式为:
c(CH3COO—)+c(OH—)=c(Na+)+c(H+),等物质的量浓度的CH3COOH与CH3COONa的混合溶液中CH3COOH的电离程度大于CH3COO—的水解程度,c(Na+)>
c(CH3COOH),A项错;
B项,点②所示溶液pH=7,c(OH—)=c(H+),此时溶液中电荷守恒关系式为:
c(CH3COO—)+c(OH—)=c(Na+)+c(H+),所以c(Na+)=c(CH3COO—),B项错;
C项,点③所示溶液碱性较弱,c(CH3COO—)应大于c(OH—),C项错;
D项,当加入少量的NaOH溶液,此时溶液相当于少量CH3COONa与较多量的CH3COOH的混合溶液,离子浓度可能出现:
c(OH—),D项正确。
【类题拓展】离子浓度大小关系式通常有等式和不等式两种
1.等式
对于等式通常有三个,即电荷守恒、物料守恒、质子守恒,一些复杂的等式往往是对三个守恒关系式经过变形而得,或代入某些题给已知条件而得。
2.不等式
对于不等式,要具体分析溶液中各种电离方程式、水解离子方程式、溶液的酸碱性,对于连写的不等式,要注意抓住一些明显的错误,只要有一处错误整个式子就错了。
11.(2010·
山东高考·
T14·
4分)下列与实验相关的叙述正确的是
A.稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中
B.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出
C.酸碱滴定时,若加入待测液前用待测液润洗锥形瓶,将导致测定结果偏高
D.检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCL2溶液和稀盐酸
【命题意图】考查实验基本操作知识、教材中几个重要实验所涉及的误差分析及离子检验。
稀释浓硫酸的操作是“酸入水”,故A错;
配制溶液时,若将多余的水取出,会使浓度偏小,加水超过容量瓶刻度线的唯一办法是重新配制,故B错;
用待测液润洗锥形瓶,则消耗的标准液会偏多,导致结果偏高,C正确;
D的操作中,若溶液中含有Ag+,也会有不溶解于盐酸的白色沉淀生成,故D错。
12.(2010·
T15·
4分)某温度下,
(s)、
(s)分别在
溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。
据图分析,下列判断错误的是
A.
<
B.加适量NH4Cl固体可使溶液由a点变到b点
C.c、d两点代表的溶液中c(H+)与c(OH-)乘积相等
D.
分别在b、c两点代表的溶液中达到饱和
【命题意图】借助沉淀溶解平衡曲线,考查对沉淀溶解平衡的计算,外界因素对水的离子积的影响等。
【思路点拨】比较KSP时注意要找到基准点;
水的离子积不受浓度的影响,只受温度的影响;
沉淀溶解平衡曲线上的点表示饱和状态,下方上的点表示不饱和状态。
A项,b、c两点金属阳离子的浓度相等,设都为x,分别对应的c(OH-)=KW/c(H+)=10-12.7,c(OH-)=KW/c(H+)=10-9.6,Ksp[Fe(OH)3]=x×
(10-12.7)3、Ksp[Cu(OH)2]=X×
(10-9.6)2,Ksp[Fe(OH)3]<Ksp[Cu(OH)2],故A正确;
由a点到b点的碱性增强,而NH4Cl溶解于水后水解显酸性,故B错;
温度一定,溶液中的Kw为定值,故C正确;
溶度积曲线上的点代表的溶液都是饱和溶液,曲线左下方的点都不饱和,右上方的点都是QC>KSP,要析出沉淀,故D正确。
1.公式:
对于沉淀溶解平衡:
MmNn(s)
mMn+(aq)+nNm-(aq)。
固体纯物质不列入平衡常数。
上述反应的平衡常数为:
Ksp=[c(Mn+)]m[c(Nm-)]n,符号为Ksp
2.影响因素:
在一定的温度下,它是一个常数,称为溶度积常数,简称溶度积,它只受温度影响,不受溶液中物质浓度的影响。
3.溶度积的应用:
通过比较溶度积和溶液中有关离子浓度幂的乘积(离子积QC)的相对大小,可以判断难溶电解质在给定条件下沉淀能否生成或溶解。
QC>Ksp溶液过饱和,有沉淀析出,直至溶液饱和达到新的平衡状态
QC=Ksp溶液饱和,沉淀与溶解处于平衡状态
QC<Ksp溶液未饱和,无沉淀析出,若加入过量难溶电解质,难溶电解质溶解直至溶液饱和。
13.(2010·
天津高考·
T4·
6分)下列液体均处于25℃,有关叙述正确的是
A.某物质的溶液pH<
7,则该物质一定是酸或强酸弱碱盐
B.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍
C.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同
D.pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>
c(CH3COO-)
【命题立意】综合考查了电解质溶液中的有关知识,包括盐类的水解、溶液的pH与c(H+)的关系、沉淀溶解平衡的移动和溶液中离子浓度大小的比较。
【思路点拨】利用电荷守恒式可以比较离子浓度的大小。
某些强酸的酸式盐pH<7,如NaHSO4,故A项错误;
pH=4.5,c(H+)=10-4.5mol·
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考化学 考点汇总 考点7 电解质溶液 高考 化学 考点 汇总 电解质 溶液
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
