 高考三轮冲刺专题工艺流程一Word下载.docx
高考三轮冲刺专题工艺流程一Word下载.docx
- 文档编号:17856161
- 上传时间:2022-12-11
- 格式:DOCX
- 页数:13
- 大小:683.74KB
高考三轮冲刺专题工艺流程一Word下载.docx
《高考三轮冲刺专题工艺流程一Word下载.docx》由会员分享,可在线阅读,更多相关《高考三轮冲刺专题工艺流程一Word下载.docx(13页珍藏版)》请在冰豆网上搜索。
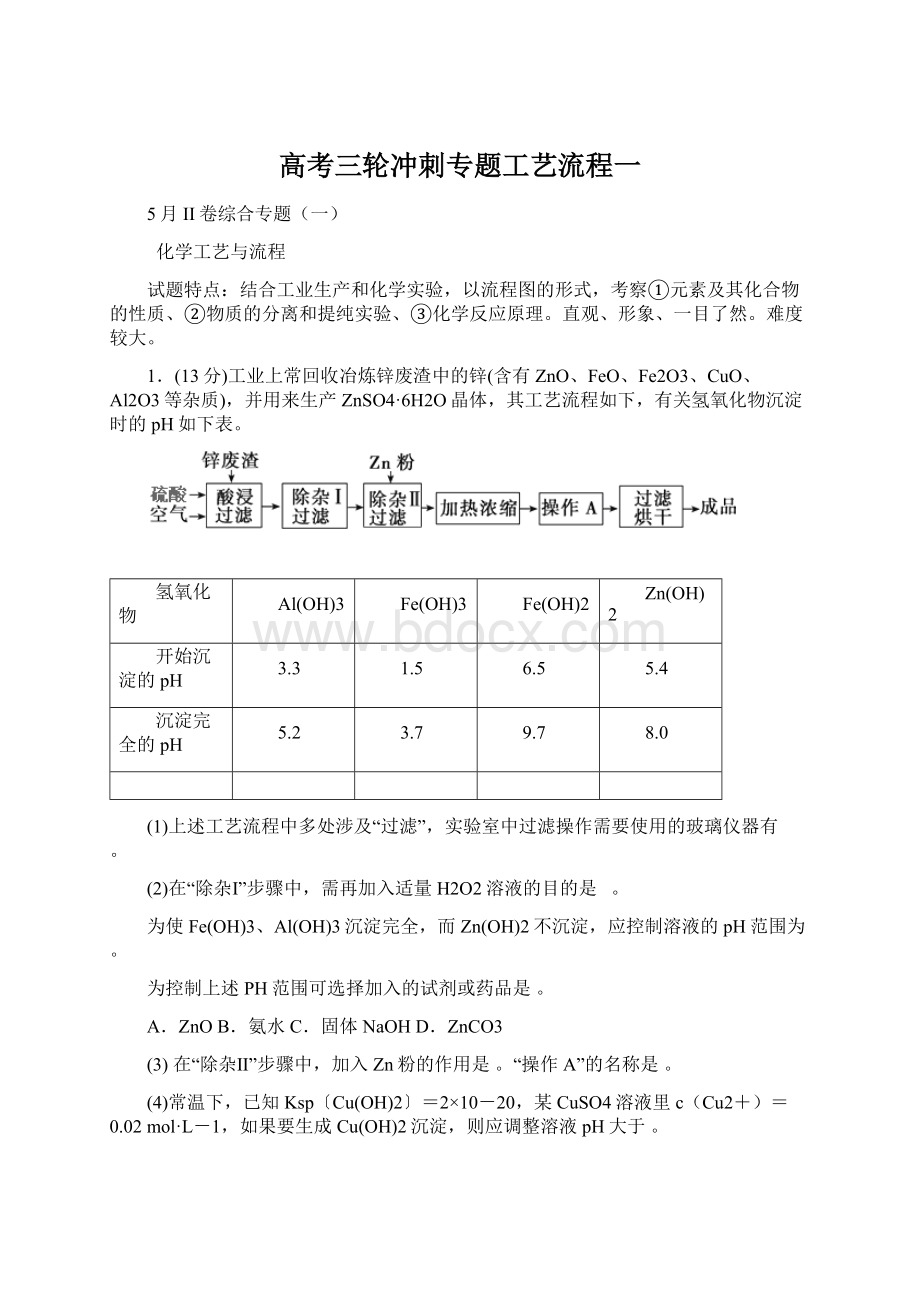
9.7
8.0
(1)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有。
(2)在“除杂Ⅰ”步骤中,需再加入适量H2O2溶液的目的是。
为使Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为。
为控制上述PH范围可选择加入的试剂或药品是。
A.ZnOB.氨水C.固体NaOHD.ZnCO3
(3)在“除杂Ⅱ”步骤中,加入Zn粉的作用是。
“操作A”的名称是。
(4)常温下,已知Ksp〔Cu(OH)2〕=2×
10-20,某CuSO4溶液里c(Cu2+)=0.02mol·
L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于。
2.(14分)硫酸亚锡(SnSO4)是一种重要的硫酸盐,广泛应用于镀锡工业。
某研究小组设计SnSO4制备路线如下:
查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡,Sn相对原子质量为119
回答下列问题:
(1)锡原子的核电荷数为50,与碳元素属于同一主族,锡元素在周期表中的位置是。
(2)操作Ⅰ是。
(3)SnCl2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因。
(4)加入Sn粉的作用有两个:
①调节溶液pH②。
(5)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是。
(6)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是。
(7)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:
Sn+2HCl===SnCl2+H2↑;
②加入过量的FeCl3;
③用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:
6FeCl2+K2Cr2O7+14HCl===6FeCl3+2KCl+2CrCl3+7H2O
取1.226g锡粉,经上述各步反应后,共用去0.100mol/LK2Cr2O7溶液32.0ml。
锡粉中锡的质量分数是。
3.(14分)某矿渣的成分为Cu2O、Al2O3、Fe2O3、SiO2,工业上用该矿渣获取铜和胆矾的操作流程如下:
已知:
①Cu2O+2H+=Cu+Cu2++H2O
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)为了加快反应I的速率,可以采取的措施是(写2点)。
(2)固体混合物A中的成分是
(3)反应I完成后,铁元素的存在形式为(填离子符号);
写出生成该离子的离子方程式
(4)操作1主要包括:
、、。
洗涤CuSO4•5H2O粗产品不能用大量水洗,而用冰水洗涤。
原因是
(5)用惰性电极电解胆矾溶液一段时间,加人0.1moI的Cu可恢复溶液原况(浓度、成分),则电解时转移电子的物质的量为
(6)用NaCl0调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式为
4.(17分)Ⅰ.某矿样含有大量的CuS、少量铁的氧化物及少量其它不溶于酸的杂质。
某化学课外小组设计以下流程,以该矿样为原料生产CuCl2·
2H2O晶体。
(1)在焙烧过程产生的尾气中,有一种是主要的大气污染物。
若在实验室中以碱液吸收处理之,下列装置可行的是_________(填字母)。
(2)步骤②酸浸过程中,需要用到3mol·
L-1的盐酸100mL,配制该盐酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器有_________________________;
(3)步骤④中,加入的X物质可以是________,作用是_____________。
Ⅱ.已知FeSO4在高温下分解生成Fe2O3、SO3和SO2用下图所示装置设计实验,检验FeSO4在高温下分解生成的气态物质,并测定已分解的FeSO4质量.
已知:
B装置、烧瓶E中所加试剂依次为氢氧化钠溶液、水(滴有数滴BaCl2溶液),请回答下列问题:
(1)D装置中所加试剂名称_____________________________________________。
(2)按气流方向连接各仪器,用字母表示接口的连接顺序:
c→_______________→e。
(3)检验后,用烧瓶E中混合物测定已分解的FeSO4质量,此实验操作的第一步:
_________________________________________;
第二步:
过滤混合物,在过滤器上将沉淀洗净后,灼烧并冷却至室温,称量其质量为ag,再次灼烧冷却至室温称量其质量为bg,且b<
a,继续灼烧、冷却并称重,直到连续两次称量的质量差不超过0.1g为止。
(4)若最终得到沉淀cg,则已经分解的FeSO4质量________________(填计算式)。
5.(14分)铬铁矿是最难分解的矿石之一,加工前需将矿样充分粉碎。
其主要成分可表示为FeO·
Cr2O3,还含有SiO2、Al2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的过程如下图所示。
请回答:
(1)煅烧前应将铬铁矿充分粉碎,其目的是____。
灼烧是中学化学中常用的操作方法。
如在实验室中将铬铁矿和NaOH固体混合物灼烧,从以下各实验仪器中选择必要的有。
A.陶瓷坩埚B.铁坩埚C.三脚架D.泥三角
(2)煅烧过程中FeO·
Cr2O3发生反应的化学方程式是。
(3)制备过程中杂质SiO2、Al2O3最终分别以(写化学式)____、____的形式被除去。
(4)向黄色的滤液2中加稀硫酸,观察到溶液逐渐变为橙色。
请结合化学平衡原理和必要的文字,对此过程给予合理解释。
(5)向Na2Cr2O7溶液加入KC1固体,获得K2Cr2O7晶体能庙橐作并衣次是:
加热浓缩、____、过滤、洗涤、干燥。
6.(16分)电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质,工业上通过“中温焙烧-钾氧化法”回收K2Cr2O7等物质。
①水浸后溶液中存在K2CrO4、KAlO2、K2ZnO2等物质
②除去滤渣2后,溶液中存在如下反应:
2CrO2-4+2H+
Cr2O2-7+H2O
(1)水浸后的溶液呈(填“酸”、“碱”、“中”)性
(2)完成氧化焙烧过程中生成K2CrO4的化学方程式。
Cr(OH)3+K2CO3+K2CrO4+CO2+________
(3)滤渣2的主要成分有Zn(OH)2、
(4)“系列操作”中为:
继续加入H2SO4,冷却结晶,过滤.继续加入H2SO4目的是________________________________________________________________。
(5)工业上还可以在水浸过滤后的K2CrO4溶液中加入适量H2SO4,用石墨做电极电解生产金属铬,写出生成铬的电极反应方程式:
_________________________________。
7.(16分)工业上利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等金属,回收流程如下:
CaSO4
已知部分物质沉淀的pH及CaSO4的溶解度曲线如下:
Fe3+
Cu2+
Cr3+
开始沉淀pH
2.1
4.7
4.3
完全沉淀pH
3.2
6.7
a
(1)在浸出过程中除了生成Fe2(SO4)3、Cr2(SO4)3外,主要还有
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:
①加入石灰乳调节pH到;
②将浊液加热到80℃,。
(3)写出还原步骤中加入NaHSO3生成Cu2O固体的离子反应方程式,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是。
(4)当离子浓度≤1×
10—5mol•L-1认为沉淀完全,若要使Cr3+完全沉淀则要保持C(OH—)≥。
Ksp[Cr(OH)3]=6.3×
10-31,
)
8.(10分)水钴矿中除SiO2外,还有9.24%CoO、2.78%Fe2O3、0.96%MgO、0.084%CaO。
从中提取钴的主要工艺流程如下:
(1)请配平下列除铁的化学方程式:
Fe2(SO4)3+H2O+Na2CO3=Na2Fe6(SO4)4(OH)12↓+Na2SO4+CO2↑
(2)“除钙、镁”的原理反应为:
MgSO4+2NaF=MgF2↓+Na2SO4;
CaSO4+2NaF=CaF2↓+Na2SO4
已知KSP(CaF2)=1.11×
10-10,KSP(MgF2)=7.40×
10-11,加入过量NaF溶液反应完全后过滤,则滤液中
。
(3)“沉淀”中含杂质离子主要有SO42-、F-、和;
“操作X”包括和。
(4)向氯化铜溶液中加入一定量的铁粉和铝粉混合物,充分反应后,下列情况可能出现的是________(填编号)
a.溶液中有Cu2+、Fe2+、Al3+,不溶物为Cu
b.溶液中有Fe2+、Al3+,不溶物为Cu、Fe
c.溶液中有Fe3+、Al3+,不溶物为Cud.溶液中有Fe2+,不溶物为Cu、Al
(5)某锂离子电池正极是LiCoO2,含Li+导电固体为电解质。
充电时,Li+还原为Li,并以原子形式嵌入电池负极材料碳-6(C6)中(如图所示)。
电池反应为LiCoO2+C6CoO2+LiC6,写出该电池放电时的正极反应式。
9.(16分)锅炉水垢既会降低燃料的利用率、影响锅炉的使用寿命,还可能造成安全隐患。
(1)某锅炉水垢的主要成分有CaCO3、CaSO4、Mg(OH)2、Fe2O3,用酸洗法可除去该水垢,其基本原理如下图所示。
①酸洗时,为使水垢尽可能溶解,不宜选用的是(填标号)。
A.稀硫酸B.盐酸C.硝酸D.醋酸
②不溶物用碳酸钠溶液浸泡时,反应的离子方程式是。
③洗出液中的Fe3+会腐蚀铁质管道,反应的离子方程式是,因此,常在洗出液中加入具有强还原性的SnCl2溶液,反应中的Sn2+与Fe3+的物质的量之比为1∶2,Sn2+转化为②(填离子符号)。
④柠檬酸(用H3R表示)可用作酸洗剂,溶液中H3R、H2R-、HR2-、R3-的含量与pH的关系如右图所示。
图中a曲线所代表的微粒的百分含量随溶液pH的改变而变化的原因是。
调节柠檬酸溶液的pH=4,有利于除去水垢中的氧化铁。
pH=4时,溶液中上述4种微粒含量最多的是。
(2)利用如右图所示装置对锅炉水(含Ca2+、Mg2+、HCO3—)进行预处理,可有效防止锅炉水垢的形成。
电解过程中,Ca2+、Mg2+在(填“a”或“b”)极附近形成沉淀。
化学工艺与流程
1.
(1)烧杯、玻璃棒、漏斗(3分);
(2)将Fe2+完全氧化为Fe3+,便于完全沉淀(2分);
5.2~5.4(2分);
AD(2分)
(3)除去溶液中的Cu2+(1分);
冷却结晶(1分) (4)5(2分)
2.(14分)
(1)五周期ⅣA族(2分)
(2)加热浓缩、冷却结晶、过滤、洗涤(2分)
(3)SnCl2+H2O
Sn(OH)Cl+HCl,加入盐酸,使该平衡向左移动,抑制Sn2+水解(2分)
(4)防止Sn2+被氧化(2分)
(5)Sn2++CO32-===SnO↓+CO2↑(2分)
(6)Sn2++H2O2+2H+===Sn4++2H2O(2分)
(7)93.2%(2分)
4.(17分)
Ⅰ.
(1)AB(2分)
(2)量筒、100ml容量瓶(2分)(3)CuO【或Cu(OH)2、CuCO3、Cu2(OH)2CO3】
(2分)调节溶液的PH,除去Fe3+(2分)
Ⅱ.
(1)品红溶液(2分)
(2)abfgd(2分)(3)向E中逐滴加入氯化钡溶液,直到不再产生新的沉淀为止(2分)
(4)c×
152×
2/233g(3分)
5.(14分,每空2分)
(1)增大表面积,提高反应速率,反应更充分;
BCD
(2)4FeO·
Cr2O3+7O2+20NaOH=8Na2CrO4+4NaFeO2+10H2O
(3)H2SiO3和Al(OH)3
(4)由于2CrO42-+2H+
Cr2O72-+H2O的存在,加稀硫酸增大了H+的浓度,平衡正向移动,使CrO42-浓度减小,Cr2O72-浓度增大,溶液由黄色变为橙色。
(5)冷却结晶
6(16分)
(1)碱(2分)
(2)4Cr(OH)3+4K2CO3+3O2
4K2CrO4+4CO2+6H2O(4分)
(3)Al(OH)3(2分)
(4)蒸发浓缩(2分),促进平衡CrO2-4+2H+⇌Cr2O2-7+H2O向正反应方向移动,尽可能生成更多溶解度更大的K2Cr2O7(3分)
(5)CrO2-4+8H++8e-=Cr+4H2O(3分)
7.
(1)CuSO4(3分)
(2)①3.2(2分)②趁热过滤(2分)(3)2H2O+HSO3—+2Cu2+=Cu2O↓+SO42—+5H+(3分);
产生SO2污染环境(3分)(4)4.0×
10-9mol•L-1(3分)
8.(10分)
(1)3,6,6,1,5,6(2分)
3Fe2(SO4)3+6H2O+6Na2CO3=Na2Fe6(SO4)4(OH)12↓+5Na2SO4+6CO2↑
(2)1.5(2分)
(3)NH4+(1分)、Na+(1分);
洗涤(1分)、干燥(1分);
(4)ab(2分)(5)CoO2+Li++e-=LiCoO2(2分)
9.(16分)
(1)①A(2分)②CaSO4+CO32-
CaCO3+SO42-(3分)
③2Fe3++Fe=3Fe2+(3分)Sn4+(2分)
④随溶液pH增大,平衡H3R
H2R-+H+向右移动,所以,H3R的百分含量减小(2分)H2R-(2分)
(2)b(2分)
10.(15分)
(1)TiO2++3H2O
H4TiO4+2H+;
将溶液中的Fe3+还原为Fe2+,消耗溶液中的H+促进TiO2+水解(两点答出一点给1分)
(2)H4TiO4
TiO2+2H2O;
TiO2+4e-==Ti+2O2-
(3)Fe2++2HCO==FeCO3↓+CO2↑+H2O;
(1分,其余均为2分)
(4)防止Fe2+被空气中的氧气氧化(5)165.9
11.(14分)Ⅰ:
(1)250mL容量瓶(1分,漏掉“250mL”0分)
(2)①升高反应温度,②搅拌,③过滤后再向滤渣中加入硫酸(多次浸取),④适当延长浸取时间(只要答出任意一点即可,其它答案合理亦可)(1分)(3)1,3,11H2O,2,1(2分,错写、漏写0分)(4)氧化+3价Cr使之转变成+6价Cr(或氧化Cr3+为Cr2O72-),以便于与杂质离子分离(2分,第一句意思表达出来2分)
Fe3+和Al3+(2分,各1分,漏写1分,出现错误0分,不写成离子符号0分)
(5)Ca2+、Mg2+(2分,各1分,漏写1分,出现错误0分,不写成离子符号0分)
Ⅱ:
Fe-2e-=Fe2+(2分),8.48(全对2分,若多写单位,扣1分)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 三轮 冲刺 专题 工艺流程
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《雷雨》中的蘩漪人物形象分析 1.docx
《雷雨》中的蘩漪人物形象分析 1.docx
