 人教版高中化学学业水平测试知识点必修1、2化学与生活总结.doc
人教版高中化学学业水平测试知识点必修1、2化学与生活总结.doc
- 文档编号:1776631
- 上传时间:2022-10-24
- 格式:DOC
- 页数:16
- 大小:281.50KB
人教版高中化学学业水平测试知识点必修1、2化学与生活总结.doc
《人教版高中化学学业水平测试知识点必修1、2化学与生活总结.doc》由会员分享,可在线阅读,更多相关《人教版高中化学学业水平测试知识点必修1、2化学与生活总结.doc(16页珍藏版)》请在冰豆网上搜索。
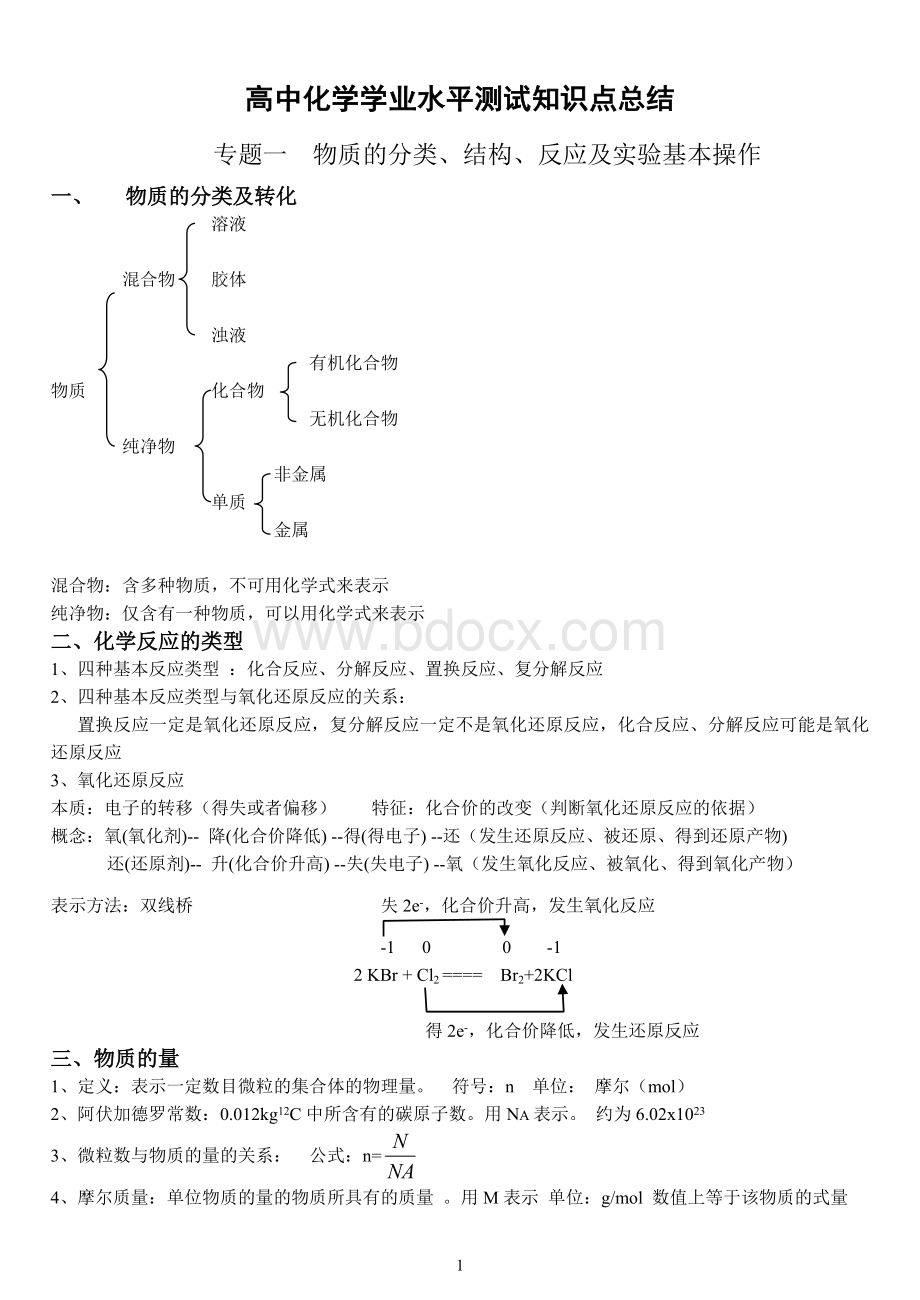
高中化学学业水平测试知识点总结
专题一物质的分类、结构、反应及实验基本操作
一、物质的分类及转化
溶液
混合物胶体
浊液
有机化合物
物质化合物
无机化合物
纯净物
非金属
单质
金属
混合物:
含多种物质,不可用化学式来表示
纯净物:
仅含有一种物质,可以用化学式来表示
二、化学反应的类型
1、四种基本反应类型:
化合反应、分解反应、置换反应、复分解反应
2、四种基本反应类型与氧化还原反应的关系:
置换反应一定是氧化还原反应,复分解反应一定不是氧化还原反应,化合反应、分解反应可能是氧化还原反应
3、氧化还原反应
本质:
电子的转移(得失或者偏移)特征:
化合价的改变(判断氧化还原反应的依据)
概念:
氧(氧化剂)--降(化合价降低)--得(得电子)--还(发生还原反应、被还原、得到还原产物)
还(还原剂)--升(化合价升高)--失(失电子)--氧(发生氧化反应、被氧化、得到氧化产物)
表示方法:
双线桥失2e-,化合价升高,发生氧化反应
-100-1
2KBr+Cl2====Br2+2KCl
得2e-,化合价降低,发生还原反应
三、物质的量
1、定义:
表示一定数目微粒的集合体的物理量。
符号:
n单位:
摩尔(mol)
2、阿伏加德罗常数:
0.012kg12C中所含有的碳原子数。
用NA表示。
约为6.02x1023
3、微粒数与物质的量的关系:
公式:
n=
4、摩尔质量:
单位物质的量的物质所具有的质量。
用M表示单位:
g/mol数值上等于该物质的式量
5、质量与物质的量的关系:
公式:
n=
6、体积与物质的量的关系:
公式:
n=标准状况下,1mol任何气体的体积都约为22.4L
7、阿伏加德罗定律:
同温同压下,相同体积的任何气体都含有相同的分子数
8、物质的量浓度:
单位体积溶液中所含溶质B的物质的量。
符号CB单位:
mol/L
9、物质的量浓度与物质的量的关系:
公式:
CB=
物质的量浓度与质量分数的关系:
公式:
10、物质的量浓度的配制:
配制前要检查容量瓶是否漏水
容量瓶规格:
100mL、250mL、500mL、1000mL。
步骤:
①.计算m=c×V×M②.称量③.溶解④.转移(洗涤2---3次洗涤液转入容量瓶)
⑤.定容⑥.摇匀⑦.装瓶贴签
四、分散系
溶液胶体浊液
1、分散质大小(nm)<1nm1nm~100nm>100nm
2、胶体的性质:
丁达尔现象(光亮的通路)用于区分溶液与胶体
3、电解质:
在水溶液中或者熔化状态下能导电的化合物
酸:
HCl、H2SO4、HNO3、H3PO4、H2SO3等
电解质碱:
NaOH、KOH、Ba(OH)2、Ca(OH)2、Cu(OH)2、Mg(OH)2、Al(OH)3、Fe(OH)3等
盐:
Na2CO3、NaHCO3、CaCO3、BaSO4、Na2SO4、NaCl、AgCl等
活泼金属氧化物:
Na2O、CaO、Al2O3、ZnO等
4、非电解质:
在水溶液中和熔化状态下都不能导电的化合物
非金属氧化物:
CO、CO2、NO、NO2、P2O5、SO2、SO3等
非电解质多数有机物:
蔗糖、酒精、甲烷等
非酸性的非金属氢化物:
NH3等
五、物质的分离与提纯
1、溶解过滤法:
适用于分离一种组分可溶,另一种不溶的固态混合物。
如:
粗盐的提纯
2、蒸发法:
适用于分离可溶性溶质与溶剂。
3、重结晶:
混合物中各组分物质在溶剂中溶解性的差异。
4、蒸馏法:
适用于分离各组分互溶,但沸点不同的液态混合物。
如:
酒精与水的分离
主要仪器:
蒸馏烧瓶、冷凝器
5、分液:
分离互不相溶的两种液体。
6、萃取:
溶质在互不相溶的溶剂里溶解度不同。
如:
CCl4萃取碘水中的碘,萃取后静止分层,上层呈无色下层呈紫红色,不用酒精萃取。
主要仪器:
分液漏斗
六、离子的检验
焰色反应钠的焰色:
黄色钾的焰色:
紫色(透过蓝色钴玻璃)
Cl-检验:
先加稀硝酸酸化,再加硝酸银,会产生白色沉淀
SO42-检验:
先加盐酸酸化,再加氯化钡,会产生白色沉淀
NH4+检验:
加入NaOH加热,产生气体使湿润的红色石蕊试纸变蓝
Fe3+检验:
加入KSCN溶液出现血红色;加碱出现红褐色沉淀
Fe2+检验:
加入KSCN溶液不变色,继续加入氯水变成血红色;加碱出现白色沉淀,迅速变成灰绿色最终变成红褐色。
Al3+检验:
加入NaOH先出现白色沉淀,随着NaOH过量沉淀消失
七、原子结构
质子Z
原子核
1、原子AZX中子N=A-Z
核外电子Z
2、质量数=质子数+中子数
3、核电荷数==质子数==原子核外电子数=原子序数
4、同位素:
有相同质子数不同中子数的不同原子互称11H21H31H
八、离子反应
1、发生的条件:
(1)生成难溶物(沉淀)
(2)生成挥发性的物质(气体)(3)生成难电离物质(水等)
2、书写步骤:
⑴.写⑵.改(易溶易电离物质改成离子形式,难溶难电离的物质,气体、单质、氧化物保留化学式)⑶.删⑷.查(电荷守衡,原子个数守恒)
强酸:
HCl、H2SO4、HNO3
强碱:
NaOH、KOH、Ba(OH)2
易溶易电离的物质含Na+、K+、NH4+、NO3-的盐
除BaSO4外的硫酸盐
易溶盐除AgCl外的氯化物
碳酸钠、碳酸钾、碳酸铵、所有碳酸氢盐
磷酸钠、磷酸钾、磷酸铵、所有磷酸氢盐
弱酸:
H2S、H2SO3、CH3COOH、
弱碱:
NH3·H2O、Mg(OH)2、Cu(OH)2、Al(OH)3
难溶难电离物质难溶物:
CaCO3、BaCO3、BaSO4、AgCl、Cu(OH)2、Mg(OH)2、Fe(OH)3
单质:
O2、H2、Fe、Mg、Al
气体:
CO2、SO2、H2S
氧化物:
CaO、Fe2O3、CuO、SO3、P2O5、H2O
专题二氯、钠
一.氯气
1.物理性质:
氯气是黄绿色、有刺激性气味、能溶于水、密度比空气大、易液化的有毒气体。
2.化学性质:
氯气具有强氧化性
(1)能跟金属(如Na、Fe、等)反应:
2Na+Cl22NaCl2Fe+3Cl22FeCL3
(2)和水的反应:
Cl2+H2O==HCl+HClO
次氯酸的性质:
(弱酸性、不稳定性、强氧化性)见光易分解方程式:
2HClO2HCl+O2↑
新制氯水含Cl2、HClO、HCl等成分;久置氯水变成稀盐酸。
(3)与碱的反应:
2NaOH+Cl2=NaCl+NaClO+H2O(用于尾气处理及制漂白液)
2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O(制漂白粉)
3.溴、碘的提取
(1)2KI+C12=2KCl+I2
(2)2KI+Br2=2KBr+I2(3)2KBr+Cl2=2KCl+Br2
二、钠
1.钠的物理性质:
银白色、有金属光泽的固体,热、电的良导体,质软、密度小、熔点低
2.钠的化学性质
⑴钠与水反应
现象及解释:
①浮:
(说明钠的密度比水的密度小)②熔:
(说明钠的熔点低;该反应为放热反应)
③游:
(说明有气体产生)④响:
(说明有气体产生)⑤红:
溶液中滴入酚酞显红色;(说明生成的溶液呈碱性)。
化学方程式为2Na+2H2O=2NaOH+H2↑,离子方程式为2Na+2H2O=2Na++2OH-+H2↑。
⑵与氧气反应:
4Na+O2=2Na2O(白色)2Na+O2Na2O2(淡黄色)
三、碳酸钠与碳酸氢钠的比较
名称
碳酸钠
碳酸氢钠
化学式
Na2CO3
NaHCO3
俗名
纯碱、苏打
小苏打
溶解性
易溶
易溶溶解度比碳酸钠小
热稳定性
稳定
不稳定:
2NaHCO3Na2CO3+H2O+CO2↑
与盐酸反应
Na2CO3+2HCl=2NaCl+H2O+CO2↑
比Na2CO3剧烈NaHCO3+HCl=NaCl+H2O+CO2↑
与NaOH反应
———
NaHCO3+NaOH=Na2CO3+H2O
相互转化
除杂:
Na2CO3固体(NaHCO3)充分加热Na2CO3溶液(NaHCO3)NaOH
鉴别碳酸钠和碳酸氢钠两种固体的方法:
加热出现气体的是碳酸氢钠
专题三铝、铁、硅
一、铝及其化合物
铝是地壳中最多的金属元素,主要是以化合态存在。
1.铝的性质
化学性质:
铝是比较活泼的金属,具有较强的还原性
①与氧气反应
常温下与空气中的氧气反应生成坚固的氧化膜,所以铝有良好的抗腐蚀能力。
4Al+3O2==2Al2O3
②与非氧化性酸反应:
2Al+6HCl==2AlCl3+3H2↑2Al+3H2SO4==Al2(SO4)3+3H2↑
③常温下铝与浓硫酸浓硝酸钝化
④与强碱反应:
2Al+2NaOH+2H2O===2NaAlO2+3H2↑(唯一一个金属与强碱溶液的反应)
⑤铝热反应:
2Al+Fe2O32Fe+Al2O3焊接铁轨,冶炼难熔金属
2.Al2O3(两性氧化物)
与硫酸反应:
Al2O3+3H2SO4==Al2(SO4)3+3H2O
与氢氧化钠反应:
Al2O3+2NaOH==2NaAlO2+H2O
离子方程式:
Al2O3+2OH-==2AlO2-+H2O
3.Al(OH)3(两性氢氧化物)
与酸反应:
Al(OH)3+3HCl==3AlCl3+3H2O
与氢氧化钠反应:
Al(OH)3+NaOH==NaAlO2+2H2O
离子反应:
Al(OH)3+OH-==Al
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 人教版 高中化学 学业 水平 测试 知识点 必修 化学 生活 总结
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 保育笔记.doc
保育笔记.doc
 幼儿园日常安全检查记录表.xls
幼儿园日常安全检查记录表.xls
