 选修5第一章认识有机化合物复习1文档格式.docx
选修5第一章认识有机化合物复习1文档格式.docx
- 文档编号:17648313
- 上传时间:2022-12-07
- 格式:DOCX
- 页数:16
- 大小:327.93KB
选修5第一章认识有机化合物复习1文档格式.docx
《选修5第一章认识有机化合物复习1文档格式.docx》由会员分享,可在线阅读,更多相关《选修5第一章认识有机化合物复习1文档格式.docx(16页珍藏版)》请在冰豆网上搜索。
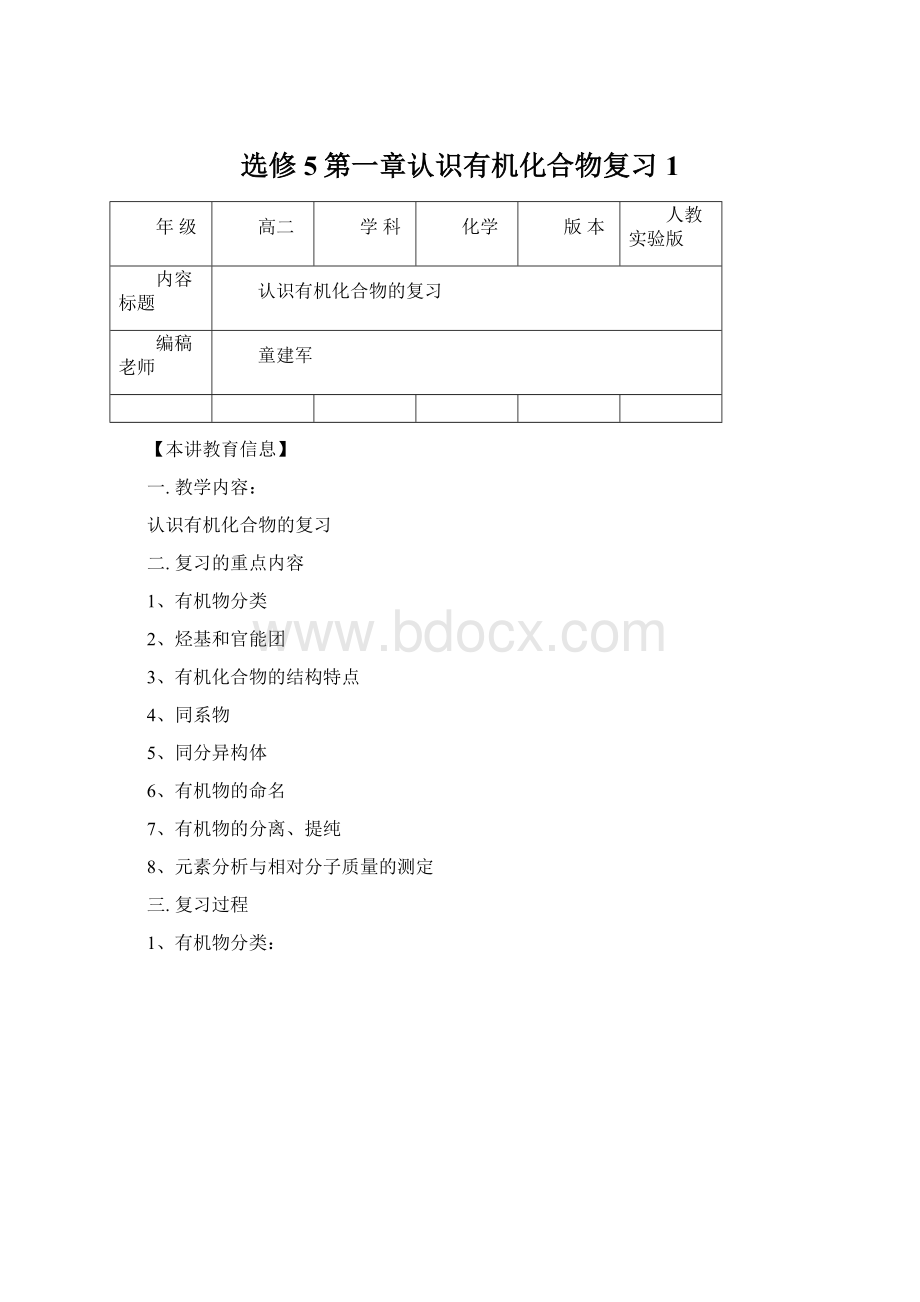
C—C、C=C、C≡C;
③碳原子的结合方式有二种:
碳链和碳环
(2)有机物分子里原子共线、共面:
共线、共面其实是分子的构型问题,掌握并会画出以下分子的构型:
(1)
:
正四面体,键角109о28′,若是
则仅是四面体,不是正四面体;
(2)
平面型结构,键角120о,6个原子在同一平面上;
(3)
直线型结构,键角180о,4个原子在同一直线上;
(4)
平面型结构,键角120о,12个原子在同一平面上;
(5)1,3-丁二烯分子中,四个碳原子和六个氢原子都在同一平面上,键角接近120о。
分子中有饱和碳则所有原子不可能共面。
[练习3]某烃结构式如下:
-C≡C-CH=CH-CH3,有关其结构说法正确的是( )
A.所有原子可能在同一平面上
B.所有原子可能在同一条直线上
C.所有碳原子可能在同一平面上
D.所有氢原子可能在同一平面上
结构相似,在分子组成上相差一个或若干个CH2原子团的物质,互称为同系物。
同系物应是同类物质,应具有同一通式。
对结构相似的正确理解,务必把握并运用以下两个要点:
(1)两个相同:
若含有官能团,则不仅含相同种类的官能团,且同一种官能团的数目也要相同,如:
CH3OH与HO—CH2—CH2—OH(乙二醇)、CH2=CH2与CH2=CH—CH=CH2都不互为同系物。
(2)结构相似(而不是相同)是指属于同一类物物质。
更确切地说是指:
①碳键和碳链特点相同;
②官能团种类、个数相同;
③官能团与其他原子的连接方式相同。
[练习4]下列物质一定属于同系物的是()
A.①和②B.④和⑥C.⑤和⑦D.④和⑧
凡分子式相同,但分子结构不同,因而性质也不同的几种化合物互称同分异构体。
同分异构体可以属于同一类物质,也可以属于不同类物质。
(1)结构不同指:
碳链骨架不同或官能团在碳链上的位置不同或官能团种类、个数不同。
(2)同分异构体之间分子式相同,其式量也一定相等,但式量相等的物质不一定是同分异构体。
如式量为44的化合物有:
CO2、C3H8、C2H4O、N2O;
式量为28的化合物有CO、N2、C2H4但它们不是同分异构体。
(3)同分异构体之间各元素的质量分数(最简式)均相同。
但化合物之间各元素质量分数(最简式)均相同的物质不一定为同分异构体。
如符合最简式为CH2O的有:
HCHO、CH3COOH、HCOOCH3、C6H12O6、HOCH2CHO等。
(4)同分异构体不一定是同类物质,其物理性质、化学性质可能相似,也可能有较大的差异。
(5)同分异构体不仅存在于有机物之间,还存在于有机物与无机物之间[如尿素CO(NH)2与氰酸铵NH4CNO]、无机物和无机物之间。
(6)书写同分异构体顺序可按类型异构→碳链异构→位置异构的思维顺序。
[练习5]组成为
的烷烃有九种,其中仅能由一种单烯烃加氢而制得的有()
A.1种B.2种C.3种D.4种
[练习6]萘的分子结构可表示为
或
,两者是等同的。
苯并[α]芘是强致癌物,其分子由5个苯环拼和而成,可表示为如下
(1)或
(2),这两者也是等同的。
现有结构式(A)~(D)
(1)
(2)
(A)(B)(C)(D)
试回答下列问题:
与
(1)
(2)式等同的结构式是。
A、D
与
(1)
(2)式是同分异构体的是。
B
有机物的种类繁多,命名时总体可分为不含官能团和含有官能团的两大类。
命名的原则是“一长、二多、三近”。
命名的关键是掌握确定主链和编号的原则。
无官能团
有官能团
类别
烷烃
烯、炔、卤代烃、烃的含氧衍生物
主链条件
碳链最长
同碳数支链最多
含官能团的最长碳链
编号原则
(小)取代基最近
官能团最近、兼顾取代基尽量近
名称写法
支位一支名母名
支名同,要合并
支名异,简在前
支位―支名―官位―母名
符号使用
数字与数字间用“,”数字与中文间用“—”,文字间不用任何符号
[练习7]下列有机物实际存在且命名正确的是()
A.2,2-二甲基丁烷B.2-甲基-5-乙基-1-己烷
C.3-甲基-2-丁烯D.3,3-二甲基-2-戊烯
[练习8]某烯烃与氢气加成后得到2,2-二甲基戊烷,烯烃的名称是()
A.2,2-二甲基-3-戊烯B.2,2-二甲基-4-戊烯
C.4,4-二甲基-2-戊烯D.2,2-二甲基-2-戊烯
[练习9]有A、B、C三种烃,分子式都是C5H10,经在一定条件下与足量H2反应,结果得到相同的生成物,这三种烃可能的结构简式为:
____________________________________
有机物分离、提纯的基本原则:
不增、不减、易分、复原。
(1)蒸馏:
常用于分离提纯液态有机物。
蒸馏的原理:
利用混合物中各种成分的沸点不同而使其分离的方法。
如石油的分馏。
蒸馏的条件:
有机物热稳定性较强、含少量杂质、与杂质沸点相差较大(30℃左右)。
(2)重结晶:
利用被提纯物质与杂质在同一溶剂中的溶解度不同而将其杂质除去的方法。
加热溶解趁热过滤
重结晶的关键是选择适当的溶剂。
重结晶选择溶剂的条件是杂质在溶剂中的溶解度很小或很大;
被提纯的有机物在此溶剂中的溶解度受温度的影响较大。
重结晶时,为了得到更多的晶体,不是温度越低越好,温度过低,杂质的溶解度也会降低,部分杂质也会析出,达不到提纯苯甲酸的目的;
温度极低时,溶剂(水)也会结晶,给实验操作带来麻烦。
重结晶的步骤是:
粗产品→热溶解→热过滤→冷却结晶→提纯产品
(3)萃取:
利用混合物中一种溶质在互不相溶的两种溶剂中的溶解性不同,用一种溶剂把溶质从它与另一种溶剂组成的溶液中提取出来的方法。
萃取的主要仪器:
分液漏斗。
萃取的分类:
①液—液萃取:
是利用有机物在两种互不相溶的溶剂中的溶解性不同,将有机物从一种溶剂转移到另一种溶剂的过程。
②固—液萃取:
是用有机溶剂从固体物质中溶解出有机物的过程。
(专用仪器设备)
[练习10]下列有四组混合物:
①硝酸钾和氯化钠②溴化钠和单质溴的水溶液③乙醇和丁醇④乙酸乙酯和乙酸钠溶液,分离以上各混合液的正确方法依次是:
()
A.分液、萃取、蒸馏、结晶B.分液、蒸馏、萃取、结晶
C.萃取、蒸馏、分液、结晶D.结晶、萃取、蒸馏、分液
[练习11]现有一瓶A和B的混合液,已知A和B的某些性质如下:
物质
分子式
熔点℃
沸点℃
密度g•cm-3
水溶性
A
C3H6O2
-98
57.5
0.93
可溶
C4H8O2
-84
77
0.90
由此,分离A和B的最佳方法是()
A.萃取B.升华C.分馏D.分液
(1)元素分析:
定性分析:
有机物的组成元素分析。
定量分析:
分子内各元素原子的质量分数。
(2)相对分子质量的测定——质谱法:
用高能电子流轰击样品,使分子失去电子变成带正电荷的分子离子和碎片离子,在磁场的作用下,由于它们的相对质量不同而使其到达检测器的时间也先后不同,其结果被记录为质谱图。
(3)分子结构的鉴定
①红外光谱:
在有机物分子中,组成化学键或官能团的原子处于不断振动的状态,其振动频率与红外光的振动频率相当。
所以,当用红外线照射有机物分子时,分子中的化学键或官能团可发生振动吸收,不同的化学键或官能团吸收频率不同,在红外光谱图上将处于不同的位置,从而可获得分子中含有何种化学键或官能团的信息。
②核磁共振氢谱:
氢原子核具有磁性,如用电磁波照射氢原子核,它能通过共振吸收电磁波能量,发生跃迁。
用核磁共振仪可以记录到有关信号,处在不同环境中的氢原子因产生共振时吸收电磁波的频率不同,在图谱上出现的位置也不同,各类氢原子的这种差异被称作化学位移;
而且吸收峰的面积与氢原子数成正比。
[练习12]某有机物由C、H、O三种元素组成,它的红外吸收光谱表明有羟基O-H键和烃基C-H键的红外吸收峰,且烃基与羟基上氢原子个数之比为2:
1,它的相对分子质量为62,试写出该有机物的结构简式。
[练习13]核磁共振谱是测定有机物分子结构最有用的工具之一。
瑞士科学家维特里希等三人即是利用核磁共振技术测定生物大分子的三维结构而获得2002年诺贝尔化学奖。
在有机物分子中,不同位置的氢原子在质子核磁共振谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目。
例如:
乙醛的结构式为:
,其PMR谱中有2个信号峰,其强度之比为3∶1。
⑴下列有机物分子中,在质子核磁共振谱中只给出一种峰(信号)的是()
A.CH3-CH3B.CH3CH2OHC.CH3OCH3D.CH3CH2Cl
⑵化合物A和B的分子式都是C2H4Br2,A的PMR谱上只有1个峰,则A的结构简式为。
B的PMR谱上有个峰,强度比为
【模拟试题】
第Ⅰ卷(选择题共36分)
考生注意:
本试卷共24题,总分100分,考试时间90分钟。
可能用到的相对原子质量:
H1,C12,N14,O16
一、本题共有12个小题,每小题3分,共36分;
每小题有一个或两个选项符合题意)
1.某有机物在氧气中充分燃烧,生成等物质的量的水和二氧化碳,则该有机物必须满足的条件是()
A.分子中的C、H、O的个数比为1:
2:
3
B.分子中C、H个数比为1:
2
C.该有机物的相对分子质量为14
D.该分子中肯定不含氧元素
2.某化合物6.4g在氧气中完全燃烧,只生成8.8gCO2和7.2gH2O。
下列说法正确的是()
A.该化合物仅含碳、氢两种元素
B.该化合物中碳、氢原子个数比为1:
4
C.无法确定该化合物是否含有氧元素
D.该化合物中一定含有氧元素
3.下列分子式表示的物质,具有同分异构体的是()
A.C3H7ClB.C3H8C.CH2Cl2D.C2H6O
4.A、B两种烃,它们含碳质量分数相同,下列关于A和B的叙述正确的是()
A.A和B一定是同分异构体B.A和B不可能是同系物
C.A和B最简式一定相同D.A和B的化学性质相似
5.mmolC2H2跟nmolH2在密闭容器中反应,当该可逆反应达到平衡时,生成pmolC2H4。
将反应后的混合气体完全燃烧,生成CO2和H2O,所需要氧气的物质的是()
A.(3m+n)molB.
C.(3m+n+2p)molD.
6.在密闭容器中某气态烃和氧气按一定比例混和,点火爆炸后恢复到原温度(20℃),压强减小至原来的一半,若加NaOH的溶液则气体全部被吸收,则此烃为()
A.C3H8B.C2H4C.C2H6D.C6H6
7.下列物质一定属于同系物的是()
A.④和⑧B.①、②和③C.⑤和⑦D.④、⑥和⑧
8.wg含有双键的不饱和烃X能与VL的氢气(标准状况)完全反应,若X的相对分子质量为M,阿伏加德罗常数为NA,则1molX中含有双键数目为()
A.
B.
C.
D.
9.有机物
的正确命名为()
A.2-乙基-3,3-二甲基-4-乙基戊烷
B.3,3-二甲基-4-乙基戊烷
C.3,3,4-三甲基己烷
D.2,3,3-三甲基己烷
10.乙烷受热分解生成乙烯和氢气,现有乙烷部分分解的产物,取1体积使其充分燃烧生成1.6体积的二氧化碳气体(在相同条件下测定),则乙烷的分解率为()
A.20%B.25%C.50%D.75%
11.1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和6体积氯气发生取代反应。
由此可以断定原气态烃是(气体体积均在相同条件下测定)()
A.乙炔B.丙炔C.丁炔D.丁二烯
12.拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是 ()
A.属于芳香烃B.属于卤代烃
C.在酸性条件下不水解D.在一定条件下可以发生加成反应
第Ⅱ卷(非选择题共64分)
13.(5分)按官能团的不同,可以对有机物进行分类,请指出下列有机物的种类,填在横线上。
CH3CH2CH2COOH________;
___________;
____________
________________;
14.(5分)请设计实验方案区分己烷、溴乙烷、乙醇三种液态有机物。
15.(4分)下列各组中的两种有机物,可能是相同的物质、同系物或同分异构体等,请判断它们之间的关系
(1)2-甲基丁烷和丁烷________________
(2)正戊烷和2,2-二甲基丙烷___________________
(3)间二甲苯和乙苯_____________________
(4)1-己烯和环己烷____________________________
16.(10分)写出丁烷(C4H10)、戊烷(C5H12)的各种同分异构体并用系统命名法给其命名。
17.(6分)有机物的结构可用“键线式”简化表示。
CH3—CH=CH-CH3可简写为
。
有机物X的键线式为:
(1)有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式。
(2)Y与乙烯在一定条件下发生等物质的量聚合反应,写出其反应的化学方程式:
(3)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有种。
18.(6分)某同学为测定维生素C中碳、氢的质量分数,取维生素C样品研碎,称取该试样0.352g,置于铂舟并放入燃烧管中,不断通入氧气流。
用酒精喷灯持续加热样品,将生成物先后通过浓硫酸和碱石灰,两者分别增重0.144g和0.528g,生成物完全被吸收。
试回答以下问题:
(1)维生素C中碳的质量分数是_______________,氢的质量分数__________________
(2)维生素中是否含有氧元素?
为什么?
(试通过计算说明)
____________________________________________________________________________
(3)如果需要你确定维生素C的分子式,你还需要哪些信息?
19.(5分)下列两幅谱图是结构简式为CH3CH2CH2OH和CH3CH(OH)CH3的两种有机化合物的1H核磁共振谱图。
请判断哪一幅是CH3CH(OH)CH3的1H-NMR谱图,并说明理由。
20.(8分)在抗击非典型性肺炎期间,过乙酸(过氧乙酸)曾被广泛用作消毒剂。
已知硫酸和过硫酸的结构简式如下:
请从以下八个式子中选择答案回答下列问题(答案用编号表示,选错要倒扣分)。
(1)过乙酸(过氧乙酸)的结构简式是。
(2)过乙酸的同分异构体是。
(3)过乙酸的同系物是。
(4)氧的质量分数最小的物质是。
21.(2分)已知胰岛素含硫的质量分数为3.4%,相对分子质量为5734,则每个胰岛素分子中所含的硫原子数为多少?
___________________
22.(6分)某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90。
取有机物样品1.8g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g。
试求该有机物的分子式。
23.(7分)某混合气体由一种气态烷烃和一种气态烯烃组成,在同温同压下,混合气体对氢气的相对密度为13,在标准状况下,将56.0L混合气体通入足量溴水,溴水质量增重35.0g,通过计算回答:
(1)混合气体中气态烷烃的化学式:
(2)混合气体中两种气体的物质的量之比:
(3)写出混合气体中气态烯烃可能的结构简式:
。
【试题答案】
一、选择题(本题错选不得分,漏选得1分,共36分)
题号
1
3
5
6
7
8
9
10
11
12
答案
BD
AD
C
D
AB
AC
13.羧酸类,酚类,芳香烃,酯类,羧酸类(每空1分,共5分)
14.分别取一定量的三种液体于三支试管中,再分别向其中加入少量水。
若无分层现象出现,则为乙醇;
若出现分层现象且水在上层的为溴乙烷;
若出现分层现象且水在下层的为己烷。
(操作过程2分,结论每个1分,共5分)
15.
(1)同系物,
(2)同分异构体,(3)同分异构体(4)同分异构体(每空1分,共4分)
16.CH3CH2CH2CH3(丁烷);
CH3CH(CH3)2(2-甲基丙烷)
CH3CH2CH2CH2CH3(戊烷);
CH3CH2CH(CH3)2(2-甲基丁烷);
C(CH3)4(2,2-二甲基丙烷)(每个1分,共10分)
17.
(1)
(3)2
(每小题2分,共6分)
18.
(1)40.91%,4.55%
(2)已知,m(H)=0.144g÷
9=0.016g,m(C)=0.528g×
12÷
44=0.144g,m(H)+m(C)=0.016g+0.144g=0.160g<0.352g,又因产物中只有H2O和CO2,故维生素中必含有氧。
(3)若要确定其分子式,还要知其相对分子质量。
(每小题2分,共6分)
19.A是CH3CH(OH)CH3的1H-NMR谱图,因为从结构上分析,CH3CH(OH)CH3有三种不同化学环境的H,而分析CH3CH2CH2OH有四种不同的H,故从图上分析,A上有三个峰,而B有四个峰,故A是CH3CH(OH)CH3的1H-NMR谱图。
(判断2分,解释3分,共5分)
20.
(1)b
(2)a,d(3)f(4)f(每小题2分,共8分)
21.6个(2分)
22.解:
已知m(H)=1.08g×
2÷
18=0.12g,m(C)=2.64g×
44=0.72g
则m(O)=1.8g-0.12g-0.72g=0.96g(2分)
则n(C)∶n(H)∶n(O)=0.72÷
12∶0.12÷
1∶0.96÷
16=1∶2∶1,则其实验式为CH2O;
(2分)
故可设其分子式为(CH2O)n,则有30n=90,解之得:
n=3,故分子式为C3H6O3(2分)
(其它解法合理也得分)
23.解:
已知混合气体的平均相对分子质量为:
13×
2=26,则烷烃一定为CH4,混合烃总质量为
M(混合烃)=56.0L÷
22.4L/mol×
26g/mol=65g(2分)
因烯烃的分子量最小为C2H4的28。
可设烯烃的分子式为CnH2n,则有m(CnH2n)=35g,m(CH4)=65g-35g=30g;
则有65÷
(30÷
16+35÷
14n)=26,解得:
n=4,
则烯烃为C4H8;
n(CH4):
n(C4H8)=30÷
16:
35÷
56=3:
1(2分)
(1)CH4
(2)3:
(3)CH2=CH-CH2CH3,CH3-CH=CH-CH3,CH2=C(CH3)2(3分)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 选修 第一章 认识 有机化合物 复习
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
