 学年山东省青岛市经济技术开发区育才初级中学高三化学下学期期末试题Word文档格式.docx
学年山东省青岛市经济技术开发区育才初级中学高三化学下学期期末试题Word文档格式.docx
- 文档编号:17459404
- 上传时间:2022-12-01
- 格式:DOCX
- 页数:12
- 大小:246.31KB
学年山东省青岛市经济技术开发区育才初级中学高三化学下学期期末试题Word文档格式.docx
《学年山东省青岛市经济技术开发区育才初级中学高三化学下学期期末试题Word文档格式.docx》由会员分享,可在线阅读,更多相关《学年山东省青岛市经济技术开发区育才初级中学高三化学下学期期末试题Word文档格式.docx(12页珍藏版)》请在冰豆网上搜索。
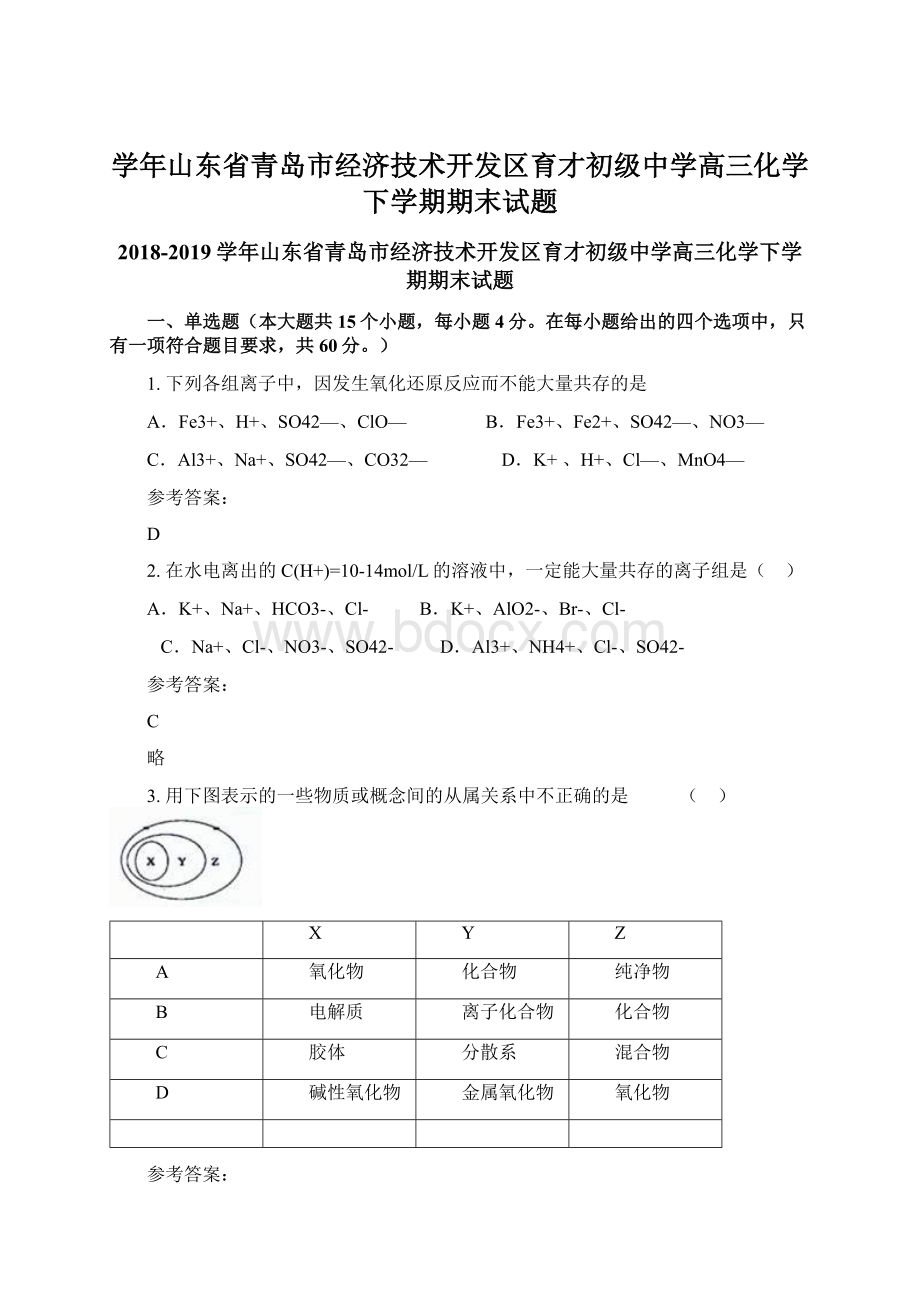
化合物
纯净物
B
电解质
离子化合物
胶体
分散系
混合物
碱性氧化物
金属氧化物
4.下列反应的离子方程式正确的是(
)
A.过氧化钠溶于水:
↑
B.铜片加入稀硝酸中:
↑
C.氯化铝溶液中加入过量氨水:
D.在
溶液中加入过量NaOH溶液:
C
5.已知常温下,在溶液中发生如下反应:
①:
16H++10Z-+2XO4-=2X2++5Z2+8H2O
②:
2A2++B2=2A3++2B-
③:
2B-+Z2=B2+2Z-
由此推断下列说法错误的是(
A.反应Z2+2A2+=2A3++2Z-可以进行
B.Z元素在①、③的反应中均被还原
C.氧化性是XO4->
Z2>
B2>
A3+
D.还原性是A2+>
B->
Z->
X2+
6.向10ml0.2mol/L的NaAlO2溶液中逐滴加入未知浓度的盐酸,测得滴加盐酸10ml与滴加20ml时生成的沉淀相等。
则该盐酸的浓度为:
A、0.1mol/L
B、0.13mol/L
C、0.20mol/L
D、0.16mol/L
7.向CH3COOH
CH3COO-+H+的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变小的是
A.H2O
B.CH3COONa
C.NH3·
H2O
D.H2SO4
8.下列各组离子一定能大量共存的是
A.在含有大量AlO2-的溶液中:
NH4+、Na+、Cl-、H+
B.在强碱溶液中:
Na+、K+、CO32-、NO3-
C.在pH=12的溶液中:
NH4+、Na+、SO42-、Cl-
D.在c(H+)=0.1mol·
L-1的溶液中:
K+、I-、Cl-、NO3-
9.一定温度下,在氢氧化钡的悬浊液中,存在氢氧化钡固体与其电离的离子间的溶解平衡关系:
Ba(OH)2(固体)
Ba2++2OH-。
向此种悬浊液中加入少量的氧化钡粉末,下列叙述正确的是
A.溶液中钡离子数目减小
B.溶液中钡离子浓度减小
C.溶液中氢氧根离子浓度增大
D.pH减小
10.YBa2Cu8Ox(Y为元素钇)是磁悬浮列车中的重要超导材料,关于
的说法正确的是
A.Y在周期表中的位置是第4周期ⅢB族
B.属于非金属元素
C.核素
的质子数与中子数之差为50
D.
和
是两种不同的核素
试题分析:
A、Y元素为39号元素,属于第五周期第ⅢB族。
A错误;
B、该元素是副族元素,所以是金属元素,B错误;
C、Y的质子数为39,质量数为89,中子数=质量数-质子数=89-39=50,质子数与中子数之差为-11,C错误;
D、
的质子数相同,中子数不相同的同一元素,所以是不同的两种核素,D正确;
答案选D。
【名师点晴】该题的难点是元素在周期表中物质的推测,由原子序数确定元素位置的规律:
只要记住了稀有气体元素的原子序数(He—2、Ne—10、Ar—18、Kr—36、Xe—54、Rn—86),就可由主族元素的原子序数推出主族元素的位置。
(1)若比相应的稀有气体元素多1或2,则应处在下周期的第ⅠA族或第ⅡA族,如88号元素:
88-86=2,则应在第七周期第ⅡA族;
(2)若比相应的稀有气体元素少1~5时,则应处在同周期的第ⅦA族~第ⅢA族,如84号元素应在第六周期第ⅥA族;
(3)若预测新元素,可与未发现的稀有气体元素(118号)比较,按上述方法推测知:
114号元素应为第七周期第ⅣA族。
11.物质的量浓度相同时,下列既能跟NaOH溶液反应,又能跟盐酸反应的溶液中,pH最大的是
A.Na2CO3溶液
B.NH4HCO3溶液
C.NaHCO3溶液
D.NaHSO4溶液
12.实验室需配制一种仅含五种离子(水电离出的离子可忽略)的混合溶液,且在混合溶液中五种离子的物质的量浓度均为1mol/L.,下面四个选项中能达到此目的的是(
A.Al3+、K+、SO42-、Cl-、Al[(OH)4]-
B.Al3+、Na+、Cl-、SO42-、NO3-
C.Na+、K+、SO42-、NO3-、Cl
D.Fe2+、H+、Br-、NO3-、Cl-
知识点:
离子共存问题
答案解析:
B
解析:
A.Al3+与Al[(OH)4]-发生互促水解而不能大量共存,错误;
B.符合电荷守恒,且离子之间不发生任何反应,能大量共存,正确;
C.溶液电荷不守恒,错误;
D.符合电荷守恒,但Fe2+和NO3-在酸性条件下不能大量共存,错误。
思路点拨:
本题考查了离子共存问题,侧重于元素化合物知识的综合应用,为高考常见题型,注意把握相关离子的性质,易错点为D,注意溶液电荷守恒的应用,题目难度不大。
13.
BC
14.要将
转化为
应选用的试剂是( )
A.盐酸
B.硫酸
C.烧碱
D.二氧化碳和水
15.下列所示物质的制备方法合理的是
A.实验室从海帶中提取单质碘取样→灼烧→溶解→过滤→萃取→蒸馏
B.金红石(主要成分TiO2)
原料生产金属Ti:
金红石、焦炭
TiCl4
Ti
C.从卤水中(溶质主要是MgCl2)提取Mg
卤水
Mg(OH)2
MgCl2(aq)
MgCl(s)
Mg
D.由食盐制取漂粉精NaCl(ag)
Cl2
漂粉精
【详解】A.海带中的碘元素以I-形式存在,从海带中提取单质碘时,过滤后要加入氧化剂将碘离子氧化为碘单质,再加入萃取剂进行萃取、分液,最后经蒸馏获得单质碘,故A错误;
B.二氧化钛和焦炭、氯气反应,产物是四氯化钛和一氧化碳;
镁与TiCl4置换反应得到钛和氯化镁,稀有气体化学性质稳定,不会参与化学反应,常做保护气,故B正确;
C.直接加热蒸干水分得不到氯化镁固体,会促进氯化镁水解,最后得到氢氧化镁;
应该蒸发浓缩、冷却结晶得MgCl2·
6H2O晶体,然后在HCl气体环境中加热MgCl2·
6H2O可得MgCl2固体,故C错误;
D.澄清石灰水浓度较低,用其制备次氯酸钙效率较低,应用石灰乳,故D错误;
答案:
二、实验题(本题包括1个小题,共10分)
16.(14分)MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节。
某研究性学习小组设计了将粗MnO2(含有较多的MnO和MnCO3)样品转化为纯MnO2实验,其流程如下:
(1)第①步加稀H2SO4时,粗MnO2样品中的
▲
(写化学式)转化为可溶性物质。
(2)第②步反应的离子方程式是
□
+□ClO3—+□
=□MnO2↓+□Cl2↑+□
。
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、酒精灯、
▲
、
。
已知蒸发得到的固体中含有NaClO3和NaOH,则一定还含有
(写化学式)。
(4)若粗MnO2样品的质量为12.69g,第①步反应后,经过滤得到8.7gMnO2,并收集到0.224LCO2(标准状况下),则在第②步反应中至少需要
▲
molNaClO3。
(14分)
(1)MnO和MnCO3
(2)5Mn2+
2
4H2O
5
1
8H+
(3)蒸发皿
玻璃棒
NaCl
(4)0.02
(最后一空4分,其余每空2分)
三、综合题(本题包括3个小题,共30分)
17.二氧化硫是污染大气形成酸雨的主要有害物质之一,如果了解二氧化硫的性质,它在我们的生活中也有广泛的用途。
(1)下列可产生二氧化硫污染大气的是
(填序号)。
A.含硫矿石的冶炼
B.大量化石燃料的燃烧
C.大量烟花爆竹的燃放
D.硫酸厂排放的工业尾气
(2)某课外小组采集了一份由硫酸形成的酸雨样品,每隔一段时间测定该雨水样品的pH变化数据如下
测试时间段
1
2
3
4
雨水的pH
4.73
4.62
4.56
4.55
分析酸雨样品PH变化的原因(用文字和化学方程式说明)
(3)某实验小组欲探究二氧化硫气体的化学性质,设计如下实验,请完成实验报告。
限选试剂:
品红溶液、浓硫酸、新制的氯水、氢氧化钠溶液、氢硫酸溶液、石蕊
实验仪器:
试管、导气管
18.某无色溶液,其中可能存在Na+、Ba2+、AlO2﹣、S2﹣、SO32﹣、SO42﹣.取该溶液进行有关实验,实验结果如图所示:
请回答:
(1)沉淀甲的化学式为
.
(2)由溶液甲生成沉淀乙的离子方程式为
(3)沉淀丙中一定含有
可能含有
(4)综合上述信息,该溶液中肯定存在的离子有:
(1)S;
(2)Al3++3HCO3﹣═Al(OH)3↓+3CO2↑;
(3)BaCO3;
BaSO4;
(4)Na+、AlO2﹣、S2﹣、SO32﹣.
解析:
无色溶液可能存在Na+、Ba2+、AlO2﹣、S2﹣、SO32﹣、SO42﹣.由实验流程可知,加过量盐酸生成淡黄色沉淀甲为S,则溶液中存在S2﹣、SO32﹣,即一定不存在Ba2+;
溶液甲中有剩余的HCl,与过量碳酸氢铵反应生成气体乙为二氧化碳,由生成白色沉淀可知,沉淀为氢氧化铝,则应存在AlO2﹣,转化生成Al3+与HCO3﹣的相互促进水解生成沉淀和气体;
溶液乙中含过量的碳酸氢铵,与氢氧化钡反应生成碳酸钡沉淀和氨气,即丙为BaCO3,气体丙为氨气,溶液丙中含过量的氢氧化钡,由溶液为电中性可知,还含钠离子,而原溶液中SO42﹣不能确定,
(1)由上述分析可知,沉淀甲为S,故答案为:
S;
(2)溶液甲生成沉淀乙的离子方程式为Al3++3HCO3﹣═Al(OH)3↓+3CO2↑,故答案为:
Al3++3HCO3﹣═Al(OH)3↓+3CO2↑;
(3)由上述分析可知,硫酸根离子可能存在,则沉淀丙中一定含BaCO3,可能含BaSO4,故答案为:
BaCO3;
(4)由上述分析可知,一定存在Na+、AlO2﹣、S2﹣、SO32﹣,故答案为:
Na+、AlO2﹣、S2﹣、SO32﹣.
19.聚酯增塑剂G及某医药中间体H的一种合成路线如下(部分反应条件略去):
已知:
(1)B的名称(系统命名):
,D的分子式为
(2)反应①~⑥中属于取代反应的是
(3)G的结构简式为
(4)写出反应②和⑥的化学方程式:
②,⑥
(5)C存在多种同分异构体,写出核磁共振氢谱只有两种峰的同分异构体的结构简式:
(1)1,2-丙二醇
C6H10O4
(2)②⑤⑥
(3)
(4)②
+2NaOH
+2NaCl
⑥
(5)
或
解析:
本题考查有机物的推断与性质,注意根据有机物的结构进行推断,需要学生对给予的信息进行利用,较好的考查学生自学能力、分析推理能力,是热点题型,难度中等。
由题中各物质转化关系,丙烯与氯气加成得A为CH3CHClCH2Cl,A发生水解(取代)得B为CH3CHOHCH2OH,苯与氢气发生加成反应得C为
,C发生氧化反应得D,D与B发缩聚反应得G:
,根据题中信息,F发生取代反应生成H和E,D和E发生酯化反应(取代反应)得F为CH3CH2OOCCH2CH2CH2CH2COOCH2CH3,根据H的结构可推知E为CH3CH2OH,
(1)B为CH3CHOHCH2OH,B的名称为1,2-丙二醇,根据D的结构简式可知,D的分子式为C6H10O4;
(2)根据上面的分析可知,反应①~⑥中属于取代反应的是②⑤⑥;
(3)G为
;
(4)反应②的化学方程式为
+2NaCl,反应⑥的化学方程式为
(5)C为
,C存在多种同分异构体,其中核磁共振氢谱只有两种峰的同分异构体的结构简式为
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 学年 山东省 青岛市 经济技术 开发区 育才 初级中学 化学 学期 期末 试题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
