 高考化学58个考点精选版32水的电离和溶液的PHWord格式.docx
高考化学58个考点精选版32水的电离和溶液的PHWord格式.docx
- 文档编号:17149943
- 上传时间:2022-11-28
- 格式:DOCX
- 页数:17
- 大小:82.44KB
高考化学58个考点精选版32水的电离和溶液的PHWord格式.docx
《高考化学58个考点精选版32水的电离和溶液的PHWord格式.docx》由会员分享,可在线阅读,更多相关《高考化学58个考点精选版32水的电离和溶液的PHWord格式.docx(17页珍藏版)》请在冰豆网上搜索。
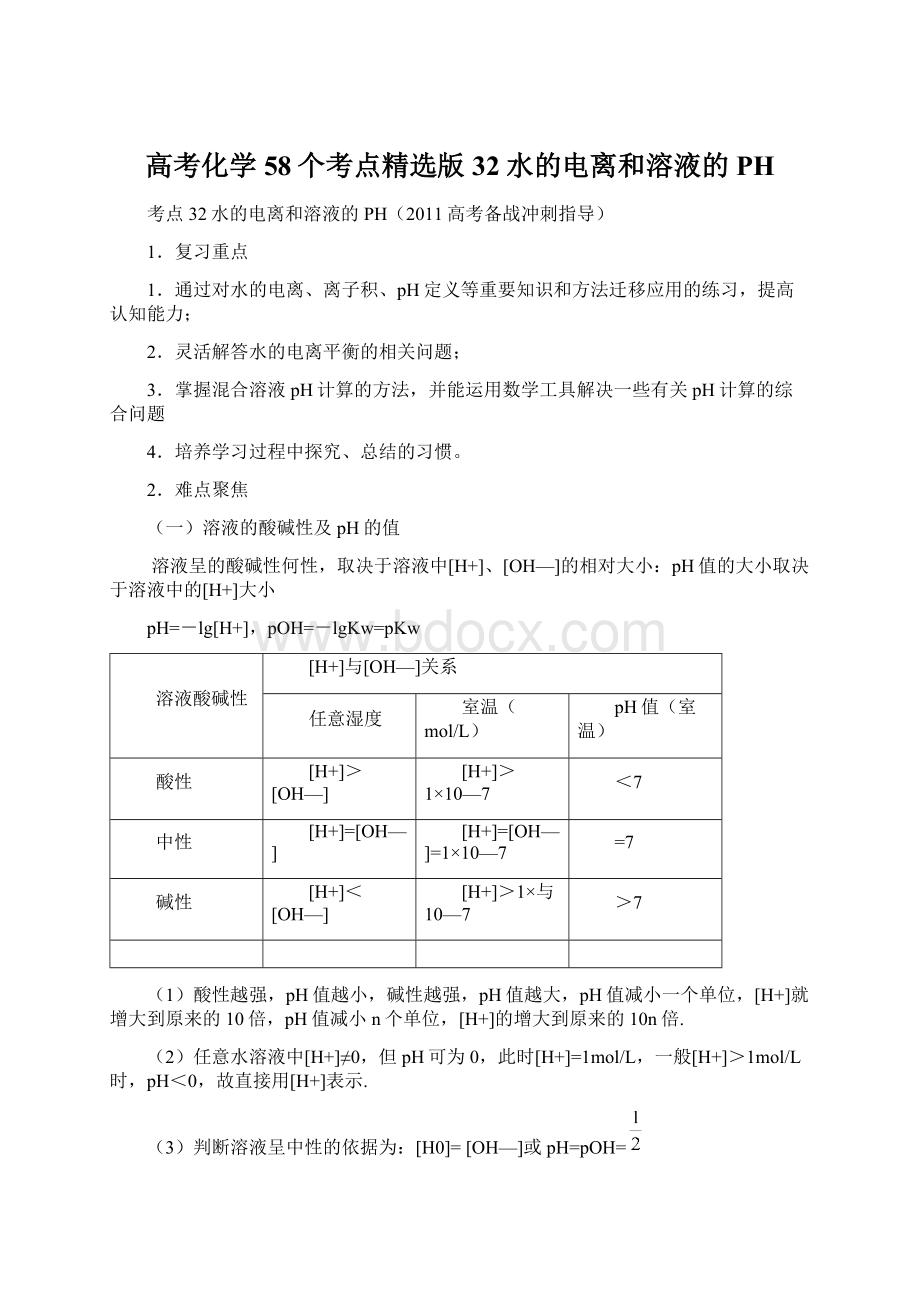
H2OH++OH-Q
由于水的电离是吸热的,湿度越高,电离程度越大,kw越大.
中性:
T↗→Kw↗→pH+pOH↘
T↘→Kw↘→pH=pOH↗
如:
100℃,KW=1×
10—12..pKw=12.
中性时Ph=
pKw=6<7.
图示:
不同湿度(T1>T2)时溶液中[H+]与[OH—],pH与pOH关系
图一图二
想一想:
图一与图二有哪些不同?
为何不同?
提示:
(①形状②T1、T2相对位置)
③简平分钱划分的两个区域酸碱性不同。
建议以[H+]、[OH—]=Kw,和pH+pOH=pKw两个关系或考虑,并注意湿度不同时Kw的影响。
)
(4)溶液pH的测定方法:
①酸碱指示剂②pH试纸③pH计其中①只传判定pH范围
②pH试纸也只能确定在某个值左右(对照标准比色卡),无法精确到小数点后1倍。
另外使用时不能预先润湿试纸。
否则相当于又稀释了待测液,测定结果误差大。
③pH计测定较精确.
(二)酸碱溶液的稀释前后pH值的变化。
由于强酸或强碱在水中完全电离,加水稀释后不会有溶质进一步电离,故仅仅是体积增大的因素导致酸溶液中的[H+]或碱溶液中的[OH—]减小.
弱酸或弱碱由于在水中不完全电离,加水稀释同时,能促使其分子进一步电离,故导致相应[H+]或[OH—]减小的幅度降低。
例如①等物质的量浓度的盐酸和醋酸,氢氧化钠和氨水分别加水稀释。
溶液的pH值变化,图示如下:
②若把上述问题,换成等pH值,图示又怎样呢?
强酸弱酸稀释强、弱碱稀释
前
后前
后
pH=apH(HCl)=a+n<7pH=bPh(NaOH)=b-n>7
pH(HAC)<a+n<7pH(NH3·
H2C)>b-n>7
△pH(HCl)=n△pH(NaOH)=n
△pH(HAC)<n△pH(NH3·
H2O)<n
△pH(HCl)>△pH(HAC)△pH(NaOH)>△pH(NH3·
H2O)
注意:
①酸无论怎样稀释,不可能成为碱性;
若无限稀释,则pH只能无限接近7且小于7.
②碱无论怎样稀释,不可能成为酸性;
若无限稀释,则pH只能无限接近7且大于7
③当起始强酸、弱酸的pH相同,稀释后为达仍相同,则稀释倍数一定是弱酸大小强酸(强碱、弱碱类同)
(三)有关pH的计算
1.溶液简单混合(不发生反应,忽略混合时体积变化)
强酸:
pH=pH小+0.3
若等体积混合,且△pH≥2
强碱:
pH=pH大-0.3
若不等体积混合,物质的量浓度强酸[H+]总=
分别为M1、M2体积分别为强碱[OH—]总=
V1、V2的一元强酸或强碱
注意:
强酸直接由[H+]总求pH值
强碱由[OH—]总求pOH,后再求pH值.
2.强酸和强碱混合(发生中和反应,忽略体积变化)可能情况有三种:
①若酸和碱恰好中和.即nH+=nOH—,pH=7.
②若酸过量,求出过量的[H+],再求pH值.
③若碱过量,求出过量的[OH—],求出pOH后求pH值.
特例:
若强酸与强碱等体积混合
①若pH酸+pH碱=14,则完全中和pH=7.
②若pH酸+pH碱>14,则碱过量pH≈pH碱-0.3
③若pH酸+pH碱<14,则酸过量pH≈pH酸+0.3
讨论:
pH=a的HCl溶液和pH=b的NaOH溶液按体积比V1:
V2混合.当混合液分别呈中性、酸性、碱性时,且V1:
V2=10n时,a+b分别为多少?
分析①呈中性:
即pH=7.
nH+=nOH—
10—a·
V1=10—(14-b)·
V2
V1:
V2=10—14+a+b
10n=10a+b-14
n=a+b-14
a+b=14+n
②若呈酸性.即pH<7
nH+>nOH—
V1>10—(14-b)·
V2>10—14+a+b
10n>10-14+a+b
a+b<14+n
③若呈碱性,即pH>7,同理可知
a+b>14+n
若V1:
V2=1:
10n=10—n,三种情况的结果又如何呢?
3.关于酸、碱混合时的定性判断(常温)
酸与碱混合时发生中和反应,但不一定恰好完呈中和。
即使恰好完全中和,也不一定溶液呈中性,由生成的盐能否水解及水解情况而定,另外酸碱的强弱不同,提供反应物的量不同也影响着反应后溶液的性质。
一般酸或碱过量化生成的盐水解对溶液的酸碱性影响大。
下面把常见的几种情况分列出来.
①等物质的量浓度的一元弱酸一元强碱溶液等体积混合溶液pH>7(由生成的强碱弱酸盐水解决定)
②等物质的量浓度的一元强酸与一元弱碱溶液等体积混合后溶液pH<7(由生成的强酸弱碱盐水解决定)
③等物质的量浓度的一元强酸与强碱溶液等体积混合后溶液pH=7(因生成强酸强碱盐不水解)
想一想:
若酸或碱之一是多元,情况又怎样?
④当pH=pOH的强酸与强碱溶液以等体积混合后pH=7(与酸、碱的几元性无尖)
⑤当pH=3的某一元酸溶液与pH=11的一元强碱以等体积混合后pH≤7。
(考虑酸有强弱之分,若分弱酸,制反应后酸过量)
⑥当pH=3的某一元强酸pH=11的一元碱溶液的以等体积混合后pH≥7(同理⑤,弱碱过量)
⑦将pH=3的酸溶液和pH=11的碱溶液以等体积混合后溶液pH=无法确定.
再想一想:
⑤⑥⑦与酸、碱的几元性有无关系?
3.例题精讲
知识点一:
水的电离
【例1】
(1)与纯水的电离相似,液氨中也存在着微弱的电离:
2NH3
NH4++NH2-
据此判断以下叙述中错误的是()
A.液氨中含有NH3、NH4+、NH2-等微粒
B.一定温度下液氨中C(NH4+)·
C(NH2-)是一个常数
C.液氨的电离达到平衡时C(NH3)=C(NH4+)=C(NH2-)
D.只要不加入其他物质,液氨中C(NH4+)=C(NH2-)
(2)完成下列反应方程式
①在液氨中投入一小块金属钠,放出气体————————————————————————————
②NaNH2溶于水的反应——————————————————————————————————
③类似于“H++OH—=H2O”的反应————————————————————————————
解析:
此题要求掌握水自偶的实质(水分子电离产生的H+与H2O结合形成H3O+)以及水的电离平衡,并能迁移应用于对于NH3电离的认识:
NH3分子电离产生H+和NH2—,H+与NH3结合生成NH4+,液氨电离产生等量的NH2—与NH4+,一定温度下离子浓度乘积为一常数;
NH4+类似于H+,NH2—类似于OH—。
具备上述知识后,就可顺利完成解题。
答案:
(1)C
(2)①2Na+2NH3=H2↑+2NaNH2
②NaNH2+H2O=NaOH+NH3↑或NH2—+H2O=OH—+NH3↑
③NH2—+NH4+=2NH3↑或NH4Cl+NaNH2=2NH3↑+NaCl
知识点二:
水的离子积
【例2】某温度下纯水中C(H+)=2×
10-7mol/L,则此时溶液中的C(OH-)=___________。
若温度不变,滴入稀盐酸使C(H+)=5×
10-6mol/L,则此时溶液中的C(OH-)=___________。
由水电离产生的H+与OH-量始终相等,知纯水中C(H+)=C(OH-)。
根据纯水中C(H+)与C(OH-)可求出此温度下水的Kw的值,由Kw的性质(只与温度有关,与离子浓度无关),若温度不变,稀盐酸中Kw仍为此值,利用此值可求出盐酸中的C(OH-)。
答案:
纯水中C(OH-)=C(H+)=2×
10-7mol/L
Kw=C(H+)·
C(OH-)=2×
10-7×
2×
10-7=4×
10-14
稀盐酸中C(OH-)=Kw/C(H+)=(4×
10-14)/(5×
10-6)=8×
10-9mol/L
【例3】.难溶化合物的饱和溶液存在着溶解平衡,例如:
AgCl(s)
Ag++Cl—,Ag2CrO4(s)
2Ag++CrO42—,在一定温度下,难溶化合物饱和溶液离子浓度的乘积为一常数,这个常数用Ksp表示。
已知:
Ksp(AgCl)=[Ag+][Cl-]=1.8×
10-10
Ksp(Ag2CrO4)=[Ag+]2[CrO42-]=1.9×
10-12
现有0.001摩/升AgNO3溶液滴定0.001摩/升KCl和0.001摩/升的K2CrO4的混和溶液,试通过计算回答:
(1)Cl-和CrO42-中哪种先沉淀?
(2)当CrO42-以Ag2CrO4形式沉淀时,溶液中的Cl-离子浓度是多少?
CrO42-与Cl-能否达到有效的分离?
(设当一种离子开始沉淀时,另一种离子浓度小于10-5mol/L时,则认为可以达到有效分离)
(1)当溶液中某物质离子浓度的乘积大于Ksp时,会形成沉淀。
几种离子共同沉淀某种离子时,根据各离子积计算出所需的离子浓度越小越容易沉淀。
(2)由Ag2CrO4沉淀时所需Ag+浓度求出此时溶液中Cl—的浓度可判断是否达到有效分离。
解答:
(1)AgCl饱和所需Ag+浓度[Ag+]1=1.8×
10-7摩/升
Ag2CrO4饱和所需Ag+浓度[Ag+]2=
=4.36×
10-5摩/升
[Ag+]1<
[Ag+]2,Cl-先沉淀。
(2)Ag2CrO4开始沉淀时[Cl-]=
=4.13×
10-6<
10-5,所以能有效地分离。
知识点三:
水的电离平衡的移动
【例4】:
某溶液中由水电离出来的C(OH—)=10-12mol/L,则该溶液中的溶质不可能是()
A、HClB、NaOHC、NH4ClD、H2SO4
由水电离反应式知:
此溶液水电离产生的C(H+)=C(OH—)=10-12mol/L,若溶液中的H+全部来自水的电离,则此溶液显碱性,是因溶有碱类物质所致,若溶液中的H+不仅为水电离所产生,则此溶液显酸性,为酸性物质电离所致。
NH4Cl不可能电离产生H+。
C
下列两题为上题的变式,分析一下变在何处?
解题方法、思路与上题是否一样?
差异何在?
(1)室温下,在纯水中加入某物质后,测得溶液中由水电离产生的C(H+)=10-12mol/L,则加入的物质可能是(假设常温下碳酸、氢硫酸的第一步电离度为0.1%)()
A、通入CO2B、通入H2SC、通入NH3D、加入NaHSO4
(2)某溶液中水电离产生的C(H+)=10-3mol/L,,该溶液中溶质可能是()
①Al2(SO4)3②NaOH③NH4Cl④NaHSO4
A、①②B、①③C、②③D、①④
【例5】能促进水的电离,并使溶液中C(H+)>
C(OH—)的操作是()
(1)将水加热煮沸
(2)向水中投入一小块金属钠(3)向水中通CO2(4)向水中通NH3(5)向水中加入明矾晶体(6)向水中加入NaHCO3固体(7)向水中加NaHSO4固体
A、
(1)(3)(6)(7)B、
(1)(3)(6)C、(5)(7)D、(5)
本题主要考查外界条件对水的电离平衡的影响,请按如下思路完成本题的解:
本题涉及到哪些条件对水的电离平衡的影响?
各自对水的电离平衡如何影响?
结果任何(C(H+)与C(OH—)相对大小)?
归纳酸、碱、盐对水的电离平衡的影响。
D
知识点四:
pH的定义方法
【例6】、下列溶液,一定呈中性的是()
A.由等体积、等物质的量浓度的一元酸跟氢氧化钠溶液混合后所形成的溶液
B.[H+]=1×
10-7mol·
L-1的溶液
C.pH=14-pOH的溶液
D.pH=pOH的溶液(2000年化学试测题)
此题要求将教材中定义pH方法迁移应用于表示pOH以及pH与pOH的关系,根据pH的定义方法,可定义pOH=―lgC(OH―),将室温下水的离子积的表达式C(H+)×
C(OH—)=10―14两边取负对数,―lgC(H+)―lgC(OH―)=―lg10―14,整理得pH+pOH=14。
应用所得关系式分析可得答案。
D
点评:
pOH=―lgC(OH―)、pH+pOH=14两个关系式及其应用均不在教学大纲和考纲范围内,我们不一定要掌握,但将教材中的知识、方法加以迁移应用,进行探究发现是教学大纲和考纲提出的能力要求。
此题作为全国高考化学测试题具有重要的指导意义,值得大家认真去领悟,在随后的2001年上海高考题以及2002年全国理科综合高考题中又出现了类似的题目。
为更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG=
,则下列叙述正确的是
A中性溶液的AG=0
B酸性溶液的AG<0
C常温下0.lmol/L氢氧化钠溶液的AG=12
D常温下0.lmol/L盐酸溶液的AG=12(2001年上海)
有人曾建议用AG表示溶液的酸度(acidityarede),AG的定义为AG=lg([H+]/[OH-])。
下列表述正确的是
A在25℃时,若溶液呈中性,则pH=7,AG=1
B在25℃时,若溶液呈酸性,则pH<7,AG<0
C在25℃时,若溶液呈碱性,则pH>7,AG>0
D在25℃时,溶液的pH与AG的换算公式为AG=2(7-pH)(2002理科综合)
知识点五:
溶液pH的计算
【例7】室温下将n体积pH=10和m体积pH=13两种NaOH溶液混合得pH=12的NaOH溶液,则n:
m=——————————————
此题是关于两种不反应的溶液混合后溶液pH值的计算,根据混合前后溶质(NaOH)量守恒,列式求解
pH=10C(H+)=10-10mol/LC(OH—)=10-4mol/L
pH=13C(H+)=10-13mol/LC(OH—)=10-1mol/L
pH=12C(H+)=10-12mol/LC(OH—)=10-2mol/L
10-4·
n+10-1·
m=(n+m)×
10-2
n:
m=100:
11
规律:
有关混合溶液的pH计算,题设条件可千变万化,正向、逆向思维,数字与字母交替出现,但基本题型只有两种:
(1)混合后不反应,
(2)混合后反应。
对于溶液的稀释,可将水作为浓度为0的溶液,仍属混合后不反应一类,这一类混合溶液的pH应介于两种溶液的pH之间,因而酸、碱溶液无论加多少水稀释,其最终pH均不可能等于纯水的pH(即常温不可能为7)。
混合溶液pH的计算方法也很简单,即设法求出混合溶液的C(H+),若是溶液显碱性,则必须先求出溶液的C(OH—),然后再换算为C(H+)或按OH—量守恒列式求解。
【例8】25º
C,若10体积的某强碱溶液与1体积的某强酸溶液混合后,溶液呈中性,则混合之前,该碱的pH与强酸的pH之间该满足的关系是_______________________
分析:
由题意知,本题为酸、碱混合后完全中和,根据中和反应的实质可知,酸中n(H+)与碱中n(OH-)相等,故有C(H+)酸V酸==C(OH-)碱V碱,由此关系列式可求得结果。
设酸的pH为a,C(H+)酸=10-a,碱的pH为b,C(OH-)碱=10-14/10-b=10-(14-b)
因为混合后溶液呈中性,所以C(H+)酸V酸==C(OH-)碱V碱
10-a×
V=10-(14-b)×
10V=10-(13-b)×
V
10-a=10-(13-b)
两边取负对数:
-lg10-a=-lg10-(13-b),a=13-ba+b=13
即酸的pH与碱的pH之和为13
上面解法尽管可顺利地得出本题的解,但题中的酸碱体积比可以任意变换,则每一变换都得重新求解,这就启发我们能否找出酸、碱pH与两者体积比之间的关系呢?
同时若混合后不显中性其关系又会怎样呢?
将上面的解改为:
C(H+)酸V酸==C(OH-)碱V碱
10-a×
V酸=10-(14-b)×
V碱
10-a·
10-b=10-14·
(V碱/V酸)
两边取负对数得:
a+b=14―lg(V碱/V酸)
若混合后溶液显酸性————————————————————————:
若混合后溶液显碱性—————————————————————————:
同学们在学习中要善于总结、积累,把自己积累的经验、成果用于指导自己的学习。
例如掌握了上述关系后,解下列题目就很轻松。
在20℃时,有PH值为x(x6)的盐酸和PH值为y(y8)的NaOH溶液,取Vx升该盐酸同该NaOH溶液中和,需Vy升NaOH溶液
(1)若x+y=14时,则
=
(2)若x+y=13时,则
(3)若x+y>
14时,则
=(表达式),且VxVy(填<
、>
或=)
4.实战演练
一选择题
1.水是一种极弱的电解质,在室温下平均每n个水分子只有一个水分子能电离,则n是()
A.1×
10-4B.55.6×
107C.1×
107D.6.02×
1021
2.将1mol·
L-1H2SO4溶液100mL与质量分数为10%的NaOH溶液50g混合均匀后,滴入甲基橙指示剂,此时溶液的颜色是()
A.浅紫色B.黄色C.红色D.无色
3.pH定义为pH=-lg{c(H+)},pOH定义为pOH=-lg{c(OH-)},Kw表示25℃时水的离子积常数,则弱酸性溶液中的c(H+)可表示为()
A、Kw/pOHmol/LB、10pOH-14mol/L
C、1014-pOHmol/LD、10-pOHmol/L
4.能使水的电离平衡正向移动,而且所得溶液呈酸性的是()
A.将水加热到100℃时,水的pH=6B.向水中滴加少量稀硫酸
C.向水中滴加少量NaHCO3D.向水中加入少量明矾晶体
5.常温下某溶液中水电离出的C(H+)=1×
10-13mol/L,则下列说法中正确的是()
A.该溶液一定呈酸性B.该溶液一定呈碱性
C.该溶液中一定有C(OH-)=0.1mol/LD.该溶液的pH值为1或13
6.25℃时,在水电离出的C(H+)=1×
10-5摩/升的溶液中,一定能大量共存的是()
A.Al3+、NH4+、SO42-、Cl-B.Mg2+、K+、SO42-、HCO3-
C.K+、Na+、Cl-、SO42-D.Ba2+、Cl-、Na+、PO43-
7.有①、②、③三瓶体积相等,浓度都是1mol/L的HCl溶液,将①加热蒸发至体积减小一半,在②中加入CH3COONa固体(加入后溶液仍呈酸性),③不作改变,然后以酚酞作指示剂,用溶液滴定上述三种溶液,消耗的NaOH溶液的体积是()
A、①=③>
②B、③>
②>
①C、①=②=③D、①<
②=③
8.NH4Cl溶于重水(D2O)生成一水合氨和水合离子的化学式为()
A、NH3·
D2O和HD2O+B、NH3·
HDO和D3O+
C、NH2D·
D2O和DH2O+D、NH2D·
HDO和D3O+
9.室温时,pH=10的氨水和Na2CO3溶液中,水电离产生的C(H+)前者与后者之比()
A.1∶1B.10¯
10∶10¯
4C.10¯
4∶10¯
10D10¯
7
10.25℃,向VmLpH=a的NaOH溶液中滴加pH=b的盐酸10VmL时,溶液中Cl—的物质的量恰好等于加入Na+的物质的量,则此时(a+b)的值为()
A、13B、14C、15D、无法判断
11.在医院中,为酸中毒病人输液不应采用()
A0.9%氯化钠溶液B0.9%氯化铵溶液
C1.25%碳酸氢钠溶液D5%葡萄糖溶液
12.若室温时PH=a的氨水与PH=b的盐酸等体积混和,恰好完全反应,则该氨水的电离度可表示为()A.10(a+b-12)%B.10(a+b-14)%C.10(12-a-b)%D.10(14-a-b)%
13.把40毫升Ba(OH)2溶液加入到120毫升盐酸中,所得的溶液的PH值为2。
如果混和前Ba(OH)2和盐酸两种溶液PH值之和为14,则盐酸的物质的量浓度接近于()
A.0.015摩/升B.0.02摩/升C.0.03摩/升D.0.04摩/升
14.已知NaHSO4在水中的电离方程式为NaHSO4=Na++H++SO42—。
某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液pH为2,对于该溶液,下列叙述不正确的是()
A、该温度高于25℃
B、水电离出来的c(H+)=1.0×
10-10mol/L
C、c(H+)=c(OH—)+C(SO42—)
D、该温度下加入等体积pH值为12的NaOH溶液可使反应后的溶液恰好呈中性
15.能表示人体大量喝水时,胃液的pH变化的是()
pHpHpHpH
7777
0V(H2O)0V(H2O)0V(H2O)0V(H2O)
ABCD
16.4体积pH=9的Ca(OH)2溶液跟1体积pH=13的NaOH溶液混合后,溶液中氢离子浓度为()
A.5×
10-13mol/LB.2×
10-12mol/L
C.1/5(4×
10-9+1×
10-13)mol/LD.1/5(4×
10-5+1×
10-1)mol/L
17.a、b、c、d四种溶液PH值都小于7,已知四种溶液中[H+]和[O
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 化学 58 考点 精选 32 电离 溶液 PH
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
