 高中化学复习知识点等效平衡的建立文档格式.docx
高中化学复习知识点等效平衡的建立文档格式.docx
- 文档编号:17054137
- 上传时间:2022-11-28
- 格式:DOCX
- 页数:16
- 大小:226.42KB
高中化学复习知识点等效平衡的建立文档格式.docx
《高中化学复习知识点等效平衡的建立文档格式.docx》由会员分享,可在线阅读,更多相关《高中化学复习知识点等效平衡的建立文档格式.docx(16页珍藏版)》请在冰豆网上搜索。
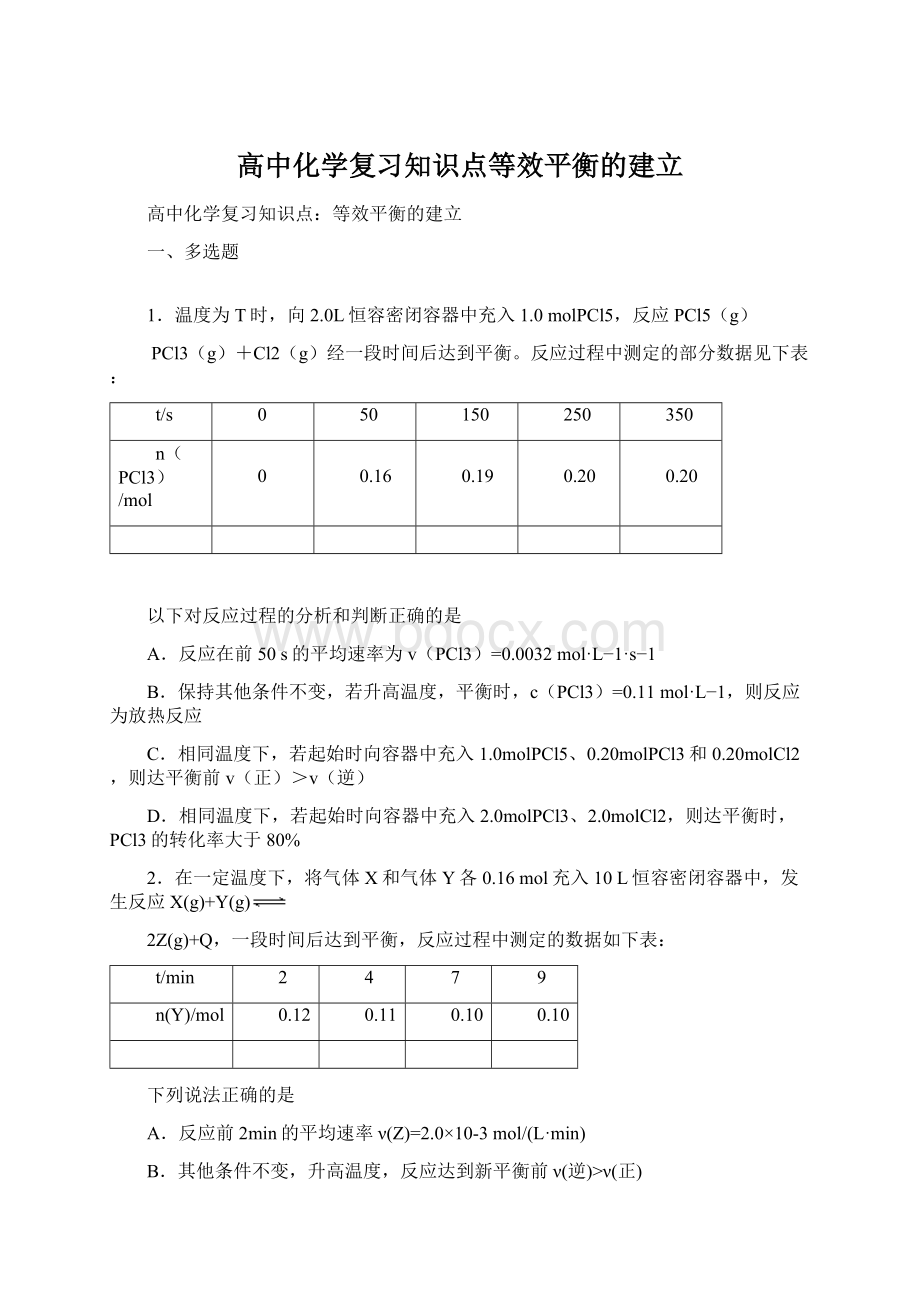
A.反应前2min的平均速率ν(Z)=2.0×
10-3mol/(L·
min)
B.其他条件不变,升高温度,反应达到新平衡前ν(逆)>
ν(正)
C.若无表中数据,可以计算出平衡混合气体的平均相对分子质量
D.其他条件不变,再各充入0.16mol气体X和气体Y,平衡时Z的体积分数增大
二、单选题
3.温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)
PCl3(g)+Cl2(g)经过一段时间后达到平衡。
A.反应在前50s的平均速率,v(PCl3)=0.0032mol·
L-1·
s-1
B.保持其他条件不变,升温,平衡时c(PCl3)=0.11mol/L,则该反应是放热反应
C.相同条件下,起始充入2.0molPCl3和2.0molCl2,达到平衡时,PCl3的转化率小于80%
D.相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,反应达到平衡前v(正)>v(逆)
4.相同温度下,容积相同的甲、乙两个恒容密闭容器中均发生如下反应:
2SO2(g)+O2(g)
2SO3(g)△H=-197kJ/mol,实验测得有关数据如下:
容器编号
起始时各物质的物质的量/mol
达到平衡时体系能量的变化/kJ
SO2
O2
SO3
甲
1
放出热量:
Q1
乙
1.8
0.9
0.2
Q2
下列判断中正确的是
A.两容器中反应的平衡常数不相等
B.达到平衡时SO2的体积分数:
甲<
C.197>
Q1>
D.生成1molSO3(l)时放出的热量等于98.5kJ
5.温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)⇌PCl3(g)+Cl2(g),经过一段时间后达到平衡。
下列说法正确的是( )
A.反应在50s时的速率v(PCl3)=0.0016mol•L﹣1•s﹣1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol•L﹣1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,反应达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0molPCl3和2.0molCl2,达到平衡时,PCl3的转化率小于80%
6.一定温度下,在三个容积均为2L的恒容密闭容器中按不同方式投入反应物,发生反应CO(g)+H2O(g)
CO2(g)+H2(g)△H<
0,测得反应的相关数据如下表所示。
下列说法错误的是()
A.达到平衡时,容器I和容器II中正反应速率:
vI(H2)>
vII(H2)
B.达到平衡时,容器II中c(CO2)>
1.75mol·
L-1
C.达到平衡时,容器I和容器II中的转化率:
αI(CO)=αII(H2O)
D.达到平衡时,容器II和容器I中的平衡常数:
KII>
KI
7.甲、乙两个恒容密闭容器中均发生反应:
C(s)+2H2O(g)=CO2(g)+2H2(g)ΔH>0,有关实验数据如下表所示:
容器
容积/L
温度/℃
起始量/mol
平衡量/mol
平衡常数
C(s)
H2O(g)
H2(g)
T1
2.0
4.0
3.2
K1
T2
1.0
1.2
K2
A.K1=12.8
B.T1<T2
C.T1℃时向甲容器中再充入0.1molH2O(g),则平衡正向移动,CO2(g)的体积分数增大
D.若T2温度下,向2L恒容密闭容器中充入1.0molCO2和2.0molH2,达平衡时,CO2的转化率大于40%
8.两个完全相同的恒容容器A和B,已知A装有SO2和O2各1g,B中装有SO2和O2各2g,在相同温度下达到平衡,设A中SO2的转化率为a%,B中SO2的转化率为b%,则A、B两个容器中SO2的转化率的关系是
A.a%>
b%B.a%=b%
C.a%<
b%D.无法确定
9.如图,在一定温度下,Ⅰ为恒压密闭容器,Ⅱ为恒容密闭容器。
在Ⅰ、Ⅱ中分别加入2molA和2molB,起始时容器体积均为VL,发生如下反应并达到化学平衡状态:
2A十B→xC(g),平衡时两容器中A、B、C的物质的量之比均为1:
3:
6。
下列说法一定正确的是()
A.x的值为2
B.B物质可为固体或液体
C.Ⅰ、Ⅱ容器中从起始到平衡所需时间相同
D.平衡时,Ⅰ容器的体积小于VL
10.如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。
其它条件相同时,在Ⅰ、Ⅱ中分别加入3molZ,起始时容器体积均为VL,发生反应并达到平衡(X、Y状态未知):
aX(?
)+2Y(?
)
3Z(g)。
此时Ⅱ中X、Y、Z的物质的量之比为3:
2:
2,则下列说法一定正确的是()
A.若X、Y均为气态,则平衡时气体平均摩尔质量:
Ⅰ>Ⅱ
B.若X、Y不均为气态,则平衡时X的产率:
C.若X、Y均为气态,则从起始到平衡所需时间:
Ⅰ>
Ⅱ
D.若X为固态,Y为气态,达平衡后若在Ⅱ中再加入1molZ,则新平衡时Z的体积分数变大
三、综合题
11.合成氨技术的创立开辟了人工固氮的重要途径。
回答下列问题:
(1)德国化学家F.Haber从1902年开始研究N2和H2直接合成NH3。
在1.01×
105Pa、250℃时,将1molN2和1molH2加入aL刚性容器中充分反应,测得NH3体积分数为0.04;
其他条件不变,温度升高至450℃,测得NH3体积分数为0.025,则可判断合成氨反应为____填“吸热”或“放热”)反应。
(2)在1.01×
105Pa、250℃时,将2moIN2和2molH2加入aL密闭容器中充分反应,H2平衡转化率可能为___(填标号)。
A=4%B<
4%C4%~7%D>
11.5%
(3)我国科学家结合实验与计算机模拟结果,研究了在铁掺杂W18049纳米反应器催化剂表面上实现常温低电位合成氨,获得较高的氨产量和法拉第效率。
反应历程如图所示,其中吸附在催化剂表面的物种用*标注。
需要吸收能量最大的能垒(活化能)E=____ev,该步骤的化学方程式为____,若通入H2体积分数过大,可能造成___。
(4)T℃时,在恒温恒容的密闭条件下发生反应:
反应过程中各物质浓度的变化曲线如图所示:
①表示N2浓度变化的曲线是____(填“A”、“B”或“C’,)。
与
(1)中的实验条件(1.01×
105Pa、450℃)相比,改变的条件可能是_____。
②在0~25min内H2的平均反应速率为____。
在该条件下反应的平衡常数为___mol-2.L2(保留两位有效数字)。
12.恒温、恒压下,在一个容积可变的容器中发生如下反应:
A(g)+B(g)⇌C(g)
(1)若开始时放入1molA和1molB,达到平衡后,生成amolC,这时A的物质的量为__mol。
(2)若开始时放入3molA和3molB,达到平衡后,生成C的物质的量为__mol
(3)若开始时放入xmolA、2molB和1molC,达到平衡后,A和C的物质的量分别为ymol和3amol,则x=__,y=__。
平衡时,B的物质的量__(填编号)。
A.大于2molB.等于2molC.小于2molD.可能大于、等于或小于2mol
(4)若在(3)的平衡混合物中再加入3molC,待再次达到平衡后,C的物质的量分数是__。
(5)若维持温度不变,在一个与反应前起始体积相同,且容积固定的容器中发生上述反应。
开始时放入1molA和1molB到达平衡后生成bmolC。
将b与
(1)小题中的a进行比较__(填编号)。
作出此判断的理由是__。
A.a>bB.a<bC.a=bD.不能比较a和b的大小。
参考答案
1.CD
【解析】
【分析】
【详解】
A.反应在前50s的平均速率为
,故A错误;
B.原平衡时c(PCl3)=0.1mol·
L−1,保持其他条件不变,若升高温度,平衡时,c(PCl3)=0.11mol·
L−1,则平衡正向移动,升温向吸热反应即正反应为吸热反应,故B错误;
C.根据数据得出平衡时n(PCl3)=0.2mol,n(Cl2)=0.2mol,n(PCl5)=1mol−0.2mol=0.8mol,因此平衡常数
,相同温度下,若起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,
,则反应正向进行,即达平衡前υ(正)>υ(逆),故C正确;
D.相同温度下,若起始时向容器中充入1.0molPCl3、1.0molCl2,则达平衡时,与原平衡达到等效,n(PCl3)=0.2mol,n(Cl2)=0.2mol,n(PCl5)=0.8mol,因此PCl3的转化率等于80%,若起始时向容器中充入2.0molPCl3、2.0molCl2,相当于两个容器各充入1.0molPCl3、1.0molCl2,则达平衡时,转化率为80%,将两个容器压缩到一个容器,平衡向生成PCl5方向移动,PCl3消耗,则达平衡时,PCl3的转化率大于80%,故D正确。
综上所述,答案为CD。
2.BC
A.2min内Y物质的量变化为△n(Y)=0.16mol-0.12mol=0.04mol,故ν(Y)=
=2.0×
min),用不同物质表示同一反应时速率之比等于化学计量数之比,故ν(Z)=2ν(Y)=4.0×
min),A错误;
B.该反应正反应是放热反应,升高温度,化学平衡向吸热的逆反应移动,反应达到新平衡前ν(逆)>
ν(正),B正确;
C.该反应是反应前后气体体积相等的反应,气体的物质的量不变,气体的质量不变,所以即使无表格数据,该混合气体的平均相对分子质量也不变,C正确;
D.由于该反应是反应前后气体体积不变的反应,在其它条件不变时,再充入0.16mol气体X和Y,压强增大,化学平衡不移动,平衡时Z的体积分数不变,D错误;
故合理选项是BC。
3.D
A.反应在前50s的平均速率,v(PCl3)=
=0.0016mol·
s-1,A错误;
B.平衡时c(PCl3)=
=0.1mol,保持其他条件不变,升温,平衡时c(PCl3)=0.11mol/L,说明升高温度,平衡正向移动,正反应是吸热反应,B错误;
C.同条件下,起始充入2.0molPCl3和2.0molCl2,等效为起始加入2.0molPCl5,与原平衡相比,压强增大,平衡向逆反应方向移动,平衡时PCl5的转化率较原平衡低,故平衡时PCl3的物质的量小于0.4mol,参加反应的PCl3的物质的量大于1.6mol,则达到平衡时PCl3的转化率大于
×
100%=80%,C错误;
D.对于可逆反应:
所以平衡常数K=
=0.025mol/L,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,起始时PCl5的浓度为0.5mol/、PCl3的浓度为0.1mol/L、Cl2的浓度为0.1mol/L,浓度熵Qc=
=0.02mol/L,Qc<K,说明反应向正反应方向进行,v(正)>v(逆),D正确。
答案选D。
4.C
A.甲、乙两个容器内温度相等,则平衡常数相等,A错误;
B.将乙中转化为到左边,SO2、O2的起始物质的量相当于2mol、1mol,甲、乙温度、体积相等,故二者为完全等效平衡,平衡时SO2的体积分数相等,B错误;
C.甲、乙为完全等效平衡,平衡时二氧化硫的物质的量相等,故甲中参加反应的二氧化硫更多,则放出热量:
Q2,由于该反应为可逆反应,反应物不能完全反应,故197>
Q1,则放出热量:
197>
Q2,C正确;
D.同种物质,液态的能量低于气态,生成液态三氧化硫放出的热量更多,即生成1molSO3(l)时放出的热量大于98.5kJ,D错误;
故合理选项是C。
5.C
A.反应在前50s内的平均速率
,不是50s时,故A错误;
B.平衡时c(PCl3)=0.20mol÷
2L=0.10mol·
L−1,保持其他条件不变,升高温度,c(PCl3)增加,说明平衡正向移动,即正向是吸热反应,即反应的△H>
0,故B错误;
C.平衡时平衡常数为
,相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,此时浓度商
,向正方向进行,则反应达到平衡前υ(正)>υ(逆),故C正确;
D.相同温度下,起始时向容器中充入2.0molPCl3和2.0molCl2,等效为起始加入2.0molPCl5,可以理解为先用两个相同大小的容器每个容器装1molPCl5,达到平衡时,每个容器中有0.2molPCl3,总共有0.4molPCl3,则消耗1.6molPCl3,PCl3的转化率
,将两个容器压缩到一个容器中,压强增大,平衡向逆反应方向移动,消耗PCl3物质的量大于1.6mol,则转化率大于80%,故D错误。
综上所述,答案为C。
【点睛】
化学谈速率一般是指一段时间内的平均速率,不是瞬时速率。
6.C
A.达到平衡时,容器I和容器II中达到平衡时,由于T1温度高,速度越快,因此正反应速率:
vI(H2)>
vII(H2),故A正确;
B.达到平衡时,容器II中如果在T1温度时,c(H2)=1.75mol·
L-1,c(CO2)=1.75mol·
L-1,在T2时,降低温度,平衡向放热方向即正向移动,因此c(CO2)>
L-1,故B正确;
C.达到平衡时,容器I和容器Ⅲ中的转化率两者相等即αI(CO)=αⅢ(H2O),但由于容器II温度低,平衡正向移动,因此αII(H2O)>
αⅢ(H2O),所以αII(H2O)>
αI(CO),故C错误;
D.达到平衡时,T2时,降低温度,平衡向放热方向即正向移动,因此容器II和容器I中的平衡常数:
KI,故D正确。
7.A
A.根据表中数据可知甲容器中反应达到平衡时,c(H2O)=0.4mol·
L-1,c(CO2)=0.8mol·
L-1,c(H2)=1.6mol·
L-1,K1=
=12.8,A正确;
B.乙容器中反应达到平衡时,c(H2O)=0.8mol·
L-1,c(CO2)=0.6mol·
L-1,c(H2)=1.2mol·
L-1,K2=
=1.35,K1>K2,该反应为吸热反应,K减小说明反应逆向进行,则温度降低,即T1>T2,B错误;
C.向容器中再充入0.1molH2O(g),相当于增大压强,平衡逆向移动,则CO2的体积分数减小,C错误;
D.与乙容器中的量比较,1.0molCO2和2.0molH2相当于1.0molC和2.0molH2O,若体积不变,则平衡时是完全等效的,即CO2为0.6mol,CO2的转化率为40%,但由于体积增大,压强减小,反应向生成CO2的方向移动,则CO2的转化率小于40%,D错误;
故答案为:
A。
8.C
2SO2+O2
2SO3,是体积缩小的反应,加压后平衡正向移动,SO2的转化率变大。
先假定乙的体积是甲的两倍,达到平衡后将乙加压使体积与甲相同,此反应是气体体积减小的反应,缩小体积是,乙的压强增大,平衡正向移动.所以,若甲容器中SO2的转化率为a%,则乙的SO2的转化率将大于甲的,即大于a%<
b%。
答案选C。
9.C
在一定温度下,Ⅰ为恒压密闭容器,Ⅱ为恒容密闭容器,平衡时两容器中A、B、C的物质的量之比均为1:
6,说明A、B转化率相同,则A、B的平衡状态相同,说明反应2A+B⇌xC(g)中,反应前后气体的化学计量数之和相等,列“三段式”
由题意:
(2-2a):
(2-a):
ax=1:
3:
6,则:
,
,解得a=
,x=3,由此可得A、B、C都为气体,以此解答该题。
A.根据分析,x=3,故A错误;
B.根据分析,B为气体,不能为固体或液体,故B错误;
C.反应2A+B⇌xC(g)中,反应前后气体的化学计量数之和相等,气体的压强不变,体积不变,达到平衡用的时间相同,故C正确;
D.平衡时,Ⅰ容器的体积等于VL,故D错误;
10.C
设达平衡时Z反应的物质的量为3x,则:
aX(?
)+2Y(?
3Z(g)
起始量:
0
3
转化量:
ax
2x
3x
平衡量:
2x
3-3x
由(ax):
(2x):
(3-3x)=3:
2:
2可得x=0.6,a=3,以此进行分析。
A.若X、Y均为气态,反应方程式为3X(g)+2Y(g)
3Z(g),I是恒压密闭容器,II是恒容密闭容器。
则反应Ⅱ压强大于反应Ⅰ压强,根据压强增大,反应向体积减小的方向移动可知,Ⅰ中气体的总物质的量大于Ⅱ中气体的总物质的量,量容器中气体的质量相等,则平衡时气体平均摩尔质量:
I<II,选项A错误;
B.若X、Y不均为气态,如X为气态,则该反应方程式中气体的化学计量数之和左右相等,压强对平衡没有影响,则平衡时X的产率:
I═II;
如Y为气态,则反应中反应物的气体的计量数小于生成物气体的化学计量数,增大压强平衡左移,则平衡时X的物质的量:
I>II,选项B错误;
C.若X、Y均为气态,反应方程式为3X(g)+2Y(g)
则反应Ⅱ压强大于反应Ⅰ压强,根据压强增大,化学反应速率增大,则,则从起始到平衡所需时间:
I>II,选项C正确;
D.若X为固态,Y为气态,由于反应前后气体的化学计量数不相等,到达平衡后若在II中再加入1molZ,相当于在原来基础上缩小体积为原来的一半,压强增大,则平衡逆向移动,Z的体积分数减小,选项D错误;
11.放热D1.54NH3*+NH3=2NH3占据催化剂活性位点过多B加压强或降温0.006mol·
min-10.73
(1)升高温度,NH3体积分数降低;
105Pa、250℃时,将2moIN2和2molH2加入aL密闭容器中充分反应,与在1.01×
105Pa、250℃时,将1moIN2和1molH2加入aL密闭容器中充分反应比,相当于加压;
(3)吸收能量最大的能垒,即相对能量的差最大;
根据图示写方程式;
(4)根据反应方程式,N2、H2、NH3的变化量比为1:
2;
图氢气的转化率为25%,
(1)中氢气的转化率是11.5%,根据转化率的变化分析;
②A表示氢气的浓度变化,根据
计算H2的平均反应速率;
根据
计算平衡常数;
(1)升高温度,NH3体积分数降低,说明升高温度平衡逆向移动,正反应放热;
,x=0.0384,H2平衡转化率
,在1.01×
105Pa、250℃时,将2moIN2和2molH2,相当于加压,平衡正向移动,氢气转化率增大,H2平衡转化率>
11.5%,故选D;
(3)根据图示,吸收能量最大的能垒,即相对能量的差最大是-1.02-(-2.56)=1.54;
根据图示,该步的方程式是NH3*+NH3=2NH3;
若通入H2体积分数过大,氢分子占据催化剂活性位点过多;
(4)①根据反应方程式,N2、H2、NH3的变化量比为1:
2,所以表示N2浓度变化的曲线是B;
(1)中氢气转化率11.5%,1:
3时氢气转化率更低,图中氢气转化率25%,故只能考虑压强、温度的影响,可以采用加压或降温的方法;
②A表示氢气的浓度变化,
0.006mol·
min-1;
mol-2.L2。
12.1﹣a3a23(1﹣a)D
A因为本小题中容器容积不变,而
(1)小题中容器的容积缩小,所以本小题的容器中的压力小于
(1)小题容器中的压力,有利于逆向反应
(1)由方程式可知,生成C的物质的量=参加反应A的物质的量,平衡时A的物质的量=A的起始物质的量-参加反应的A的物质的量;
(2)恒温恒压下,若开始时放入3molA和3molB,与
(1)中A、B的物质的量之比均为1:
1,则为等效平衡,平衡时反应物的转化率相同;
(3)若开始时放入xmolA,2molB和1molC,完全转化到左边满足3molA和3molB,与
(1)中A、B的物质的量之比均为1:
1,则为等效平衡,平衡时反应物的转化率相同,可以得到3amolC,平衡时A、B的物质的量分别为
(1)中A、B的3倍,结合a<1判断;
(4)由(3)分析可知,若在(3)的平衡混合物中再加入3molC,等效为开始加入6molA和6molB,与
(1)中平衡为等效平衡,平衡时反应物的转化率相同,则平衡时C的物质的量分数与
(1)中相同;
(5)反应A(g)+B(g)⇌C(g)是气体体积减少的反应,在恒温恒容容
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 复习 知识点 等效 平衡 建立
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
