 高考化学几类重要的实验解题方法Word文件下载.docx
高考化学几类重要的实验解题方法Word文件下载.docx
- 文档编号:16774235
- 上传时间:2022-11-26
- 格式:DOCX
- 页数:10
- 大小:304.11KB
高考化学几类重要的实验解题方法Word文件下载.docx
《高考化学几类重要的实验解题方法Word文件下载.docx》由会员分享,可在线阅读,更多相关《高考化学几类重要的实验解题方法Word文件下载.docx(10页珍藏版)》请在冰豆网上搜索。
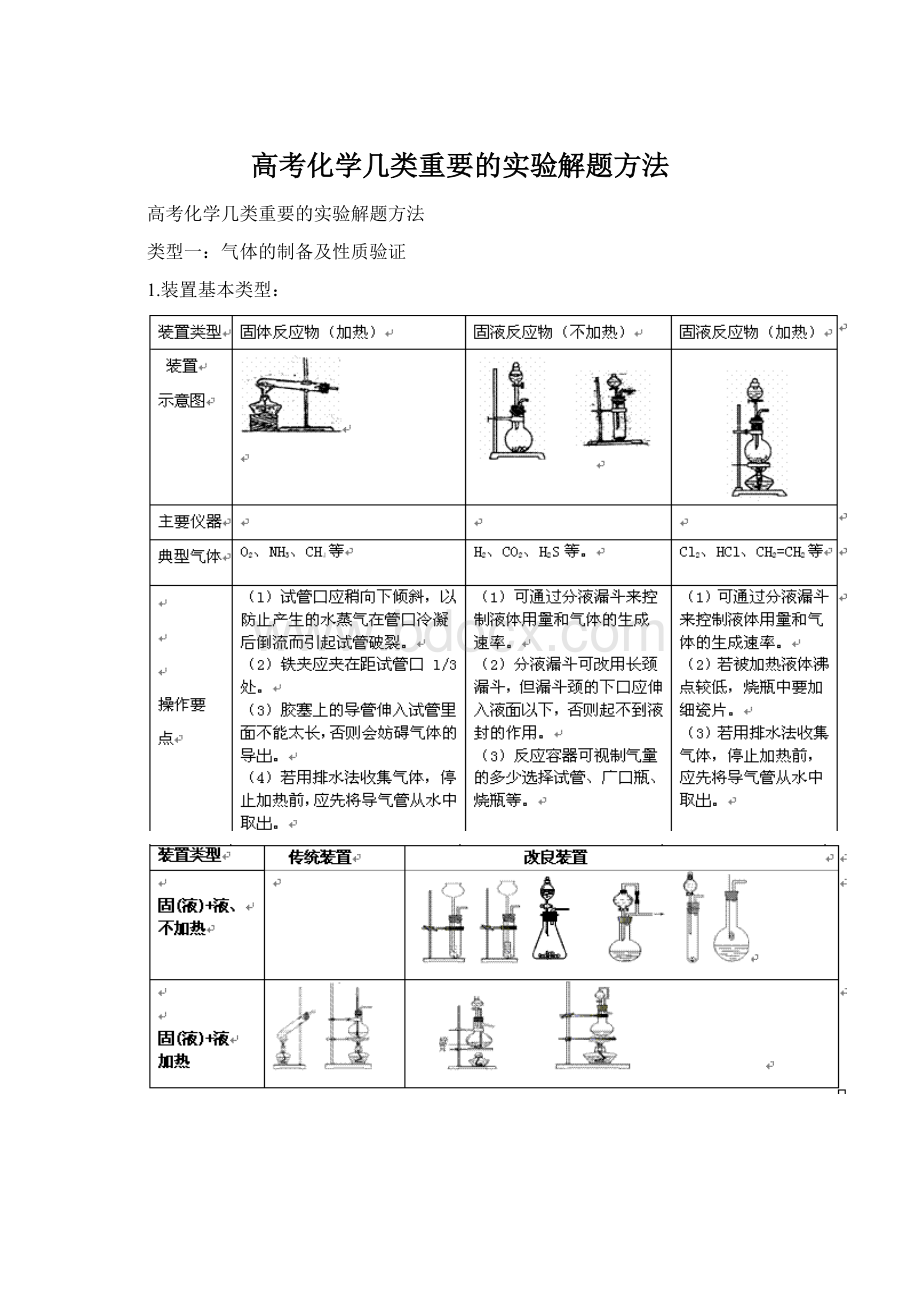
有还原性的气体不能选用有氧化性的干燥剂。
能与气体反应的物质不能选作干燥剂,如不能用CaCI2来干燥NH3(因生成CaCl2·
8NH3),不能用浓H2SO4干燥NH3、H2S、HBr、HI等。
(4)气体净化与干燥装置连接次序
洗气装置总是进气管插入接近瓶底,出气管口略出瓶塞。
干燥管总是大口进,小口出气。
一般情况下,若采用溶液作除杂试剂,则是先除杂后干燥;
若采用加热除去杂质,则是先干燥后加热。
对于有毒、有害的气体尾气必须用适当的溶液加以吸收(或点燃),使它们变为无毒、无害、无污染的物质。
如尾气Cl2、SO2、Br2(蒸气)等可用NaOH溶液吸收;
尾气H2S可用CuSO4或NaOH溶液吸收;
尾气CO可用点燃法,将它转化为CO2气体。
4、收集装置
5、尾气处理装置-安全装置
(1)直接吸收
(2)防止倒吸装置的设计
①切断装置:
将有可能产生液体倒吸的密闭装置系统切断,以防止液体倒吸,如实验室中制取氧气、甲烷时,通常用排水法收集气体,当实验结束时,必须先从水槽中将导管拿出来,然后熄灭酒精灯。
②设置防护装置:
a.倒立漏斗式:
这种装置可以增大气体与吸收液的接触面积,有利于吸收液对气体的吸收。
当易溶性气体被吸收液吸收时,导管内压强减少,吸收液上升到漏斗中,由于漏斗容积较大,导致烧杯中液面下降,使漏斗口脱离液面,漏斗中的吸收液受自身重力的作用又流回烧瓶内,从而防止吸收液的倒吸。
下一个装置所示,对于易溶于水难溶于有机溶剂的气体,气体在有机溶剂不会倒吸。
B.肚容式:
当易溶于吸收液的气体由干燥管末端进入吸收液被吸收后,导气管内压强减少,使吸收液倒吸进入干燥管的吸收液本身质量大于干燥管内外压强差,吸收液受自身重量的作用又流回烧杯内,从而防止吸收液的倒吸。
这种装置与倒置漏斗很类似。
C.蓄液式:
当吸收液发生倒吸时,倒吸进来的吸收液被预先设置的蓄液装置贮存起来,以防止吸收液进入受热仪器或反应容器。
这种装置又称安全瓶。
d.平衡压强式:
为防止分液漏斗中的液体不能顺利流出,用橡皮管连接成连通装置(见恒压式);
e.防堵塞安全装置式:
为防止反应体系中压强减少,引起吸收液的倒吸,可以在密闭装置系统中连接一个能与外界相通的装置,起着自动调节系统内外压强差的作用,防止溶液的倒吸。
F.为防止粉末或糊状物堵塞导气管,可将棉花团置于导管口处。
g.液封装置:
为防止气体从长颈漏斗中逸出,可在发生装置中的漏斗末端套住一只小试管
(3)防污染安全装置:
燃烧处理或袋装
①有毒、污染环境的气体不能直接排放。
②尾气吸收要选择合适的吸收剂和吸收装置。
直接吸收:
Cl2、H2S、NO2防倒吸:
HCl、NH3、SO2
常用吸收剂:
水,NaOH溶液,硫酸铜溶液
③可燃性气体且难用吸收剂吸收:
燃烧处理或袋装。
如CO。
类型二:
探究性实验题
一、探究性实验的一般思路
1、准确地把握实验目的2、利用已学知识,分析如何实现这个目的--实验原理3、结合实验材料,初步确定设计对策--实验方案
基础题型:
一般是判断反应产物、判断氧化剂还原剂、判断结论是否正确等,题目容易,属于必得分部分。
2010年广东高考题第33题:
(16分)某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。
(1)请完成SO2与过量NaOH溶液反应的化学方程式:
SO2+2NaOH=________________。
(2)反应Cl2+Na2SO3+2NaOH===2NaCl+Na2SO4+H2O中的还原剂为________________。
提高题型,一般是推断产物的成分,提出对产物成分的假设,题目有一定难度,但题目一般会先做出1-2个假设例子,只要理解了题目的意图,也比较容易得分。
对于提出假设通常有两种类型:
第一种是提出三个假设:
假设1、×
×
存在;
假设2、×
假设3、×
和×
都存在或都不存在(判断依据在于两者能否反应);
第二种类型是有三个以上的假设:
假设4、×
存在……最后一般仅要求验证某个假设。
这就要求我们认真审题,根据要求验证的假设来设计鉴定实验。
如2010年广东高考题第33题:
(3)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO42-。
请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响)。
①提出合理假设。
假设1:
只存在SO32-;
假设2:
既不存在SO32-也不存在ClO-;
假设3:
_____________。
拓展题型,一般是结合所给的实验材料,设计实验方案。
在设计时要遵循以下四个原则:
科学性原则;
对照性原则;
等量性原则;
控制变量原则。
②设计实验方案,进行实验。
请在答题卡上写出实验步骤以及预期现象和结论。
限选实验试剂:
3moL/LH2SO4、1moL/LNaOH、0.01mol/LKMnO4、淀粉-KI溶液、紫色石蕊试液。
实验操作预期现象与结论
步骤1:
取少量吸收液于试管中,滴加3moL/LH2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中.
预期现象与结论
步骤2:
步骤3:
三设计、评价或改进实验方案的要求
原理正确,步骤简捷条件适宜,操作简单原料丰富,价格低廉转化率高,减少污染四、答题模式
(1)取适量的物质(药品)进行实验(操作)如果有现象,则得出(结论)
(2)(对另一种情况设计判断)另取等量的物质(药品)进行对照实验(操作)如果有(现象),则得出(结论)。
发生装置生成……产生……制取……
除杂装置除去(吸收)……防止……干扰(影响)除去……中的杂质,以免影响测量结果
性质实验装置(收集装置)与……反应验证……说明……比较……
尾气吸收装置吸收……防止……的污染(影响)
要求:
1、全面2、准确3、有时需要指明何处海(溶液)1、颜色由…变成…2、液面上升或下降(形成液面差)3、溶液变混浊4、生成(产生)…沉淀5、溶液发生倒吸6、产生大量气泡7、有气体从溶液中逸出8、有液体溢出
陆(固体)1、固体表面产生大量气泡2、固体逐渐溶解3、固体体积逐渐变小(变细)4、颜色由…变成…
空(气体)1、生成…色(味)气体2、气体由…色变成…色3、先变…后…(加深、变浅、褪色)
4.规范书写操作目的、原因、理由
答题思路:
1、这样做有什么好处2、不这样做有什么影响好处:
1、直接作用2、根本目的“坏处”:
如果(不这样)……那么会(怎样)
例1、(2011广东)某种催化剂为铁的氧化物。
化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:
将适量稀硝酸加入少许样品中,加热溶解;
取少许溶液,滴加KSCN溶液后出现红色。
一位同学由此得出该催化剂中铁元素价态为+3的结论。
(1)请指出该结论是否合理并说明理由
。
(2)请完成对铁元素价态的探究:
限选实验仪器与试剂:
烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹:
3mol·
L-1H2SO4/3%H2O2、6mol·
L-1HNO3/0.01mol·
L-1KmnO4、NaOH稀溶液、0.1mol·
L-1Kl、20%KSCN、蒸馏水。
①提出合理假设假设1:
;
假设3:
。
②设计实验方案证明你的假设③实验过程:
根据②的实验方案,进行实验。
例2.某白色粉末可能含有K2SO4、NH4Cl、NaCl。
请设计合理实验探究该白色粉末的组成。
限选实验仪器与试剂:
烧杯、试管、玻璃棒、量筒、胶头滴管、药匙、酒精灯、火柴、试管夹、镊子;
红色石蕊试纸、1mol·
L-1硫酸、1mol·
L-1硝酸、1mol·
L-1盐酸、BaCl2溶液、2mol·
L-1NaOH溶液、Ba(NO3)2溶液、AgNO3溶液、蒸馏水。
完成以下实验探究过程:
(1)提出假设:
根据题意,该白色粉末的组成有____种可能的情况
(2)设计实验方案基于该粉末中上述三种盐均存在这一假设,设计出实验方案(不要作答)。
(3)根据②的实验方案(K2SO4、NH4Cl、NaCl均存在),叙述实验操作、预期现象和结论。
实验步聚
实验操作
预期现象和结论
第一步
第二步
第三步
第四步
类型三:
工艺流程题
化学工艺流程题近几年是高考的热点,所占的分值也相当重,但由于此类试题陌生度高,对学生的能力要求也大,加上有的试题文字量大,学生在没做之前往往就会产生畏惧感,所以这类题的得分不是很理想。
要解好这一类题,学生最重要的是要克服畏惧心理,认真审题,找到该实验的目的。
一般来说,流程题只有两个目的:
一是从混合物中分离、提纯某一物质;
另一目的就是利用某些物质制备另一物质。
此类型题目的基本步骤是:
①从题干中获取有用信息,了解生产的产品。
②分析流程中的每一步骤,从几个方面了解流程:
A、反应物是什么B、发生了什么反应C、该反应造成了什么后果,对制造产品有什么作用。
抓住一个关键点:
一切反应或操作都是为获得产品而服务。
③从问题中获取信息,帮助解题。
了解流程后着手答题。
对反应条件的分析可从以下几个方面着手:
1、对反应速率有何影响?
2、对平衡转化率有何影响?
3、对综合生产效益有何影响?
如原料成本,原料来源是否广泛、是否可再生,能源成本,对设备的要求,环境保护(从绿色化学方面作答)。
常见文字叙述套路:
1、洗涤沉淀:
往漏斗中加入蒸馏水至浸没沉淀,待水自然流下后,重复以上操作2-3次。
2、从溶液中得到晶体:
蒸发浓缩-冷却结晶-过滤-(洗涤)。
注意:
①在写某一步骤是为了除杂是,应该注明“是为了除去XX杂质”,只写“除杂”等一类万金油式的回答是不给分的。
②看清楚是写化学反应方程式还是离子方程式,注意配平。
1、海水的综合利用可以制备金属镁,其流程如下图所示:
(1)若在空气中加热MgCl2·
6H2O生成的是Mg(OH)Cl或MgO,写出相应反应的化学方程式;
用电解法制取金属镁时,需要无水氯化镁。
写出用电解法制取金属镁的化学方程式。
(2)Mg(OH)2沉淀中混有Ca(OH)2应怎样除去?
写出实验步骤。
________________________________________________________________________
。
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明这三种情况下使用玻璃棒的目的:
溶解时:
_________________________________________________________;
过滤时:
蒸发时:
_________________________________________________________。
2、氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为;
与电源负极相连的电极附近,溶液PH(选填:
不变、升高或下降)。
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为:
(3)如果精盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是(选填:
a、b、c);
a.Ba(OH)2b.Ba(NO3)2c.BaCl2
(4)为有效除去Ca2+、Mg2+、SO42-加入试剂的合理顺序为(选填:
a.先加NaOH,后加NaCO3,再加钡试剂b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过、冷却、(填操作名称)除去NaCl。
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;
采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为。
3.硅单质及其化合物应用范围很广。
请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。
三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
①写出由纯SiHCl3制备高纯硅的化学反应方程式。
②整个制备过程必须严格控制无水无氧。
SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式;
H2还原SiHCl3过程中若混O2,可能引起的后果是。
(2)下列有关硅材料的说法正确的是(填字母)。
A、碳化硅化学性质稳定,可用于生产耐高温水泥
B、氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
C、高纯度二氧化硅可用于制造高性能通讯材料—光导纤维
D、普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
E、盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅
(3)硅酸钠水溶液俗称水玻璃。
取少量硅酸钠溶液于试管中,逐滴加入饱和氯化铵溶液,振荡。
写出实验现象并给予解释
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 化学 重要 实验 解题 方法
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
