 高三一轮复习第一讲化学物质的组成性质和分类文档格式.docx
高三一轮复习第一讲化学物质的组成性质和分类文档格式.docx
- 文档编号:16519971
- 上传时间:2022-11-24
- 格式:DOCX
- 页数:22
- 大小:561.65KB
高三一轮复习第一讲化学物质的组成性质和分类文档格式.docx
《高三一轮复习第一讲化学物质的组成性质和分类文档格式.docx》由会员分享,可在线阅读,更多相关《高三一轮复习第一讲化学物质的组成性质和分类文档格式.docx(22页珍藏版)》请在冰豆网上搜索。
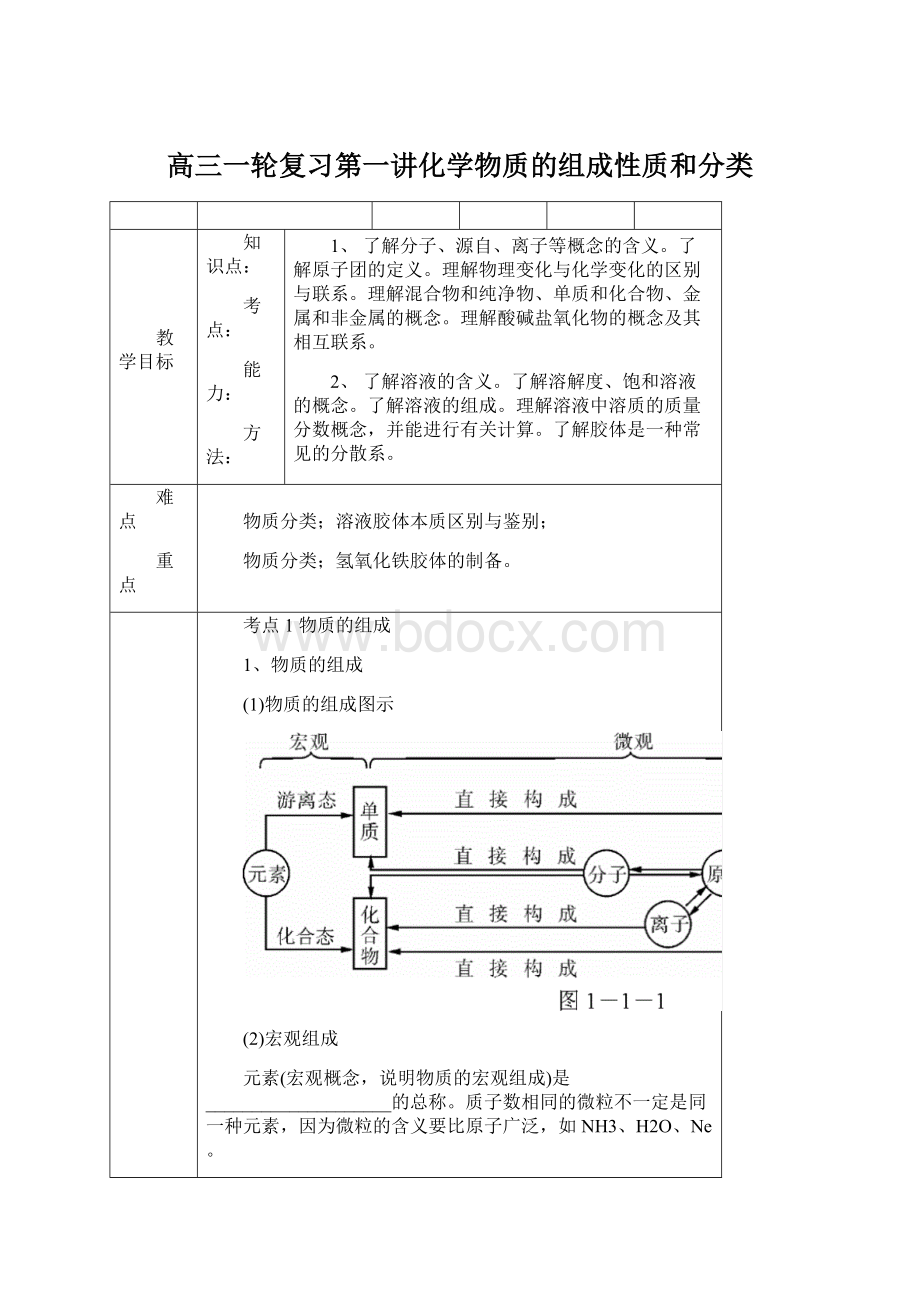
1.由分子构成的物质有哪些?
4.不同类别的物质,根据其组成特点,化学式的书写有哪些规律?
答:
①金属单质由金属原子构成,金属单质的化学式就是其元素符号;
②非金属单质(除金刚石、硅等直接用元素符号表示)一般多原子分子用元素符号加数字角标表示;
稀有气体为单原子分子;
③化合物一般可根据下列规律书写:
化学式中各元素的化合价代数和为零。
5.H2O表示的含义有哪些?
①表示水;
②表示水由氢、氧两种元素组成;
③表示一个水分子;
④表示每个水分子由两个氢原子和一个氧原子构成。
6.由离子构成的物质(离子化合物)有哪些?
绝大多数盐、强碱、活泼金属氧化物等都是离子化合物基础跟踪练习:
1、下列有关微粒之间关系和特征描述正确的是
2、以下说法正确的是
A.1molH2O分子中含有2molH元素和1molO元素
B.1个CO2分子由1个C原子和1个O2分子组成
C.2molKClO3中含有2molCl-
D.35Cl和37Cl是两种不同的Cl原子
考点2物质的变化与性质
1、物质的变化
物理变化
化学变化
区别
从微观的角度看,构成物质的分子本身没有发生变化,只是分子之间的距离发生了改变
构成物质的分子本身发生了变化,生成了新的分子,但原子和元素的种类并不发生变化
关系
物质发生物理变化时不一定发生了化学变化,但发生化学变化时一定伴随着物理变化
2.物质的性质
(1)物理性质
不需要通过化学变化就能表现出来的性质。
通常为物质的颜色、气味、状态、熔点、沸点、密度、硬度、溶解性等。
(2)化学性质
需要通过化学变化才能表现出来的性质。
如钠可以和氧气、氯气、水、酸等反应。
2、物质变化的表示方法
1.常见物理变化:
①升华、②萃取、③分液、④蒸馏(分馏)、⑤吸附、⑥渗析、⑦盐析、⑧胶体聚沉、⑨电泳、⑩金属导电、⑪焰色反应、⑫电离等。
2.常见化学变化:
①风化、②裂化、③电解质溶液导电、④老化、⑤炭化、⑥干馏、⑦脱水、⑧蛋白质变性、⑨水解、⑩同素异形体互变、⑪电解、⑫熔融盐导电等。
化学之“化”
风化——结晶水合物在自然条件下失去部分或全部结晶水的过程。
催化——催化剂改变反应速率的过程。
催化剂本身参与化学反应,但其质量和性质在反应前后都不改变。
歧化——同一物质中同一元素且为同一价态原子间发生的氧化还原反应。
酸化——向某物质中加入稀酸使溶液呈酸性的过程。
钝化——常温下浓硫酸、浓硝酸使Fe、Al等金属表面氧化而生成一种致密的氧化膜的现象。
水化——物质与水作用的过程。
氢化(硬化)——液态油在一定条件下与H2发生加成反应生成固态脂肪的过程
皂化——油脂在碱性条件下发生水解反应的过程。
老化——橡胶、塑料等制品露置于空气中,因受空气氧化、日光照射等作用而变硬发脆的过程。
硫化——向橡胶中加硫,改变结构以改善橡胶的性能,减缓其老化速度的过程。
裂化——在一定条件下,分子量大、沸点高的烃断裂为分子量小、沸点低的烃的过程。
酯化——醇与酸反应,生成酯和水的过程。
硝化——苯环上的H被—NO2取代的过程。
磺化——苯环上的H被—SO3H取代的过程。
基础跟踪练习:
3.下列说法正确的是()
A.明矾净水过程中不涉及化学变化B.由同种元素组成的物质一定是纯净物
C.风化、石油分馏和碘的升华都是物理变化
D.在化学反应中,反应前后原子种类、数目和质量一定不变
考点3物质的分类
1.物质的分类
(1)物质的分类方法:
①交叉分类法;
②树状分类法。
(2)物质的树状分类
2.几组常见物质比较
(1)纯净物与混合物
纯净物
混合物
由组成
区
别
物质种类
只有一种
至少有两种
组成特点
固定
不固定,各成分保持其原有性质
表达式
能用一个化学式表示
不能用一个化学式表示
联系
(2)单质和化合物
单质
化合物
由_________组成的纯净物
由____________组成的纯净物
1只由一种元素组成;
2②不能发生分解反应
1至少由两种元素组成;
2②在一定条件下可能发生分解反应
相同点
都是纯净物
(3)氧化物
类别
注意点
酸性氧化物(酸酐)
有非金属氧化物,也有金属氧化物,但酸酐不一定是酸性氧化物(如乙酸酐)
碱性氧化物
均为金属氧化物
两性氧化物
与酸和碱反应都可生成盐和水的氧化物
(4)酸和盐的分类
(1)酸:
根据分子中最多能够电离出的H+数,分为一元酸、二元酸、三元酸、多元酸。
如:
H3PO3(分子结构如图1-1-3)只有2个-OH直接与
中心原子成键,最多可电离2个H+,故为二元酸。
(2)盐:
分为正盐、酸式盐、碱式盐、复盐。
H3PO4是三元酸,其钠盐有正盐(Na3PO4)、酸式盐(NaH2PO4、
Na2HPO4);
碱式盐如Cu2(OH)2CO3;
复盐如KAl(SO4)2·
12H2O。
3.化学反应的分类
1.常见混合物种类:
①高分子(如蛋白质、纤维素、聚合物、淀粉等);
②分散系(如溶液、胶体、浊液等);
③同分异构体(如二甲苯总是混合物,含邻、间、对三种)。
2.生活生产中常见的混合物:
①氨水、氯水、王水、水玻璃、福尔马林、盐酸、浓硫酸;
②爆鸣气(2体积氢气跟1体积氧气)、水煤气、天然气、焦炉气(氢气、甲烷)、石油气、裂解气(甲烷及碳二至碳五烯烃和烷烃)、空气;
③钢、生铁、漂白粉、碱石灰、铝热剂、玻璃、煤;
④煤焦油(主要含有苯、甲苯、二甲苯、萘、蒽等芳烃,以及芳香族含氧化合物)、石油及其各种馏分、植物油和动物油。
3.金属氧化物一定是碱性氧化物吗?
非金属氧化物一定是酸性氧化物吗?
酸性氧化物一定是非金属氧化物吗?
碱性氧化物一定是金属氧化物吗?
4、氧化物的两种分类及相互关系
5.物质分类的依据通常有组成和性质。
下列物质分类中,只考虑组成的是
A.Na2SO4是钠盐、硫酸盐、正盐B.HNO3是一元酸、强酸、挥发性酸
C.Mg(OH)2是二元碱、难溶性碱、中强碱D.Al2O3是两性氧化物、金属氧化物、最高价氧化物
6、分类是化学学习和研究的常用手段。
下列分类依据和结论都正确的是
A.HClO、HNO3、H2SO4都具强氧化性,都是氧化性酸
B.H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物
C.HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质
D.HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸
7.(双选)用图1-1-2表示的一些物质或概念间的从属关系不正确的是()
考点4分散系、胶体、溶液
1.分散系
(1)概念
物质的粒子分散于另一物质里所组成的体系叫分散系。
其中被分散的物质称作分散质,分散其他物质的物质称作分散剂。
即分散系=分散质+分散剂。
分散系包括:
溶液、胶体和浊液。
(2)三种分散系的比较
分散系
溶液
胶体
浊液
分散质微粒直径
外观
均一、透明、稳定
多数均一、透明、稳定
不均一、不稳定
分散质微粒组成
单个分子或离子
分子集合体或有机高分子
许多分子集合体
能否透过滤纸
能否透过半透膜
实例
食盐水、碘酒
淀粉溶液、蛋白质溶液
泥水
鉴别方法
无丁达尔现象
有丁达尔现象
静置沉淀(分层)
分离方法
蒸发、结晶
渗析、盐析
过滤(分液)
2.胶体
(1)定义(本质特征):
分散质的大小介于1nm~100nm之间的分散系叫做胶体。
(2)胶体的分类
①按分散质的组成分:
粒子胶体,如Fe(OH)3胶体,Al(OH)3胶体;
分子胶体,如蛋白质溶液,淀粉溶液。
②按分散剂的状态分:
液溶胶,如Na2SiO3溶于水所得分散系,肥皂水;
固溶胶,如有色玻璃;
气溶胶,如烟、云、雾。
(3)胶体的性质:
丁达尔效应、电泳现象、胶体的凝聚等。
3.溶液
溶液:
一种或几种物质分散到另一种物质里所形成的均一的稳定的混合物。
溶质:
被溶解的物质(即分散质)。
溶剂:
能溶解其他物质的物质(即分散剂)。
(2)分类
①饱和溶液:
一定温度下一定量的溶液不能再溶解某溶质时叫做这种溶质的饱和溶液。
②不饱和溶液:
一定温度下一定量的溶液还能继续溶解某溶质时叫做这种溶质的不饱和溶液。
(3)溶解度、溶质的质量分数
溶解度:
溶质的质量分数:
(4)溶解度曲线
如图1-1-3是硝酸钾和氯化钠的溶解度曲线,是根据不同温度下它们的溶解度值绘制的。
1.Fe(OH)3胶体是怎样制备的?
将氯化铁饱和溶液滴加到沸水中并加热至液体呈红褐色,停止加热。
2.利用硝酸钾和氯化钠的溶解度的不同,能分离二者的混合物吗?
若能,用什么方法分离?
能。
分离方法为重结晶(冷却热饱和溶液)。
3.丁达尔效应是不是一种化学变化?
怎样提纯胶体?
丁达尔效应是物理变化而不是化学变化。
可用渗析法提纯胶体,由于胶体粒子较大不能透过半透膜,而离子、分子较小可以透过半透膜,用此法可以将胶体粒子和溶液中的离子、分子分开。
4、哪些胶粒带正电荷,哪些带负电荷?
金属氢氧化物、金属氧化物的胶体粒子带正电荷。
非金属氧化物、金属硫化物、土壤的胶体粒子带负电荷。
但并非所有胶粒都带电荷。
7.根据中央电视台报道,近年来,我国的一些沿江或沿海城市多次出现大雾天气致使高速公路禁驶,航班停飞。
雾属于下列分散系中的()
A.溶液B.悬浊液C.乳浊液D.胶体
8.下列有关溶液性质的叙述,正确的是
A.室温时饱和的二氧化碳水溶液,冷却到0℃时会放出一些二氧化碳气体
B.20℃,100g水中可溶解34.2gKCl,此时KCl饱和溶液的质量分数为34.2%
C.强电解质在水中溶解度一定大于弱电解质D.胶体有丁达尔效应,溶液无此现象
9、已知氢氧化钙的溶解度随温度的升高而降低,将某温度下的澄清石灰水①加入少量生石灰后恢复原来的温度;
②降低温度。
这两种情况下,前后均保持不变的是()
A.溶液的质量B.氢氧化钙的溶解度C.溶液中钙离子的数目D.溶液中溶质的质量分数
10、下列关于胶体和溶液的说法中,正确的是
A.胶体不均一、不稳定,静置后易产生沉淀;
溶液均一、稳定,静置后不产生沉淀
B.布朗运动是胶体粒子特有的运动方式,可以据此把胶体与溶液、悬浊液区分开
C.光线通过时,胶体产生丁达尔现象,溶液则无丁达尔现象
D.只有胶状物如胶水、果冻类的物质才能称为胶体
高频热点突破:
热点1正确使用化学用语
【典例1】
(双选)正确掌握化学用语和化学基本概念是学好化学的基础,下列有关表述中正确的是
拓展训练:
1.从下列括号中选择合适的用语,填写在①~⑩的横线上,使它跟各种变化的情况相符(分解、潮解、溶解、蒸发、干馏、蒸馏、结晶、化合、挥发、升华、风化)。
①食盐放入水中逐渐消失:
________;
②碘加热逐渐消失:
③不盖灯帽的酒精灯,灯内酒精会逐渐减少,最后消失:
④烧碱固体吸收空气中的水分:
⑤生石灰吸收空气中的水分:
⑥胆矾受热后变成白色粉末:
⑦纯碱晶体在空气中变成白色粉末:
⑧氢氧化铜加热后变成黑色固体:
⑨煤隔绝空气加强热后生成黑色固体:
⑩饱和KNO3溶液降温,出现晶体:
________。
热点2物质的分类
【典例2】科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行深入的研究。
下列各组物质中有一种物质与其它物质不属于同一类,请将其挑出来。
2.某合作学习小组讨论辨析以下说法:
①粗盐和酸雨都是混合物;
②沼气和水煤气都是可再生能源;
③冰和干冰既是纯净物又是化合物;
④不锈钢和目前流通的硬币都是合金;
⑤盐酸和食醋既是化合物又是酸;
⑥纯碱和熟石灰都是碱;
⑦豆浆和雾都是胶体。
上述说法正确的是()
A.①②③④B.①②⑤⑥C.③⑤⑥⑦D.①③④⑦
热点3胶体的性质
胶体的本质特征和重要性质应用是历年高考的常见考点。
在复习过程中,要抓住胶体的本质特征(胶体微粒直径在1nm~100nm之间)。
命题角度为胶体的特性(丁达尔现象)、Fe(OH)3胶体的制备及胶体知识在生活中的应用等。
【典例3】“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化及军事科学中,“纳米材料”是指研究、开发出的直径从几纳米至几十纳米的材料,如将纳米材料分散到液体分散剂中,所得混合物可能具有的性质是(1纳米=10-9m)
A.能全部透过半透膜B.有丁达尔现象C.所得液体一定是溶液D.所得物质一定是浊液
3.下列说法中正确的是
A.胶体区别于其它分散系的本质特性是丁达尔现象B.利用半透膜可除去淀粉溶液中的少量NaCl
C.Fe(OH)3胶体带正电荷D.加入电解质,胶体能发生凝聚
4、取少量Fe2O3粉末(红棕色)加入适量盐酸,所发生反应的化学方程式为:
________________________,反应后得到的溶液呈________色。
用此溶液进行以下实验:
(1)取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为:
___________________,此反应属于____________(填反应类型)。
(2)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸直至溶液呈______色,即可制得Fe(OH)3胶体。
(3)取另一小烧杯也加入20mL蒸馏水,向烧杯中加入1mLFeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到____烧杯中的液体产生丁达尔现象。
这个实验可以用来区别____________________________。
(4)已知明矾能够净水,其原理是______________________
南粤真题实战
1、某合作学习小组讨论辨析:
①漂白粉和酸雨都是混合物;
②煤和石油都是可再生能源;
③不锈钢和目前流通的硬币都是合金;
④硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;
⑤蛋白质溶液、淀粉溶液和雾都是胶体。
上述说法正确的是
A.①③⑤B.①②④C.②③④D.③④⑤
2、下列说法正确的是
A.MgSO4固体中只存在离子键B.含Ca2+、Mg2+的水都是硬水
C.雾是气溶胶,在阳光下可观察到丁达尔效应D.玻璃是氧化物,成分可表示为Na2O·
CaO·
6SiO2
3、下列说法正确的是
A.胶体带电,而溶液不带电,所以胶体能发生电泳现象而溶液不能
B.由一种元素组成的物质是纯净物而由多种元素组成的物质为混合物
C.虽然NO2溶于水能生成HNO3,但NO2不是酸性氧化物D.水溶液呈酸性的盐称为酸式盐
4、下列说法正确的是
A.丁达尔现象可以用来区别胶体和溶液B.水银、水玻璃、胆矾都是纯净物
C.HCl、NH3、BaSO4都是电解质D.H2、D2、T2属于同素异形体
5、在下列变化中,只发生物理变化的是
A.荔枝酿酒B.酸雨侵蚀建筑物C.空气液化制取氮气D.生石灰遇水成为熟石灰
6、(双选)下列推断正确的是
A.SiO2是酸性氧化物,能与NaOH溶液反应
B.Na2O、Na2O2组成元素相同,与CO2反应产物也相同
C.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
D.新制氯水有酸性和强氧化性,故滴入少量紫色石蕊的现象是先变红,后褪色
7、化学工业是国民经济的支柱产业,下列生产过程中不涉及化学变化的是
A.氮肥厂用氢气和氮气合成氨B.钢铁厂用热还原法冶炼铁
C.硫酸常用接触法生产硫酸D.炼油厂用分流阀生产汽油
8、下列与化学概念有关的说法正确的是
A.化合反应均为氧化还原反应B.金属氧化物均为碱性氧化物
C.催化剂能改变可逆反应达到平衡的时间D.石油是混合物,其分馏产品汽油为纯净物
9、下列说法不正确的是
A.化学变化不产生新元素,产生新元素的变化不是化学变化
B.根据分散质微粒直径大小可以将分散系分为溶液、浊液和胶体
C.往25mL沸水中逐滴加入2mLFeCl3饱和溶液,继续煮沸可以制得Fe(OH)3胶体
D.某微粒的电子数等于质子数,则该微粒可能是一种分子或一种离子
10、下列家庭小实验中不涉及化学变化的是()
A.用熟苹果催熟青香蕉B.用少量食醋除去水垢
C.用糯米、酒曲和水制成甜酒酿D.用鸡蛋壳和蒸馏水除去淀粉中的食盐
11、许多国家十分重视海水资源的综合利用。
不需要化学变化就能够从海水中获得的物质是
A.溴、碘B.钠、镁C.烧碱、氯气D.食盐、淡水
12、化学在生产生活中有着重要的作用,下列说法不正确的是
A.明矾水解形成Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B.在海伦外壳上镶入锌块,可减缓船体的腐蚀速度
C.MgO的熔点高,可用于制作耐高温材料
D.电解MgCl2的饱和溶液,可制得金属镁
13、下列说法正确的是
A.医用酒精的质量分数为95%B.单质硅是将太阳能转化为电能的常用材料
C.淀粉、纤维素和油脂都属于天然高分子化合物D.合成纤维和光导纤维都是新型无机非金属材料
14、根据化学性质,判断其应用错误的是()
A.究竟能使蛋白质变性,可用于杀死细菌B.氧化钙能与二氧化硫反应,可做工业废气的脱硫剂C.明矾水解时产生具有吸附性的胶体粒子,可做漂白剂
D.镧镍合金能吸收氢气形成金属氢化物,可作储氢材料
14、下列说法中正确的是
课后作业:
1.物质发生化学反应时:
①电子总数,②原子总数,③分子总数,④物质的种类,⑤物质的总质量,⑥物质的总能量,反应前后肯定不发生变化的是()。
A.①②③⑤B.②⑤⑥C.④⑤⑥D.①②⑤
2、(双选)下列说法正确的是
A.由不同原子组成的纯净物一定是化合物
B.非金属氧化物一定是酸性氧化物,碱性氧化物一定是金属氧化物
C.含金属元素的离子不一定都是阳离子D.胆矾是纯净物,水泥是混合物
3.下列物质按不同类别分组,所得组合最不合理的是
4、下列有关物质分类或归类正确的是
①混合物:
盐酸、漂白粉、水玻璃、水银②化合物:
CaCl2、NaOH、HCl、HD
③电解质:
明矾、石膏、冰醋酸、石炭酸④同素异形体:
C60、C70、金刚石、石墨
⑤同系物:
CH2O2、C2H4O2、C3H6O2、C4H8O2
⑥同分异构体:
乙二酸二乙酯、乙二酸乙二酯、二乙酸乙二酯
A.①③④B.②③④C.③④D.②④⑥
5、下列说法正确的是
A.可用丁达尔现象区分溶液与胶体B.生石灰与水混合的过程只发生物理变化
C.O3是由3个氧原子构成的化合物D.CuSO4·
5H2O是一种混合物
6、(双选)下列说法正确的是()
A.硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
B.蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
C.Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到
D.天然气、沼气和水煤气分别属于化石能源、可再生能源和二次能源
7、下列有关化学用语表示正确的是
A.乙酸的结构简式:
C2H4O2B.F-的结构示意图:
C.中子数为20的氯原子:
1720ClD.NH3的电子式:
8、将铝粉逐渐投入饱和氯化铁的黄色溶液中,首先看到溶液变成红褐色,并产生气泡;
后来有少量的红褐色的沉淀,并有少量的能被磁铁吸引的黑色沉淀物质生成,请回答下列问题:
(1)红褐色溶液是____________,红褐色的沉淀是_______,气泡的成分是____________,黑色物质是____________。
(2)除去红褐色溶液中少量沉淀的实验方法是_________。
(3)试用简洁的文字和化学方程式解释上述实验现象:
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 一轮 复习 第一 化学物质 组成 性质 分类
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
