 高中化学论文三轮复习指导纲要第一部分 化学基本概念和基本理论.docx
高中化学论文三轮复习指导纲要第一部分 化学基本概念和基本理论.docx
- 文档编号:1625306
- 上传时间:2022-10-23
- 格式:DOCX
- 页数:30
- 大小:239.95KB
高中化学论文三轮复习指导纲要第一部分 化学基本概念和基本理论.docx
《高中化学论文三轮复习指导纲要第一部分 化学基本概念和基本理论.docx》由会员分享,可在线阅读,更多相关《高中化学论文三轮复习指导纲要第一部分 化学基本概念和基本理论.docx(30页珍藏版)》请在冰豆网上搜索。
高中化学论文三轮复习指导纲要第一部分化学基本概念和基本理论
化学三轮复习指导纲要
第一部分化学基本概念和基本理论
【考纲要求】1.物质的组成、性质和分类
(1)了解物质的分子、原子、离子、元素等概念的含义;初步了解原子团的定义。
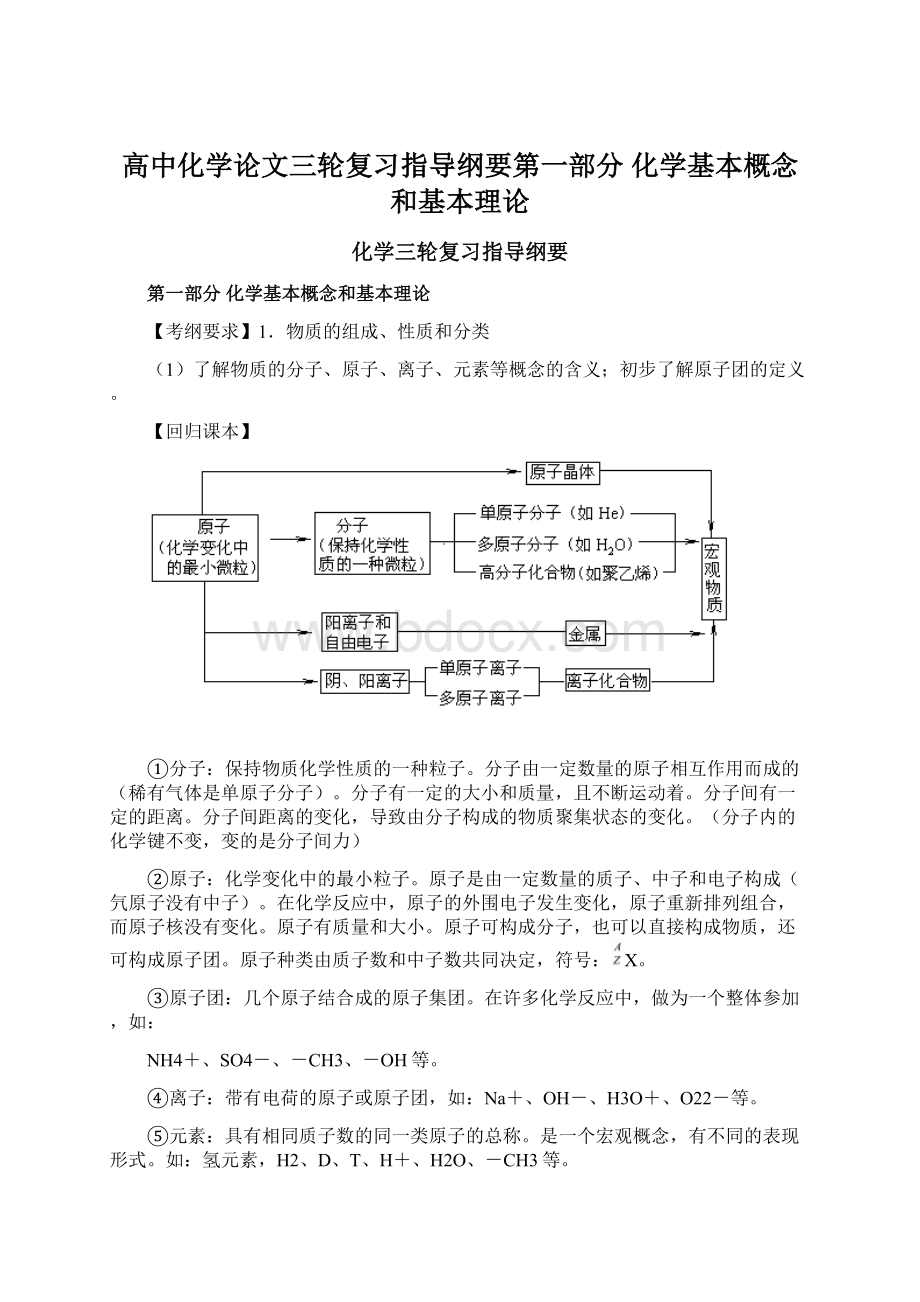
【回归课本】
①分子:
保持物质化学性质的一种粒子。
分子由一定数量的原子相互作用而成的(稀有气体是单原子分子)。
分子有一定的大小和质量,且不断运动着。
分子间有一定的距离。
分子间距离的变化,导致由分子构成的物质聚集状态的变化。
(分子内的化学键不变,变的是分子间力)
②原子:
化学变化中的最小粒子。
原子是由一定数量的质子、中子和电子构成(氕原子没有中子)。
在化学反应中,原子的外围电子发生变化,原子重新排列组合,而原子核没有变化。
原子有质量和大小。
原子可构成分子,也可以直接构成物质,还可构成原子团。
原子种类由质子数和中子数共同决定,符号:
X。
③原子团:
几个原子结合成的原子集团。
在许多化学反应中,做为一个整体参加,如:
NH4+、SO4-、-CH3、-OH等。
④离子:
带有电荷的原子或原子团,如:
Na+、OH-、H3O+、O22-等。
⑤元素:
具有相同质子数的同一类原子的总称。
是一个宏观概念,有不同的表现形式。
如:
氢元素,H2、D、T、H+、H2O、-CH3等。
【仿真模拟】
1.1999年诺贝尔化学奖授予了开创“飞秒(10-5s)化学”新领域的科学家,使运用激光光谱技术观测化学反应时分子中原子的运动成为可能。
你认为该技术做不到的是
A.观察“电子云”B.观察水电解生成氢气和氧气的过程
C.分析酯化反应的断键方式D.观察钠原子变成钠离子的过程。
【答案】AD
2.X、Y、Z和R分别代表四种元素。
如果aXm+、bYn+、CZn—、dRm—四种离子的电子层结构相同(a,b,C,d为元素的原子序数),则下列关系正确的是
A.a-c=m-nB.a-b=n-mC.c-d=m+nD.b-d=n+m
【答案】D
3.在我们的日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品。
这里的碘、铁、钙、硒、氟应理解为
A.元素B.单质C.分子D.氧化物
【答案】A
4.下列说法:
①元素的相对原子质量是该元素一个原子的质量与12C原子质量的1/12的比值;②分子是保持物质性质的一种微粒;③原子是构成物质的最小微粒;④任何元素的原子都由质子、中子、电子构成;⑤具有相同质量的原子,其化学性质基本相同;⑥具有相同质子数的微粒属于同一种元素;⑦同种元素组成的物质是单质。
其中正确的说法是
A.全都正确B.全都错误C.只有①、⑤、⑦正确D.除⑦外都正确
【答案】B
【考纲要求】
(2)理解物理变化与化学变化的区别与联系。
(3)理解混合物、纯净物、单质和化合物、金属和非金属的概念。
(4)了解同素异形体的概念。
【回归课本】
①氧化物与酸性、碱性、两性氧化物的关系:
两性、碱性氧化物一定是金属氧化物,其余不一定。
②酸酐:
是酸中的-OH间去水后的生成物(价态不变),酸酐不一定都是氧化物(如:
乙酸酐等)。
③.酸的氧化性和氧化性酸不同。
④.盐的构成元素:
一定含非金属元素,不一定含金属元素。
⑤.金属与非金属:
金属是指在反应中只能失去电子的单质,非金属是指在反应中可以失去电子也可得到电子的单质。
从化合价来看,金属元素在化合物中只能显正价,非金属元素在化合物中的化合价有正也有负。
⑥物理、化学变化的本质是化学键的变化(不能只看分子式相同)
⑦同素异形体一定是指同一元素的性质(结构)不同的单质。
【仿真模拟】
1.下列说法中错误的是
A.磺化、硝化、水化、风化、钝化等都是化学变化
B.干馏、常压分馏、减压分馏、都是物理变化
C.水煤气、裂解气、焦炉气、天然气都是混合物
D.甘油不是油,纯碱不是碱,酚醛树脂不是酯,干冰不是冰
2.澳大利亚研究人员最近开发出被称为第五形态的固体碳,这种新的碳结构称作“纳米泡沫”, 他外形类似海绵,比重极小,并具有磁性。
纳米泡沫碳与金刚石的关系是
A.同系物B.同分异构体C.同位素D.同素异形体
3.最近,意大利科学家使用普通氧分子和带正电荷的氧离子制造出了由4个氧原子构成的氧分子,并用质谱仪探测到了它存在的证据。
若该氧分子具有空间对称结构,下列关于该氧分子的说法正确的是
A.是一种新的氧化物 B.不可能含有极性键
C.是氧元素的一种同位素 D.是臭氧的同分异构体
4.目前,科学家拟合成一种“二重构造”的球形分子,即把足球型的C60分子熔进Si60的分子中,外面的硅原子与里面的碳原子以共价键结合。
下列说法正确的是
A.它是由两种单质组成的混合物B.它是一种硅酸盐
C.它是一种新型化合物D.它是一种高聚物
5.目前人类已发现的非金属元素除稀有气体外,共有16种,下列对这16种非金属元素的相关判断:
1都是主族元素,最外层电子数都大于4②单质在反应中都只能作氧化剂
3氢化物常温下都是气态,所以又叫都气态氢化物④氧化物常温下都可以与水反应生成酸
A.只有①②正确B.只有①③正确
C.只有③④正确D.①②③④均不正确
【答案】1.B2.D3.B4.C5.D
【考纲要求】(5)理解酸、碱、盐、氧化物的概念及其相互联系。
【回归课本】
【仿真模拟】
1.对盐类物质可有下列分类:
如氯化硝酸钙[Ca(NO3)Cl]是一种混盐,硫酸铝钾KAl(SO4)2是一种复盐,冰晶石(六氟合铝酸钠)Na3AlF6是一种络盐。
对于组成为CaOCl2的盐可归类于
A.混盐B.复盐C.络盐D.无法归属于上述类别
2.下列说法确有例证的是:
①两种弱酸反应生成两种强酸;②某弱碱通过反应生成某强碱;
③两种弱酸盐反应生成两种强酸盐;④有单质参与的反应不一定是氧化还原反应。
A.②④B.①③C.①②③D.①②③④
3.下列反应,一定不会有气体产生的是
A.盐与碱溶液的反应B.盐与盐在水溶液中反应
C.酸与碱在溶液里的中和反应D.非金属与氧组成的化合物与水反应
【答案】1.A2.D3.C
【考纲要求】2.化学用语
(1)熟记并正确书写常见元素的名称、符号、离子符号。
(2)熟悉常见元素的化合价。
能根据化合价正确书写化学式(分子式),并能根据化学式判断化合价。
(3)掌握电子式、原子结构示意图、分子式、结构式和结构简式的表示方法。
(4)理解质量守恒定律的含义。
理解热化学方程式的含义。
能正确书写化学方程式、热化学方程式、电离方程式、离子方程式、电极反应式。
【回归课本】掌握各种化学用语的书写方法和注意事项。
高考中的Ⅱ卷(20个空左右)几乎都是用化学用语来表达。
热化学方程式应引起重视。
【仿真模拟】
1.火星探测器发回的信息表明,火星上存在针铁矿[Goethite,化学式:
FeO(OH)]和黄钾铁矾[Jarosite],从而证明火星表面曾经存在过水。
这一发现被《人民日报》评为2004世界十大新闻之首。
已知两种矿物中铁的价态相同,则黄钾铁矾{化学式记为:
KFe3(SO4)2(OH)n}中n值为:
A.4B.5C.6D.7
2.在同温同压下,下列各组热化学方程式中,a.>b的一组是
A.CH4(g)+2O2(g)=CO2(g)+2H2O
(1);△H=akJ/mol
CH4(g)十2O2(g)=CO2(g)+2H2O(g);△H=bkJ/mol
B.2H2(g)+O2(g)=2H2O
(1);△H=akJ/mol
H2(g)+O2(g)=H2O
(1);△H=bkJ/mol
C.C(s)+O2(g)=CO(g);△H=akJ/mol,C(s)+O2(g)=CO2(g);△H=bkJ/mol
D.S(g)十O2(g)=SO2(g);△H=akJ/mol,S(s)+O(g)=SO2(g);△H=bkJ/mol
3.下列离子方程式书写正确的是
A.二氧化氮溶于水:
3NO2+H2O=2HNO3+NO
B.将标准状况下112mL氯气通入10mL浓度为1mol·L-1的溴化亚铁溶液中:
2Fe2++4Br—+3Cl2=3Fe3++6Cl—+2Br2
C.次氯酸钙溶液中通入过量二氧化碳:
Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO
D.氯化亚铁溶液中加入硝酸:
3Fe2++4H++NO3—=3Fe3++2H2O+NO↑
4.根据联合国世界卫生组织调查,当今缺铁性贫血是世界上最流行的营养性问题。
50亿人口中有10亿人口患营养性贫血症,联合国已正式将EDTAFeNa(化学名:
三水合乙二胺四乙酸铁钠,分子式为C10H12FeN2NaO8·3H2O)列入食品添加剂,江苏等省从2004年5月起已推行以“强铁化酱油”为主的“补铁”工程。
已知EDTA的结构式为(HOOCCH2)2NCH2CH2N(CH2COOH)2,下列说法正确的是
A.EDTAFeNa铁为+3价B.EDTAFeNa中铁为+2价
C.EDTAFeNa溶液显强碱性D.人体血液中血红蛋白中铁显+3价
【答案】1.C2.C3.D4.A
【考纲要求】3.化学中常用计量
(1)了解相对原子质量、相对分子质量的定义。
(2)了解物质的量的单位——摩尔(mol),摩尔质量、气体摩尔体积(相应单位为g·mol-1、L·mol-1)的含义。
理解物质的量浓度(mol·L-1)、阿伏加德罗常数的含义。
掌握物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系。
【回归课本】
1.NA是宏观物理量与微观物理量的桥梁
NA
物质体积V微粒体积V
摩尔体积Vm微粒质量m
物质质量m微粒直径d
摩尔质量M微粒间间隙L
物质密度ρ
2.宏观物理量与微观物理量的相互关系
3.阿佛加德罗定律及推论
在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子。
主要推论:
(1)同温同压下,任何气体的体积比等于它们的分子数之比,也等于它们的物质的量之比。
(2)同温同压下的任何气体,它们密度与其摩尔质量成正比,即和其分子量成正比。
(3)同温同体积下,不同压强的任何气体,压强之比等于它们的物质的量之比。
【仿真模拟】
1.NA表示阿伏加德罗常数的值,下列说法正确的是:
A.常温常压下,1mol氦气含有2NA个核外电子
B.常温常压下,当活泼金属转移2NA个电子时,可从盐酸中置换出22.4LH2
C.标准状况下,0.5NA个CCl4所占的体积约为11.2L
D.39gNa2O2固体含有的离子数为2NA
2.设NA表示阿伏加德罗常数,下列有关叙述不正确的是
A.1molOH—所含的电子数为10NA
B.含0.01molFeCl3的饱和溶液制成的氢氧化铁胶体中所含胶粒数小于0.01NA
C.常温常压下,NA个氢分子的体积大于22.4L
D.0.1molKO2与水反应生成氧气和氢氧化钾时,转移的电子数为0.1NA
【答案】1.A2.D
【考纲要求】4.化学反应与能量
(1)掌握化学反应的四种基本类型:
化合、分解、置换、复分解。
(2)理解氧化还应反应,了解氧化剂和还原剂等概念。
掌握重要氧化剂、还原剂之间的常见反应。
能判断氧化还原反应中电子转移的方向和数目,并能配平反应方程式。
(3
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学论文三轮复习指导纲要第一部分 化学基本概念和基本理论 高中化学 论文 三轮 复习 指导 纲要 第一 部分 化学 基本概念 基本理论
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 12处方点评管理规范实施细则_精品文档.doc
12处方点评管理规范实施细则_精品文档.doc
 17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
