 链霉菌实验操作文档格式.docx
链霉菌实验操作文档格式.docx
- 文档编号:16227100
- 上传时间:2022-11-21
- 格式:DOCX
- 页数:37
- 大小:43.60KB
链霉菌实验操作文档格式.docx
《链霉菌实验操作文档格式.docx》由会员分享,可在线阅读,更多相关《链霉菌实验操作文档格式.docx(37页珍藏版)》请在冰豆网上搜索。
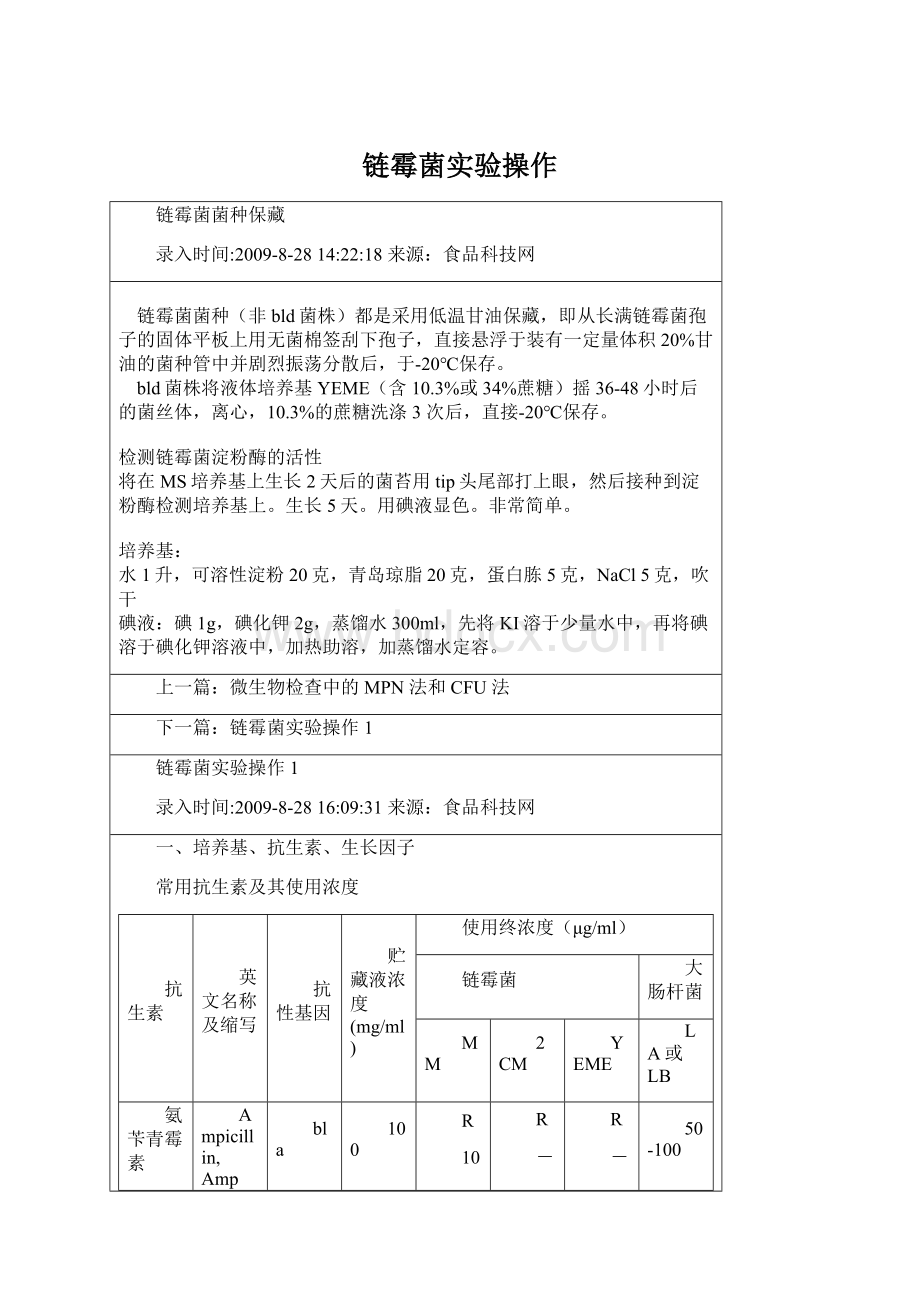
壮观霉素
链霉素
硫链丝菌素
红霉素
阿泊拉霉素
Ampicillin,Amp
Chloramphenicol,Cml
Hygromycin,Hyg
Kanamycin,Km
Spectinomycin,Spc
Streptomycin,Str
Thiostrepton,Thio
Erythomycin,Ery
Apramycin,Am
bla
cat
hyg
aac或aph
aadA
str
tsr
ermE
aac(3)IV
100
25(无水乙醇配)
50
25
25(DMSO配)
R
10
2?
5
-
2.5
50-100
不敏感
20
30-50
*–表示无记录或不能使用,贮存液除特别说明外均用无菌水配制
*此表仅供参考!
!
*R表示不敏感
*Km和Am有交叉抗性,所以同时具有这两种抗性基因时应适当提高抗生素的量,并作好对照。
*Hyg易见光分解,应用锡箔纸包好。
*有些抗生素需要在低盐的环境(如DNA培养基)下筛选效率较高,如Hyg,Km,Vio
LB(Luria-Bertani)培养基
胰蛋白胨10g,
酵母抽提物5g,
NaCl5g,葡萄糖1g,
蒸馏水加至1000ml,
pH7.3左右(灭菌后第一次用时还要调一次)
LA
LB中加入终浓度为1.5-2%的琼脂粉(不同的琼脂加的量不同,如青岛琼脂大概需1.5%,而华美的需要2%)。
*做蓝白斑筛选时不加葡萄糖
基本培养基(MM)
溶液:
L-天冬酰胺0.5g,
K2HPO4
0.5g,
MgSO4·
7H2O
0.2g,
FeSO4·
7H2O
0.01g,
蒸馏水至1000ml
将每250ml溶液分装到装有2.5g琼脂的500ml三角瓶中,灭菌,使用时每瓶加入50%葡萄糖(8磅灭菌)5ml,调pH7.0。
配置MM的琼脂有labagar、Iceagar(IA)
R5(1L)链霉菌原生质体转化时用
蔗糖
103g
K2SO4
0.25g
MgCl2·
6H2O
10.12g
葡萄糖
10g
Difco酪蛋白氨基酸
0.1g
微量元素溶液
2ml
Oxoid酵母提取物
5g
TES
5.73g
加蒸馏水至
1000ml
称取5.5gDifco琼脂放入500ml三角瓶中,倒入250ml上述溶液,然后塞上塞子后8磅灭菌(114度15分种)。
使用时,将培养基融化,每瓶中加入:
KH2PO4(0.5%)
2.5ml
CaCl2·
2H2O(5M)
1ml
L-脯氨酸(20%)
3.75ml
NaOH(1M)调pH至7.3
对营养缺陷型菌株加入适当的营养因子(请参考《手册》)
YEME(酵母膏-麦芽膏培养基)1L(液体培养链霉菌)
3g
Oxoid蛋白胨Tryptone
5g
麦芽提取物(BD公司原Difco公司218630)
10g
蔗糖*
340g
蒸馏水
至1000ml
高压灭菌后加入:
(8磅灭菌,113-114゜C,15min,自动灭菌锅一次不能灭过多东西,否则会灭不彻底。
)
6H2O(2.5M)
2ml/L
制备原生质体时,还要加入:
甘氨酸(20%)
*
25ml/L
蔗糖的主要作用是维持链霉菌生长时的渗透压。
甘氨酸被认为能干扰链霉菌细胞壁的形成,使菌丝体片段更短,利于溶菌,有利于外源DNA的导入。
TSBY(1L)(液体培养链霉菌)
Oxoid胰胨豆汤粉(TSB)
30g
蔗糖*
340g
Oxoid酵母抽提物
蒸馏水
至1000ml
*不同菌株培养需要不同浓度的蔗糖,蔗糖的主要作用是维持链霉菌生长时的渗透压。
MS培养基
将黄豆饼粉加蒸馏水煮2到3小时,用纱布过滤得到滤液,将每250ml滤液分装到装有5g琼脂,5g甘露醇的500ml三角瓶中,10磅灭菌,使用时调pH7.2-7.3。
2CMY培养基(用于井岗的接合转移)
可溶性淀粉
10g
胰蛋白胨
2g
NaCl
1g
(NH4)2SO4
K2HPO4
1g
CaCO3
2g
无机盐溶液*
1ml
琼脂
20g
蒸镏水
1000ml
PH7.2
无机盐溶液(每升)
FeSO4.7H2O
MgCl.6H2O
ZnSO4.7H2O
YMS培养基(阿维,井岗产孢)
酵母抽提物
4g
麦芽糖
CoCl..6H2O
5mg
YD培养基
麦芽糖
葡萄糖
MgCl
CaCl
1.5g
15g
生长因子补充物的使用浓度
天蓝色链霉菌1258、J1501等都是营养缺陷型菌株,培养这些菌株时一般需向培养基中补加营养因子,使用浓度如表
生长因子补充物的使用浓度表
化合物
储存液(mg/ml)1
终作用浓度(μg/ml)
组氨酸(Histidine)
其它氨基酸2
7.5
37
腺嘌呤,鸟嘌呤,
胸腺嘧啶,尿嘧啶
1.5
维生素
0.1
0.5
1.
储存液用无菌去离子水配置,8磅灭菌后4oC保存。
2.
对于半胱氨酸营养缺陷型菌株,补充光氨酸。
链霉菌实验操作2
53:
29来源:
大肠杆菌质粒的抽提
苯酚/氯仿溶液抽提法
接种5mlLB,37℃摇床过夜培养(12小时)
离心,3000rpm,5min去上清
3.
振荡混匀沉淀,分装在2个离心管中,spin一下,吸去上清,加入150μl的溶液I(50mmol/L葡萄糖,
25mmol/L
Tris·
Cl(PH8.0),
10mmol/LEDTA(PH8.0)在10lbf/in2(6.895×
104Pa)高压蒸气下灭菌15min(8磅),贮存于4℃),剧烈振荡5分钟打散菌体(菌体不打散容易在产物中出现较多蛋白)。
4.
加入300μl溶液II(0.2mol/LnaOH,1%SDS,用2倍的溶液现配现用)后立即振荡混合均匀,处理2分钟后加入225μl溶液III(5mol/L乙酸钾60ml,冰乙酸11.5ml,水28.5ml)混合均匀,12000rpm离心5min,取上清液中于新的离心管。
5.
加120μl酸性苯酚/氯仿溶液,振荡混匀,12000rpm离心5min,再取上清液中于新的离心管中。
6.
用120ul氯仿重复操作5。
7.
加等体积的异丙醇或2倍体积的乙醇,混匀,12000rpm离心7min。
8.
沉淀用70%乙醇洗涤两次,每次10min。
50℃烘干后加适量无菌去离子水(ddH2O)溶解,-20℃保存。
氯化锂抽提法
前四部同苯酚/氯仿溶液抽提法(用SolutionIIIIII处理)
加等体积的异丙醇,混匀,沉淀DNA,12000rpm离心7min。
去上清,尽量去干净。
用少量70%乙醇洗一下(洗去异丙醇),离心去尽酒精,50℃烘干沉淀,用适量ddH2O(100ul)充分溶解(可在50度水浴中助溶)后加入4/5体积的氯化锂溶液(浓度约10mol/L)处理1min沉淀RNA和蛋白。
12000rpm离心5min,取上清液于新的离心管中,用等体积的异丙醇混匀,12000rpm离心8min,去上清。
将沉淀用70%乙醇洗涤两次,每次10min。
50℃烘干后加一定量的无菌去离子水(ddH2O)溶解,-20℃保存。
酶连反应
一般采用10μl反应体系:
T4连接酶1μl,连接酶缓冲液1μl,外源片段与载体按DNA摩尔含量3:
1加入即可。
如果是粘端连接,则需把外源片段和载体的混合物在50度处理10分钟使粘端变性,然后立即放入冰中5分钟。
平端连接采用14度,粘端连接采用16度,连接4小时以上(一般可过夜)。
*外源片段与载体按DNA摩尔含量为3:
1或外源更多。
DNA片段凝胶回收
1试剂盒回收(离心法)(详见说明书)
(1)
在长波紫外灯下切下含有目标DNA的琼脂糖凝胶,用纸巾吸干凝胶表面的液体并切小.计算凝胶的重量,该重量作为一个凝胶体积(如1oomg=1ooul)
(2)
根据凝胶的浓度,加DE-A液
凝胶浓度
DE-A溶液体积
≤1.0%
3个凝胶体积
≤1.5%
4个凝胶体积
≤2.0%
5个凝胶体积
混匀后于75oC加热,(低熔点琼脂糖凝胶于45oC加热),间断混合,直到凝胶熔化(6-8分钟).
(3)
加0.5个DE-A体积的DE-B溶液,混匀(是否需调整PH值,见注意事项1);
当分离的DNA片段小与400bp时,加入异丙醇至终浓度为20%;
(4)
吸3中的混合液,转移到DNA制备管,3600rpm离心1分钟.如制备管中有残留,适当提高速度,再离心1分钟,去滤液;
(5)
将制备管置回离心管,加0.5mlW1溶液,3600rpm离心30,弃滤液;
(6)
将制备管置回离心管,加0.7mlW2溶液,3600rpm离心30,弃滤液,重复一次;
(W2中含有酒精,应保证瓶子密封。
(7)
将制备管置回离心管,最高速度离心1分钟;
(8)
将制备管置洁净的1.5ml离心管中,在DNA制备膜正中央加25ul水或洗脱液,室温静置1分钟.最高速度离心1分钟洗脱DNA.
注意事项;
此法适合从TAE或TBE琼脂糖凝胶中回收DNA,用其他缓冲液时,加DE-B溶液后,溶液的PH要调整到6.5以下.
勿将DNA长时间暴露在高温下,线型DNA于高温条件下易水解.勿将凝胶长时间暴露在紫外灯,减少紫外灯对DNA的损伤.
2步骤中的凝胶必须完全熔化,否则将严重影响DNA的回收效率.
步骤4中吸回滤液到DNA制备管中再吸附一次,可提高回收效率.将洗脱液或水加热到60゜C,可提高回收效率。
(重要)
DNA分子呈酸性,建议在洗脱液中保存。
(试剂盒中提供的洗脱液好像对PCR有某种抑制作用。
2
silica回收
1在长波紫外灯下切下含有目标DNA的琼脂糖凝胶,用纸巾吸干凝胶表面的液体并切小.计算凝胶的重量;
加入2-3倍体积的6MKI或NaI(避光4度保存);
65oC温浴,间断混合,直到凝胶熔化;
加适量的振匀的silica悬液(10ul)充分混匀,冰上放置15分钟(或更长),间断混合;
5000rpm离心3分钟,弃上清;
加1ml预冷的NEWbuffer(先用100ul打散沉淀,再用900ul混匀),冰上洗盐2分钟,间断混合;
12000rpm离心10s,弃上清;
重复6,7步骤1次;
于50oC烘箱烘干;
加10ul的去离子水用枪头打匀,65oC水浴15分钟,间断混匀;
9.
12000rpm离心10s,把上清转移到另外洁净的离心管中;
10.
跑胶检测回收效率.
注意事项
*4----8步均在冰上操作,防止解吸附,silica只在低温下对DNA有吸附作用。
*NEWBuffer:
(100ml)
1ml5MNacl,1ml1MpH7.5This-HCl,0.5ml0.5MEDTA,50ml100%ETOH,去离子水加至100ml。
(-20度保存)
*Silica配法见:
TIGJanuary1995Vol.11No.1.AninexpensivealternativetoglassmilkforDNApurifyication.
DNA纯化
用苯酚:
氯仿抽提
把样品至置于离心管中,加入等体积的苯酚:
氯仿,
混匀,使之成为乳浊状;
12000rpm离心,5分钟:
用枪头把水相移到另一离心管中.
加入等体积氯仿并重复2—4
用2/3体积的异丙醇(或2倍无水乙醇),1/10体积的3M醋酸钠,沉淀10分钟(-20度长时间沉淀可提高产量)
12000rpm离心5分钟,弃液体
70%的乙醇洗盐10分钟,去上清,
重复8一次,再12000rpm离心弃液体.
50度烘干.
11.
去离子水溶解。
LiCl抽提
1把样品至置于离心管中,加4/5体积10MLiCl
2室温下静置1分钟
312000rpm离心5分钟
4把液体转移到另一离心管中
5.加2/3体积的异丙醇沉淀10分钟
往下的步骤同于上面的8-12
E.coil总DNA的提取
1
将过夜培养的大肠杆菌离心去上清。
加500μl水重悬浮,加入500μl2%SDS,混合振荡约1min,55℃温育15min,直到溶液的粘度显著下降。
3
加入0.1倍体积的3mol/L醋酸钠(自然pH)。
4
加入150μl中性苯酚,混合振荡均匀后,12000rpm离心5min,移取上清液,弃去白色中间层。
5
用中性苯酚/氯仿重复抽提直至看不见(或非常少)中间层为止,
6
加入1倍体积的异丙醇(或2倍体积的无水乙醇),上下颠倒混合直至出现白色絮状DNA沉淀团,用吸头挑出DNA沉淀团。
7
用70%乙醇洗涤DNA沉淀团两次。
8
烘干,溶解DNA沉淀。
链霉菌质粒DNA的小量提取(还需改进)
将适量的菌体悬浮于500μl溶菌酶溶液(2%)中,37℃温育1hr左右至完全溶菌,
加入500μl碱性SDS溶液(0.3mol/LNaOH,2%SDS),立即振荡混合完全,
打开管盖,在70℃放置15min(对大于20kb的质粒则最好放在55℃,30min),然后于水浴中冷却至室温,
加入100μl酸性苯酚/氯仿溶液,用混合器振荡至液体彻底混合均匀,12000rpm离心5min,移取上清液,弃去白色中间层。
用中性苯酚/氯仿重复抽提直至看不见(或非常少)中间层为止。
在上清液中加入1/10体积的3MNaAc溶液和1倍体积的异丙醇沉淀5分钟(或2.2倍体积的无水乙醇沉淀1h),12000rpm离心8min,
7用70%乙醇洗涤沉淀两次,
8干燥后加一定量的TE(d2H2O)缓冲液溶解。
另:
可使用抽提总DNA的试剂盒,将总DNA与质粒DNA一起抽提。
去磷酸化处理(详见分子克隆实验指南以及Takara的CIAP使用说明)
注:
CIAP一般为原酶,酶量过大会失去粘性末端,因此应适当减小酶的用量,一般0.5ul即可。
也可减少温浴时间,如37℃,10~20min即可。
AT克隆(详见说明书)
所用的载体:
pGEM-T,pGEM-TEasyVetorSystem
1.酶连
体系
10ul
standardReation
Positivecontrol
Backgroundcontrol
2XRapidLigationBuffer,T4DNALigation
5ul
5ul
5ul
pGEM-T,pGEM-TEasyVetor(50ng)
1ul
1ul
PCRproduct
Xul
---
---
ControlinsertDNA
---
2ul
---
T4DNALigase(3weissuntis/ul)
Deionizedwatertoafinalvolumeof
10ul
(2).反应
4oC过夜
注
:
PCR产物和载体的摩尔比为:
(ngofvectorxkbsizeofinsert)/(kbsizeofvector)*(insert:
vectorration)=ngofinsert
一般外源和载体的摩尔比例为3:
1
T载体大小为3bkb
50ng
转化
取大肠杆菌感受态细胞100ul,连接产物2-5ul加入1.5ml的离心管中,混匀.冰上放置20分钟.
42oC热激90秒.(不要摇动)
立即置冰上3-5分钟.
加1mlSOC培养基(室温)
37oC培养1.5小时(约150rpm摇动).
离心,去上清,余下的混匀涂皿(LB/抗生素/IPTG/X-Gal).
37oC培养16—24小时,挑白斑.
*所用的培养基:
SOC培养基
0.5g
1M
NaCl
1ml
KCl
0.25ml
2MMg2+储液
2M葡萄糖
*Mg2+储液
MgCl.6H2O
20.33g
MgSO4.7H2O
24.65g
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 霉菌 实验 操作
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
