 级无机化学期末考试A.docx
级无机化学期末考试A.docx
- 文档编号:1608213
- 上传时间:2022-10-23
- 格式:DOCX
- 页数:15
- 大小:29.20KB
级无机化学期末考试A.docx
《级无机化学期末考试A.docx》由会员分享,可在线阅读,更多相关《级无机化学期末考试A.docx(15页珍藏版)》请在冰豆网上搜索。
级无机化学期末考试A
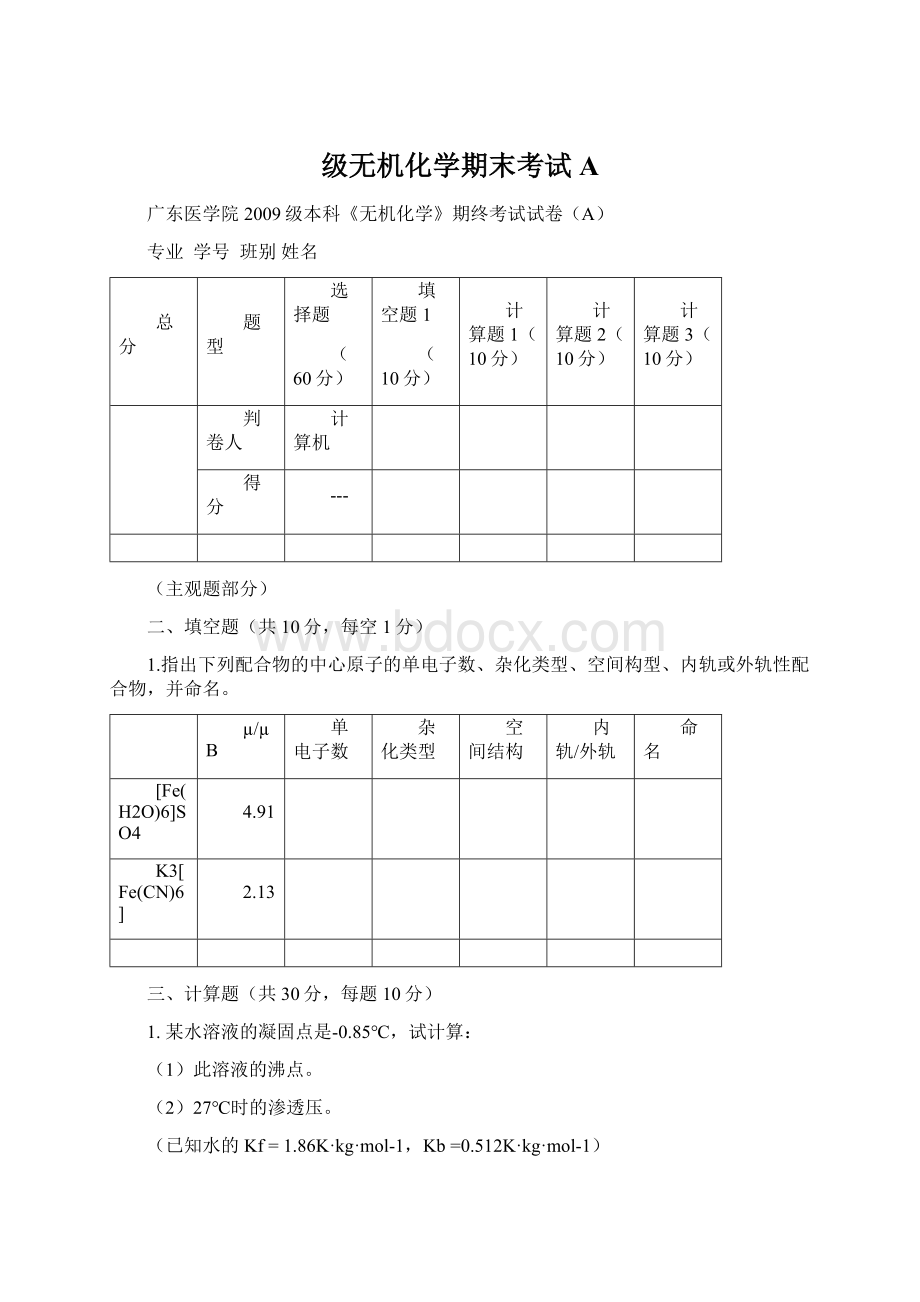
广东医学院2009级本科《无机化学》期终考试试卷(A)
专业学号班别姓名
总分
题型
选择题
(60分)
填空题1
(10分)
计算题1(10分)
计算题2(10分)
计算题3(10分)
判卷人
计算机
得分
---
(主观题部分)
二、填空题(共10分,每空1分)
1.指出下列配合物的中心原子的单电子数、杂化类型、空间构型、内轨或外轨性配合物,并命名。
µ/µB
单电子数
杂化类型
空间结构
内轨/外轨
命名
[Fe(H2O)6]SO4
4.91
K3[Fe(CN)6]
2.13
三、计算题(共30分,每题10分)
1.某水溶液的凝固点是-0.85℃,试计算:
(1)此溶液的沸点。
(2)27℃时的渗透压。
(已知水的Kf=1.86K·kg·mol-1,Kb=0.512K·kg·mol-1)
2.计算下列溶液的pH值:
(1)0.10mol·L-1NH3·水溶液与0.050mol·L-1HCl溶液等体积混合。
(2)0.10mol·L-1NH3水溶液与0.10mol·L-1HAc溶液等体积混合。
(已知:
NH3:
Kb=1.76×10-5,HAc:
Ka=1.79×10-5,不考虑离子强度)
3.已知φ(Cu2+/Cu)=+0.34V,φ(Ag+/Ag)=+0.80V。
现将反应
2Ag++Cu=2Ag+Cu2+设计成原电池,若[Cu2+]=0.1mol·L-1,[Ag+]=0.01mol·L-1。
(1)写出该电池的组成式。
(2)计算此电池的电动势E并判断该反应进行的方向。
(3)计算标准状态下反应的平衡常数K⊖。
广东医学院2009级本科《无机化学》期终考试试卷(A)
(客观题部分,答在答题卡上)
一、选择题(共60分,每小题1.5分,只有一个正确答案)
(1)答第一题前,考生务必先将考试科目、专业、年级和姓名用黑色签字笔写在答题卡上,同时一定要把学号用2B铅笔涂写在考号处。
考试结束,将试卷与答题卡一并交回。
(2)每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案标号,不能答在试题卷上。
1.红细胞在下列哪一种溶液中可保持正常状态()
A.310mmol·L-1NaClB.150mmol·L-1NaCl
C.100mmol·L-1NaHCO3D.0.380mol·L-1葡萄糖
2.欲使被半透膜隔开的两种稀溶液间不发生渗透,应使两溶液(A,B中的基本单元均以溶质分子式表示)()
A.物质的量浓度相同B.质量摩尔浓度相同
C.质量浓度相同D.渗透浓度相同
3.下列四种溶液(浓度都是0.1mol·L-1)的凝固点最低的是()
A.Al2(SO4)3B.CaCl2C.MgSO4D.C6H5SO3H
4.盐碱地的农作物长势不良,甚至枯萎,其主要原因为()
A.天气太热B.很少下雨C.肥料不足D.水分从植物向土壤倒流
5.根据酸碱质子理论,下列物质中属于两性物质的是()
A.H2SB.CH3COO-C.NH2CH2COOHD.NH4+.
6.已知HF的Ka=3.35x10-4,NH3的Kb=1.79x10-5,由此可知F-与NH3.H2O相比,其碱性()
A.比NH3.H2O的强B.比NH3.H2O弱C.与NH3.H2O的碱性相等D.无法比较
7.0.1mol·L-1的H2S溶液中[S2-]是()(已知H2S的Ka1=8.91×10-8,Ka2=1.12×10-12)
A.8.91×10-8B.1.12×10-12C.9.97×10-12D.4.46×10-8
8.已知固体Ksp[Mn(OH)2]=2.06×10-14,0.01mol·L-1MnCl2固体溶于1LpH=10的溶液中,则下列说法正确的是()
A.溶液刚好饱和,无Mn(OH)2沉淀生成
B.溶液未达到饱和,无Mn(OH)2沉淀生成
C.有Mn(OH)2沉淀生成D.与溶液pH无关,无Mn(OH)2沉淀生成
9.在AgCl的饱和溶液中,有AgCl固体存在,当加入等体积的下列哪一种溶液
会使AgCl的溶解度更大一些()
A.AgCl的饱和溶液B.1mol.L-1NaClC.1mol.L-1AgNO3D.2mol.L-1NaNO3;
10.HgCl2的Ksp=4×10-15,则HgCl2饱和溶液中,Cl-离子的浓度是()
A.4×10-8B.2×10-15C.1×10-15D.2×10-5
11.列关于电极电势φ的叙述中,正确的是()
A.电对的φ越小,表明该电对的氧化态得电子倾向越大,是越强的的氧化剂
B.电对的φ越大,其还原态越易得电子,是越强的的还原剂
C.电对的φ越小,其还原态越易失去电子,是越强的的还原剂
D.电对的φ越大,其氧化态是越弱的的氧化剂
12.利用离子电子法配平反应方程式
Mn2++BiO3-=MnO4-+Bi3++H2O(酸性介质)
配平后,H2O的系数应为()
A.3B.7C.11D.16
13.由标准锌半电池和标准银半电池组成原电池:
(-)Zn(s)|ZnSO4(a=1)‖AgNO3(a=1)|Ag(s)(+)
若在AgNO3溶液中加入氨水,电池电动势将()
A.变大B.变小C.不变D.无法判断
14.根据公式lgK=nEө/0.0592,可以看出溶液中氧化还原反应的平衡常数K(严格地说应为Kө)应()
A.与温度无关B.与浓度无关C.与反应本性无关D.与反应方程式的书写无关
15.己知Cu2+/Cu=0.34伏,Sn4+/Sn2+=0.15伏,Fe3+/Fe2+=0.77伏,判断标准状态时还原性从强到弱的顺序是()
A.Sn4+,Fe3+,Cu2+B.Cu2+,Sn4+,Fe3+C.Fe2+,Cu,Sn2+D.Sn2+,Cu,Fe2+
16.原子基态的电子构型为[Ar]3d104s1,它在元素周期表中的位置是()
A.s区B.p区C.d区D.ds区
17.下列离子的电子构型可以用[Ar]3d5表示的是()
A.Mn2+B.Fe2+C.Co2+D.Ni2+
18.下列各组量子数中,合理的一组是()
A.n=3,l=1,m1=+1,ms=+1/2B.n=4,l=5,m1=-1,ms=+1/2
C.n=3,l=3,m1=+1,ms=-1/2D.n=4,l=2,m1=+3,ms=-1/2
19.Cu2+的电子排布式为()
A.[Ar]3d84s1B.[Ar]3d94s1C.[Ar]3d94s0D.[Ar]3d104s0
20.描述一确定的电子运动状态,需用以下参数()
A.n.lB.n.l.mC.n.l.m.msD.只需n
21.下列说法不正确的是()
A.氢原子中,电子的能量只取决于主量子数n
B.多电子原子中,电子的能量不仅与n有关,还与l有关
C.波函数由四个量子数确定D.ms=±½表示电子的自旋有两种方式
22.H2S分子的空间构型、中心原子的杂化方式分别为:
()
A.直线形、sp等性杂化B.V形、sp2不等性杂化
D.V形、sp3不等性杂化D.V形、sp3等性杂化
23.在酒精的水溶液中,分子间主要存在的作用力为()
A.取向力B.诱导力C.色散力和诱导力、取向力
D.取向力、诱导力、色散力、氢键
24.BF3分子中,N原子与三个氯原子成键所采用的轨道是()
A.二个sp轨道,一个p轨道成键B.三个sp3轨道成键
C.pxpypz轨道成键D.三个sp2轨道成键
25.下列离子或分子有顺磁性的是()
A.O22-B.N2C.NOD.NO+
26.在[Co(en)2(NH3)Cl]2+中,Co3+的配位数是()
A.4B.5C.6D.7
27.AgCl的Ksp=a,[Ag(NH3)2]+的Ks=b,则下列反应
AgCl+2NH3-↔[Ag(NH3)2]++Cl-
的平衡常数为()
A.abB.a+bC.b/aD.a/b
28.Na2S2O3可作为重金属中毒时的解毒剂,这是利用它的()
A.还原性B.氧化性C.配位性D.与重金属离子生成难溶物。
29.将化学组成为CoCl3·4NH3的紫色固体配制成溶液,向其中加入足量的AgNO3溶液后,只有1/3的氯从沉淀析出。
该配合物的内界含有
A.2个Cl–和1个NH3B.2个Cl–和2个NH3
C.2个Cl–和3个NH3D.2个Cl–和4个NH3
30.下列同一浓度的溶液中,所含粒子数最多的是()
A.FeSO4B.(NH4)2Fe(SO4)2C.(NH4)4[Fe(CN)6]D.Fe2[Fe(CN)6]
31.下列命名正确的是()
A.[Co(ONO)(NH3)5Cl]Cl2亚硝酸根二氯•五氨合钴(III)
B.[Co(NO2)3(NH3)3]三亚硝基•三氨合钴(III)
C.[CoCl2(NH3)3]Cl氯化二氯•三氨合钴(III)
D.[CoCl2(NH3)4]Cl氯化四氨•氯气合钴(III)
32.影响中心离子(或原子)配位数的主要因素有()
A.中心离子(或原子)能提供的价层空轨道数
B.空间效应,即中心离子(或原子)的半径与配位体半径之比越大,配位数越大
C.配位数随中心离子(或原子)电荷数增加而增大D.以上三条都是
33.分子中既存在离子键,共价键还存在配位键的有()
A.Na2SO4B.AlCl3C.[Co(NH3)6]Cl3D.KCN
34.选择下列哪一种弱酸及其共轭碱较合适配制pH值为9的缓冲溶液()
A.HCOOH,a=1.77×10-4B.H2CO3,a=4.4×10-7
C.HAc,a=1.75×10-5D.NH4+,a=5.56×10-10
35.下列两种溶液等体积混合,可以配成缓冲溶液的是()
A.0.5mol·L-1HCl和1.0mol·L-1NaOHB.1.0mol·L-1HCl和0.5mol·L-1NaOH
C.0.5mol·L-1HCl和1.0mol·L-1NH3D.1.0mol·L-1HCl和0.5mol·L-1NH3
36.下列有关缓冲溶液的叙述中,错误的是()
A.总浓度一定时,缓冲比为1时,值最大
B.缓冲范围大体为pKa1
C.缓冲容量越大,溶液的缓冲能力越强
D.缓冲溶液稀释后,pH不变
37.人体血浆中最重要的共轭碱是()
A.H2PO4-B.HPO42-C.HCO3-D.H2CO3
38.阴离子交换树脂不能够选择交换的离子是()
A.HCO3-
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 无机化学 期末 考试
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 12处方点评管理规范实施细则_精品文档.doc
12处方点评管理规范实施细则_精品文档.doc
 17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
 创办企业.ppt
创办企业.ppt
