 酸碱盐常用基础默写Word文档格式.docx
酸碱盐常用基础默写Word文档格式.docx
- 文档编号:16014327
- 上传时间:2022-11-17
- 格式:DOCX
- 页数:14
- 大小:34.06KB
酸碱盐常用基础默写Word文档格式.docx
《酸碱盐常用基础默写Word文档格式.docx》由会员分享,可在线阅读,更多相关《酸碱盐常用基础默写Word文档格式.docx(14页珍藏版)》请在冰豆网上搜索。
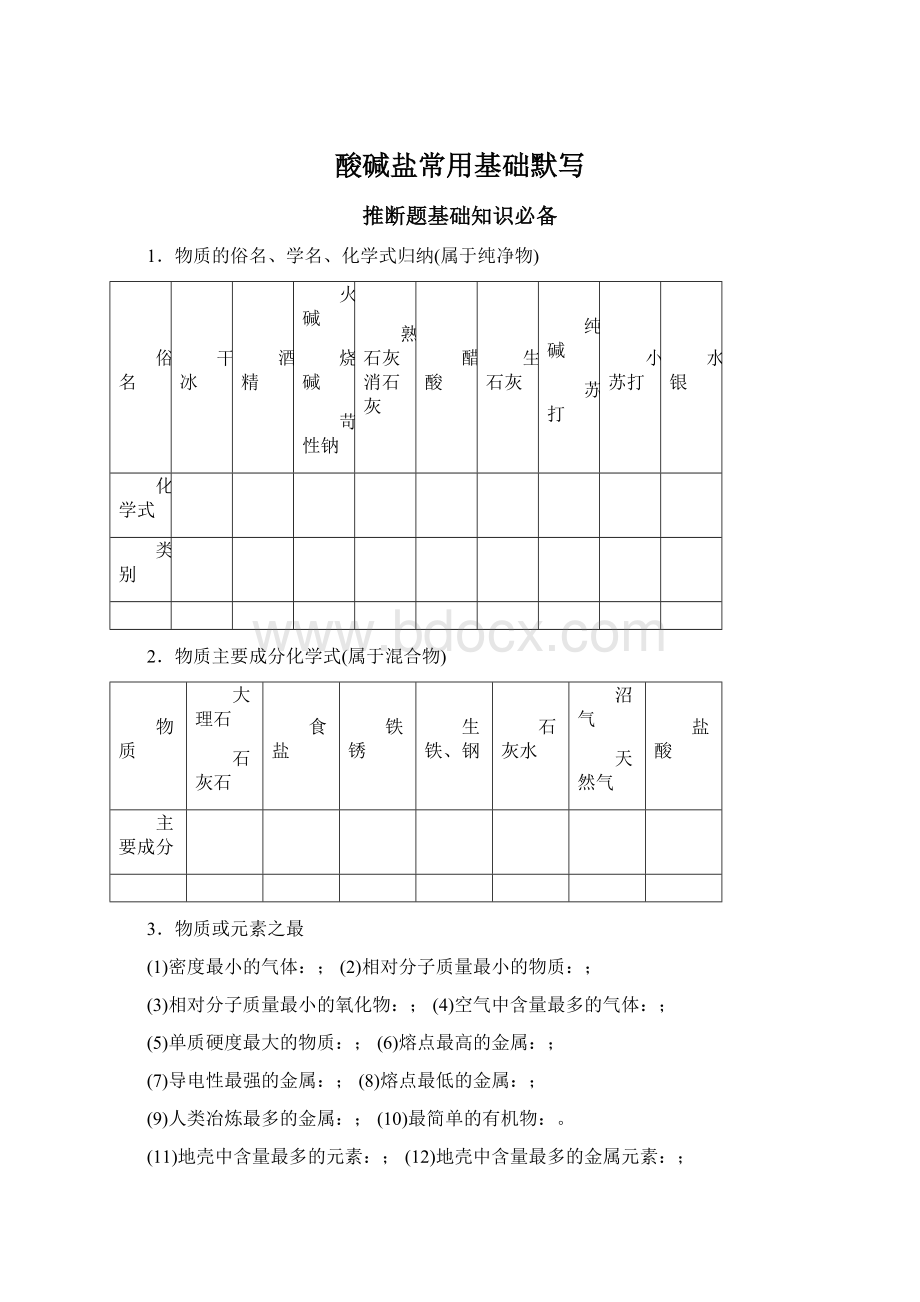
食盐
铁锈
生铁、钢
石灰水
沼气
天然气
盐酸
主要成分
3.物质或元素之最
(1)密度最小的气体:
;
(2)相对分子质量最小的物质:
(3)相对分子质量最小的氧化物:
(4)空气中含量最多的气体:
(5)单质硬度最大的物质:
(6)熔点最高的金属:
(7)导电性最强的金属:
(8)熔点最低的金属:
(9)人类冶炼最多的金属:
(10)最简单的有机物:
。
(11)地壳中含量最多的元素:
(12)地壳中含量最多的金属元素:
(13)形成化合物种类最多的元素:
(14)生物细胞中含量最多的元素:
(15)人体中含量最高的金属元素:
4.常见物质的颜色
(1)白色固体:
(2)黑色固体:
;
(3)红色固体:
(4)紫黑色固体、淡黄色固体、绿色粉末、蓝色晶体;
(5)溶液呈蓝色含,溶液呈浅绿色含,溶液呈黄色含,溶液呈紫红色含其余溶液一般无色;
(6)沉淀的颜色:
BaSO4(白色)、AgCl(白色)不溶于水也不溶于酸,CaCO3(白色)、BaCO3(白色)、Mg(OH)2(白色)、Cu(OH)2(蓝色)、Fe(OH)3(红褐色)不溶于水而溶于酸;
(7)无色有刺激性气味的气体:
,无色无味的气体:
,无色有刺激性气味的液体:
盐酸、硝酸、醋酸(酒精为有特殊气味的液体)。
5.有毒物质
SO2、HCl、CO(有毒气体);
CH3OH(甲醇,有毒液体);
黄曲霉素、亚硝酸钠和甲醛(危害人体健康的物质)。
6.物质用途
(1)助燃剂:
(2)灭火剂和人工降雨:
(3)冶炼金属的还原剂:
、、;
(4)改良酸性土壤以及配制波尔多液:
(5)建筑材料:
(6)助消化、除铁锈、胃酸的主要成分:
(7)调味品、融雪剂:
(8)食品干燥剂:
(9)食物脱氧剂:
(10)“钡餐”透视用盐:
(11)制作发酵粉:
(12)实验室制取氢气的金属:
(13)霓虹灯中充入的气体:
7.物质的特征组成
(1)一定含有碳元素:
(2)酸中一定含有氢元素,不一定含有氧元素;
(3)碱中一定含有氢、氧元素,不一定含有金属元素;
(4)具有相同元素组成的气体是:
、;
(5)具有相同元素组成的液体是:
(6)具有相同元素组成的固体是:
和,、和,和,以及、、和等等;
(7)常见气体单质有:
(8)常见无色气体有:
(9)常温下呈液态的物质有:
、和。
8.物质反应时的特征现象
(1)能使澄清石灰水变浑浊的无色无味气体是:
(2)能使黑色CuO变红(或红色Fe2O3变黑)的气体是:
或,固体是:
(3)能使燃烧着的木条正常燃烧的气体是:
,燃烧得更旺的气体是:
,熄灭的气体是:
或;
能使带火星的木条复燃的气体是:
(4)能使白色无水CuSO4粉末变蓝的气体是:
能使湿润的红色石蕊试纸变蓝的气体是:
能使湿润的蓝色石蕊试纸变红的气体是:
(5)在O2中燃烧火星四射的物质是:
,燃烧时发出耀眼的白光的是:
(6)在空气中燃烧生成CO2和H2O的物质是:
,如:
、等。
(7)在O2中燃烧有蓝紫色火焰且生成刺激性气味气体的是:
(8)在空气中燃烧有淡蓝色火焰且只生成无色液体的气体:
(9)在空气中燃烧只生成能使澄清石灰水变浑浊的气体的是:
9.物质特征反应条件
(1)“通电”:
(2)“高温”:
①,②指;
(3)“MnO2作催化剂”:
(4)“点燃”:
(5)在光照和叶绿素条件下进行:
(6)双沉淀的反应,如:
(7)生成三种物质的分解反应是:
10.各物质之间的转化规律(详见反应规律专题)
酸碱盐化学方程式(练习)
一.两个置换反应规律
1.酸+金属==盐+氢气
反应条件:
①酸不能用强氧化性酸,如硝酸、浓硫酸,(常用稀硫酸、盐酸)
②金属必须位于氢以前(常用Mg、Al、Zn、Fe)
Mg+HCl==Mg+H2SO4==
Al+HCl==Al+H2SO4==
Zn+HCl==Zn+H2SO4==
Fe+HCl==Fe+H2SO4===
2.盐+金属==新盐+新金属
①盐(反应物)必须溶于水
②金属单质(反应物)比盐中金属活泼,不用钾、钙、钠
Fe+CuSO4==Al+CuSO4==Zn+CuSO4==
Cu+AgNO3==Cu+Hg(NO3)2==
二.三个分解反应规律
1.酸(含氧酸)==非金属氧化物+水===H2O+CO2↑
2.碱(难溶性)==金属氧化物+水
Cu(OH)2Fe(OH)3
3.碳酸盐(难溶性)==金属氧化物+二氧化碳
CaCO3
三.四个化合反应规律
1.金属+氧气==金属氧化物
Mg+O2Fe+O2Cu+O2
2.金属氧化物+水==碱(可溶性)
CaO+H2O==Na2O+H2O==
3.非金属+氧气==非金属氧化物
S+O2P+O2C+O2(碳充分燃烧)
C+O2(碳不充分燃烧)H2+O2
4.非金属氧化物+水==酸CO2+H2O==SO3+H2O==SO2+H2O==
四.五个复分解反应规律(亚硫酸)
1.酸+碱==盐+水Cu(OH)2+HCl==Al(OH)3+HCl==
Cu(OH)2+H2SO4==Mg(OH)2+HNO3==
2.酸+盐==新酸+新盐反应条件:
符合复分解反应发生的条件(实际反应条件很复杂)
CaCO3+HCl==Na2CO3+HCl==AgNO3+HCl==
Na2CO3+H2SO4==H2SO4+BaCl2==H2SO4+Ba(NO3)2==
3.盐+碱==新盐+新碱反应条件:
反应物都溶于水,生成物至少有一种不溶(前溶后沉)
CuSO4+NaOH==FeCl3+NaOH==
Na2CO3+Ca(OH)2==CuSO4+Ba(OH)2==
4.盐+盐==新盐+新盐反应条件:
NaCl+AgNO3==Na2SO4+BaCl2==Na2SO4+Ba(NO3)2==
5.酸+金属氧化物==盐+水
Fe2O3+HCl==Fe2O3+H2SO4==CuO+HCl==
CuO+H2SO4==MgO+HNO3==
五.其它反应
1.碱+非金属氧化物==盐+水(不属于四种化学反应基本类型)
NaOH+CO2==NaOH+SO2==NaOH+SO3==Ca(OH)2+CO2==
2.三种还原剂(H2、、C、O2)跟氧化物反应
H2+CuO(置换反应)CO+CuO
CO+Fe2O3C+CuO(置换反应)
C+CO2(化合反应)
3.实验室制取三种气体(常用方法)
KMnO4KClO3
Zn+HCl==Zn+H2SO4==CaCO3+HCl==
4.盐分解
Cu2(OH)2CO3CaCO3
5.三种有机物燃烧
CH4+O2C2H5OH+O2
CH3OH+O2
酸碱盐化学方程式(答案)
Mg+2HCl==MgCl2+H2↑Mg+H2SO4==MgSO4+H2↑
2Al+6HCl==2AlCl3+3H2↑2Al+3H2SO4==2Al2(SO4)3+3H2↑
Zn+2HCl==ZnCl2+H2↑Zn+2H2SO4==ZnSO4+H2↑
Fe+2HCl==FeCl2+H2↑Fe+H2SO4===FeSO4+H2↑
2.盐+金属==新盐+新金属
Fe+CuSO4==FeSO4+Cu2Al+3CuSO4==Al2(SO4)3+3Cu
Zn+CuSO4==ZnSO4+CuCu+2AgNO3==Cu(NO3)2+2Ag
Cu+Hg(NO3)2==Cu(NO3)2+Hg
1.酸(含氧酸)==非金属氧化物+水
H2CO3===H2O+CO2↑
Cu(OH)2CuO+H2O2Fe(OH)3Fe2O3+3H2O
CaCO3CaO+CO2↑
2Mg+O22MgO3Fe+2O2Fe3O42Cu+O22CuO
CaO+H2O==Ca(OH)2Na2O+H2O==2NaOH
S+O2SO24P+5O22P2O5C+O2CO2(碳充分燃烧)
2C+O22CO(碳不充分燃烧)2H2+O22H2O
4.非金属氧化物+水==酸
CO2+H2O==H2CO3SO3+O2==H2SO4SO2+O2==H2SO3
1.酸+碱==盐+水
Cu(OH)2+2HCl==CuCl2+H2OAl(OH)3+3HCl==AlCl3+3H2O
Cu(OH)2+H2SO4==CuSO4+2H2OMg(OH)2+2HNO3==Mg(NO3)2+2H2O
2.酸+盐==新酸+新盐
CaCO3+2HCl==CaCl2+H2O+CO2↑Na2CO3+2HCl==2NaCl+H2O+CO2↑
AgNO3+HCl==AgCl↓+HNO3
Na2CO3+H2SO4==Na2SO4+H2O+CO2↑H2SO4+BaCl2==2HCl+BaSO4↓
H2SO4+Ba(NO3)2==2HNO3+BaSO4↓
3.盐+碱==新盐+新碱
CuSO4+2NaOH==Cu(OH)2↓+Na2SO4FeCl3+3NaOH==Fe(OH)3↓+3NaCl
Na2CO3+Ca(OH)2==2NaOH+CaCO3↓CuSO4+Ba(OH)2==Cu(OH)2↓+BaSO4↓
4.盐+盐==新盐+新盐
NaCl+AgNO3==NaNO3+AgCl↓Na2SO4+BaCl2==2NaCl+BaSO4↓
Na2SO4+Ba(NO3)2==2NaNO3+BaSO4↓
Fe2O3+6HCl==2FeCl3+3H2OFe2O3+3H2SO4==Fe2(SO4)3+3H2O
CuO+2HCl==CuCl2+H2OCuO+H2SO4==CuSO4+H2O
MgO+2HNO3==Mg(NO3)2+H2O
2NaOH+CO2==Na2CO3+H2O2NaOH+SO2==Na2S
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 酸碱 常用 基础 默写
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
