 高中化学大全一Word格式.docx
高中化学大全一Word格式.docx
- 文档编号:15950738
- 上传时间:2022-11-17
- 格式:DOCX
- 页数:27
- 大小:83.62KB
高中化学大全一Word格式.docx
《高中化学大全一Word格式.docx》由会员分享,可在线阅读,更多相关《高中化学大全一Word格式.docx(27页珍藏版)》请在冰豆网上搜索。
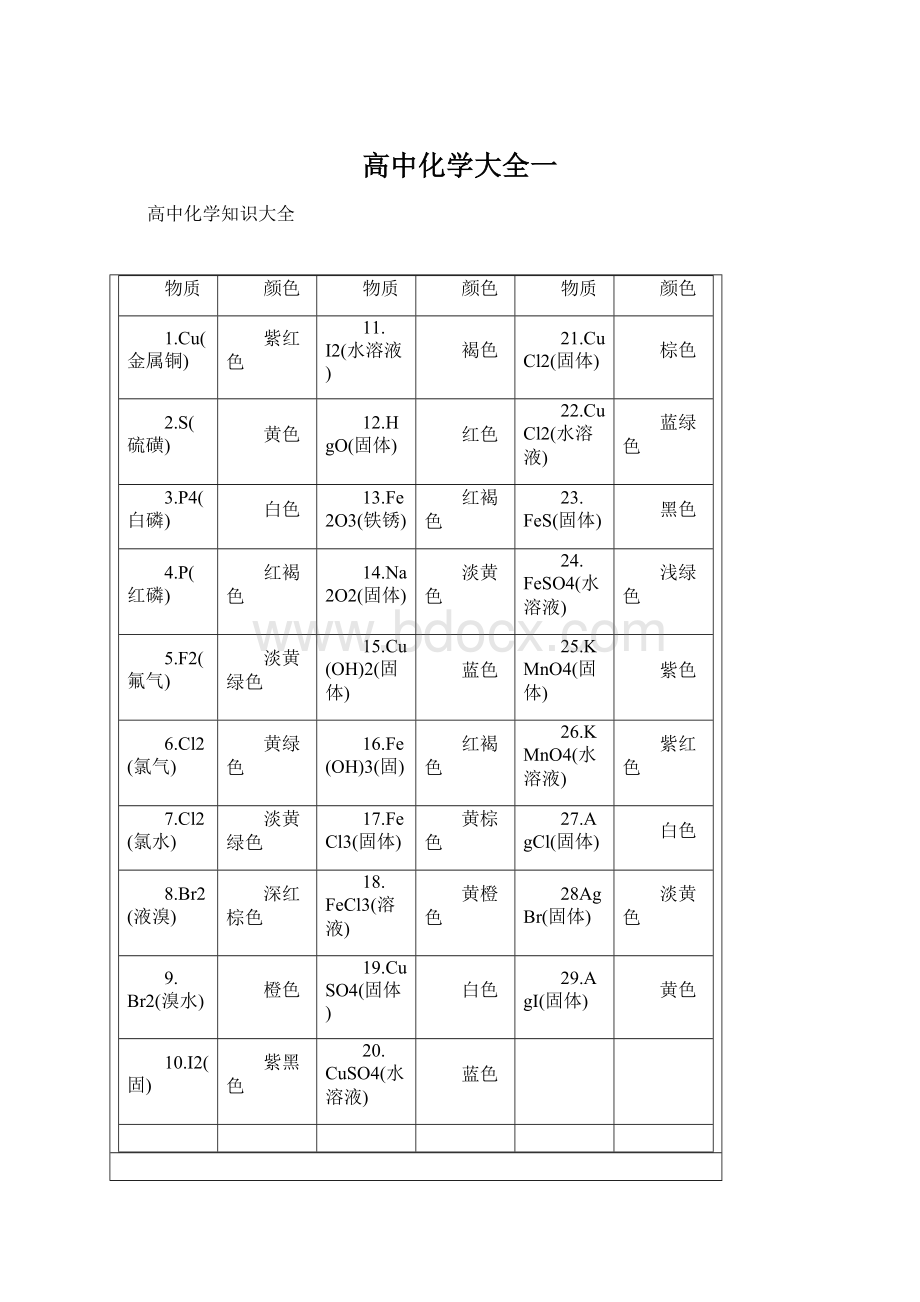
25.KMnO4(固体)
紫色
6.Cl2(氯气)
黄绿色
16.Fe(OH)3(固)
26.KMnO4(水溶液)
7.Cl2(氯水)
17.FeCl3(固体)
黄棕色
27.AgCl(固体)
8.Br2(液溴)
深红棕色
18.FeCl3(溶液)
黄橙色
28AgBr(固体)
9.Br2(溴水)
橙色
19.CuSO4(固体)
29.AgI(固体)
10.I2(固)
紫黑色
20.CuSO4(水溶液)
引起物质量浓度误差的操作
操作
m
v
C
1、天平的砝码沾有其他物质或已生锈
增大
不变;
偏大
2、调整天平零点时,游砝放在了刻度线的右端
3、药品、砝码左右位置颠倒
减小
偏小
4、称量易潮解的物质(如NaOH)时间过长
5、用滤纸称易潮解的物质(如NaOH)
6、溶质含有其它杂质
7、用量筒量取液体时,仰视读数
8、用量筒量取液体时,俯视读数
9、溶解前烧杯内有水
无影响
10、搅拌时部分液体溅出
11、未洗烧杯和玻璃棒
12、未冷却到室温就注入容量瓶定容
13、向容量瓶转移溶液时有少量液体流出
14、定容时,水加多了,用滴管吸出
15、整个过程不摇动
16、定容后,经振荡、摇匀、静置、液面下降再加水
17、定容后,经振荡、摇匀、静置、液面下降
18、定容时,俯视读刻度数
19、定容时,仰视读刻度数
20、配好的溶液转入干净的试剂瓶时,不慎溅出部分溶液
常见物质(离子)的检验
物质(离子)
方法及现象
CO32-
与含Ba2+的溶液反应,生成白色沉淀,该沉淀溶于硝酸(或盐酸),生成无色无气味、能使澄清石灰水变浑浊的气体(CO2)。
SO42-
与含Ba2+的溶液反应,生成白色沉淀,不溶于稀盐酸。
Cl-
与硝酸银溶液反应,生成不溶于稀硝酸的白色沉淀。
NH4+
与NaOH浓溶液反应,微热,放出使湿润的红色石蕊试纸变蓝的刺激性气味气体(NH3)。
Na+
焰色反应呈黄色
K+
焰色反应呈紫色(透过蓝色钴玻璃)
I2
遇淀粉显蓝色
蛋白质
灼烧有烧焦羽毛气味;
加浓硝酸后微热显黄色
焰色反应:
1.钠或钠的化合物在无色火焰上灼烧,火焰染上黄色
2.钾或钾的化合物焰色反应为紫色(要隔着蓝色玻璃观察)
常见物质除杂质的方法
实例
所加试剂
方法
Na2SO4溶液中混少量Na2SO3
稀H2SO4
CO2↑气体生成
MgCl2溶液中混少量MgSO4
适量BaCl2
BaSO4↓过滤
FeCl3溶液中含少量FeCl2
通适量氯气
(Fe2+被氧化为Fe3+)
FeCl2溶液中含少量FeCl3
适量铁屑
过滤
FeSO4溶液中含少量CuSO4
过量铁屑
NaCl中含NaI
加热、升华
Na2CO3粉末中含NaHCO3
加热、分解
Na2CO3溶液中含NaHCO3
适量NaOH
(酸式盐转化为正盐)
NaHCO3溶液中含Na2CO3
通过量CO2
(正盐转化为酸式盐)
CuS中混少量FeS
足量盐酸
溶解、过滤
Al2O3中含Fe2O3
过量NaOH溶液通CO2
过滤(滤液AlO2-)
沉淀、过滤(Al(OH)3)
灼烧Al2O3
苯中含苯酚
NaOH溶液
分液
溴苯中含Br2
稀NaOH溶液
苯中含甲苯
酸性高锰酸钾溶液
甲苯生成苯甲酸分液
硝基苯中含硝酸、硫酸
大量水
溴乙烷中含乙醇
水
乙酸乙酯中含乙酸
Na2CO3饱和溶液
95%乙醇中的水
CaO,静置
蒸馏
乙醇中少量乙酸
CaO
乙醚中含微量乙醇
Na
淀粉中少量葡萄糖
渗析
常见漂白剂及其应用
常见漂白剂
漂白原理及用途
HClO
HClO有强氧化性,常用于自来水消毒。
Ca(ClO)2
Ca(ClO)2与CO2、水生成HClO而呈漂白性,常用于衣服、织物的漂白
Na2O2
Na2O2有强氧化性,常用于织物、丝稠、麦秆等漂白
O3
O3有极强的漂白性,常用于消毒。
H2O2
H2O2有强氧化性,3%的双氧水常用于医疗消毒。
SO2
化合性漂白,与有机色素结合成无色的物质,新物质分解后颜色会复原。
木炭或活性碳
物理吸附性漂白,可以做脱色剂,除臭剂,去味剂,防毒面具的滤毒罐等。
滴加顺序不同,现象不同
1.AgNO3与NH3·
H2O:
AgNO3向NH3·
H2O中滴加——开始无白色沉淀,后产生白色沉淀
NH3·
H2O向AgNO3中滴加——开始有白色沉淀,后白色沉淀消失
2.NaOH与AlCl3:
NaOH向AlCl3中滴加——开始有白色沉淀,后白色沉淀消失
AlCl3向NaOH中滴加——开始无白色沉淀,后产生白色沉淀
3.HCl与NaAlO2:
HCl向NaAlO2中滴加——开始有白色沉淀,后白色沉淀消失
NaAlO2向HCl中滴加——开始无白色沉淀,后产生白色沉淀
4.Na2CO3与盐酸:
Na2CO3向盐酸中滴加——开始有气泡,后不产生气泡
盐酸向Na2CO3中滴加——开始无气泡,后产生气泡
一、俗名
无机部分:
纯碱、苏打、天然碱、口碱:
Na2CO3小苏打:
NaHCO3大苏打:
Na2S2O3石膏(生石膏):
CaSO4.2H2O熟石膏:
2CaSO4·
.H2O 莹石:
CaF2重晶石:
BaSO4(无毒)碳铵:
NH4HCO3石灰石、大理石:
CaCO3生石灰:
CaO食盐:
NaCl熟石灰、消石灰:
Ca(OH)2芒硝:
Na2SO4·
7H2O(缓泻剂)烧碱、火碱、苛性钠:
NaOH绿矾:
FaSO4·
7H2O干冰:
CO2明矾:
KAl(SO4)2·
12H2O漂白粉:
Ca(ClO)2、CaCl2(混和物)泻盐:
MgSO4·
7H2O胆矾、蓝矾:
CuSO4·
5H2O双氧水:
H2O2皓矾:
ZnSO4·
7H2O硅石、石英:
SiO2刚玉:
Al2O3水玻璃、泡花碱、矿物胶:
Na2SiO3铁红、铁矿:
Fe2O3磁铁矿:
Fe3O4黄铁矿、硫铁矿:
FeS2铜绿、孔雀石:
Cu2(OH)2CO3菱铁矿:
FeCO3赤铜矿:
Cu2O波尔多液:
Ca(OH)2和CuSO4石硫合剂:
Ca(OH)2和S玻璃的主要成分:
Na2SiO3、CaSiO3、SiO2过磷酸钙(主要成分):
Ca(H2PO4)2和CaSO4重过磷酸钙(主要成分):
Ca(H2PO4)2天然气、沼气、坑气(主要成分):
CH4水煤气:
CO和H2硫酸亚铁铵(淡蓝绿色):
Fe(NH4)2(SO4)2溶于水后呈淡绿色
光化学烟雾:
NO2在光照下产生的一种有毒气体王水:
浓HNO3与浓HCl按体积比1:
3混合而成。
铝热剂:
Al+Fe2O3或其它氧化物。
尿素:
CO(NH2)2
有机部分:
氯仿:
CHCl3电石:
CaC2电石气:
C2H2(乙炔)TNT:
三硝基甲苯酒精、乙醇:
C2H5OH
氟氯烃:
是良好的制冷剂,有毒,但破坏O3层。
醋酸:
冰醋酸、食醋CH3COOH
裂解气成分(石油裂化):
烯烃、烷烃、炔烃、H2S、CO2、CO等。
甘油、丙三醇:
C3H8O3
焦炉气成分(煤干馏):
H2、CH4、乙烯、CO等。
石炭酸:
苯酚蚁醛:
甲醛HCHO
福尔马林:
35%—40%的甲醛水溶液蚁酸:
甲酸HCOOH
葡萄糖:
C6H12O6果糖:
C6H12O6蔗糖:
C12H22O11麦芽糖:
C12H22O11淀粉:
(C6H10O5)n
硬脂酸:
C17H35COOH油酸:
C17H33COOH软脂酸:
C15H31COOH
草酸:
乙二酸HOOC—COOH使蓝墨水褪色,强酸性,受热分解成CO2和水,使KMnO4酸性溶液褪色。
二、颜色
铁:
铁粉是黑色的;
一整块的固体铁是银白色的。
Fe2+——浅绿色Fe3O4——黑色晶体
Fe(OH)2——白色沉淀Fe3+——黄色Fe(OH)3——红褐色沉淀Fe(SCN)3——血红色溶液
FeO——黑色的粉末Fe(NH4)2(SO4)2——淡蓝绿色Fe2O3——红棕色粉末FeS——黑色固体
铜:
单质是紫红色Cu2+——蓝色CuO——黑色Cu2O——红色CuSO4(无水)—白色CuSO4·
5H2O——蓝色Cu2(OH)2CO3—绿色Cu(OH)2——蓝色[Cu(NH3)4]SO4——深蓝色溶液
BaSO4、BaCO3、Ag2CO3、CaCO3、AgCl、Mg(OH)2、三溴苯酚均是白色沉淀
Al(OH)3白色絮状沉淀H4SiO4(原硅酸)白色胶状沉淀
Cl2、氯水——黄绿色F2——淡黄绿色气体Br2——深红棕色液体I2——紫黑色固体
HF、HCl、HBr、HI均为无色气体,在空气中均形成白雾
CCl4——无色的液体,密度大于水,与水不互溶KMnO4--——紫色MnO4-——紫色
Na2O2—淡黄色固体Ag3PO4—黄色沉淀S—黄色固体AgBr—浅黄色沉淀
AgI—黄色沉淀O3—淡蓝色气体SO2—无色,有剌激性气味、有毒的气体
SO3—无色固体(沸点44.80C)品红溶液——红色氢氟酸:
HF——腐蚀玻璃
N2O4、NO——无色气体NO2——红棕色气体NH3——无色、有剌激性气味气体
三、现象:
1、铝片与盐酸反应是放热的,Ba(OH)2与NH4Cl反应是吸热的;
2、Na与H2O(放有酚酞)反应,熔化、浮于水面、转动、有气体放出;
(熔、浮、游、嘶、红)
3、焰色反应:
Na黄色、K紫色(透过蓝色的钴玻璃)、Cu绿色、Ca砖红、Na+(黄色)、K+(紫色)。
4、Cu丝在Cl2中燃烧产生棕色的烟;
5、H2在Cl2中燃烧是苍白色的火焰;
6、Na在Cl2中燃烧产生大量的白烟;
7、P在Cl2中燃烧产生大量的白色烟雾;
8、SO2通入品红溶液先褪色,加热后恢复原色;
9、NH3与HCl相遇产生大量的白烟;
10、铝箔在氧气中激烈燃烧产生刺眼的白光;
11、镁条在空
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 大全
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
