 安徽省高考考试说明化学题型示例Word文档格式.docx
安徽省高考考试说明化学题型示例Word文档格式.docx
- 文档编号:15906577
- 上传时间:2022-11-17
- 格式:DOCX
- 页数:24
- 大小:734.19KB
安徽省高考考试说明化学题型示例Word文档格式.docx
《安徽省高考考试说明化学题型示例Word文档格式.docx》由会员分享,可在线阅读,更多相关《安徽省高考考试说明化学题型示例Word文档格式.docx(24页珍藏版)》请在冰豆网上搜索。
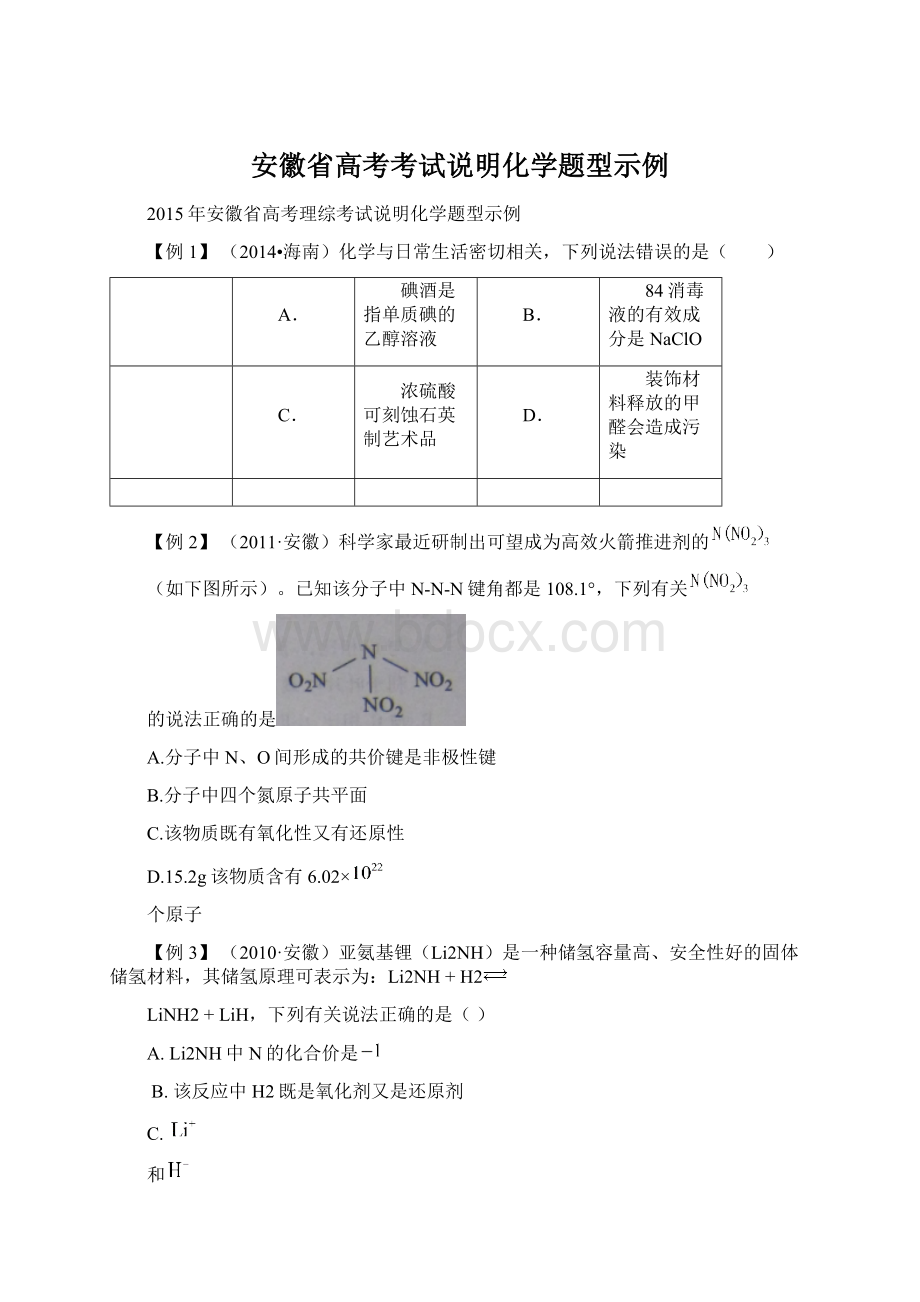
C.
和
的离子半径相等D.此法储氢和钢瓶储氢的原理相同
【例4】(2011·
安徽)下列有关实验操作、现象和解释或结论都正确的是
选项
实验操作
现象
解释或结论
A
过量的Fe粉中加入
,
充分反应后,滴入KSCN溶液
溶液呈红色
稀
将Fe氧化为
B
Agl沉淀中滴入稀KCl溶液
有白色沉淀出现
AgCl比Agl更难溶
C
Al箔插入稀
中
无现象
Al箔表面被
氧化,形成致密的氧化膜
D
用玻璃棒蘸取浓氨水点到红色石蕊试纸上
试纸变蓝色
浓氨水呈碱性
【例5】(2014·
江苏)设NA为阿伏伽德罗常数的值。
下列说法正确的是()
A.1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA
B.0.1mol丙烯酸中含有双键的数目为0.1NA
C.标准状况下,11.2L苯中含有分子的数目为0.5NA
D.在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA
【例6】(2010·
上海)将0.4gNaOH和1.06gNa2CO3混合配成溶液,向溶液中滴加0.1mol·
L-1稀盐酸。
下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是()
【例7】(2011·
安徽)室温下,将1.000mol
盐酸滴入20.00mL1.000mol
氨水中,溶液pH和温度随加入盐酸体积变化曲线如右图所示。
下列有关说法正确的是
A.a点由水电离出的
B.b点:
C.c点:
D.d点后,容易温度略下降的主要原因是
电离吸热
【例8】右图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是()
A.
原子半径:
Z>
Y>
X
B.气态氢化物的稳定性:
W>
R
C.WX3和水反应形成的化合物是离子化合物
D.Y和Z两者最高价氧化物对应的水化物能相互反应
【例9】(2014·
山东)下表中对应关系正确的是()
A
CH3CH3+Cl2
CH3CH2Cl+HCl
CH2=CH2+HCl
CH3CH2Cl
均为取代反应
由油脂得到甘油
由淀粉得到葡萄糖
均发生了水解反应
Cl2+2Br‾=2Cl‾+Br2
Zn+Cu2+=Zn2++Cu
均为单质被还原的置换反应
2Na2O2+2H2O+4NaOH+O2↑
Cl2+H2O=HCl+HClO
均为水作还原剂的氧化还原反应
电解
【例10】
(2013·
天津)为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以A1作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。
反应原理如下:
电池:
Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l),电解池:
2Al+3H2O=====Al2O3+3H2↑
电解过程中,以下判断正确的是
电池
电解池
H+移向Pb电极
每消耗3molPb
生成2molAl2O3
正极:
PbO2+4H++2e—=Pb2++2H2O
阳极:
2Al+3H2O-6e—=Al2O3+6H+
【例11】(2012·
福建)一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如右图所示。
A.50min时,PH=2和PH=7时R的降解百分率相等
B.溶液酸性越强,R的降解速率越小
C.R的起始浓度越小,降解速率越大
D.在20-25min之间,PH=10时R的平均降解速率为0.04mol/(L.min)
【例12】(2013·
安徽)实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。
仅用此装置和表中提供的物质完成相关实验,最合理的选项是
a中的物质
b中的物质
C中收集
的气体
d中的物质
浓氨水
CaO
NH3
H2O
浓硫酸
Na2SO3
SO2
NaOH溶液
稀硝酸
Cu
NO2
浓盐酸
MnO2
Cl2
【例13】(2014·
全国Ⅰ)利用右图所示装置进行下列实验,能得出相应实验结论的是()
①
②
③
实验结论
稀硫酸
Na2S
AgNO3与AgCl的浊液
Ksp(AgCl)>Ksp(Ag2S)
蔗糖
溴水
浓硫酸具有脱水性、氧化性
稀盐酸
Ba(NO3)2溶液
SO2与可溶性钡盐均可以生成白色沉淀
浓硝酸
Na2CO3
Na2SiO3溶液
酸性:
硝酸>碳酸>硅酸
【例14】(2014·
广东)常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液
等体积混合后,所得溶液中部分微粒组分及浓度
如图5所示,下列说法正确的是
A、HA为强酸
B、该混合液pH=7
C、图中X表示HA,Y表示OH-,Z表示H+
D、该混合溶液中:
c(A-)+
c(Y)=c(Na+)
【例15】
(2012·
安徽)下列离子或分子在溶液中能大量共存,通入CO2后仍能大量共存的一组是
A.K+、Ca2+、Cl-、NO3-B.K+、Na+、Br-、SiO32-
C.H+、Fe2+、SO42-、Cl2D.K+、Ag+、NH3·
H2O、NO3-
【例16】
江苏)短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13。
X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素。
下列说法正确的是
A.原子半径的大小顺序:
r(Y)>
r(Z)>
r(W)
B.元素Z、W的简单离子的电子层结构不同
C.元素Y的简单气态氢化物的热稳定性比Z的强
D.只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物
【例17】
(2014·
安徽)臭氧是理想的烟气脱硝试剂,其反应为:
2NO2(g)+O3(g)
N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断准确的是
升高温度,平衡常数减小
0~3s内,反应速率为:
v(NO2)=0.2mol/L
t1时仅加入催化剂,平衡正向移动
达平衡时,仅改变x则x为c(O2)
【例18】(2013·
福建)某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO。
其过程如下:
mCeO2
(m-x)CeO2·
xCe+xO2
xCe+xH2O+xCO2
mCeO2+xH2+xCO
下列说法不正确的是
A.该过程中CeO2没有消耗
B.该过程实现了太阳能向化学能的转化
C.右图中△H1=△H2+△H3
D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH——2e—=CO32-+2H2O
【例19】(2013·
上海)已知氧化性Br2>Fe3+。
FeBr2溶液中通入一定量的Cl2,发生反应的离子方程式为:
aFe2++bBr-+cCl2→dFe3++eBr2+fCl-
下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是
A.243226B.021012
C.201202D.222214
【例20】
(2011·
福建)25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(
),发生反应:
,体系中c(Pb2+)和c(Sn2)变化关系如右图所示。
下列判断正确的是()
A.往平衡体系中加入少量金属铅后,c(Pb2+)增大
B.往平衡体系中加入少量
固体后,c(Sn2)变小
C.升高温度,平衡体系中c(Pb2+)增大,说明该反应
D.25℃时,该反应的平衡常数K=2.2
【例21】(2012·
山东)下列与含氯化合物有关的说法正确的是
A.HClO是弱酸,所以NaClO是弱电解质
B.向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
C.HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物
D.电解NaCl溶液得到22.4LH2(标准状况),理论上需要转移NA个电子(NA阿伏伽德罗常数)
【例22】(2014·
全国Ⅰ)化学与社会、生活密切相关。
对下列现象或事实的解释正确的是
现象或事实
解释
用热的烧碱溶液洗去油污
Na2CO3可直接和油污反应
漂白粉在空气中久置变质
漂白粉中的CaCl2与空气中的CO2反应生成CaCO3
施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用
K2CO3与NH4Cl反应生成氨气会降低肥效
FeCl3溶液可用于铜质印刷线路板制作
FeCl3能从含有Cu2+的溶液中置换出铜
【例23】(2011·
山东)室温下,向100mlpH=3的醋酸溶液中加水稀释后,下列说法正确的是()
A.溶液中导电粒子的数目减少
B.溶液中
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10mLpH=11的NaOH溶液,混合液的pH=7
【例24】(2012·
北京)下列说法正确的是
A.天然植物油常温下一般呈液态,难溶于水.有恒定的熔点、沸点
B.麦芽糖与蔗糖的水解产物均含葡萄糖,故二者均为还原型二糖、
C.若两种二肽互为同分异构体,则二者的水解产物不一致
D.乙醛、氯乙烯和乙二醇均可作为合成聚合物的单体
【例25】(2014·
全国Ⅱ)2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系。
下列叙述错误的是
A、a为电池的正极
B、电池充电反应为LiMn2O4
Li1-xMn2O4+xLi
C、放电时,a极锂的化合价发生变化
D、放电时,溶液中Li+从b向a迁移
【例26】
全国)从香荚兰豆中提取的一种芳香化合物,其分子式为C8H8O3,遇FeCl3溶液会呈现特征颜色,能发生银镜反应。
该化合物可能的结构简式是()
A.B.C.D.
【例27】(2014·
安徽)Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第_____周期第_____族;
S的基态原子核外有____个未成对电子;
Si的基态原子核外电子排布式为_______
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 安徽省 高考 考试 说明 化学 题型 示例
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《雷雨》中的蘩漪人物形象分析 1.docx
《雷雨》中的蘩漪人物形象分析 1.docx
![ISO-8501[1].1-2007-涂装表面清洁度的目视评定-(中文译本).doc](/Images/s.gif)