 成都树德中学高一期末复习基础知识归纳总结Word文档格式.docx
成都树德中学高一期末复习基础知识归纳总结Word文档格式.docx
- 文档编号:15860392
- 上传时间:2022-11-16
- 格式:DOCX
- 页数:19
- 大小:99.87KB
成都树德中学高一期末复习基础知识归纳总结Word文档格式.docx
《成都树德中学高一期末复习基础知识归纳总结Word文档格式.docx》由会员分享,可在线阅读,更多相关《成都树德中学高一期末复习基础知识归纳总结Word文档格式.docx(19页珍藏版)》请在冰豆网上搜索。
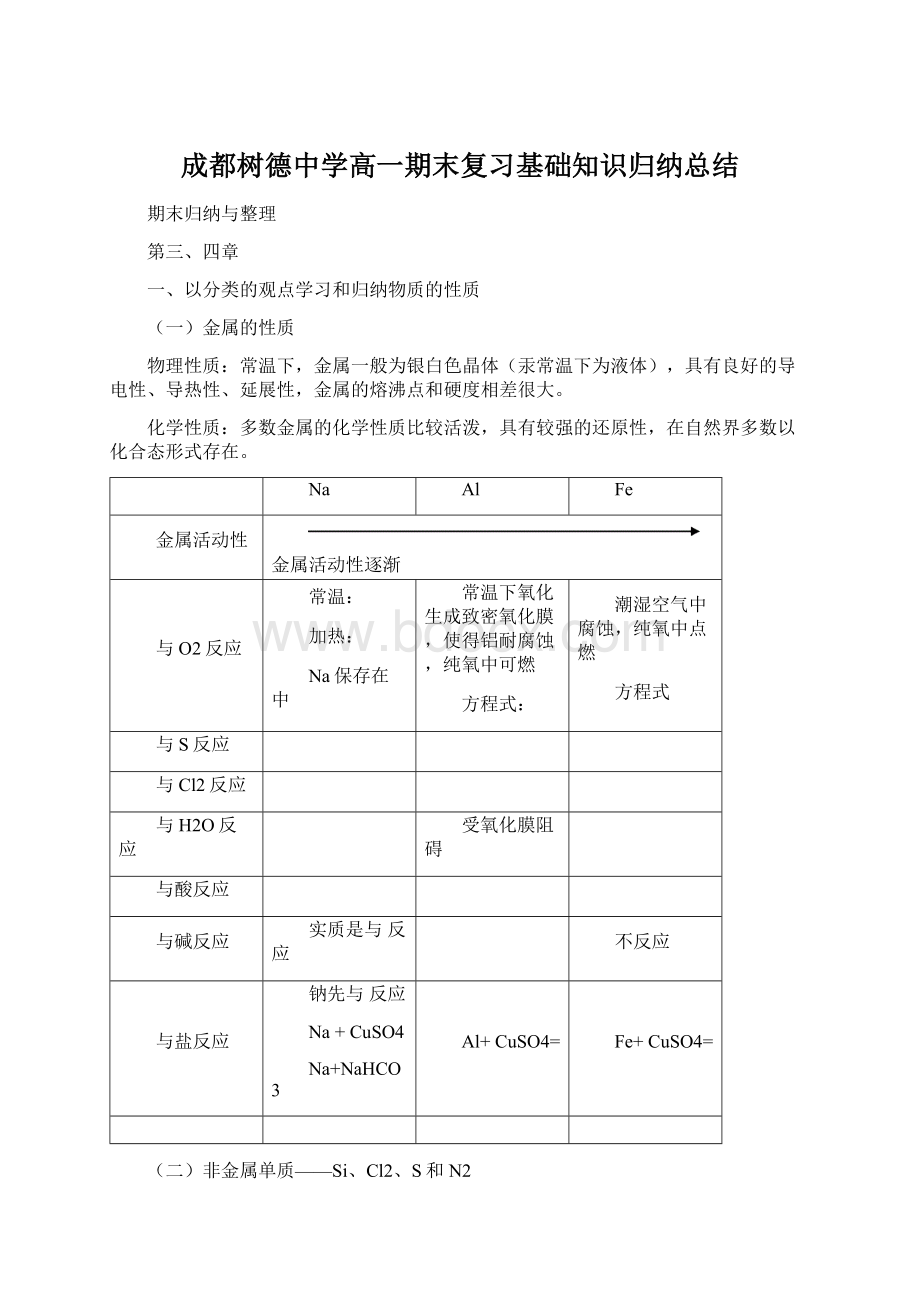
实质是与反应
不反应
与盐反应
钠先与反应
Na+CuSO4
Na+NaHCO3
Al+CuSO4=
Fe+CuSO4=
(二)非金属单质——Si、Cl2、S和N2
1.Si的主要性质
⑴常温下与、、反应。
请写出方程式:
⑵高温或点燃条件下与、和反应,写出反应的方程式:
⑶制备粗硅的反应:
2.Cl2的主要性质和用途
⑴与金属反应:
Na+Cl2=;
Fe+Cl2=;
Cu+Cl2=;
Cl2与变价金属反应生成价金属氯化物。
⑵与非金属反应:
H2+Cl2========;
P+Cl2(少)=;
P+Cl2(过)=;
⑶与水反应:
Cl2+H2O=。
离子方程式为
⑷与碱反应:
Cl2+NaOH=。
Cl2+Ca(OH)2=。
若用的是石灰乳,该反应的离子方程式为
3.S的主要性质:
S是一种色的体。
溶于水,溶于酒精,溶于CS2。
⑴弱氧化性:
H2+S==;
Na+S==;
Fe+S==;
Cu+S==;
S与变价金属反应生成价金属硫化物。
⑵还原性:
S+O2===
4.N2的主要性质:
N2+O2====;
N2+H2========;
(三)氧化物
1.分类(请将I和II,II和III连线)
I(非金属氧化物)II(从性质分类)III(金属氧化物)
⑴H2O2⑴酸性氧化物⑴Na2O2、KO2等
⑵CO、NO、NO2、H2O⑵碱性氧化物⑵Na2O、CaO、MgO、FeO、Fe2O3、CuO等
⑶SiO2、CO2、SO2、SO3等⑶两性氧化物⑶Mn2O7、CrO3
⑷特殊氧化物⑷Al2O3和ZnO等
⑸不成盐氧化物
特殊氧化物:
过氧化物(Na2O2)、超氧化物(KO2)等。
与水反应生成对应的可溶性酸
酸性氧化物(如Mn2O7、CrO3)→酸性氧化物通性与碱反应生成盐和水
CO2、SO2等与碱性氧化物反应生成盐
氧Na2O、K2O、CaO与水反应生成碱
化成盐氧化物碱性氧化物(大多数金属氧化物)→碱性氧化物的通性与酸反应生成盐和水
物与酸性氧化物反应生成盐
与酸反应生成盐和水
两性氧化物(Al2O3和ZnO等)→两性氧化物的通性与强碱反应生成盐和水
2.几种常见的金属氧化物(下列表格中,是离子反应的请用离子方程式表示)
Na2O2
Na2O
Al2O3
Fe2O3
FeO
Fe3O4
颜色状态
粉末
色粉末
色的晶体
属性
特殊化合物,可看成FeO·
与水反应
实质是与水反应
与CO
FexOy+CO===
3.几种常见的酸性氧化物
CO2
SiO2
SO2
SO3
类别
酸性氧化物的通性
与水
与CaO
与Ca(OH)2
少量:
过量:
氧化性
还原性
无
可以被
等氧化。
特性
⑴
⑵
⑶
可以与有机色素发生
反应而漂白,是性的。
H2SO4(浓)+nSO3=
H2SO4·
nSO3
实验室制法
自然界大量存在,不需要制备
4.不成盐氧化物——NO和NO2
⑴NO:
色的气体。
容易被氧气氧化而变成红棕色,方程式为。
利用该反应可以检验NO。
⑵NO2:
可以溶解于水,方程式为
(四)金属氢氧化物(下列表格中,是离子反应的请用离子方程式表示)
NaOH
Al(OH)3
Fe(OH)2
Fe(OH)3
碱性氢氧化物
两性氢氧化物
与强酸反应
与强碱反应
热稳定性
稳定
无还原性
Fe(OH)2+O2+H2O=
现象:
制备
略
用途
化工原料
脱色净水、中和胃酸
净水
(五)酸
1.非氧化性酸的通性:
⑴酸溶液能与酸碱指示剂作用(石蕊遇酸变红,酚酞遇酸不变色)
⑵酸+活泼金属→盐+氢气:
反应条件:
金属活动顺序表H以前的金属置换酸中的H
⑶酸+碱性氧化物→盐+水⑷酸+碱→盐+水⑸酸+盐→新盐+新酸
2.两种常见的氧化性酸——硝酸和浓硫酸
浓硫酸
硝酸
酸的通性
与无还原性的金属氧化物、盐和碱反应体现酸的通性
CuO+H2SO4=
Ba(OH)2+H2SO4=
CuO+HNO3=
Ba(OH)2+HNO3=
强氧化性
与金属反应
⑴常温下,浓硫酸可以使钝化
⑵在加热条件下可以与除Pt、Au外的金属反应,生成硫酸盐+SO2+H2O
Cu+H2SO4(浓)===
硫酸起作用
⑴常温下,浓硝酸可以使钝化(稀硝酸不可以)
⑵在常温下,浓硝酸和稀硝酸可以与除Pt、Au外的金属反应,生成高价金属的硝酸盐+NO2(或NO)+H2O
Cu+HNO3(浓)===
Cu+HNO3(稀)===
硝酸起作用
与非金属反应
在加热时,浓硫酸与C、S、P等非金属反应,生成最高价稳定性酸或最高价氧化物,浓硫酸被还原为SO2
C+H2SO4(浓)===
S+H2SO4(浓)===
浓硫酸起作用
在加热时,浓硝酸与C、S、P等非金属反应,生成最高价稳定性酸或最高价氧化物,浓硝酸被还原为NO2
C+HNO3(浓)===
S+HNO3(浓)===
与还原性化合物反应
能氧化-2的S、-1的I+2的Fe
能氧化-2的S、-1的I、+4的S、+2的Fe
吸水性
可以做干燥剂,不能干燥
脱水性
有
稳定性
很稳定
不稳定。
方程式为
保存方法
色的试剂瓶
(六)几种盐
1、碳酸钠和碳酸氢钠
名称
Na2CO3
NaHCO3
俗名
水溶性
水溶液的酸碱性
与CO2反应
Ca(OH)2
Ca(OH)2(少)
Ca(OH)2(过)
与盐
CaCl2
主要用途
相互转化
2.亚硫酸盐和亚硫酸氢盐
Na2SO3类似于Na2CO3,NaHSO3类似于NaHCO3,只是亚硫酸盐和亚硫酸氢钠具有还原性,能被O2、O3、H2O2、Na2O2、Fe3+、X2、KMnO4、硝酸等氧化剂氧化,均生成Na2SO4。
3.铁盐和亚铁盐
亚铁盐——FeCl2
铁盐——FeCl3
溶液颜色
化学性质
与碱溶液
与NaOH
与氨水
与KSCN
与Fe之前的金属单质反应
Zn+Fe2+=
与Ag之前的金属、S2-、I-、SO32-等反应
Fe3++Fe=
Fe3++Cu=
Fe3++Zn(过)=
与O2、Cl2、H2O2、硝酸等氧化剂反应
Fe2++Cl2=
(“有”或“无”)还原性
检验方法
⑴观察法:
溶液为色的是Fe3+,色的是Fe2+。
⑵加碱:
生成色沉淀的是Fe3+,生成色沉淀,迅速变成色,最后转化为色沉淀的是的是Fe2+。
⑶KSCN法(特效试剂):
溶液是Fe3+;
溶液不变色,再加,溶液变的是Fe2+。
二、同种元素的单质及其化合物的转化关系
(一)Na及其化合物的转化
(请在下图中填写物质转化的条件和其他的反应物,并按要求填空)
⑴Na与酸混合时,首先与反应,再与反应,一般可以认为Na反应完全,且Na与H2的物质的量之比为。
⑵Na与除酸以外的其他溶液混合,一般先于反应,再考虑生成的NaOH是否与反应。
Na加入到饱和的Ca(OH)2溶液中会观察到现象。
⑶当有H2O、CO2同时存在时,我们认为Na2O2首先与反应。
Na2O2与H2O、CO2和酸反应时,氧化剂是,还原剂是,它们的物质的量之比为,1molNa2O2反应转移的电子数为,生成1molO2转移电子的物质的量为。
⑷CO2与Na2O2反应时,1molCO2充分,反应固体的增加量相等于1molCO,即g。
H2O与Na2O2反应时,1molH2O充分,反应固体的增加量相等于1molH2,即g。
若某物质可以看成(CO)m(H2)n(m和n均≥0,但不同时为0时),ag该物质充分燃烧后的产物与Na2O2充分反应,固体的增加量为g。
⑸碳酸钠、碳酸氢钠分别与盐酸反应,速率较快的是。
若Na2CO3和NaHCO3的质量相同,消耗盐酸多的是,生成CO2多的是。
若Na2CO3和NaHCO3的物质的量相同,消耗盐酸多的是,生成CO2。
(二)Al及其化合物的转化
请在下图中填写物质转化的条件和其他的反应物,并按要求填空
1.请用离子方程式表示制备Al(OH)3的三种方法:
①②
③
2.若相同量的铝与物质的量相同的HCl和NaOH反应,反应的离子方程式分别为,。
若铝完全消耗,生成的H2的物质的量之比为;
若酸和碱均消耗完,生成的H2的物质的量之比为;
若生成的H2物质的量之比为1:
2,则盐酸烧杯中,反应完,装NaOH烧杯中,反应完。
(三)Fe及其化合物的转化
⑴Fe→Fe2+:
可以加入等弱氧化剂。
⑵Fe→Fe3+:
可以加入等强氧化剂。
⑶Fe2+→Fe3+:
可加入等氧化剂。
⑷Fe2+→Fe:
可加入等还原剂。
⑸Fe3+→Fe2+:
⑹Fe3+→Fe:
(四)硅及其化合物的转化
1.请写出生产玻璃的两个反应方程式
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 成都 树德 中学 一期 复习 基础知识 归纳 总结
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《雷雨》中的蘩漪人物形象分析 1.docx
《雷雨》中的蘩漪人物形象分析 1.docx
