 高中化学新课程人教版必修一第二章复习学案Word格式文档下载.doc
高中化学新课程人教版必修一第二章复习学案Word格式文档下载.doc
- 文档编号:15039687
- 上传时间:2022-10-27
- 格式:DOC
- 页数:4
- 大小:57KB
高中化学新课程人教版必修一第二章复习学案Word格式文档下载.doc
《高中化学新课程人教版必修一第二章复习学案Word格式文档下载.doc》由会员分享,可在线阅读,更多相关《高中化学新课程人教版必修一第二章复习学案Word格式文档下载.doc(4页珍藏版)》请在冰豆网上搜索。
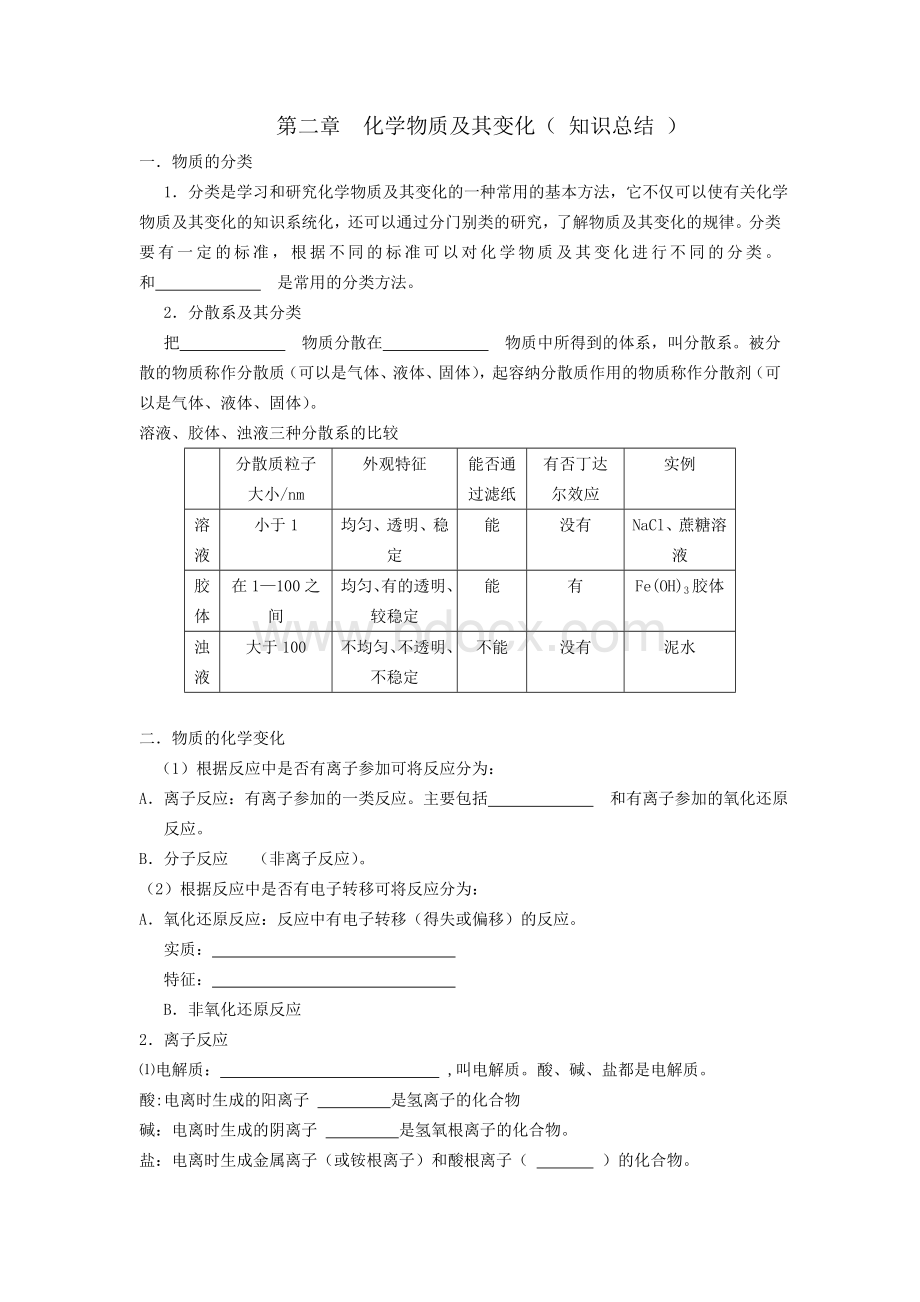
能
没有
NaCl、蔗糖溶液
胶体
在1—100之间
均匀、有的透明、较稳定
有
Fe(OH)3胶体
浊液
大于100
不均匀、不透明、不稳定
不能
泥水
二.物质的化学变化
1.
(1)根据反应中是否有离子参加可将反应分为:
A.离子反应:
有离子参加的一类反应。
主要包括和有离子参加的氧化还原反应。
B.分子反应(非离子反应)。
(2)根据反应中是否有电子转移可将反应分为:
A.氧化还原反应:
反应中有电子转移(得失或偏移)的反应。
实质:
特征:
B.非氧化还原反应
2.离子反应
⑴电解质:
叫电解质。
酸、碱、盐都是电解质。
酸:
电离时生成的阳离子是氢离子的化合物
碱:
电离时生成的阴离子是氢氧根离子的化合物。
盐:
电离时生成金属离子(或铵根离子)和酸根离子()的化合物。
在水溶液中或熔化状态下都不能导电的化合物,叫非电解质。
①电解质、非电解质都是化合物,不同处是在水溶液中或融化状态下能否导②电解质的导电是有条件的:
电解质必须在水溶液中或熔化状态下才能导电。
③能导电的物质并不全部是电解质:
如铜、铝、石墨等。
④非金属氧化物(SO2、SO3、CO2)、大部分的有机物为非电解质。
⑵离子方程式:
用实际参加反应的离子符号来表示反应的式子。
它不仅表示一个具体的化学反应,而且表示的离子反应。
复分解反应这类离子反应发生的条件是:
生成沉淀、气体或水。
书写方法:
写:
写化学方程式拆:
把易溶于水、易电离的物质拆写成离子形式
删:
将不参加反应的离子从方程式两端删去查:
查方程式两端原子个数和电荷数是否相等
⑶离子共存问题
所谓离子在同一溶液中能大量共存,就是指离子之间不发生任何反应;
若离子之间能发生反应,则不能大量共存。
A.结合生成难溶物质的离子不能大量共存:
如Ba2+和SO42-、Ag+和Cl-、Ca2+和CO32-、Mg2+和OH-
B.结合生成气体或易挥发性物质的离子不能大量共存:
如H+和C32-O,HCO3-,SO32-,OH-和NH4+等。
C.结合生成难电离物质(水)的离子不能大量共存:
如H+和OH-、CH3COO-,OH-和HCO3-等。
D.发生氧化还原反应、水解反应的离子不能大量共存(待学)。
注意:
题干中的条件:
如无色溶液应排除有色离子:
Fe2+、Fe3+、Cu2+、MnO4-等离子,酸性(或碱性)则应考虑所给离子组外,还有大量的H+(或OH-)。
⑷离子方程式正误判断(六看)
一看反应是否符合事实:
主要看反应能否进行或反应产物是否正确。
二看能否写出离子方程式:
纯固体之间的反应不能写离子方程式。
三看化学用语是否正确:
化学式、离子符号、沉淀、气体符号、等号等的书写是否符合事实。
四看离子配比是否正确。
五看原子个数、电荷数是否守恒。
六看与量有关的反应表达式是否正确(过量、适量)。
3.氧化还原反应
氧化还原反应概念的发展比较
得氧失氧的观点(狭义)
化合价升降观点(广义)
电子转移观点(本质)
氧化反应
得氧的反应
化合价升高的反应
失去(或偏离)电子的反应
还原反应
失氧的反应
化合价降低的反应
得到(或偏向)电子的反应
氧化还原反应
有氧得失的反应
有化合价升降的反应
有电子转移(得失或偏移)的反应
氧化还原反应中概念及其相互关系如下:
化合价高——去电子——被化(发生氧化反应)——是原剂(有还原性)。
化合价低——到电子——被原(发生还原反应)——是化剂(有氧化性)。
一、选择题
1.下列各组变化中,后者一定包括前者的是()。
A.化学变化、物理变化B.氧化还原反应、复分解反应
C.氧化还原反应、化合反应D.中和反应、复分解反应
2.能证明胶体微粒比溶液中电解质微粒大的操作是( )
A.丁达尔效应B.布朗运动C.渗析D.电泳现象
3.下列物质中属于电解质的是( )
①氢氧化钠 ②硫酸钡 ③铜 ④蔗糖 ⑤二氧化硫
A.①②B.①②⑤C.③④D.①⑤
4.绿柱石又称绿宝石,其组成可表示为A3B2(SiO4)3,式中A、B均为金属元素,Si用双线桥法标明电子转移的方向和数目显+4价,则A、B对应的化合价依次为()。
A.+2,+3B.+3,+2C.+2,+2D.+3,+3
5.下列叙述中,正确的是( )
A.有氧元素参加的反应一定是氧化还原反应
B.反应前后元素化合价没有变化的反应一定不是氧化还原反应
C.有单质参加或生成的反应一定是氧化还原反应
D.氧化还原反应中,一种物质被氧化,另一种物质必被还原
6.不能用离子方程式Ba2++SO===BaSO4↓表示的化学反应有( )
A.BaCl2溶液与稀硫酸反应
B.Ba(OH)2溶液与Na2SO4溶液反应
C.Ba(NO3)2溶液与NaHSO4溶液反应
D.Ba(OH)2溶液与MgSO4溶液反应
7.无论在酸性还是碱性溶液中,都能大量共存的离子组是( )
A.K+、SO、S2-、SOB.Na+、Cu2+、SO、Cl-
C.Br-、Ba2+、Cl-、K+D.Ca2+、K+、CO、NO
8.人体血红蛋白中含有Fe2+离子,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+离子转变为Fe3+离子,生成高铁血红蛋白而丧失与O2结合的能力。
服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有( )
A.酸性B.碱性C.氧化性D.还原性
9.从硫元素的化合价态上判断,下列物质中的硫元素不能表现氧化性的是( )
A.Na2SB.SC.SO2D.H2SO4
10.下列反应的离子方程式书写正确的是( )
A.饱和石灰水与稀硝酸反应:
Ca(OH)2+2H+===Ca2++2H2O
B.稀硫酸与锌反应:
H2SO4+Zn===Zn2++SO+H2↑
C.碳酸钙与稀盐酸反应:
CaCO3+2H+===Ca2++CO2↑+H2O
D.小苏打溶液与NaOH反应:
HCO+OH-===H2O+CO
11.R、X、Y和Z是四种元素,其常见化合价均为+2价,且X2+与单质R不反应;
X2++Z=X+Z2+;
Y+Z2+=Y2++Z。
这四种离子被还原成0价时,表现的氧化性强弱符合( )
A.R2+>X2+>Z2+>Y2+B.X2+>R2+>Y2+>Z2+
C.Y2+>Z2+>R2+>X2+D.Z2+>X2+>R2+>Y2+
12.已知氧化性:
Br2>
Fe3+>
I2;
还原性:
I->
Fe2+>
Br-,则下列反应能发生的是( )
A.I2+2Fe2+===2Fe3++2I-B.2Br-+I2===Br2+2I-
C.2Fe3++2I-===2Fe2++I2D.2Fe3++2Br-===2Fe2++Br2
13下列反应中必须加入还原剂才能进行的是
A.CO2→HCO3- B.Zn→Zn2+ C.H2→H2O D.CuO→Cu
14.下列反应完成后没有沉淀的是( )
A.BaCl2溶液与Na2CO3溶液反应后加足量稀H2SO4
B.Ba(OH)2溶液与KNO3溶液反应后加足量稀H2SO4
C.AgNO3溶液与Na2CO3溶液反应后加足量稀HCl
D.Ca(OH)2溶液与FeCl3溶液反应后加足量稀HNO3
15.在下列反应中,HCl作氧化剂的是( )
A.NaOH+HCl=NaCl+H2O
B.Zn+2HCl=ZnCl2+H2↑
C.MnO2+4HCl(浓)MnCl2+2H2O+Cl2↑
D.CuO+2HCl=CuCl2+H2O
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 新课程 人教版 必修 第二 复习
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 保育笔记.doc
保育笔记.doc
 幼儿园日常安全检查记录表.xls
幼儿园日常安全检查记录表.xls
