 高三化学总复习:元素及其化合物知识点Word下载.doc
高三化学总复习:元素及其化合物知识点Word下载.doc
- 文档编号:14789626
- 上传时间:2022-10-24
- 格式:DOC
- 页数:10
- 大小:306.46KB
高三化学总复习:元素及其化合物知识点Word下载.doc
《高三化学总复习:元素及其化合物知识点Word下载.doc》由会员分享,可在线阅读,更多相关《高三化学总复习:元素及其化合物知识点Word下载.doc(10页珍藏版)》请在冰豆网上搜索。
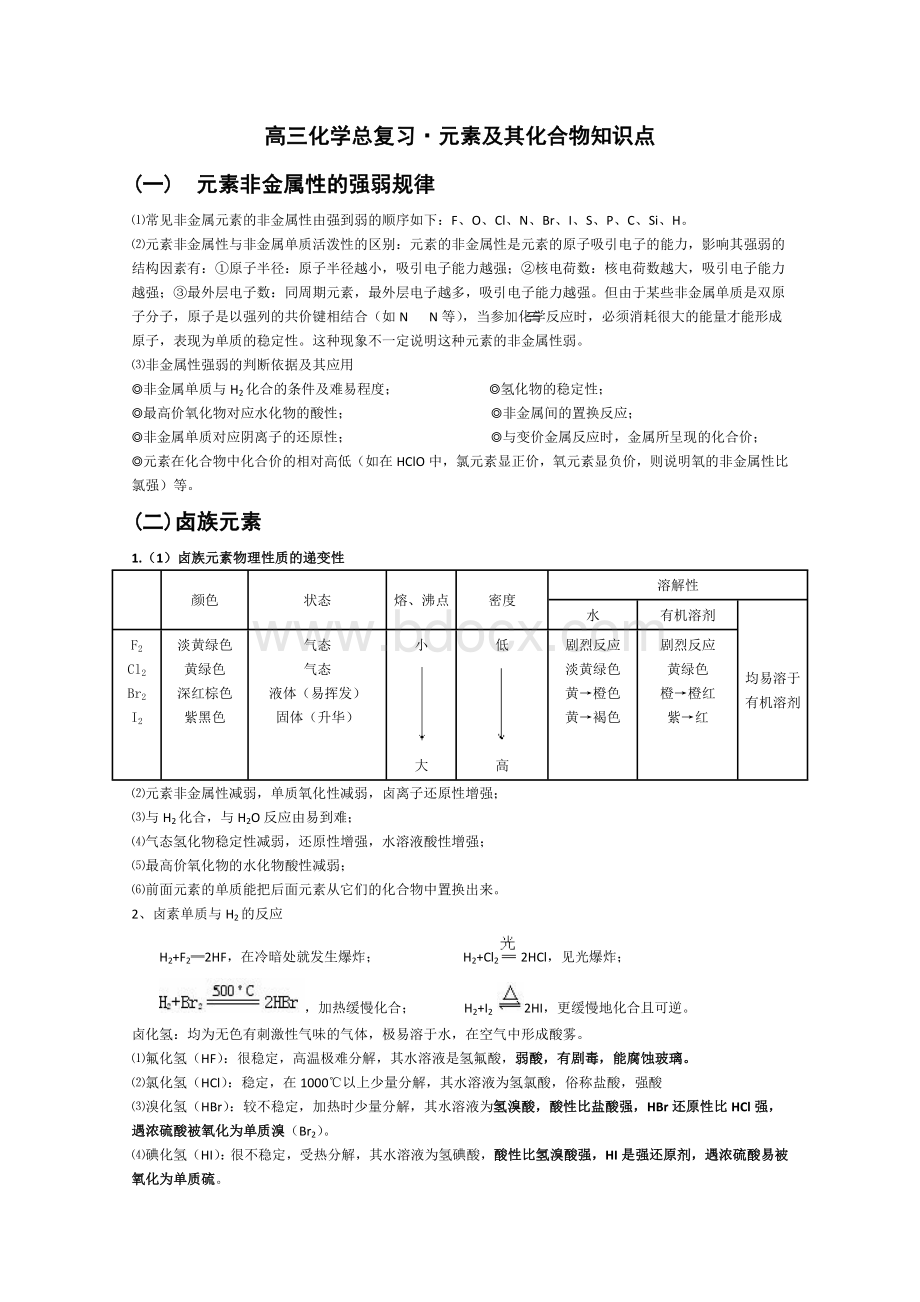
◎元素在化合物中化合价的相对高低(如在HClO中,氯元素显正价,氧元素显负价,则说明氧的非金属性比氯强)等。
(二)卤族元素
1.
(1)卤族元素物理性质的递变性
颜色
状态
熔、沸点
密度
溶解性
水
有机溶剂
均易溶于有机溶剂
F2
Cl2
Br2
I2
淡黄绿色
黄绿色
深红棕色
紫黑色
气态
液体(易挥发)
固体(升华)
小
大
低
高
剧烈反应
黄→橙色
黄→褐色
橙→橙红
紫→红
⑵元素非金属性减弱,单质氧化性减弱,卤离子还原性增强;
⑶与H2化合,与H2O反应由易到难;
⑷气态氢化物稳定性减弱,还原性增强,水溶液酸性增强;
⑸最高价氧化物的水化物酸性减弱;
⑹前面元素的单质能把后面元素从它们的化合物中置换出来。
2、卤素单质与H2的反应
H2+F2═2HF,在冷暗处就发生爆炸;
H2+Cl22HCl,见光爆炸;
,加热缓慢化合;
H2+I22HI,更缓慢地化合且可逆。
卤化氢:
均为无色有刺激性气味的气体,极易溶于水,在空气中形成酸雾。
⑴氟化氢(HF):
很稳定,高温极难分解,其水溶液是氢氟酸,弱酸,有剧毒,能腐蚀玻璃。
⑵氯化氢(HCl):
稳定,在1000℃以上少量分解,其水溶液为氢氯酸,俗称盐酸,强酸
⑶溴化氢(HBr):
较不稳定,加热时少量分解,其水溶液为氢溴酸,酸性比盐酸强,HBr还原性比HCl强,遇浓硫酸被氧化为单质溴(Br2)。
⑷碘化氢(HI):
很不稳定,受热分解,其水溶液为氢碘酸,酸性比氢溴酸强,HI是强还原剂,遇浓硫酸易被氧化为单质硫。
3、卤素及其化合物主要特性
⑴氟及其化合物的特殊性质
①卤素单质Cl2、Br2、I2与H2化合都需要一定条件,惟独F2在黑暗处就可与H2化合爆炸。
②卤素单质Cl2、Br2、I2与水反应的通式为:
X2+H2O===HX+HXO(I2与水反应极弱)
但F2与H2O反应相当剧烈!
2F2+2H2O===4HF+O2
③氟无正价,其他都有正价
④HF有毒,其水溶液为弱酸,其他氢卤酸为强酸,HF能腐蚀玻璃;
⑤CaF2不溶于水,AgF易溶于水,氟可与某些稀有气体元素形成化合物。
⑵溴的特性:
溴在常温下为红棕色液体(惟一的液态非金属单质),极易挥发产生红棕色有毒的溴蒸气,因而实验室通常将溴密闭保存在阴冷处,并在盛有液溴的试剂瓶内常加适量水。
盛装溴的试剂瓶不能用橡皮塞(腐蚀橡胶)。
⑶碘的特性:
是紫黑色固体,具有金属光泽,易升华(常用于分离提纯碘),遇淀粉变蓝色(常用来检验碘的存在),碘的氧化性较其他卤素弱,与变价金属铁反应生成FeI2而不是FeI3。
4.富集在海水中的元素---氯
√氯气的化学性质
(1)与金属反应:
Cl2+2Na2NaCl3Cl2+2Fe2FeCl3Cl2+CuCuCl2
(2)与非金属反应:
Cl2+H22HCl
(3)与水反应Cl2+H2OHCl+HClO
①、新制的氯水能氧化Fe2+、Br-:
Cl2+2Fe2+=2Fe3++2Cl—
②、新制的氯水加入镁粉,氯水褪色:
Cl2+Mg=MgCl2
③、新制的氯水加入硝酸银产生沉淀:
Cl-+Ag+=AgCl
④、新制的氯水与碳酸氢钠反应:
H++HCO3-=H2O+CO2
⑤、新制的氯水使石蕊先变红后褪色:
H+HClO
(4)与碱反应:
①工业制漂白粉或漂粉精2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
漂白粉的主要成分为:
CaCl2+Ca(ClO)2;
有效成分为:
Ca(ClO)2
漂白粉的使用:
Ca(ClO)2+2HCl=CaCl2+2HClO
Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO(通过此反应可比较得出酸性强弱:
H2CO3>HClO)
②氯气的尾气处理Cl2+2NaOH=NaCl+NaClO+H2O漂白液的有效成分:
NaClO
(5)与某些盐溶液反应Cl2+2KI=I2+2KClCl2+2Fe2+=2Fe3++2Cl—
制备氯气:
MnO2+4HCl(浓)MnCl2+Cl2+2H2O
包括四个基本环节即制备(原料、原理、反应发生装置)、净化(除杂、干
燥)、收集(收集方法、验满)、尾气处理
√次氯酸、漂白粉的性质:
HClO分子的结构式为H-O-Cl(氧处于中心),所以电子式为。
次氯酸、次氯酸钙等有多方面的性质,经常用到以下几方面性质:
(1)HClO是一种弱酸,H2CO3>HClOCa(ClO)2+CO2+H2O=CaCO3↓+2HClO
(2)ClO-是一种弱酸的酸根离子,能发生水解反应:
ClO-+H2OHClO+OH-,所以次氯酸钙溶液显碱性。
(3)HClO和ClO-都具有强氧化性,无论酸性、碱性条件下都可以跟亚铁盐、碘化物、硫化物等发生氧化还原反应,能使品红溶液褪色。
(4)HClO见光易分解:
2HClO2HCl+O2↑
(三)氧族元素
1、氧族元素的相似性和递变性
最外层均为6个电子,电子层数依次增加,次外层O为2个,S为8个,Se、Te均为18个电子。
氧通常显-2价,硫、硒、碲常见的化合物为:
-2价、+4价、+6价,都能与多数金属反应。
氧化物有两种RO2和RO3,其对应水化物H2RO3、H2RO4均为含氧酸,具有酸的通性。
它们的氢化物除H2O外,其余的H2S、H2Se、H2Te均为气体,有恶臭、有毒,溶于水形成无氧酸,都具有还原性。
核电荷数增加,电子层数依次增多,原子半径逐渐增大,核对最外层电子的引力逐渐减弱,原子得电子能力逐渐减弱,而失电子的能力逐渐增强。
单质的状态由气态到固态,熔沸点也依次升高,非金属性逐渐减弱,金属性逐渐增强,氧化性依次减弱。
含氧酸的酸性依次减弱,气态氢化物的稳定性逐渐减弱,还原性逐渐增强。
2、硫酸根离子的检验
值得注意的是,检验SO42-时会受到许多离子的干扰。
⑴Ag+干扰:
用BaCl2溶液或盐酸酸化时防止Ag+干扰,因为Ag++Cl-===AgCl↓。
⑵CO32-、SO32-、PO43-干扰:
因为BaCO3、BaSO3、Ba3(PO4)2也是白色沉淀。
与BaSO4白色沉淀所不同的是,这些沉淀溶于强酸中。
因此检验SO42—时,必须用酸酸化。
如:
BaCO3+2H+===H2O+CO2↑+Ba2+ 但不能用硝酸酸化,同理所用钡盐也不能是Ba(NO3)2溶液,因为在酸性条件下SO32-、HSO3—、SO2等会被溶液中的NO3—氧化为SO42-,从而可使检验得出错误的结论。
为此,检验SO42-离子的正确操作为:
被检液取清液有无白色沉淀(有无SO42-)
由此可见,浓硫酸和稀硫酸都具有氧化性,但产生氧化性的原因是不同的,因此其氧化能力也有强与弱的差别,被还原产物也不相同。
3.硫、硫氧化物、硫酸、硫化氢
(一)硫:
俗称硫磺。
淡黄色固体,难溶于水,可溶于酒精,易溶于CS2,熔沸点都很低。
化学性质:
①氧化性:
与绝大多数金属反应与非金属反应:
H2+SH2S
②还原性:
与氧气发生反应
③自身氧化还原反应3S+6NaOH===2Na2S+Na2SO3+3H2O
(二)二氧化硫:
具有相对不稳定的漂白性
1、物理性质:
二氧化硫是一种无色、有刺激性气味、有毒、比空气重、容易液化、易溶于水的气体
2、化学性质
(1)酸性氧化物------亚硫酐
①二氧化硫与水反应:
SO2
+H2OH2SO3(亚硫酸)
②二氧化硫与碱的反应
若二氧化硫不过量:
SO2
+2NaOH==Na2SO3+H2O
若二氧化硫过量:
+NaOH==NaHSO3[SO2
+2NaOH==Na2SO3+H2O;
Na2SO3+H2O+SO2==2NaHSO3]
③与碱性氧化物反应SO2+CaO==CaSO3
(2)二氧化硫的氧化性:
SO2+2H2S===3S↓+2H2O
(3)二氧化硫的还原性
与卤素单质反应:
SO2+Br2+2H2O=H2SO4+2HBr
(SO2+X2+2H2O=H2SO4+2HX)
与某些强氧化剂的反应:
2KMnO4+2H2O+5SO2===K2SO4+2MnSO4+2H2SO4
SO2的催化氧化2SO2+O22SO3
(5)用途:
制H2SO4;
作漂白剂;
杀菌,消毒
(6)SO2的实验室制法:
◎反应原理:
Na2SO3+H2SO4===Na2SO4+SO2↑+H2O
◎制备装置:
固体和液体不加热制备气体的装置
◎净化干燥装置:
盛放浓硫酸的洗气瓶
◎收集方法:
向上排空气法或排饱和NaHSO3溶液
◎检验:
湿润的蓝色石蕊试纸---变红湿润的品红试纸---褪色
◎尾气处理:
用NaOH溶液和倒扣漏斗装置防倒吸
(7)SO2的污染:
酸雨:
空气中SOX和NOX随雨水下降成为酸雨,pH<
5.6
(三)三氧化硫
又名硫酸酐,是一种无色易挥发的晶体,溶沸点都很低。
2、化学性质:
具有酸的氧化物的通性,与水反应放出大量的热,具有较强的氧化性。
(四)硫化氢:
无色、有臭鸡蛋气味的气体,密度比空气大,能溶于水,有剧毒。
实验室制法:
由强酸制弱酸的原理FeS+H2SO4==FeSO4+H2S↑
FeS+2HCl==FeCl2+H2S↑FeS+2H+==Fe2++H2S↑
检验:
用湿润的Pb(CH3COO)2试纸Pb(CH3COO)2+H2S==PbS↓+2CH3COOH试纸变黑
化学性质
(1)可燃性2H2S+3O22H2
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 化学 复习 元素 及其 化合物 知识点
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 保育笔记.doc
保育笔记.doc
 幼儿园日常安全检查记录表.xls
幼儿园日常安全检查记录表.xls
